2022届吉林省东北师大附中长春十一中等五校高三1月联合模拟考试理科综合化学试题含解析
展开吉林省东北师大附中长春十一中等五校2022届高三1月联合模拟考试理科综合化学试题
一、单选题
1.化学与生产、生活密切相关,下列说法正确的是
A.含钙、钡、铁等金属元素的物质有绚丽的颜色,可用于制造焰火
B.将煤气化后再作为能源,可减少PM2. 5引起的危害
C.用激光笔分别照射盛有蓝墨水、FeCl3溶液的玻璃杯均出现光亮的通路
D.为了获得更好的消毒效果,医用酒精的浓度通常为95%
2.下列离子方程式书写正确的是
A.铝和过量NaOH溶液反应:Al+4OH-=+2H2O
B.惰性电极电解MgCl2水溶液:2Cl- +2H2O2OH-+Cl2↑十H2↑
C.酸性高锰酸钾溶液与草酸溶液反应:5+2+16H+ = 2Mn2++10CO2↑+8H2O
D.水玻璃中通入过量二氧化碳:+2CO2+2H2O = H2SiO3↓+2
3.X、Y、Z、W为原子序数依次增大的短周期元素。已知X的气态氢化物溶于水后显碱性;Y是非金属性最强的元素,且Y与W同主族;金属Z的最外层电子数是最内层电子数的一半。下列说法正确的是
A.Z、W两种元素形成的化合物,室温下能导电
B.Y、W两种元素形成的氢化物沸点较高的是W
C.X的气态氢化物能与其最高价氧化物的水化物反应
D.Z与氧元素组成的化合物与水反应生成物只有其对应的碱
4.利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A
B
C
D
验证硫的非金属性强于碳
制备溴苯并验证有HBr产生
制备无水MgCl2
在铁上镀铜
A.A B.B C.C D.D
5.一种碳纳米管新型二次电池的装置如图所示。下列说法中正确的是
A.离子交换膜选用阳离子交换膜(只允许阳离子通过) B.正极的电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
C.导线中通过1mol电子时,理论上负极区溶液质量增加1g D.充电时,碳电极与电源的正极相连
6.莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是
A.分子式为C7H10O5属于芳香族化合物
B.该分子中所有原子一定不能共平面,该分子中含有3个手性碳原子
C.1mol莽草酸与适量浓硫酸混合加热,仅发生消去反应
D.1mol莽草酸与足量的NaHCO3溶液反应可放出4molCO2气体
7.H2X为二元弱酸,常温下,现配制一组c(H2X)+c(HX- )+c(X2-)=0. 01mol/L的溶液,在不同pH环境下,不同形态的粒子(H2X、HX-、 X2-) 的组成分数(平衡时某种含X元素微粒的物质的量占含X元素微粒物质的量之和的分数)如图所示,其中b、c点对应的pH分别为9.3、11.下列说法中正确的是
A.c点对应的溶液中存在c(H+) = c(HX- )+2c(X2-)+c (OH-)
B.在NaHX溶液中存在c(H+) > c(OH- )
C.室温下,将Na2X与NaHX按物质的量1:1混合加入纯水中,此时pH=11
D.室温下,a、b、c三点对应的溶液中,由水电离的c(H+)水与c(OH-) 水的乘积c(H+)水·c(OH- )水数值由大到小顺序:c>b>a
二、工业流程题
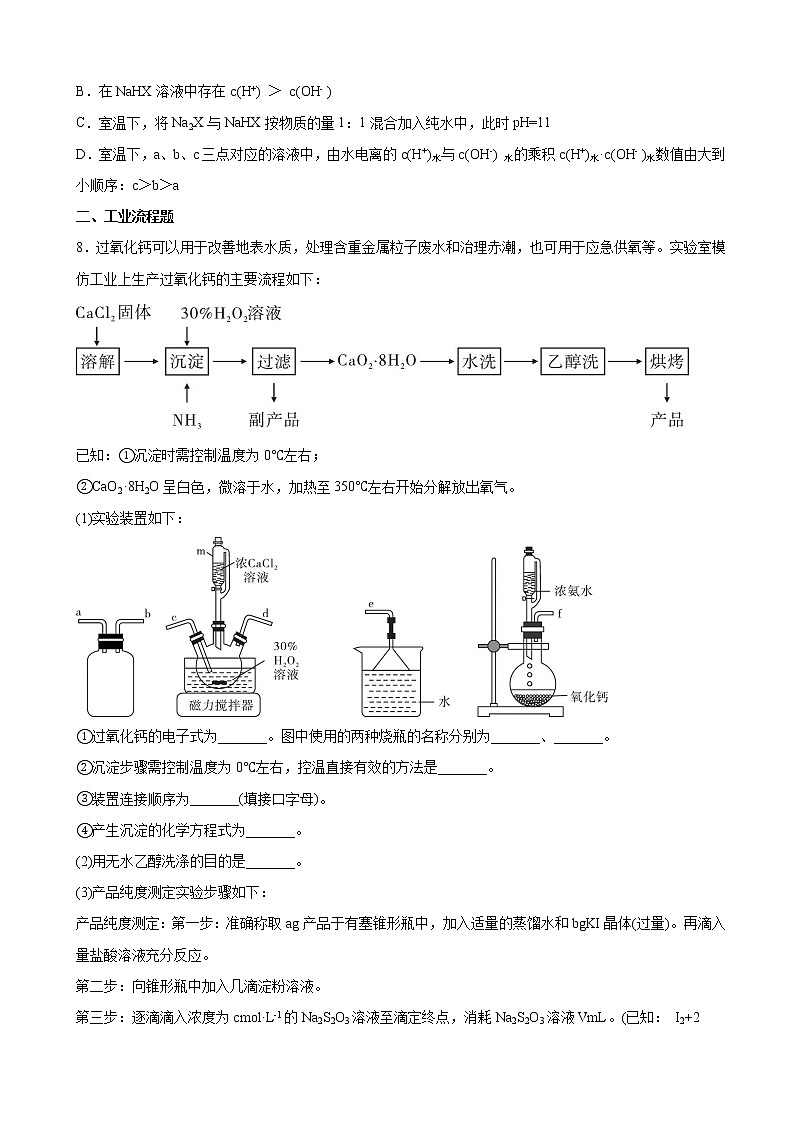
8.过氧化钙可以用于改善地表水质,处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。实验室模仿工业上生产过氧化钙的主要流程如下:
已知:①沉淀时需控制温度为0℃左右;
②CaO2·8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气。
(1)实验装置如下:
①过氧化钙的电子式为_______。图中使用的两种烧瓶的名称分别为_______、_______。
②沉淀步骤需控制温度为0℃左右,控温直接有效的方法是_______。
③装置连接顺序为_______(填接口字母)。
④产生沉淀的化学方程式为_______。
(2)用无水乙醇洗涤的目的是_______。
(3)产品纯度测定实验步骤如下:
产品纯度测定:第一步:准确称取ag产品于有塞锥形瓶中,加入适量的蒸馏水和bgKI晶体(过量)。再滴入量盐酸溶液充分反应。
第二步:向锥形瓶中加入几滴淀粉溶液。
第三步:逐滴滴入浓度为cmol·L-1的Na2S2O3溶液至滴定终点,消耗Na2S2O3溶液VmL。(已知: I2+2 =2I -+)。
①滴定终点判断标志_______。
②产品(CaO2)的纯度为_______ (列出计算式)。
9.碳酸锶(SrCO3)是一 种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO3, 少量MgCO3、CaCO3、 BaCO3等)制备高纯碳酸锶的工艺流程如下:
Sr(OH)2在水中的溶解度
温度/℃
10
20
30
40
60
80
90
100
溶解度/(g/100g)
1.25
1.77
2.64
3.95
8.42
20.2
44.5
91.2
(1)菱锶矿、焦炭混合粉碎的目的是_______。
(2)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为_______。进行高温煅烧反应的装置称为“立窑”,该装置的内层“衬里”应选择_______(填“石英砂砖”或“碱性耐火砖”)做耐火材料。
(3)“浸取”中用热水浸取而不用冷水的原因是_______;滤渣1含有焦炭、MgO和_______。
(4)“沉锶”中反应的化学方程式为_______。
(5)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则为_______(取整数)。
(6)NiSO4在强碱溶液中被NaClO氧化可得NiOOH,该物质能用作碱性镍镉电池的正极材料。其电池反应式:Cd (s) +2NiOOH(s) +2H2O (1) Cd (OH)2(s) +2Ni (OH)2(s)
①放电一段时间后,溶液的pH将_______(填 “增大”“减小”或“不变”)。
②充电时,阳极发生的电极反应式为_______。
三、原理综合题
10.CO2作为未来的重要碳源,其选择性加氢合成CH3OH 一直是研究热点。在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应i:CO2(g) +3H2(g)CH3OH(g)+H2O(g)△H1<0
反应ii:CO2(g) +H2(g)CO(g) +H2O(g) △H2
(1)反应i在_______(填“高温”“低温”或“任意温度”)下可以自发进行。
(2)在特定温度下,由稳定态单质生成1mol化合物的焓变叫该物质在此温度下的标准生成焓()。下表为几种物质在298K的标准生成焓,则反应ii的△H2=_______kJ·mol-1.
物质
H2(g)
CO2(g)
CO(g)
H2O(g)
(kJ·mol-1)
0
-394
-111
-242
(3)在CO2加氢合成CH3OH的体系中,下列说法错误的是_______(填标号)。A.增大H2浓度有利于提高CO2的转化率
B.若气体的平均相对分子质量保持不变,说明反应体系已达平衡
C.体系达平衡后,若压缩体积,则反应i平衡正向移动,反应ii平衡不移动。
D.选用合适的催化剂可以提高平衡之前CH3OH在单位时间内的产量
(4)某温度下,向容积为1L的密闭容器中通入1molCO2 (g)和5molH2(g), 10min后体系达到平衡,此时H2的转化率为8%,CH3OH 的选择性为50%。已知:CH3OH的选择性x=
①用CO2表示0~10min内平均反应速率v(CO2)=_______。
②反应i的平衡常数K_______(写出计算式即可)。
(5)维持压强和投料不变,将CO2和H2按一定流速通过反应器,二氧化碳的转化率α(CO2) 和甲醇的选择性x(CH3OH)随温度变化的关系如图所示:
已知催化剂活性受温度影响变化不大。结合反应i和反应ii,分析235℃后曲线变化的原因。
①甲醇的选择性随温度升高而下降的原因是_______;
②二氧化碳的转化率随温度升高也在下降的可能原因是_______。
四、结构与性质
11.中国冶金报指出,钢铁行业作为国民经济重要的基础产业,碳排放量在国内占比13-15%,因此钢铁行业应承担起碳减排的主体责任,努力成为碳减排的先行者。已知,铁有α、γ、δ三种晶体结构,并且在一定条件下可以相互转化(如图),请回答相关的问题:
(1)铁元素在元素周期表中的位置_______,Fe2+的外围电子排布式_______,铁的三种晶体之间的转化属于_______变化(填“物理”或“化学”),理由是:_______。
(2)铁的α、γ、δ三种晶体结构中,Fe原子的配位数之比为: _______。
(3)设α-Fe晶胞边长为a cm,δ-Fe晶胞边长为b cm, 计算确定:两种晶体的密度比为:_______。(用a、b的代数式表示)
(4)Fe3C是工业炼铁生产过程中产生的一种铁的合金,在Fe3C晶体中,每个碳原子被6个位于顶角位置的铁原子所包围,成八面体结构,即碳原子配位数为6,那么,铁原子配位数为_______。
(5)事实上,Fe3C是C与铁的晶体在高温下形成的间隙化合物(即碳原子填入铁晶体中的某些空隙),根据相关信息,你认为形成碳化铁的铁的三种晶体结构中,最有可能的是:_______,(选填“α-Fe”、“γ-Fe”或“δ-Fe”)
(6)摩尔盐[ (NH4)2 SO4·FeSO4·6H2O]是一种复盐, 它易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,不易被氧化,试分析该晶体中亚铁离子可稳定存在的原因_______。
五、有机推断题
12.可降解塑料在完成使用功能后,能在自然环境条件下较快速降解,成为易被环境利用的碎片或碎末,最终回归自然,且在降解过程中产生和降解后残留的物质对环境无害或无潜在危害。由化合物A制备可降解环保塑料PHB和一种医药合成中间体J的合成路线如图:
已知:i.(R1、R2、R3均为烃基)
ii.+2RBr+2HBr
回答下列问题:
(1)A的分子式为_______,B的结构简式为 _______。
(2)C的官能团名称为_______。
(3)D→F反应类型为_______。
(4)写出C→PHB反应的化学方程式_______。
(5)写出H→I的第一步反应的化学方程式_______。
(6)J的同分异构体X能与碳酸氢钠溶液反应放出气体,且无环状结构,则X的结构共_______种(考虑立体异构,包括顺反异构和手性异构),其中核磁共振氢谱有三组峰且峰面积之比为1:1:6,则X的结构简式为_______。
参考答案:
1.B
【解析】
【详解】
A.铁元素不能发生焰色反应,不能用于制造焰火,含钙、钡等金属元素的物质,灼烧时火焰有绚丽的颜色,可用于制造焰火,A错误;
B.将煤气化后得到可燃性气体,再作为能源,燃烧充分减少污染物排放,可减少PM2.5引起的危害,B正确;
C.FeCl3溶液不是胶体,无丁达尔效应,C错误;
D.为了获得更好的消毒效果,医用酒精的浓度通常为75%,D错误;
故答案为:B。
2.D
【解析】
【详解】
A.原离子方程式电荷不守恒,故铝和过量NaOH溶液反应的离子方程式为:2Al+2OH-+2H2O=2+3H2↑,A错误;
B.已知Mg2+和OH-结合成Mg(OH)2沉淀,故惰性电极电解MgCl2水溶液的离子方程式为:Mg2++2Cl- +2H2OMg(OH)2↓+Cl2↑十H2↑,B错误;
C.已知H2C2O4是弱酸,离子方程式书写时不能拆,故酸性高锰酸钾溶液与草酸溶液反应的离子方程式为:5H2C2O4+2+6H+ = 2Mn2++10CO2↑+8H2O,C错误;
D.水玻璃中通入过量二氧化碳生成硅酸沉淀和碳酸氢钠,故离子方程式为:+2CO2+2H2O = H2SiO3↓+2,D正确;
故答案为:D。
3.C
【解析】
【分析】
X、Y、Z、W为原子序数依次增大的短周期元素,X的气态氢化物溶于水后显碱性,可知该气体为氨气,则X为N元素;Y是非金属性最强的元素,则Y为F元素,且Y与W同主族,可知W为Cl元素;金属Z的最外层电子数是最内层电子数的一半,则Z为Na元素,据此分析作答。
【详解】
A.Na和Cl元素形成的化合物为NaCl,在室温下不能导电,A项错误;
B.Y、W两种元素形成的氢化物分别是:HF和HCl,因为HF分子之间存在氢键,则沸点较高的是HF,B项错误;
C.X的气态氢化物是氨气,其最高价氧化物的水化物为硝酸,两者能反应,C项正确;
D.钠与氧元素组成的化合物过氧化钠能与水反应,生成物为氢氧化钠和氧气,D项错误;
答案选C。
4.C
【解析】
【详解】
A.实验中蔗糖变黑,接着变得疏松多孔,同时澄清石灰水变浑浊,说明浓硫酸具有脱水性和强氧化性,同时产生SO2,但不能说明产生CO2,也不能验证硫的非金属性强于碳,A不合题意;
B.由于液溴易挥发,挥发出的液溴能与水反应生成HBr,同样可以观察到AgNO3溶液中生成淡黄色沉淀,即不能验证有HBr产生,B不合题意;
C.由于MgCl2易发生水解,水解产物HCl易挥发,从而促进其水解,故需要在HCl的气流中加热蒸发MgCl2·6H2O来制备无水MgCl2,C符合题意;
D.在铁上镀铜,铁接电源的负极作阴极,铜接电源的正极作阳极,D不合题意;
故答案为:C。
5.B
【解析】
【详解】
根据装置图,碳电极通入氢气,发生氧化反应,电极反应为H2-2e-+ 2OH-=2H2O,Ni电极NiO(OH)→Ni(OH)2发生还原反应,电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-,碳电极是负极,Ni电极是正极。根据以上分析,离子交换膜选用阴离子交换膜(只允许阴离子通过),故A错误;正极的电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-,故B正确;导线中通过1mol电子时,负极生成1mol水,理论上负极区溶液质量增加18g,故C错误;充电时,负极与电源负极相连,所以碳电极与电源的负极相连,故D错误。
6.B
【解析】
【详解】
A.由题干有机物结构简式可知,其分子式为C7H10O5,但分子不含苯环故不属于芳香族化合物,A错误;
B.由题干有机物结构简式可知,分子中的六元环不是苯环,有多个sp3杂化的碳原子,则该分子中所有原子一定不能共平面,同时连有四个互不相同的原子或原子团的碳原子为手性碳原子,则该分子中含有3个手性碳原子,即三个与羟基相连的碳原子均为手性碳原子,B正确;
C.由题干有机物结构简式可知,分子中含有羟基和羧基,与适量浓硫酸混合加热后能够发生酯化反应,醇羟基的分子间脱水和消去反应,C错误;
D.由题干有机物结构简式可知,1mol莽草酸分子中含有1mol羧基,故其与足量的NaHCO3溶液反应可放出1molCO2气体,D错误;
故答案为:B。
7.D
【解析】
【分析】
假设加入NaOH来调节溶液的pH值,则随着NaOH的加入,c(H2A)逐渐减小,c(HA-)逐渐增大,则从左往右曲线分别代表H2A、 HA-和A2-,据此分析解题。
【详解】
A.根据电荷守恒可知,c点对应的溶液中存在c(H+) +c(Na+)= c(HX- )+2c(X2-)+c(OH-),A错误;
B.由图示信息可知,b点对应的溶液中HX-最大,pH=9.3,所以NaHX溶液显碱性,即在NaHX溶液中存在c(H+)<c(OH- ),B错误;
C.由图示信息可知,当c(X2-)=c(HX-)时即c点,溶液pH=11,说明Ka(HX-)小于Kh(X2-),故室温下,将Na2X与NaHX按物质的量1:1混合加入纯水中,c(HX-)≠c(X2-),即此时溶液的pH≠11,C错误;
D.a→b→c过程中,溶液的酸性逐渐减弱,对水电离的抑制程度也逐渐减弱,同时HX-、X2-浓度促进增大,HX-、X2-的水解程度即对水的电离的促进作用逐渐加强,故室温下,a、b、c三点对应的溶液中,由水电离的c(H+)水与c(OH-) 水的乘积c(H+)水·c(OH- )水数值由大到小顺序:c>b>a,D正确;
故答案为:D。
8.(1) 三颈烧瓶 圆底烧瓶 冰水浴 fabcde或(fbacde) CaCl2 + H2O2 + 2NH3·H2O+ 6H2O= CaO2·8H2O + 2NH4Cl或CaCl2 + H2O2 + 2NH3+ 8H2O= CaO2·8H2O + 2NH4Cl
(2)去除晶体表面的水
(3) 最后一滴(或半滴)标准液滴入,溶液由蓝色变成无色且半分钟颜色不再变化 %
【解析】
【分析】
由流程可知,氯化钙溶解后,与氨气、过氧化氢发生反应生成CaO2•8H2O,CaO2•8H2O呈白色,微溶于水,不溶于醇类和乙醚等,则水洗、乙醇洗后、烘烤得到CaO2,据此分析并结合各小问题干知识进行解题。
(1)
①已知CaO2是离子化合物,故过氧化钙的电子式为,由题干实验装置图可知,图中使用的两种烧瓶的名称分别为三颈烧瓶、圆底烧瓶,故答案为:;三颈烧瓶;圆底烧瓶;
②由于温度较高时双氧水容易分解,会导致过氧化钙产率下降,且温度降低时过氧化钙的溶解度减小,有利于过氧化钙的析出,该反应是放热反应,温度低有利于提高CaO2•8H2O产率,所以沉淀反应时常用冰水浴控制温度在0℃左右,故答案为:冰水浴;
③仪器m为恒压漏斗,用f制取的氨气,通过安全瓶ab,到反应器反应,即(cd),后通过尾气处理e,所以连接顺序为fabcde或(fbacde)f,故答案为:fabcde或(fbacde);
④由流程可知,反应物为氯化钙、双氧水、氨气和水,生成为CaO2•8H2O和氯化铵,反应的化学方程式为:CaCl2+H2O2+2NH3+8H2O=CaO2•8H2O↓+2NH4Cl,故答案为:CaCl2+H2O2+2NH3+8H2O=CaO2•8H2O↓+2NH4Cl;
(2)
水洗后,用乙醇洗是利用乙醇的易挥发性质带走表面的水分,故答案为:去除结晶表面的水分;
(3)
①根据滴定结束前溶液为蓝色,滴定结束是溶液由蓝色变成无色,反应完全时的现象即滴定终点判断标志为:最后一滴(或半滴)标准液滴入,溶液由蓝色变为无色,且30s不恢复,故答案为:最后一滴(或半滴)标准液滴入,溶液由蓝色变为无色,且30s不恢复;
③过氧化钙氧化碘化钾生成的碘单质,用硫代硫酸钠滴定时,消耗的硫代硫酸钠的物质的量为:cmol•L-1×V×10-3L=cV×10-3mol,根据氧化还原反应中电子守恒及题中反应方程式可得关系式:CaO2~I2~2S2O32-,过氧化钙的物质的量为:n(CaO2)=n()=×cV×10-3mol,样品中CaO2的质量分数为×100%=%,故答案为:%。
9.(1)增大接触面积,加快反应速率,提高原料的转化率
(2) SrCO3+2CSr+3CO↑ 碱性耐火砖
(3) 为了增大氢氧化锶的浸取率,减少杂质氢氧化钙的溶解 Ca(OH)2
(4)Sr(OH)2+ (NH4)2CO3=SrCO3 +2NH3·H2O
(5)6
(6) 增大 Ni(OH)2+OH--e-=NiOOH+H2O
【解析】
【分析】
菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)与焦炭经过粉碎后立窑煅烧,转化成Sr、CaO、BaO、MgO等物质,加入热水浸取,将不溶于热水的氧化镁、Ca(OH)2、C等杂质除去,再加入稀硫酸后,除去钡离子,结晶后析出了氢氧化锶晶体,氢氧化锶和碳酸氢铵反应最终转化成碳酸锶,据此分析解题。
(1)
反应物的颗粒越小,比表面积越大,即反应物的接触面积越多,反应速率越快,则菱锶矿、焦炭混合粉碎的目的是增大反应物之间的接触面积,使反应更充分,加快反应反应速率,故答案为:增大反应物之间的接触面积,使反应更充分,加快反应反应速率;
(2)
分析流程图信息可知,碳酸锶和碳在高温的条件下生成锶和一氧化碳,化学方程式为:SrCO3+2CSr+3CO↑,由于石英砂砖中的SiO2在高温下能与SrCO3反应而腐蚀石英砂砖,故该装置的内层“衬里”应选择碱性耐火砖做耐火材料,故答案为:SrCO3+2CSr+3CO↑;碱性耐火砖;
(3)
氢氧化锶溶解度随温度升高而增大、氢氧化钙溶解度随温度升高而减小,则“浸取”中用热水浸取而不用冷水的原因是增大氢氧化锶的溶解度,使氢氧化钙析出;在立窑煅烧时MgCO3生成氧化镁,氧化镁是不溶物,滤渣1含有焦炭、Ca(OH)2和MgO,故答案为:为了增大氢氧化锶的浸取率,减少杂质氢氧化钙的溶解;Ca(OH)2;
(4)
沉锶”反应中氢氧化锶和NH4HCO3发生反应,产物除了碳酸锶外,还有水和一水合氨,则化学反应方程式为Sr(OH)2+NH4HCO3=SrCO3↓+NH3•H2O+H2O,故答案为:Sr(OH)2+NH4HCO3=SrCO3↓+NH3•H2O+H2O;
(5)
锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则有:,解得为6,故答案为:6;
(6)
①放电一段时间后,负极反应式为Cd-2e-+2OH-=Cd(OH)2,正极反应式为2NiOOH+2e-+2 H2O=2Ni(OH)2+2OH-,根据电极反应式知,负极消耗的n(OH-)等于正极生成的n(OH-),则溶液中n(OH-)不变,但消耗了电解质中的水,导致溶液中c(OH-)增大,则溶液的pH增大,故答案为:增大;
②放电时正极反应式为NiOOH+e-+H2O=Ni(OH)2+OH-,则充电时阳极反应式为Ni(OH)2+OH--e-=NiOOH+H2O,故答案为:Ni(OH)2+OH--e-=NiOOH+H2O。
10.(1)低温
(2)+41
(3)C
(4) 0.02mol·L-1 ·min-1
(5) 反应i为放热反应,反应ii为吸热反应,温度升高反应i平衡逆向移动,反应ii平衡正向移动 反应达平衡后,升高温度,反应i使二氧化碳的转化率减小的程度大于反应ii使二氧化碳的转化率增大的程度
【解析】
(1)
由题干信息可知,反应i:CO2(g) +3H2(g)CH3OH(g)+H2O(g)△H1<0正反应是一个熵减焓减的反应,故该反应在低温下可以自发进行,故答案为:低温;
(2)
反应的焓变等于生成物的标准焓之和减去反应物的标准焓之和,故则反应ii的△H2= (-111)+(-242) - (-394) =+41kJ·mol-1,故答案为:+41;
(3)
A.增大H2浓度,反应平衡正向移动,CO2的转化率增大,故有利于提高CO2的转化,A正确;
B.该反应CO2(g) +3H2(g)CH3OH(g)+H2O(g)前后气体的物质的量之和发生改变,即气体的平均相对分子质量一直改变,则若气体的平均相对分子质量保持不变,说明反应体系已达平衡,B正确;
C.由题干信息可知,反应i是一个气体体积减小的反应,而反应ii是气体体积不变的反应,则体系达平衡后,若压缩体积,即增大压强,则反应i平衡正向移动,导致反应体系中CO2、H2的量减少,H2O的量增大,故反应ii平衡逆向移动,C错误;
D.选用合适的催化剂,可以加快反应速率,故可以提高平衡之前CH3OH在单位时间内的产量,D正确;
故答案为:C;
(4)
某温度下,向容积为1L的密闭容器中通入1molCO2 (g)和5molH2(g),10min后体系达到平衡,此时H2的转化率为8%,CH3OH 的选择性为50%,由三段式分析可知:,,则有=8%,解得x=0.1mol,据此分析解题:
①用CO2表示0~10min内平均反应速率(CO2)===0.02 mol·L-1 ·min-1,故答案为:0.02 mol·L-1 ·min-1;
②由上述分析可知,平衡时:c(CO2)==0.8mol/L,同理c(H2)=4.6mol/L,c(CH3OH)=0.1mol/L,c(H2O)=0.2mol/L,故反应i的平衡常数K==,故答案为:;
(5)
①反应i为放热反应,升高温度,化学平衡逆向移动,反应ii为吸热反应,升高温度平衡正向移动,所以甲醇的选择性随温度升高而下降,故答案为:反应i为放热反应,反应ii为吸热反应,温度升高反应i平衡逆向移动,反应ii平衡正向移动;
②反应i为放热反应,升高温度,平衡逆向移动,二氧化碳的转化率降低,反应ii为吸热反应,升高温度平衡正向移动,二氧化碳的转化率上升,但温度升高对反应i中二氧化碳的转化率降低的影响大于反应ii中二氧化碳的转化率的促进作用,所以二氧化碳的转化率随温度升高也在下降,故答案为:反应达平衡后,升高温度,反应i使二氧化碳的转化率减小的程度大于反应ii使二氧化碳的转化率增大的程度。
11.(1) 第四周期第VIII族 3d6 物理 没有新物质生成或没有化学键变化或金属键不变
(2)4:6:3
(3)2b3:a3
(4)2
(5)γ-Fe
(6)摩尔盐中的N、O、H可形成空间网络化氢键,将亚铁离子包围起来,避免其与氧化性物质接触,所以比较稳定
【解析】
(1)
已知铁是26号元素,则26-18=8,即铁元素在元素周期表中的位置为第4周期第八纵列即第四周期第VIII族,Fe2+的外围电子排布式3d6,铁的三种晶体之间的转化过程中没有新物质的生成,仅仅是原子的排列方式发生改变,故属于物理变化,故答案为:第四周期第VIII族;3d6;物理;没有新物质生成或没有化学键变化或金属键不变;
(2)
金属晶体中离某一原子最近的等距离的原子为其配位数,由题干图示晶胞可知铁的α、γ、δ三种晶体结构中,Fe原子的配位数分别为:8,12,6,故配位数之比为:8:12:6=4:6:3,故答案为:4:6:3;
(3)
由题干晶胞示意图可知,一个α-Fe晶胞含有铁原子个数为:,设α-Fe晶胞边长为a cm,则其晶胞密度为:,一个δ-Fe晶胞含有铁原子个数为:,δ-Fe晶胞边长为b cm,则该晶胞的密度为:,则两种晶体的密度比为::=2b3:a3,故答案为:2b3:a3;
(4)
在Fe3C晶体中,每个碳原子被6个位于顶角位置的铁原子所包围形成八面体结构,碳原子的配位数是6,根据Fe、C比为3:1,故Fe、C配原子数目之比为1:3,则铁原子的配位数为2,故答案为:2;
(5)
由于在Fe3C晶体中,每个碳原子被6个位于顶角位置的铁原子所包围形成八面体结构,则形成碳化铁的铁的三种晶体结构中,最有可能的是γ-Fe,故答案为:γ-Fe;
(6)
摩尔盐[ (NH4)2 SO4·FeSO4·6H2O]中的N、O、H可形成空间网络化氢键,将亚铁离子包围起来,避免其与氧化性物质接触,所以比较稳定,故答案为:摩尔盐中的N、O、H可形成空间网络化氢键,将亚铁离子包围起来,避免其与氧化性物质接触,所以比较稳定。
12.(1) C7H10 CH3COCH2COOH
(2)羟基、羧基
(3)还原反应
(4)n CH3CH(OH)CH2COOH+(n-1)H2O
(5)+2NaOH+2CH3CH2OH
(6) 12
【解析】
【分析】
与KMnO4/H+、加热反应生成B和D,D的分子式为C3H4O4,根据题给已知i,B的结构简式为CH3COCH2COOH、D的结构简式为HOOCCH2COOH;PHB由单体C发生缩聚反应生成,由PHB的结构简式可知,C的结构简式为CH3CH(OH)CH2COOH;D与CH3CH2OH、浓硫酸共热发生酯化反应生成E,E的分子式为C7H12O4,E的结构简式为CH3CH2OOCCH2COOCH2CH3;对比D、F的分子式,D发生还原反应生成F,F的结构简式为HOCH2CH2CH2OH,F发生取代反应生成G,G的结构简式为BrCH2CH2CH2Br;E与G发生题给已知ii的反应生成H,H与NaOH反应后酸化生成I,I加热失去CO2生成J,结合J的结构简式可推知,H的结构简式为、I的结构简式为。
(1)
A的结构简式为,分子式为C7H10;B的结构简式为 CH3COCH2COOH;答案为:C7H10;CH3COCH2COOH。
(2)
C的结构简式为CH3CH(OH)CH2COOH,其中官能团的名称为羟基、羧基;答案为:羟基、羧基。
(3)
对比D、F的分子式,D→F发生加氢去氧的还原反应;答案为:还原反应。
(4)
C发生缩聚反应生成PHB,反应的化学方程式为n CH3CH(OH)CH2COOH+(n-1)H2O;答案为:n CH3CH(OH)CH2COOH+(n-1)H2O。
(5)
H→I的第一步反应为H在NaOH溶液中的水解反应,反应的化学方程式为+2NaOH+2CH3CH2OH;答案为:+2NaOH+2CH3CH2OH。
(6)
J的分子式为C5H8O2,不饱和度为2;J的同分异构体X能与NaHCO3溶液反应放出气体,则X中含1个—COOH,X中无环状结构,X中含有1个碳碳双键,X的结构简式有CH3CH2CH=CHCOOH(有两种互为顺反异构的结构)、CH3CH=CHCH2COOH(有两种互为顺反异构的结构)、CH2=CHCH2CH2COOH、(有两种互为顺反异构的结构)、(有两种互为手性异构的结构)、、、,符合题意的同分异构体共12种;其中核磁共振氢谱有三组峰且峰面积之比为1:1:6,则X的结构简式为;答案为:12;。
2024东北师大附中、长春十一高中、一中、四平一中、松原实验中学高三上学期1月联合模拟考试化学PDF版含答案: 这是一份2024东北师大附中、长春十一高中、一中、四平一中、松原实验中学高三上学期1月联合模拟考试化学PDF版含答案,文件包含吉林省东北师大附中长春市十一高中吉林一中四平一中松原实验中学2023-2024学年高三上学期1月联合模拟考试化学pdf、吉林省东北师大附中长春市十一高中吉林一中四平一中松原实验中学2023-2024学年高三上学期1月联合模拟考试化学答案pdf等2份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。
吉林省东北师大附中、长春市十一高中、吉林一中、四平一中、松原实验中学2023-2024学年高三上学期1月联合模拟考试 化学: 这是一份吉林省东北师大附中、长春市十一高中、吉林一中、四平一中、松原实验中学2023-2024学年高三上学期1月联合模拟考试 化学,共10页。
吉林省东北师大附中、长春市十一高中、吉林一中、四平一中、松原实验中学2023-2024学年高三上学期1月联合模拟考试 化学试题及答案: 这是一份吉林省东北师大附中、长春市十一高中、吉林一中、四平一中、松原实验中学2023-2024学年高三上学期1月联合模拟考试 化学试题及答案,文件包含吉林省东北师大附中长春市十一高中吉林一中四平一中松原实验中学2023-2024学年高三上学期1月联合模拟考试化学pdf、吉林省东北师大附中长春市十一高中吉林一中四平一中松原实验中学2023-2024学年高三上学期1月联合模拟考试化学答案pdf等2份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。