



高中鲁科版 (2019)第2章 元素与物质世界第3节 氧化还原反应导学案及答案
展开2.3.3 氧化还原反应的应用
考点精讲
考点1:实验室制备氯气
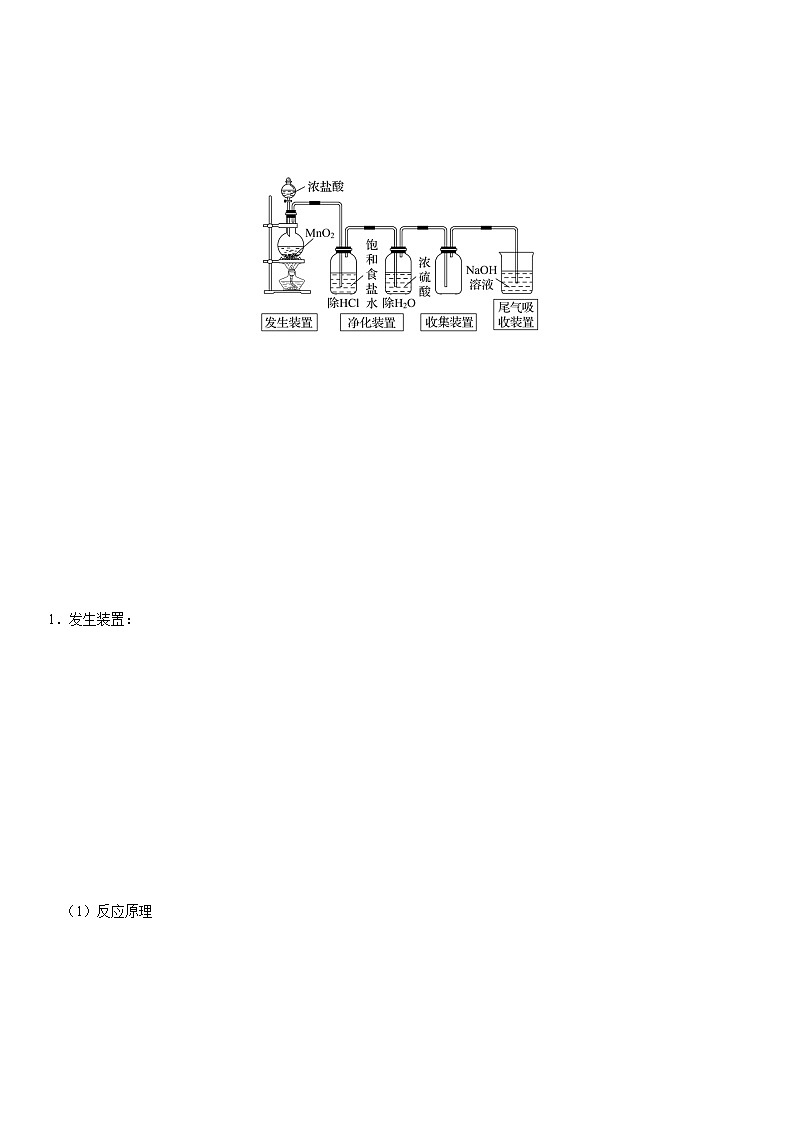
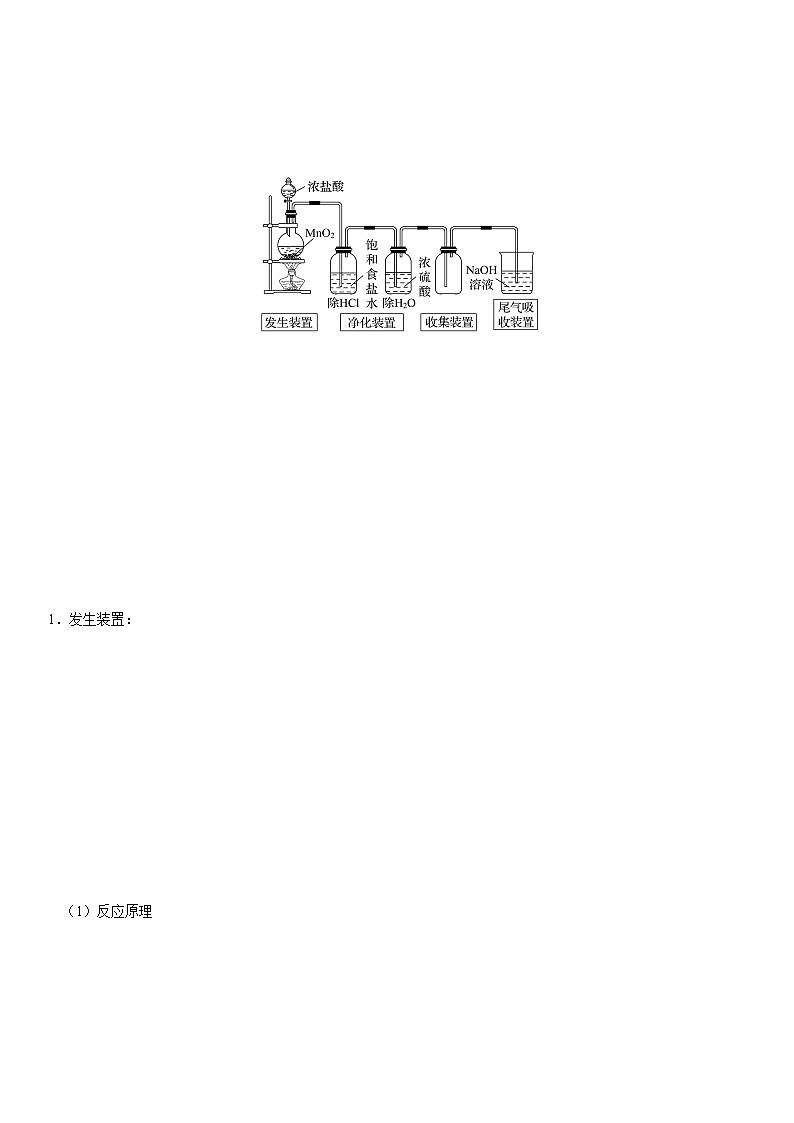
1.发生装置:
(1)反应原理
①试剂:浓盐酸和二氧化锰。
②反应的化学方程式:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O。
(2)装置类型:固体+液体气体
(3)主要仪器:圆底烧瓶、分液漏斗、酒精灯、集气瓶、铁架台、石棉网、烧杯。
2.净化装置:
先用饱和食盐水除去HCl,再用浓硫酸除去水蒸气。除去Cl2中的HCl可用图(a)所示的试剂和装置。除去Cl2中的H2O可用图(b)、图(c)和图(d)所示的试剂和装置。
3.收集装置:
(1)Cl2密度大于空气,可用向上排空气法收集,如图(e)。
(2)Cl2能溶于水,1体积水溶解2体积Cl2,用排饱和食盐水法收集,如图(f)。
排饱和食盐水法收集的Cl2较纯,但不干燥。向上排空气法可收集到干燥的Cl2,但不纯。
4.吸收装置:
因氯气有毒,在制备和使用氯气时,为了防止对环境污染,需要尾气处理。在实验室中通常用NaOH溶液吸收多余的氯气。
【特别提醒】实验室制取氯气的其他方法
实验室制备Cl2时,可用KMnO4或KClO3等强氧化剂代替MnO2,利用“固体+液体→气体(不需要加热)”装置制备:16HCl(浓)+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O,6HCl(浓)+KClO3=KCl+3Cl2↑+3H2O。
【典例1】(2021·保定高一检测)纯净干燥的氯气与熔融金属锡反应可制备SnCl4,某化学小组的同学设计了如下实验装置进行制备。
已知:①金属锡熔点为231℃,化学活泼性与铁相似;②SnCl4的沸点为114℃;③SnCl4易与水反应。请根据上图装置回答:
(1)装置I中反应的化学方程式是_________________________________。
(2)试管II中的试剂是________,试管III中的试剂是____________。
(3)装置V的作用是____________。
(4)裝置Ⅵ最好选用下列装置中的________(填标号)。
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的MnO2,需要的玻璃仪器有_________。
【举一反三】
(1)装置I中发生的反应中,浓盐酸表现的性质有哪些?
(2)为了顺利完成实验,是先点燃I处酒精灯还是Ⅳ处酒精灯?
【技巧与方法】常见的冷凝装置
类型 | 实验装置 | 说明 |
空气 |
| |
长导管起导气(平衡内外气压)和冷凝作用。 | ||
冷水冷凝 | 冷凝管下口为进水口,上口为出水口。 | |
冰水冷凝 |
| |
冰盐冷凝 | 用冰和某些盐的混合物做冷却剂,温度最低可达-55℃ |
【针对训练】
1.(2020~2021学年湖南长沙高一上期中)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验.下列收集Cl2的正确装置是( )。
A. B.
C. D.
2.某化学兴趣小组利用MnO2和浓HCl及如图装置制备Cl2。下列分析中不正确的是( )。
A.A中应用分液漏斗代替长颈漏斗
B.A中缺少加热装置
C.B中盛放的NaOH溶液可以净化Cl2
D.D中的导管口若连接倒置漏斗可防止倒吸
该用饱和食盐水除去氯化氢,氯化氢和氯气均能与氢氧化钠溶液反应,故B中不能盛放氢氧化钠溶液。
3.(2021·泉州高一检测)某研究性学习小组的同学利用MnO2、浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法正确的是( )。
A.按气流流动的先后顺序,装置连接顺序依次为DACBE
B.按气流流动的先后顺序,装置连接顺序依次为DABAE
C.装置E的主要用途是制备NaClO
D.若实验中使用到装置C且有色布条褪色,则说明湿润的氯气有漂白性
4.某学生用下列两种方法制取Cl2:①用含HCl 146g的浓盐酸与足量的MnO2反应;②用87gMnO2与足量的浓盐酸反应,则所得Cl2( )。
A.②比①多 B.①比②多 C.一样多 D.无法比较
5.(2021·山东德州高一期末)某学生设计下列实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
(1)A仪器的名称是_______________,所盛试剂是__________________。
(2)漂白粉将在U形管中产生,其化学方程式是___________________________。
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_____________________________________________。
②试判断另一个副反应是___________________________________________(写出此反应方程式)。为避免此副反应的发生,可采取的措施是__________________。
考点2:金属的冶炼
1.实质:金属阳离子得电子被还原为金属单质:Mn++ne-=M。
2.金属活动性顺序与金属冶炼方法的关系
【典例2】(2020·天津高一下期末)钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。
(1)写出在高温下发生反应①的化学方程式________________________。
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:______________________________。
(3)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有______________________________。
(4)某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是______________________________。
②两次使用D装置,其中所盛的药品依次是___________、___________。
【举一反三】
(1)写出反应④的化学方程式。
(2)冶炼金属钼的方法是什么?使用题中所给还原剂的优点是什么?
【技巧与方法】四种热还原法优缺点的比较
【针对训练】
1.下列获得金属的方法中不涉及化学变化的是( )。
A.《梦溪笔谈》“熬胆矾铁釜,久之亦化为铜”
B.《杂曲歌辞·浪淘沙》“千淘万漉虽辛苦,吹尽狂沙始到金”
C.《天工开物》“凡炉中炽铁用炭,煤炭居十七,木炭居十三……”
D.《天工开物》“炉甘石(碳酸锌)十斤,……然后逐层用煤炭……,发火缎红,……冷淀,即倭铅(锌)也”
2.(2021·湘潭高一检测)下表中金属的冶炼原理与方法完全正确的是( )。
选项 | 方法 | 冶炼原理 |
A | 湿法炼铜 | CuSO4+2Na=Cu+Na2SO4 |
B | 热分解法炼铜 | Cu2S+O2=2Cu+SO2 |
C | 电解法炼铝 | 2Al2O34Al+3O2↑ |
D | 热还原法冶炼钡 | BaO+H2Ba+H2O |
3.(2021·葫芦岛高一检测)用H2还原某二价金属的氧化物成单质.每1g H2可还原36g氧化物,则此金属可能是下列的( )。
A.Zn B.Pb C.Fe D.Cu
4.金属热还原法广泛用于冶金过程中。用金属A(或其合金)作还原剂在高温下将另一种金属B的化合物还原以制取金属B(或其合金)的方法,通常是按还原剂来命名。
(1)用铝作还原剂还原Cr2O3生产金属铬,称为铝热法,化学方程式为______________________。
(2)用硅作还原剂还原V2O5冶炼钒,称为硅热法,化学方程式为___________。
(3)试写出用镁热法还原TiCl4生产金属钛的化学方程式:________________。
合格考达标练
1.(2020·北京合格考真题)下列金属中,通常用电解法冶炼的是( )。
A.Na B.Fe C.Hg D.Ag
2.下列过程主要目的是将金属从化合态转化为游离态的是( )。
A.将镁、铝等制成合金 B.电解法冶炼铝
C.铝饮料罐回收铝 D.废旧钢铁用于炼钢
3.(2021·珠海高一检测)弗里茨·哈伯称Cl2为化学战中的“死亡之风”。实验室制取Cl2时,吸收多余Cl2的吸收剂最好选用( )。
A.水 B.饱和Ca(OH)2溶液
C.浓NaOH溶液 D.稀NaOH溶液
4.在实验室中由浓盐酸和二氧化锰制备氯气时,生成的气体一般让其通过两个洗气瓶,第一个洗气瓶中应该有( )。
A.饱和食盐水 B.浓硫酸 C.碳酸氢钠 D.浓盐酸
5.实验室制氧气的试管上粘附有MnO2,除去MnO2可用的试剂是( )。
A.蒸馏水 B.KOH溶液
C.稀盐酸 D.热的浓盐酸
6.在实验室用下列装置制取氯气并验证氯气的某些化学性质,其中能达到实验目的( )。
甲 | 乙 | 丙 | 丁 |
A.用装置甲制取氯气
B.用装置乙除去氯气中的HCl
C.用装置丙收集一试管氯气
D.用装置丁验证氯气能支持H2燃烧
7.(2021·芜湖高一检测)《宋史·食货志》记载:“浸铜之法,以生铁煅成薄铁片,排置胆水槽中,浸渍数日,铁片为胆水所薄,上生赤煤。去刮赤煤,入炉三炼成铜。”下列说法不正确的是( )。
A.生铁属于混合物
B.文中“胆水”可能是硫酸铜溶液
C.文中“赤煤”可能是铜单质
D.上述过程涉及置换、化合、分解等反应
8.(2020年1月•广东学考真题节选)氯气是一种重要的化工原料,从氯气的发现到氯元素的确认,经历了数位科学家30多年的不懈探索,根据相关信息,回答下列问题:
(1)化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合并加热,很快产生有强烈刺激性气味的黄绿色气体,完成该反应的化学方程式:MnO2+4HCl(浓)MnCl2+Cl2↑+________。最合理的氯气发生装置是________(填字母)。
(2)化学家贝托莱将Cl2的水溶液露置在阳光下,反应生成一种无色无味气体,该气体为________。
(3)化学家泰耐特将Cl2通入石灰乳中,得到一种具有漂白作用的混合液。为证明该混合液的漂白作用,进行如下实验(试剂、材料等任选),完成如表中的空白。
实验步骤 | 实验现象 | 实验结论 |
取①________与试管中,滴加适量上述混合液,振荡 | ②________________ | 该混合液具有漂白作用 |
等级考提升练
1.已知一些金属单质的发现与其金属活动性存在着某种必然的联系,你认为下列事件发生在铁器时代之前的是:①金属铝的冶炼;②青铜器时代;③金银的使用;④戴维发现金属钠;⑤15世纪中国使用锌铸币( )。
A.②③⑤ B.②③ C.①②③ D.①④⑤
2.(2021•湖北仙桃高一检测)我国明代宋应星所著《天工开物》中有关于“升炼倭铅”的记载:“炉甘石(碳酸锌)十斤,装载入一泥罐内,封裹泥固,…,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…,冷定毁罐取出,…,即倭铅也,…,以其似铅而性猛,故名之曰倭”。下列对于这段话中描述的理解错误的是( )。
A.我国历史上铅的使用早于锌
B.锌和铅有相似性但锌更活泼
C.所得产品中混有煤炭
D.属于热还原法冶炼金属
3.(2021·宝鸡高一检测)下列物质:①无水CaCl2;②碱石灰(NaOH和CaO两种固体的混合物);③浓H2SO4;④P2O5,可以用来干燥Cl2的是( )。
A.①② B.③④ C.①③④ D.①②③④
4.已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )。
A.①和②处 B.②处 C.②和③处 D.②③④处
5.(2021·湘潭高一检测)已知两瓶气体分别是HCl和Cl2,可以区别它们的方法或试剂是:①观察颜色;②打开瓶盖看有无白雾;③湿润的淀粉试纸;④湿润的红色石蕊试纸;⑤湿润的蓝色石蕊试纸;⑥AgNO3溶液( )。
A.①②③④ B.①②⑤⑥ C.①②④⑤ D.①②③⑥
6.工业上冶炼锡的第一步反应原理为2SnO2+3C2Sn+aM↑+CO2↑,则下列说法中错误的是( )。
A.反应中SnO2被还原
B.a的值为3
C.反应后有两种氧化产物
D.每生成1molCO2转移电子8mol
7.钛是一种用途广泛的活泼金属。工业上常用二氧化钛冶炼金属钛,主要反应有:①TiO2+2C+2Cl2TiCl4↑+2CO↑,②TiCl4+2Mg2MgCl2+Ti。下列关于这两个反应的叙述正确的是( )。
A.均属于置换反应
B.反应①中碳作氧化剂
C.钛在反应中均被还原
D.反应②说明金属性镁大于钛
8.(2021·丹东高一检测)实验室用MnO2和浓盐酸为原料制备并收集干燥、纯净的Cl2,下列装置中合理的是( )。
9.(2021·银川高一检测)实验室利用下面的装置制取并收集氯气,有关描述正确的是( )。
A.发生装置应先加热再逐滴加入浓盐酸
B.饱和食盐水可以用饱和碳酸氢钠溶液代替
C.若用稀盐酸代替浓盐酸不能制得氯气,说明浓盐酸的氧化性较强
D.可以通过观察集气瓶中气体的颜色判断氯气是否收集满
10.(2021·金华高一检测)实验室既可用浓盐酸与MnO2在加热时反应制备Cl2,也可用KMnO4与浓盐酸在常温下反应制备Cl2,下列有关说法不正确的是( )。
A.KMnO4的氧化性比MnO2的强
B.制备Cl2的整个实验过程中,只需要使用氧化剂与还原剂
C.用排气法收集Cl2时,不需要利用其他试剂就能确定集气瓶中已收集满
D.用足量MnO2与含有4molHCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1mol
11.(2021·珠海高一检测)钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,在自然界主要以钨(+6价)酸盐的形式存在。有开采价值的钨矿石之一黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4和MnWO4,钨酸(H2WO4)酸性很弱,难溶于水。碳和金属钨在高温下会反应生成碳化钨。黑钨矿传统冶炼工艺的第一阶段是碱熔法:
(1)黑钨矿浸入NaOH熔融液过程需通入大量空气,目的是为了使铁和锰转化为氧化物,其中一种红棕色的氧化物化学式为_____________;
(2)已知A的主要成分为Na2WO4,请写出Na2WO4与浓盐酸反应的离子方程式________________________;
(3)上述流程中B、C都是钨的化合物,则步骤(3)中B→C转化属于______(填四种基本反应类型之一)。
(4)钨冶炼工艺的第二阶段则是用碳、氢气等还原剂把氧化钨(WO3)还原为金属钨。对钨的纯度要求不高时,可用碳作还原剂。写出用碳还原氧化钨制取金属钨的化学方程式:________________________。
12.(2021•通州高一检测)如图是一个制取氯气并以氯气为原料进行特定反应的装置:
(几种气体的溶解度:常温常压下,1体积水可溶解CO2、Cl2、HCl分别为1、2、500体积)
(1)A是氯气发生装置,其中的离子反应方程式为_________________________;
(2)要将C装置接入B和D之间,正确的接法是a→_________,_________→d。
(3)实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,连接上E装置。Cl2通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为两种气体,且体积比为1∶4。试写出D中发生反应的化学方程式____________________________________,装置C的作用是__________________;为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是____________________________________。
(4)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并画出改进后的装置图______________________________________________________。
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是____________________________________。
化学必修 第一册第3节 化学中常用的物理量——物质的量学案及答案: 这是一份化学必修 第一册第3节 化学中常用的物理量——物质的量学案及答案,文件包含132气体摩尔体积-2021-2022学年高一化学精讲精练新鲁科版必修第一册解析版docx、132气体摩尔体积-2021-2022学年高一化学精讲精练新鲁科版必修第一册原卷版docx等2份学案配套教学资源,其中学案共119页, 欢迎下载使用。
鲁科版 (2019)必修 第一册第3节 氧化还原反应学案: 这是一份鲁科版 (2019)必修 第一册第3节 氧化还原反应学案,文件包含231认识氧化还原反应-2021-2022学年高一化学精讲精练新鲁科版必修第一册解析版docx、231认识氧化还原反应-2021-2022学年高一化学精讲精练新鲁科版必修第一册原卷版docx等2份学案配套教学资源,其中学案共16页, 欢迎下载使用。
高中第3章 物质的性质与转化第1节 铁的多样性导学案: 这是一份高中第3章 物质的性质与转化第1节 铁的多样性导学案,文件包含311铁与铁盐-2021-2022学年高一化学精讲精练新鲁科版必修第一册解析版docx、311铁与铁盐-2021-2022学年高一化学精讲精练新鲁科版必修第一册原卷版docx等2份学案配套教学资源,其中学案共19页, 欢迎下载使用。













