



高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验教学ppt课件
展开应用电解原理在金属或其他材料表面镀上一薄层其他金属或合金的方法。
使金属增强抗腐蚀能力,增加美观和表面硬度。
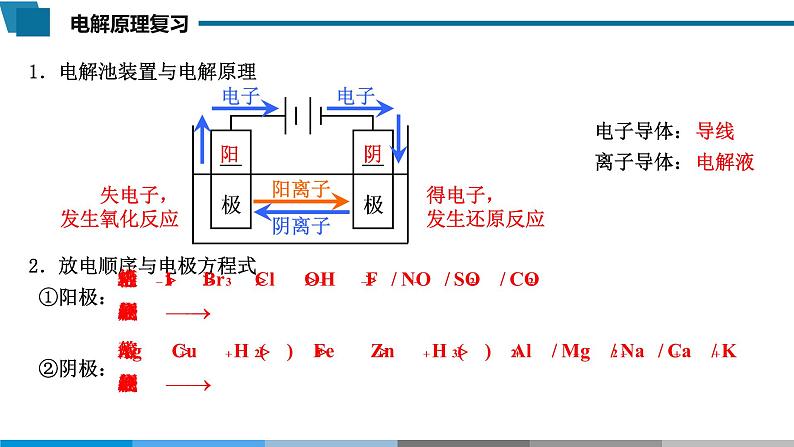
1.电解池装置与电解原理
2.放电顺序与电极方程式
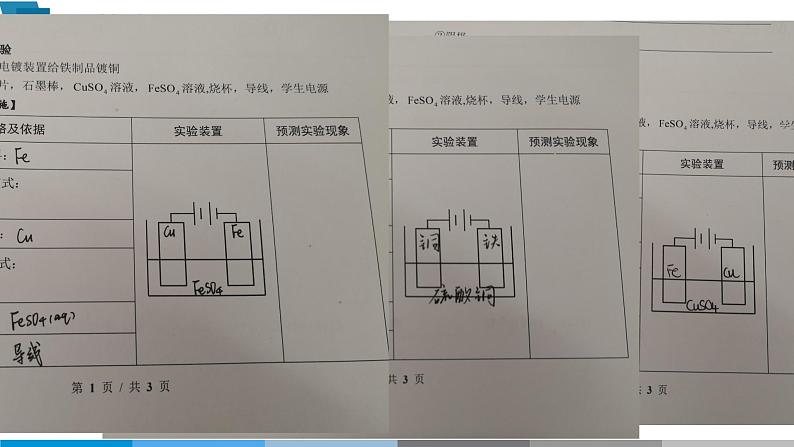
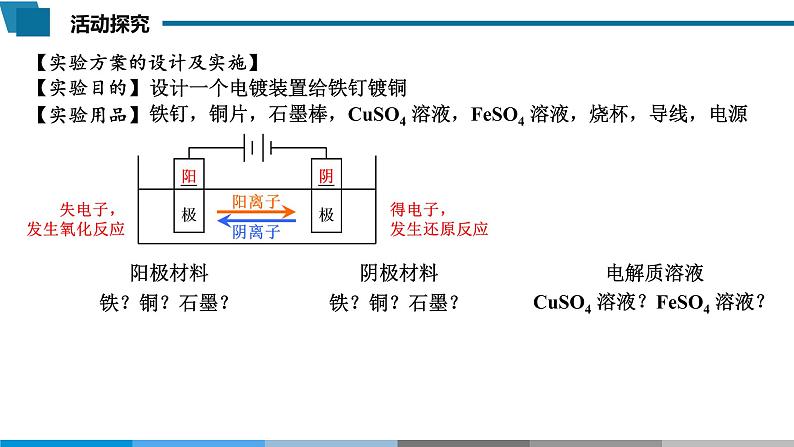
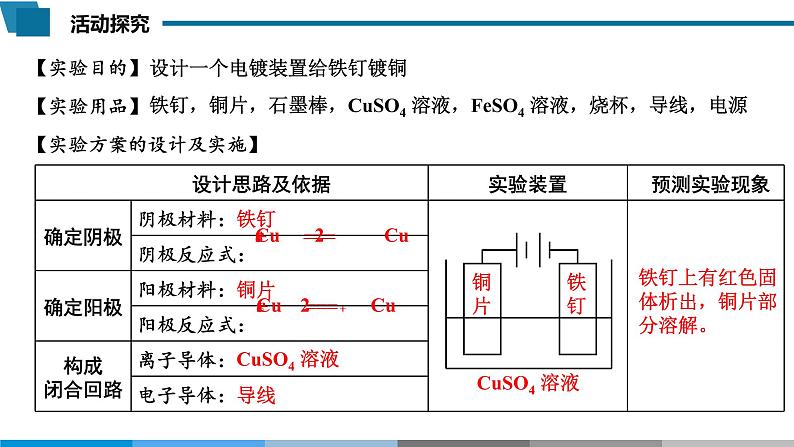
设计一个电镀装置给铁钉镀铜
铁钉,铜片,石墨棒,CuSO4 溶液,FeSO4 溶液,烧杯,导线,电源
【实验方案的设计及实施】
CuSO4 溶液?FeSO4 溶液?
铁钉上有红色固体析出,铜片部分溶解。
1.电镀后,电解质溶液中的离子浓度如何变化?
2.电镀时,如果铜片与直流电源的负极相连,铁制镀件与正极相连,电镀液仍使用 CuSO4 溶液,通电后阴极和阳极发生的反应是什么?观察到什么现象?
铜片逐渐变厚;铁制镀件逐渐溶解,变细变薄。
3.如果在铜片上镀一层银,你如何选择阳极材料、阴极材料和电镀液?
银作阳极,铜作阴极,AgNO3 溶液作电镀液。
本节课,我们复习了电解原理,并尝试用所学知识设计并进行了电镀实验。活动一:利用身边的材料,在家进行一些简易的电镀实验。 提示:处理镀件的 NaOH 可用纯碱代替,盐酸可用食醋代替。活动二:在实际生活中,我们有的电镀产品是以塑料为镀件的,有的电镀产品是镀金 的,请大家查阅相关资料,进行拓展学习。活动三:上网查阅资料,了解工业生产中影响电镀质量的因素。
1.用铁棒和铜棒做电极,模拟在铁棒上镀铜,实验装置如图所示,下列判断正确 的是( ) A.溶液中阳离子移向 b 极发生还原反应 B.铜棒的材质必须用纯铜 C.电解一段时间后加 Cu(OH)2 固体使溶液恢复原来的浓度 D.该实验过程中电解质溶液的 pH 会不断减小
2.目前市面上的很多银纪念币材料为铜芯镀银,依据你所掌握的电镀原理,你认为 这种银纪念币制作时,铜芯应作( ) A.阳极 B.阴极 C.正极 D.负极
3.利用如图所示装置可以在铜牌表面电镀一层银。下列有关说法正确的是( ) A.通电后,Ag+ 向阳极移动 B.银片与电源负极相连 C.该电解池的阴极反应可表示为 D.当电镀一段时间后,将电源反接,铜牌可恢复如初
4.依据甲、乙、丙三图,判断下列叙述中不正确的是( ) 甲 乙 丙 A.甲是原电池,乙是电镀装置 B.甲、乙装置中,锌极上均发生氧化反应 C.乙装置中,铜极因发生氧化反应而溶解 D.乙装置中,c(Cu2+) 不变,丙装置中, c(Cu2+) 减小
5.如图所示,甲为电镀银装置,下列对该装置的有关叙述中正确的是( ) 甲 乙 丙 A.P 是电源的正极 B.F 极上发生的反应为 C.电解时,甲、乙、丙三池中,除 E、F 两极外,其余电极均参加了反应 D.通电后,甲池溶液的 pH 减小,而乙、丙两池溶液的 pH 不变
高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验说课课件ppt: 这是一份高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验说课课件ppt,共15页。
高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验精品ppt课件: 这是一份高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验精品ppt课件,共9页。PPT课件主要包含了知识梳理,实验探究,随堂检测等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第四章 化学反应与电能实验活动4 简单的电镀实验示范课课件ppt: 这是一份高中化学人教版 (2019)选择性必修1第四章 化学反应与电能实验活动4 简单的电镀实验示范课课件ppt,共8页。













