



- 第11讲 物质的性质和变化探究-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册) 试卷 学案 0 次下载
- 第12讲 物质的量浓度-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册) 试卷 学案 0 次下载
- 第13讲 溶液的配制与分析-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册) 试卷 学案 0 次下载
- 第14讲 化学反应的计算-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册) 试卷 学案 0 次下载
- 第16讲 原子核外电子排布-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册) 试卷 学案 0 次下载
第15讲 原子核的构成-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册)
展开第15讲 原子核的构成
【学习目标】
1.了解人类认识原子结构的历程。
2.了解核素和质量数的概念。
3.了解同位素的概念及同位素的应用。
【基础知识】
一、人类认识原子结构的历程
1.德谟克利特的古代原子学说
2.道尔顿的近代原子学说
英国科学家道尔顿总结了一些元素形成化合物时的__________关系,提出了原子学说。认为物质由________组成,原子不能被创造,也不能被毁灭,在化学变化中不可再分割。
3.汤姆生的“葡萄干面包式”原子结构模型
英国物理学家汤姆生他在1897年发现了原子中存在________,并用实验方法测出了电子的质量。他推测这种粒子均匀地嵌在云状的___________中。
4.卢瑟福的带核原子结构模型
英国物理学家卢瑟福根据______________现象,提出了带核的原子结构模型。推测原子中心存在________,带________。电子带负电,在其周围________,就像行星围绕太阳运转一样。
5.玻尔的轨道原子结构模型
丹麦物理学家玻尔指出:原子核外,电子在一系列____________上运动,每个轨道都具有一个确定的__________;核外电子在这些_____________上运动时,既不放出能量,也不吸收能量。
6.电子云模型(现代原子结构学说)。
二、认识原子核
1.原子的构成
原子是由带正电的________和带负电的________构成的,原子核又是由________和________构成的,________带正电,________不带电。
2.质量数:
将原子核内所有的质子和中子的________取________值,加起来所得的数值。
3.原子的表示符号:
X表示________是Z,________为A的一种X原子。
如作为相对原子质量标准的C表示质子数为________,质量数为________的碳原子。
4.构成原子的微粒间的两个关系
(1)质量数(A)=________+________。
(2)核电荷数=__________=___________=原子序数。
5.元素、核素和同位素
(1)概念辨析:
元素:具有相同________的同一类原子的总称。
核素:具有一定________和一定________的一种原子。
同位素:________相同,________ (或________)不同的核素互称为同位素。
(2)氢元素的三种核素
| H(氕) | H(氘) | H(氚) |
俗称 | - | 重氢 | 超重氢 |
符号 | ________ | ________ | ________ |
质子数 | 1 | 1 | 1 |
中子数 | ________ | ________ | ________ |
(3)同位素的应用
①________在考古工作中用于测定文物的年代;
②U用于制造原子弹、核发电;
③________用于制造氢弹;
④放射性同位素释放的射线可用于育种、治疗恶性肿瘤等。
【考点剖析】
考点一:原子的组成
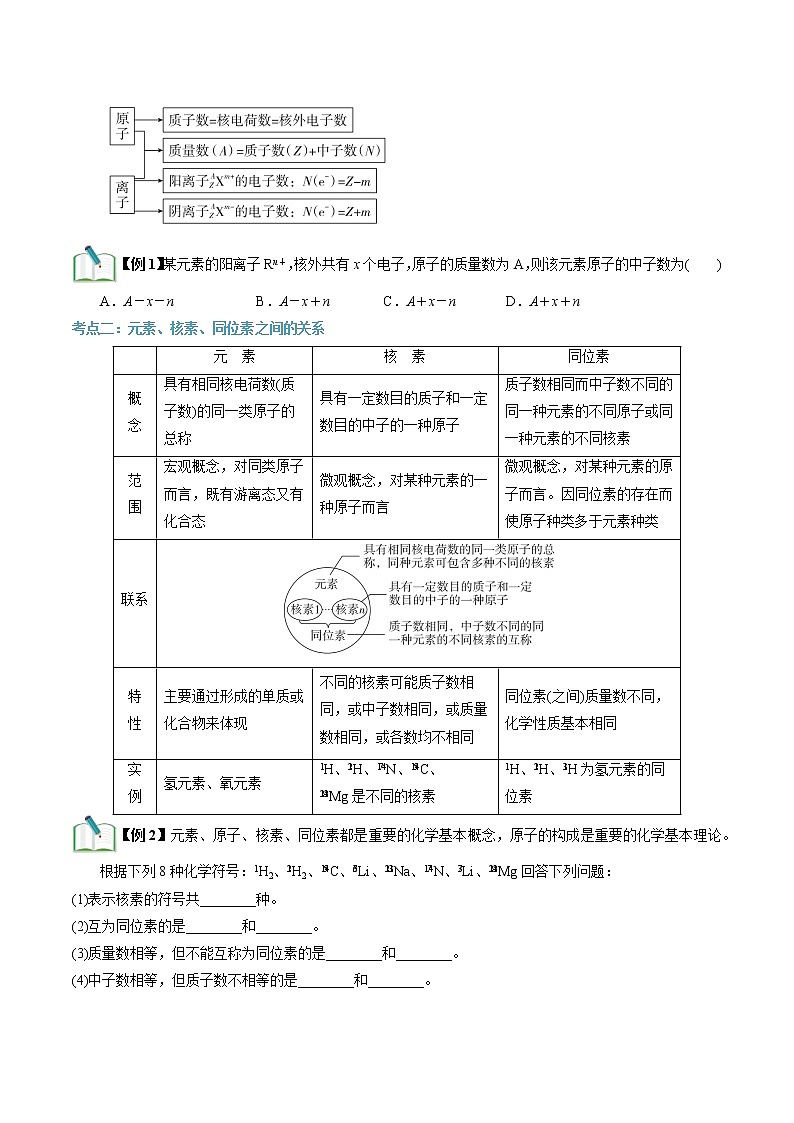
1.原子的组成
2.组成原子、离子的各种微粒及相互关系
【例1】某元素的阳离子Rn+,核外共有x个电子,原子的质量数为A,则该元素原子的中子数为( )
A.A-x-n B.A-x+n C.A+x-n D.A+x+n
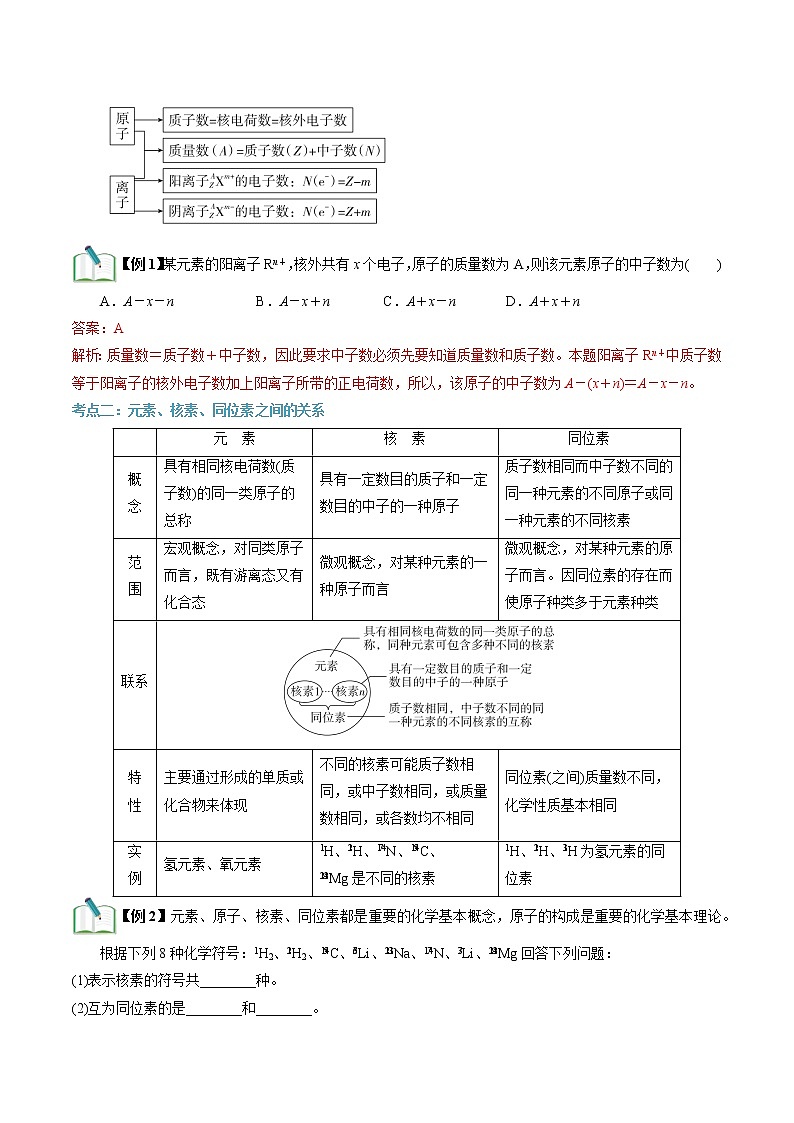
考点二:元素、核素、同位素之间的关系
| 元 素 | 核 素 | 同位素 |
概 念 | 具有相同核电荷数(质子数)的同一类原子的总称 | 具有一定数目的质子和一定数目的中子的一种原子 | 质子数相同而中子数不同的同一种元素的不同原子或同一种元素的不同核素 |
范 围 | 宏观概念,对同类原子而言,既有游离态又有化合态 | 微观概念,对某种元素的一种原子而言 | 微观概念,对某种元素的原子而言。因同位素的存在而使原子种类多于元素种类 |
联系 | |||
特 性 | 主要通过形成的单质或化合物来体现 | 不同的核素可能质子数相同,或中子数相同,或质量数相同,或各数均不相同 | 同位素(之间)质量数不同,化学性质基本相同 |
实 例 | 氢元素、氧元素 | H、H、N、C、 Mg是不同的核素 | H、H、H为氢元素的同位素 |
【例2】元素、原子、核素、同位素都是重要的化学基本概念,原子的构成是重要的化学基本理论。根据下列8种化学符号:H2、H2、C、Li、Na、N、Li、Mg回答下列问题:
(1)表示核素的符号共________种。
(2)互为同位素的是________和________。
(3)质量数相等,但不能互称为同位素的是________和________。
(4)中子数相等,但质子数不相等的是________和________。
【过关检测】
1.提出原子结构模型的科学家,从时间的先后顺序来看,下列排列正确的是( )
A.汤姆生、玻尔、卢瑟福、道尔顿
B.汤姆生、玻尔、道尔顿、卢瑟福
C.卢瑟福、道尔顿、汤姆生、玻尔
D.道尔顿、汤姆生、卢瑟福、玻尔
2.提出“有核模型”的科学家是( )
A.汤姆生 B.卢瑟福
C.道尔顿 D.玻尔
3.某元素B的核电荷数为Z。已知Bn-、Am+的核外具有相同的电子数,则A元素的质子数用Z、n、m来表示,应为( )
A.Z+n-m B.Z-n+m
C.Z-n-m D.Z+m+n
4.已知R2+核内共有N个中子,R的质量数为A,确定m g R2+中含有电子的物质的量为( )
A. mol B. mol
C. mol D. mol
5.已知阳离子R2+核外有a个电子和b个中子。表示R原子符号正确的是( )
A.R B.R C.R D.R
6.13C-NMR(核磁共振)可用于含碳化合物的结构分析,15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下列有关13C、15N的叙述正确的是( )
A.13C与15N具有相同的中子数
B.13C与C60是同一种物质
C.15N与14N互为同位素
D.15N的核外电子数与中子数相同
7.下列各组中互为同位素的是( )
A.K与Ca B.T2O与H2O
C.K与K D.金刚石与石墨
8.重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.氘(D)原子核外有1个电子
B.1H与D互为同位素
C.H2O与D2O相对分子质量相同
D.1H218O与D216O的相对分子质量相同
9.“玉兔”号月球车用Pu作为热源材料,下列关于Pu的说法正确的是( )
A.Pu与U互为同位素
B.Pu与Pu具有完全相同的物理性质
C.Pu与U具有完全相同的化学性质
D.Pu与Pu具有相同的最外层电子数
10.下列叙述正确的是( )
A.40K和40Ca原子中质子数和中子数都不相等
B.金刚石和石墨的性质相同
C.H2和D2互为同位素
D.某物质只含一种元素,该物质一定是纯净物
11.科学家发现两种微粒:第一种是由四个中子构成的微粒“四中子”;第二种是由四个氧原子构成的分子。下列关于这两种微粒的说法不正确的是( )
A.“四中子”不显电性
B.“四中子”的质量数为4
C.第二种微粒是氧元素的另一种同位素
D.第二种微粒的化学式为O4
12.据报道,某些花岗岩会产生氡(Rn),从而对人体产生伤害。请回答下列问题:
(1)该原子的质量数是________,质子数是________,中子数是________。
(2)研究发现,镭能蜕变为Rn,故将Rn称为镭射气;钍能蜕变为Rn,故将Rn称为钍射气;锕能蜕变为Rn,故将Rn称为锕射气。Rn、Rn、Rn______(填字母)。
A.属于同种元素 B.互为同位素
C.属于同种核素 D.属于同种原子
(3)由(2)可知,________决定元素种类,________决定核素种类。
第16讲 原子核外电子排布-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册): 这是一份第16讲 原子核外电子排布-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册),文件包含第16讲原子核外电子排布-暑假自学课2022年新高一化学暑假精品课苏教版2019必修第一册解析版docx、第16讲原子核外电子排布-暑假自学课2022年新高一化学暑假精品课苏教版2019必修第一册原卷版docx等2份学案配套教学资源,其中学案共12页, 欢迎下载使用。
第14讲 化学反应的计算-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册): 这是一份第14讲 化学反应的计算-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册),文件包含第14讲化学反应的计算-暑假自学课2022年新高一化学暑假精品课苏教版2019必修第一册解析版docx、第14讲化学反应的计算-暑假自学课2022年新高一化学暑假精品课苏教版2019必修第一册原卷版docx等2份学案配套教学资源,其中学案共14页, 欢迎下载使用。
第13讲 溶液的配制与分析-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册): 这是一份第13讲 溶液的配制与分析-【暑假自学课】2022年新高一化学暑假精品课(苏教版2019必修第一册),文件包含第13讲溶液的配制与分析-暑假自学课2022年新高一化学暑假精品课苏教版2019必修第一册解析版docx、第13讲溶液的配制与分析-暑假自学课2022年新高一化学暑假精品课苏教版2019必修第一册原卷版docx等2份学案配套教学资源,其中学案共15页, 欢迎下载使用。












