

化学人教版 (2019)第三节 芳香烃学案
展开课程目标
1.了解苯的结构特点及化学性质。
2.认识苯的同系物的结构与性质的关系。
3.了解常见的苯的同系物的命名。
图说考点
基 础 知 识
[新知预习]
一、苯的结构与性质
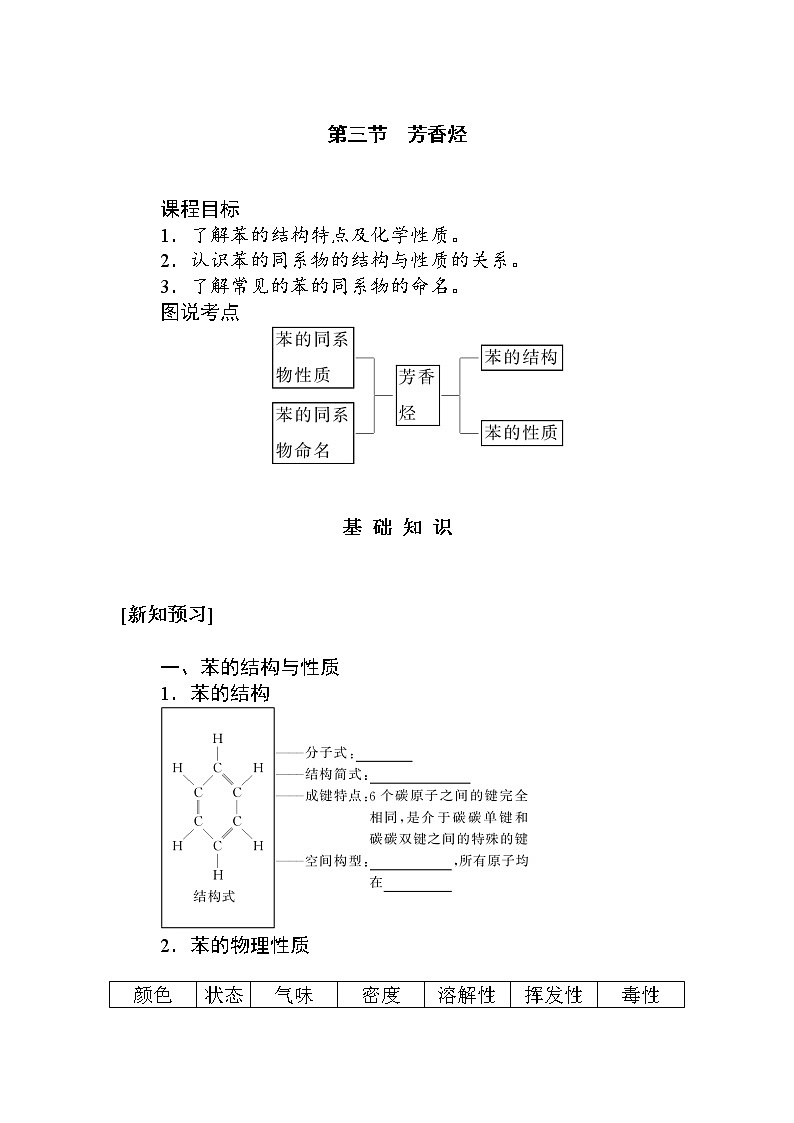
1.苯的结构
2.苯的物理性质
3.苯的化学性质
二、苯的同系物
1.概念:苯环上的氢原子被____取代的产物。
2.结构特点:分子中只有一个____,侧链都是____。
3.通式:________________。
4.化学性质:
(1)氧化反应:
①甲苯、二甲苯等大多数苯的同系物能被酸性KMnO4溶液氧化。
②均能燃烧,燃烧通式为____________________。
(2)取代反应:甲苯与浓硝酸和浓硫酸的混合物在一定条件下反应生成三硝基甲苯的化学方程式为
________________________________________________________________________。
(3)加成反应
甲苯与H2反应的化学方程式:
________________________________________________________________________。
三、苯的同系物的命名方法
1.苯的一元取代物
以苯作母体,苯环上的烃基为取代基进行命名,称为“××苯”,例如:甲苯、乙苯、正丙苯、:________。
2.苯的二元取代物
(1)习惯命名法:
当有两个取代基时,取代基在苯环上可以有“邻”“间”和“对”三种相对位置,可分别用“邻”“间”和“对”来表示,如CH3CH3:________
(2)系统命名法:
若苯环上有两个或两个以上的取代基时,则将苯环上的6个碳原子编号,以某个最简单的取代基所在碳原子的位置编号为1号,并按照所有取代基的编号和最小的原则给其他取代基编号。如邻二甲苯也可叫作:________;间二甲苯叫作:________;对二甲苯叫作:________。
又如名称为:________。
[即时性自测]
1.下列叙述正确的是( )
A.苯的分子是环状结构,其性质跟环状烷烃完全相似
B.表示苯的分子结构,其中含有碳碳单键、双键,因此苯的性质跟烯烃相同
C.苯的分子式为C6H6,分子中碳原子远远没有饱和,因此能与溴水反应
D.苯不能使酸性KMnO4溶液褪色,因此苯分子中不含碳碳双键
2.以苯为原料,不能通过一步反应制得的有机物是( )
3.下列物质一定属于苯的同系物的是( )
4.下列化合物中,苯环上的氢原子被溴原子取代,所得一溴代物有三种同分异构体的是( )
A.①③ B.①④
C.②③ D.③④
5.有4种无色液态物质:己烯、己烷、苯和甲苯,符合下列各题要求的分别是:
(1)不能与溴水或酸性KMnO4溶液反应,但在铁屑作用下能与液溴反应的是________,生成的有机物名称是________,反应的化学方程式为______________________,此反应属于________反应。
(2)不能与溴水或酸性KMnO4溶液反应的是________。
(3)能与溴水或酸性KMnO4溶液反应的是________。
(4)不与溴水反应但能与酸性KMnO4溶液反应的是________。
6.用系统命名法对下列苯的同系物进行命名:
(1)________________________________________________________________________。
(2)________________________________________________________________________。
(3)________________________________________________________________________。
技 能 素 养
提升点一 苯的两个重要实验
[例1] 某化学课外小组用下图装置制取溴苯。
先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式________________________。
(2)观察到A中的现象是________________________________________________________________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________________________,写出有关的化学方程式________________________________________________________________________。
(4)C中盛放CCl4的作用是________________________________________________________________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入________________________________________________________________________,
现象是_______________________。
eq \x(状元随笔) 溴易挥发,干扰HBr检验。
[提升1]
实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如图所示。请回答下列问题:
(1)反应需在50~60 ℃的温度下进行,图中给反应物加热的方法是________,其优点是________________________和________________________________________________________________________。
(2)在配制混合酸时应将________加入________中去。
(3)该反应的化学方程式是________________________________________________________________________。
(4)由于装置的缺陷,该实验可能会导致的不良后果是____________________________。
(5)反应完毕后,除去混合酸,所得粗产品用如下操作精制:
①蒸馏 ②水洗 ③用干燥剂干燥 ④用10% NaOH溶液洗
正确的操作顺序是______________(填序号)。
eq \x(状元随笔) (1)苯和硝酸易挥发。
(2)混酸配制类比浓硫酸稀释。
[关键能力]
苯的两个重要实验
1.卤代反应——溴苯的实验室制法
2.硝化反应——硝基苯的实验室制法
提升点二 苯与苯的同系物化学性质的比较
[例2] 苯的同系物中,有的侧链能被酸性KMnO4溶液氧化,生成芳香酸,反应如下:
(R、R′表示烷基或氢原子)
(1)现有苯的同系物甲、乙,分子式都是C10H14。甲不能被酸性KMnO4溶液氧化为芳香酸,它的结构简式是________;乙能被酸性KMnO4溶液氧化为分子式为C8H6O4的芳香酸,则乙可能的结构有________种。
(2)有机物丙也是苯的同系物,分子式也是C10H14,它的苯环上的一溴代物只有一种,试写出丙所有可能的结构简式:
________________________________________________________________________。
eq \x(状元随笔) 与苯环相连的碳原子有H才能被氧化
[提升2] 某液态烃的分子式为C8H10,实验证明它能使酸性高锰酸钾溶液褪色,但不能使溴水褪色。
(1)该有机物属于________(填“脂肪烃”或“苯的同系物”),并写出其可能的同分异构体的结构简式:________、________、________、________。
(2)若苯环上只有一个支链,该分子与氢气反应的化学方程式是________________________________________________________________________。该分子
在一定条件下易与液溴发生________反应(填反应类型)。
eq \x(状元随笔) 芳香烃的性质特点为:易取代难加成。
[关键能力]
苯和苯的同系物化学性质比较
由于苯环与侧链的相互影响,使苯的同系物的化学性质与苯的化学性质,既有相似之处又有不同之处。比较如下:
eq \x(状元随笔) (1)苯的同系物特点:一个苯环、连接烷基。
(2)苯的同系物与酸性KMnO4溶液反应的注意点:苯的同系物中,不管侧链烃基的碳链有多长,只要侧链烃基中与苯环直接相连的碳原子上有氢原子,它就能被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色,侧链烃基通常被氧化为羧基。
若侧链烃基中直接与苯环相连的碳原子上没有氢原子[如],则该有机物就不能使酸性KMnO4溶液褪色。
形成性自评
1.下列各组物质用酸性高锰酸钾溶液和溴水都能区别的是( )
A.苯和甲苯 B.1己烯和二甲苯
C.苯和1己烯 D.己烷和苯
2.要鉴别己烯中是否混有少量甲苯,正确的实验方法是( )
A.先加足量的酸性高锰酸钾溶液,然后再加入溴水
B.先加足量溴水,然后再加入酸性高锰酸钾溶液
C.点燃这种液体,然后再观察火焰的颜色
D.加入浓硫酸与浓硝酸后加热
3.下列有机物分子中的碳原子,既有sp3杂化又有sp2杂化的是( )
A.乙烷 B.苯
C.乙烯 D.甲苯
4.下列物质在一定条件下,可与苯发生化学反应的是( )
①氯气 ②溴水 ③氧气 ④酸性KMnO4溶液 ⑤KOH溶液
A.①③ B.②③
C.②④ D.①⑤
5.苯和甲苯都具有的性质是( )
A.分子中所有原子都在同一平面上
B.能与溴水发生加成反应使溴水褪色
C.能与浓硝酸在一定条件下发生取代反应
D.能与酸性KMnO4溶液反应使酸性KMnO4溶液褪色
6.下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是( )
A.甲苯与硝酸反应生成三硝基甲苯
B.甲苯能使酸性高锰酸钾溶液褪色
C.甲苯燃烧产生带浓烟的火焰
D.1 ml甲苯与3 ml H2发生加成反应
7.分子组成为C9H12的苯的同系物,已知苯环上只有一个取代基,下列说法中正确的是( )
A.该有机物不能发生加成反应,但能发生取代反应
B.该有机物不能使酸性KMnO4溶液褪色,但能使溴水褪色
C.该有机物分子中的所有原子可能在同一平面上
D.该有机物的一溴代物最多有6种同分异构体
8.如图为某学生设计的制取溴苯的装置:
(1)写出图中的错误之处:①__________________________;②____________________。
(2)按加入的顺序写出烧瓶内所装的试剂是____________________。
(3)与烧瓶口连接的垂直向上的导管的作用是____________________。
(4)反应过程中,在锥形瓶中的导管出口处会发生的现象是________,这是因为____________。
(5)反应完毕后,向锥形瓶中的溶液中滴入AgNO3溶液,现象是____________________,这是因为生成了____________________,反应的离子方程式为________________。
(6)反应完毕后,将烧瓶中的液体倒入盛有冷水的烧杯中,可以观察到烧杯底部有________色不溶于水的液体,这是因为________________________________的缘故。在粗产品溴苯中加入________________可以除去________杂质,反应的离子方程式为________________________________________________________________________。
(7)烧瓶中发生反应的化学方程式为________________________________。
eq \x(温馨提示:请完成课时作业5)
第三节 芳香烃
基础知识
新知预习
一、
1.C6H6 或 平面正六边形 同一平面上
2.无色 液态 小 不溶 易溶 有毒
3.
火焰明亮,带有黑烟 不能
二、
1.烷基
2.苯环 烷基
3.CnH2n-6(n≥6)
4.(1)CnH2n-6+eq \f(3n-3,2)O2eq \(――→,\s\up15(点燃))nCO2+(n-3)H2O
(2)
(3)
三、
1.异丙苯
2.(1)邻二甲苯 间二甲苯 对二甲苯 (2)1,2-二甲苯 1,3-二甲苯 1,4-二甲苯 1,4-二甲基-2-乙基苯
即时性自测
1.D 2.A 3.B
4.解析:中苯环上有①、②、③三种一溴代物;中有①、②两种一溴代物;中有①、②、③三种一溴代物;由于分子的对称性,苯环上仅有一种一溴代物。
答案:A
5.解析:己烯、己烷、苯、甲苯四种物质中,既能和溴水反应,又能和酸性KMnO4溶液反应的只有己烯。均不反应的为己烷和苯。不能与溴水反应但能被酸性KMnO4溶液氧化的是甲苯。苯在铁的催化作用下与液溴发生取代反应生成溴苯。
答案:(1)苯 溴苯
取代
(2)苯、己烷 (3)己烯 (4)甲苯
6.解析:(1)
(2)
(3) 然后以苯为母体写出名称即可。
答案:(1)1甲基2乙基苯 (2)1,2,4三甲基苯 (3)1,2二甲基4乙基苯
技能素养
例1 解析:本题主要考查溴苯制备过程中的具体实验知识。由于苯、液溴的沸点较低,且反应为放热反应,故A中观察到的现象为:反应液微沸,有红棕色气体充满A容器。HBr中混有的Br2在经过CCl4时被吸收;在制备的溴苯中常混有Br2,一般加入NaOH溶液中,因发生反应Br2+2NaOH===NaBr+NaBrO+H2O而除去。若该反应为取代反应则必有HBr生成,若为加成反应则没有HBr生成,故只需检查D中是否含有大量H+或Br-即可。
答案:(1)
(2)反应液微沸,有红棕色气体充满A容器
(3)除去溶于溴苯中的溴 Br2+2NaOH===NaBr+NaBrO+H2O(或3Br2+6NaOH===5NaBr+NaBrO3+3H2O)
(4)除去溴化氢气体中的溴蒸气
(5)石蕊试液 溶液变红色(其他合理答案也对)
提升1 解析:(1)反应条件中加热温度在100 ℃以下时,可以采用水浴加热法,此方法优点在于使反应物受热均匀,且易于控制温度。(2)配制混合酸时,应将浓硫酸加入浓硝酸中去。(4)由于缺乏冷凝回流装置,苯、浓硝酸等受热易挥发,造成环境污染。(5)结合苯、硝基苯、浓硫酸、浓硝酸的物理化学性质,可知粗产品先用水洗去多数酸液,再用10%的NaOH溶液洗去水洗未洗净的少量酸液,然后再水洗去NaOH溶液,经过干燥得到苯与硝基苯的混合物,再经蒸馏即可得到纯净的硝基苯。
答案:(1)水浴加热 便于控制温度 受热均匀
(2)浓硫酸 浓硝酸
(3)
(4)苯、浓硝酸等挥发到空气中,造成污染
(5)②④②③①
例2 解析:(1)据题目信息,苯的同系物能被氧化为分子式为C8H6O4的芳香酸(二元酸),说明苯环上有2个侧链,可能是2个乙基,也可能是1个甲基和1个丙基,而丙基又有2种结构(—CH2CH2CH3和),2个侧链在苯环上的位置又有邻位、间位和对位3种可能,故分子式为C10H14、有两个侧链能被酸性KMnO4溶液氧化的苯的同系物有3×3=9(种)可能的结构。
(2)分子式为C10H14的苯的同系物的苯环上的一溴代物只有一种,说明其苯环上可能只有2个相同侧链且位于对位,或有4个相同的侧链。
答案:(1) 9
(2) 、、、
提升2 答案:(1)苯的同系物
(2) 取代
形成性自评
1.C 2.B 3.D
4.答案:A
5.解析:A项,苯分子中所有原子都在同一平面上,但甲苯()分子中的—CH3是四面体结构,不可能实现所有原子都在同一平面上;B项,使溴水褪色不是发生了加成反应,而是因为Br2在有机溶剂中溶解度比在水中的溶解度大,苯和甲苯萃取了溴水中的Br2而使其褪色;C项,与浓硝酸发生硝化反应,产物虽不同,但本质上都是取代反应;D项,甲苯有侧链,能被酸性KMnO4溶液氧化为,而使KMnO4溶液褪色,苯则没有此性质。
答案:C
6.解析:苯与硝酸反应只引进一个—NO2,甲苯与硝酸反应,可以引进三个—NO2,说明侧链活化了苯环上的氢原子。
答案:A
7.解析:A项,苯环可发生加成反应,错误;B项,苯的同系物可使酸性KMnO4溶液褪色,不能使溴水因反应而褪色,错误;C项,由于苯的同系物C9H12的侧链为烷烃基(—C3H7),故不可能所有原子共平面,错误;D项,若C9H12的结构简式为,其一溴代物有6种,若结构简式为,其一溴代物有5种,正确。
答案:D
8.解析:(1)因为苯与液溴在铁催化下反应十分剧烈,可达到沸腾,所以不用加热;苯与液溴反应生成的HBr极易溶于水,因此,导管不能伸入液面以下,这样容易发生倒吸现象。(2)加入试剂的顺序应为:苯、液溴、铁粉。液溴的密度大于苯,先加苯,再加液溴是为了使苯与液溴混合均匀,待加入铁粉后,反应立即剧烈发生。因此,加入试剂的顺序不能颠倒。(3)与烧瓶连接导管的垂直向上部分兼有导气和冷凝回流的作用。因为加入铁粉后苯与液溴立即剧烈反应,可达沸腾而使部分苯和溴成为蒸气,反应物蒸气经垂直部分的导管冷凝后再流回烧瓶,减少了反应物的损失,又避免了生成物中混有过多的杂质。(4)反应过程中有HBr生成,HBr通过导管进入锥形瓶,除被吸收外,还会与锥形瓶中的水蒸气生成白色酸雾。(5)锥形瓶中的水吸收HBr后成为氢溴酸溶液,滴入AgNO3溶液后有浅黄色AgBr沉淀生成,离子方程式为:Ag++Br-===AgBr↓。(6)反应完毕后,将烧瓶中的液体倒入盛有冷水的烧杯中,烧杯底部有褐色的油状液体,这是因为溴苯的密度比水大,沉在水下,由于这样得到的溴苯中溶有少量的溴而使溴苯呈褐色。在粗产品溴苯中加入NaOH溶液,可以除去杂质溴,从而得到无色的溴苯,反应的离子方程式为:Br2+2OH-===Br-+BrO-+H2O。
答案:(1)①使用酒精灯加热 ②导管末端未离开液面1 cm~2 cm
(2)苯、液溴、Fe粉 (3)兼有导气和冷凝回流的作用
(4)生成白色酸雾 反应生成的HBr遇水形成了小液滴
(5)生成浅黄色AgBr沉淀 氢溴酸溶液 Ag++Br-===AgBr↓
(6)褐 溴苯的密度比水大,沉在水下 强碱溶液 溴 Br2+2OH-===Br-+BrO-+H2O
(7)
颜色
状态
气味
密度
溶解性
挥发性
毒性
____
____
有特殊
气味
比水
____
____于水,____于有机溶剂
沸点比较低,易挥发
____
实验原理
溴苯是无色液体,不溶于水,密度比水大。
实验方案
装置
步骤
a.安装好装置,检查气密性;
b.把苯和少量液态溴放在烧瓶中;
c.加入少量铁屑作催化剂;
d.用带导管的橡胶塞塞紧瓶口
实验现象
a.常温时,很快看到在导管口附近出现白雾(溴化氢遇水蒸气形成);
b.反应完毕后,向锥形瓶内的液体滴入AgNO3溶液,有淡黄色溴化银沉淀生成;
c.把烧瓶中的液体倒入盛有水的烧杯中,烧杯底部有褐色不溶于水的液体出现
实验原理
硝基苯是无色、有苦杏仁味的油状液体,密度比水大,不溶于水,有毒。
实验方案
装置
步骤
a.安装好装置,检查气密性;
b.配制混合酸:先将1.5 mL浓硝酸注入大试管中,再慢慢注入2 mL浓硫酸,并及时摇匀和冷却;
c.向冷却后的混合酸中逐滴加入1 mL苯,充分振荡,混合均匀;
d.将大试管放在50~60℃的水浴中加热
实验现象
将反应后的液体倒入一个盛有水的烧杯,可以观察到烧杯底部有黄色油状物质生成
与苯的化学性质相似之处
(1)燃烧:燃烧时火焰明亮并伴有浓烟,燃烧通式:
CnH2n-6+eq \f(3n-3,2)O2eq \(――→,\s\up7(点燃))nCO2+(n-3)H2O
(2)取代反应:能与卤素单质(X2)、浓硝酸等发生取代反应
(3)加成反应:与H2等发生加成反应,如
与苯的化学性质不同之处
(1)由于苯环上侧链的影响,使苯的同系物的苯环上的氢原子的活性增强,发生取代反应的位置不同。例如:
(2)甲苯能被酸性KMnO4溶液氧化而使其溶液褪色,而苯不能被酸性KMnO4溶液氧化。该性质可用于鉴别苯和苯的同系物。
注意:只有与苯环直接相连的碳原子上含有氢原子时,苯的同系物才能被酸性KMnO4溶液氧化,否则不能被氧化。
高中化学人教版 (2019)选择性必修3第三节 芳香烃学案: 这是一份高中化学人教版 (2019)选择性必修3第三节 芳香烃学案,共15页。
苏教版 (2019)选择性必修3第二单元 芳香烃导学案: 这是一份苏教版 (2019)选择性必修3第二单元 芳香烃导学案,共15页。学案主要包含了苯的结构和性质,苯的同系物 芳香烃的来源与应用等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修3第三节 芳香烃学案及答案: 这是一份高中化学人教版 (2019)选择性必修3第三节 芳香烃学案及答案,共12页。学案主要包含了苯的同系物,稠环芳香烃等内容,欢迎下载使用。













