


高中苏教版第一单元 化学反应速率说课ppt课件
展开学习目标1.了解化学反应的可逆性,了解可逆反应的概念。2.理解化学平衡状态的建立。3.掌握化学平衡状态的特征。
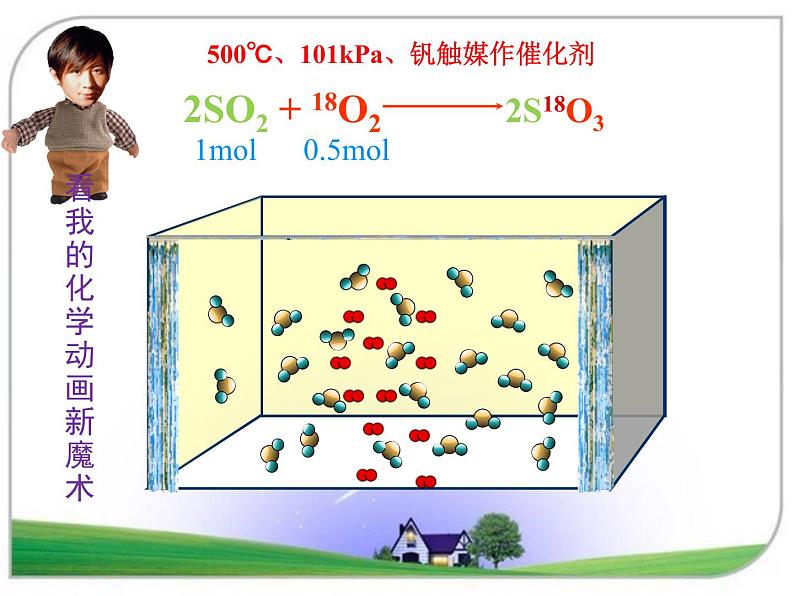
1ml 0.5ml
2SO2 + 18O2
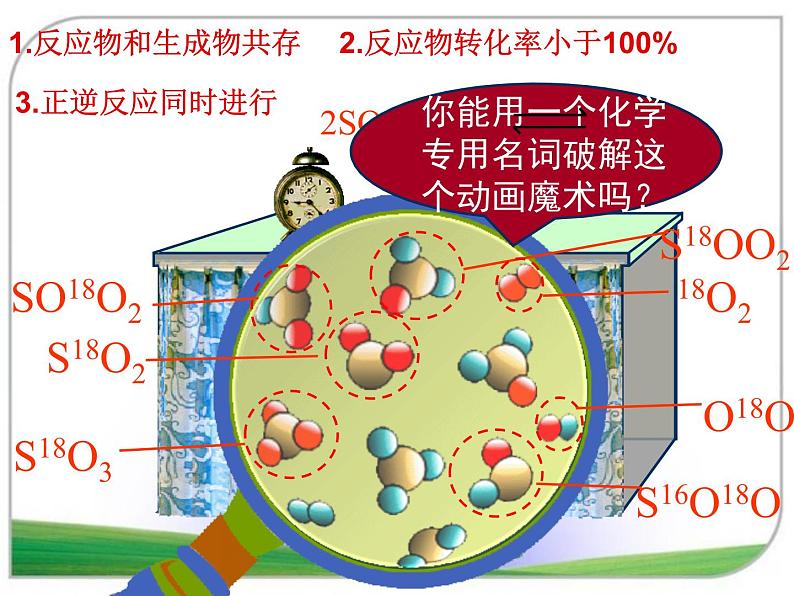
1.反应物和生成物共存
2.反应物转化率小于100%
在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫做可逆反应。
(1)同一条件下正、逆反应同时进行
(2)反应物和生成物共存(3)反应物转化率不能达到100%
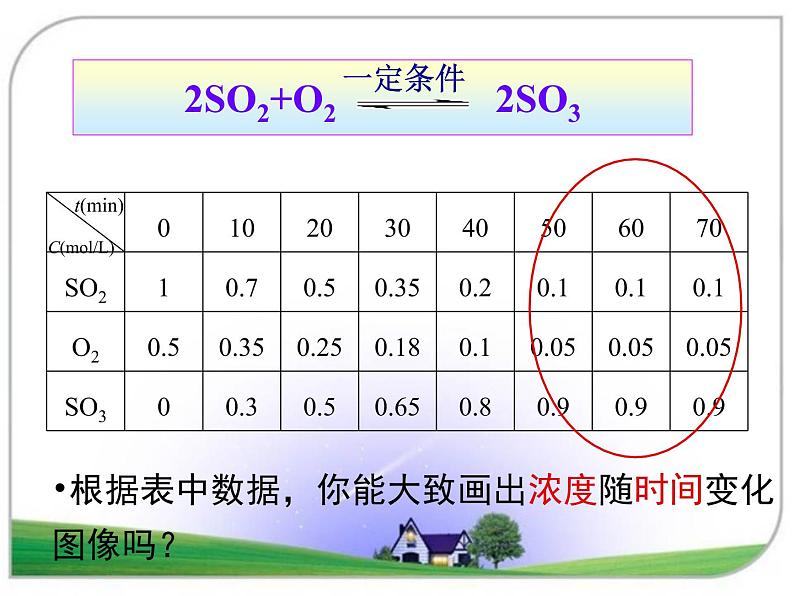
根据表中数据,你能大致画出浓度随时间变化图像吗?
2SO2+O2 2SO3
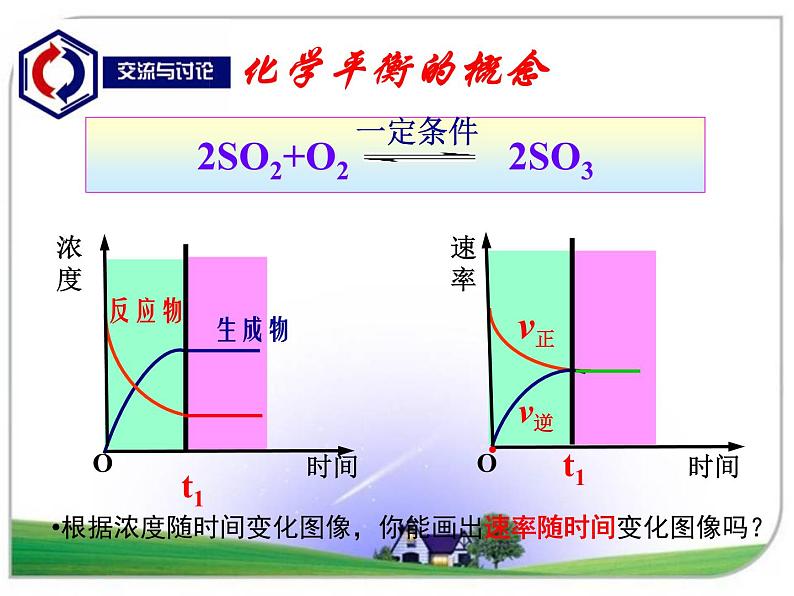
根据浓度随时间变化图像,你能画出速率随时间变化图像吗?
1.化学平衡状态的定义
化学平衡状态是指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度保持不变的状态。
2.化学平衡状态的特征
动态平衡: v(正) =v(逆) ≠0
v(正)= v(逆) ≠0
c(B) 或 n(B) 或 ω(B) 一定
条件改变→平衡可能会改变
化学平衡的研究对象是可逆反应
(2)恒浓标志 反应混合物中各组成成分的含量保 持不变(浓度标志)
1.在一定温度下,可逆反应N2(g)+3H2(g) 2NH3(g)达到平衡的标志是( D )A.NH3的生成速率与 N2分解速率相等 B.生成nml N2的同时生成3nml H2 C.N2、H2、NH3的浓度比为1:3:2 D.1个N≡N键断裂的同时,有6个N—H键断裂
v(正)= v(逆)
2.在一定温度下恒容容器中,当下列物理量不再发生变化, 表明反应A(固)+3B(气) 2C(气)+D(气)(其中只有B 气体有颜色)已达平衡状态的是 ( BCD )
A.混合气体的压强B.混合气体的密度 C.气体的平均分子量 D.气体的颜色 -
PV=nRT 气体分子不变的反应
反应进行气体颜色逐渐变浅
化学平衡状态的判断方法
1.等速:①同一种物质: v正 = v逆 ②不同种物质: v正 :v逆 =
2.恒浓:c(B) 或 n(B) 或 ω(B) 一定
①先找到一个“物理量” ②判断这个物理量是不是一个“变量” ③若这个物理量是一个“变量”,则当这个变量不再改变时,化学反应已经达到平衡
化学选择性必修1第二单元 化学反应的方向与限度教课课件ppt: 这是一份化学选择性必修1第二单元 化学反应的方向与限度教课课件ppt,共25页。PPT课件主要包含了学习目标,一化学平衡状态,三化学平衡常数等内容,欢迎下载使用。
高中化学苏教版 (2019)选择性必修1第一单元 化学反应速率说课ppt课件: 这是一份高中化学苏教版 (2019)选择性必修1第一单元 化学反应速率说课ppt课件,共26页。PPT课件主要包含了分点突破1,可逆反应及其特征,分点突破2,化学平衡状态等内容,欢迎下载使用。
苏教版 (2019)选择性必修1第一单元 化学反应速率课文课件ppt: 这是一份苏教版 (2019)选择性必修1第一单元 化学反应速率课文课件ppt,共60页。PPT课件主要包含了图说考点,基础知识,保持不变,化学平衡的特征,化学平衡,生成物,反应物,某反应物,转化率,答案A等内容,欢迎下载使用。













