

2021年度最新人教版九年级化学下册第九单元溶液期中考试卷【word可编辑】
展开最新人教版九年级化学下册第九单元溶液期中考试卷【word可编辑】
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
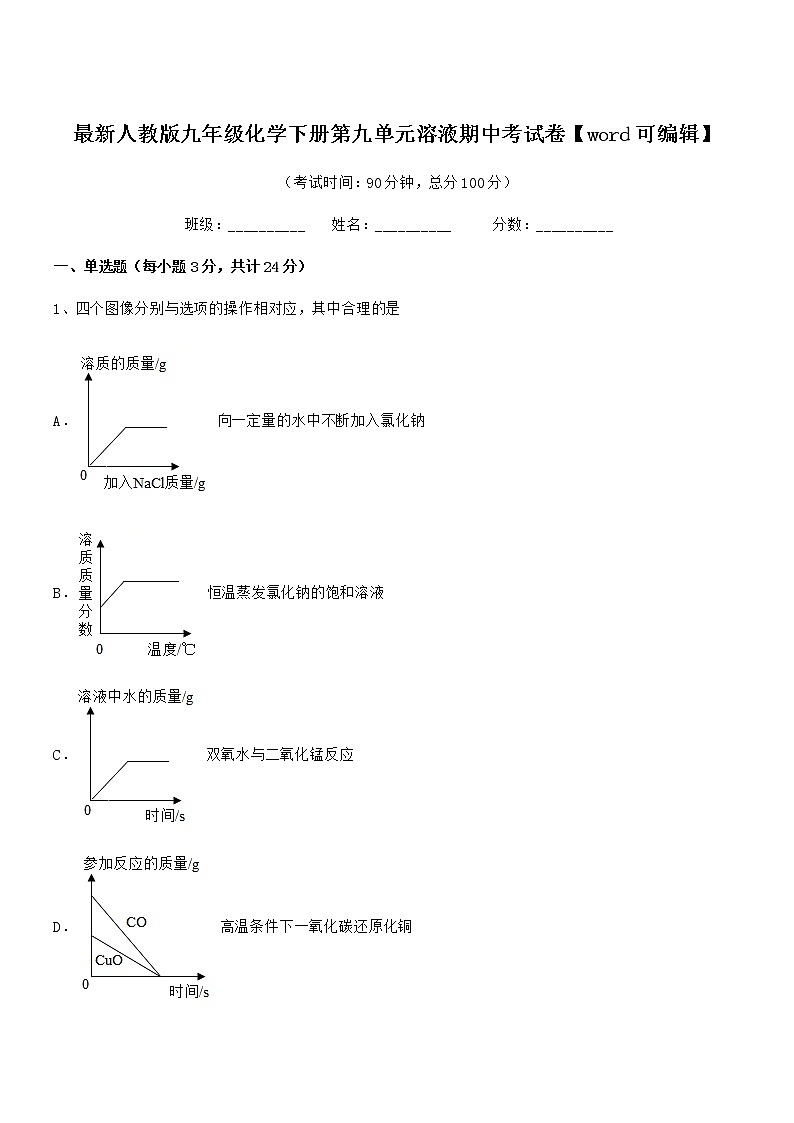
1、四个图像分别与选项的操作相对应,其中合理的是
A. 向一定量的水中不断加入氯化钠
B. 恒温蒸发氯化钠的饱和溶液
C. 双氧水与二氧化锰反应
D. 高温条件下一氧化碳还原化铜
2、能与水混合形成溶液的是
A.冰 B.蔗糖 C.植物油 D.粉笔灰
3、下列关于溶液的有关说法正确的是
A.利用洗洁精的溶解作用洗去碗上的油污 B.饱和溶液降温都能析出晶体
C.浓溶液都是饱和溶液 D.溶液都是均一、稳定的混合物
4、如图所示,向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是
A.氢氧化钠 B.碳酸钙
C.硝酸铵和氢氧化钙 D.氯化钠
5、下列关于溶液的说法正确的是
A.溶液中的溶剂一定是水 B.溶液中的溶质可以是多种
C.溶液一定是无色透明的液体 D.均一、稳定的液体一定是溶液
6、下列有关溶液的说法正确的是
A.配制溶液时,搅拌可以增大一定溶剂中固体溶质的溶解质量
B.具有均一性、稳定性的液体一定是溶液
C.饱和溶液浓度一定比不饱和溶液的浓度大
D.融雪剂的原理是利用某些物质水溶液的凝固点低于0℃
7、下列“一定”的说法正确的是
A.离子是带电粒子,所以带电的粒子一定是离子
B.置换反应会生成一种单质和一种化合物,则生成一种单质和一种化合物的反应一定是置换反应
C.分子由原子构成,则分子一定比原子大
D.饱和的硝酸钾溶液降温结晶后,一定仍为硝酸钾的饱和溶液
8、逻辑推理是化学学习常用的思维方法。下列说法正确的是
A.金属能和稀盐酸反应生成气体,所以能和稀盐酸反应生成气体的物质一定是金属
B.化合物是由不同元素组成的,则由不同种元素组成的纯净物一定是化合物
C.原子核是由质子和中子构成的,所以任何原子的原子核内都含有质子和中子
D.将不饱和溶液转化为饱和溶液,则该溶液溶质的质量分数一定增大
二、填空题(每小题4分,共计20分)
1、甲、乙、丙三种物质的溶解度曲线如图所示。据图回答:
(1)50℃时,乙物质的溶解度是______g。
(2)30℃时,三种物质的溶解度由大到小的顺序为______。
(3)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是______。
2、用下图装置完成“粗盐中难溶性杂质的去除”实验请回答下列问题:
(1)粗盐提纯实验中的操作顺序为______(填序号),以及称量精盐并计算产率。
(2)操作③中玻璃棒搅拌的作用是______。
(3)操作③中,当观察到蒸发皿内出现______时,停止加热,让余热蒸干剩余液体。
3、溶液的特征为___________、___________、混合物。一定温度下的不饱和石灰水,使它变为该温度下的饱和溶液的方法①___________,②___________。
4、化学与生产、生活联系紧密。
(1)北京冬奥会火炬“飞扬”使用液氢作为燃料,实现零碳排放,践行“绿色冬奥”理念。氢气燃烧的化学方程式为____。
(2)泰州为举办省运会新建了许多场馆,使用了大量铝制品材料。铝制品耐腐蚀的原因是____。
(3)家庭厨房中用洗洁精清洗油污,利用了洗洁精的____作用。
(4)农业上配制100kg,15%的食盐溶液用来选种,需要食盐____kg。
(5)生铁和钢性能不同主要是由于____不同。
(6)自来水生产过程中一般用氯气(Cl2)杀菌消毒,标出氯气中氯元素的化合价____。
(7)氧气的工业制法为分离液态空气法,则氮气的工业制法为____。
5、水是生活中最常见的物质之一,也是实验室常用的试剂。
(1)某同学进行下图1实验。
①由以上实验可知,溶质状态可以是_______。
②实验结束后,用洗涤剂洗净B试管,原理是_______。
(2)某工厂用电解水的方法制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味(每个具有鱼腥气味的气体分子由三个原子构成)。从元素守恒角度分析,该鱼腥气味的气体是_______(填化学式)。
(3)电解水时,在水中加入少量硫酸钠可增强导电性。某兴趣小组把4.0g硫酸钠固体加入86.8g水中,充分溶解后进行电解,一段时间后停止通电,在试管A中收集到1.2g气体(装置如图2)。则B管中收集到的气体是_______(填化学式),其质量是______g。
(4)生活中的水
Ⅰ.二氧化氯(ClO2)是一种在水处理等方面应用的高效安全消毒剂,标出二氧化氯中氯元素的化合价_______。写出质子数与水相同的一种分子的化学式_______(只填一个分子)。
Ⅱ.将浑浊的河水净化的实验过程如下图所示:
操作①必须使用的玻璃仪器有:玻璃棒、_______和烧杯。
若液体b为硬水,则操作③可以是_______。
A.过滤 B.蒸馏 C.加明矾、搅拌、静置
Ⅲ.若用质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该质量分数为10%稀硫酸490g时,需要浓硫酸的体积为_____mL(精确到0.1);用量筒量取浓硫酸时俯视读数,所配溶液溶质质量分数_____10%(填“大于”、“小于”或“等于”)。
(5)如图为甲、乙两种固体物质的溶解度曲线,请据图回答下列问题。
①t2℃时,甲、乙两种物质饱和溶液中的溶质质量分数的大小关系为:甲______乙(填“>”、“<”或“=”)。
②要从乙的饱和溶液中获得较多的晶体,宜采用的结晶方法是______结晶。
③t1℃,取等质量的甲、乙两种固体分别配成饱和溶液,需水质量较少的是_______(填“甲”或“乙”)。
三、计算题(每小题4分,共计36分)
1、 “黄铜”即铜锌合金,古代称为“俞石”。由于外观酷似黄金,常被不法商販冒充黄金出售。某实验小组为了辨别真伪,用该合金与稀盐酸反应,将三次实验所得相关的数据记录如下:
物质质量 | 第一次 | 第二次 | 第三次 |
所取合金的质量/g | 25 | 25 | 50 |
所用稀盐酸的质量/g | 120 | 160 | 100 |
充分反应后,剩余物总质量/g | 144.6 | 184.6 | 149.6 |
(1)根据上表数据分析,合金中的锌与稀盐酸恰好完全反应时,所取合金与稀盐酸的质量比为___________。
(2)计算铜锌合金中的铜的质量分数为___________。
(3)计算第3次实验完全反应后所得溶液中溶质的质量分数(计算结果精确到0.1%)。
2、将含杂质的铁样品7g放入盛有121.6g稀盐酸溶液的烧杯中,刚好完全反应(杂质既不溶于水,也不与酸反应),称得反应后烧杯内物质的总质量为128.4g。(已知:铁与稀盐酸反应生成氯化亚铁和氢气)求
(1)生成氢气的质量_____。
(2)铁样品中铁的质量分数_____。
3、69中学化学兴趣小组的同学,将用石灰石与稀盐酸制取8.8gCO2后的固液混合物206.3g,倒入废液缸中进行如下探究和处理:
已知在(1)中盐酸反应一半,(2)中盐酸恰好完全反应。
(1)实验过程中发生反应的化学方程式______;
(2)与氧化钙反应的物质质量(X)的比例式______;
(3)所用石灰石的纯度______;
(4)最后所得溶液中溶质的质量分数______;
(5)用36.5%的盐酸配置实验所需的稀盐酸400g,加水的质量为______。
4、请回答下列问题。
(1)积极应对气候变化,展现大国担当,中国向世界宣布了 2030 年前实现“碳达峰”、2060 年前实现“碳中和”的国家目标。“碳达峰”是指国家整体二氧化碳气体排放量达到峰值。有研究表明,当前全球每年人为向大气排放二氧化碳 420 亿吨,在这些二氧化碳中含碳元素的质量为多少亿吨?(写出计算过程,计算结果精确至 0.1 亿吨)
(2)20℃时,向 3 个盛有 100 克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据,回答:
实验编号 | A | B | C |
加入氯化钠的质量(克) | 20 | 36 | 50 |
溶液质量(克) | 120 | 136 | 136 |
①实验所得 3 杯溶液中,属于不饱和溶液的是_______(填实验编号)。
②求溶液 C 的溶质质量分数_______。(写出计算过程,计算结果精确至 0.1%)。
5、在生活中我经常食用食醋,根据所学知识回答下列问题。
(1)食醋中溶质醋酸的化学式___________。
(2)醋酸这种物质由___________构成。
(3)醋酸中碳元素的质量分数是___________。
(4)200 克溶质质量分数为 3%的醋酸溶液中碳元素的质量为___________。
6、如图,小明同学将200g质量分数为20%的硝酸钾溶液做如图操作,请通过计算回答:
(1)往甲烧杯溶液加入5g硝酸钾固体,完全溶解后,溶液的溶质质量分数为多少?(结果保留到0.1%)
(2)若将乙烧杯溶液稀释为溶质质量分数为5%的硝酸钾溶液,则需加水多少g?
7、为测定某CuSO4溶液的溶质质量分数,化学小组的同学取CuSO4溶液100g,向其中滴加一定浓度的NaOH溶液,至不再产生沉淀为止,共用去NaOH溶液80g,过滤,得到滤液175.1g。请计算:
(1)该反应生成沉淀______g;
(2)该CuSO4溶液中溶质的质量分数______。(温馨提示:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4)
8、2011年3月11日,日本发生8.6级地震,震中位于日本本州岛仙台港东,震源深度约24千米,东京有强烈震感,地震引发海啸。为了防止灾后疫情的发生,在震区需要喷洒大量的消毒液。
(1)800 kg质量分数为0.5%的过氧乙酸消毒液中,过氧乙酸的质量为________ kg。
(2)要配制800 kg质量分数为0.5%的过氧乙酸消毒液,需质量分数为16%的过氧乙酸溶液的质量是多少?
9、为了测定石灰石中碳酸钙的质量分数(杂质不含钙元素,不溶于水,也不与其他物质发生反应),进行了如下实验。请回答下列问题。
(1)上述实验过程中发生反应的化学方程式为_________。
(2)此石灰石中碳酸钙的质量分数为__________。
(3)若向反应后的滤液中加入 10.8g 水,则所得溶液中溶质的质量分数为__________。
四、实验探究(每小题5分,共计20分)
1、一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液。
(1)配制 200mL 质量分数为 10%的氢氧化钠溶液(密度为 1.1g/cm3),需要氢氧化钠的质量是__________g,水的质量是_________g;需要用到的仪器有托盘天平、烧杯、药匙、_________、量筒、胶头滴管、试剂瓶。
(2)某学习小组的同学对物质的溶解过程进行探究。
(查阅资料)电导率传感器用于测量溶液的导电性强弱;一定条件下,电导率的大小能反映离子浓度的大小。
(实验探究 1)物质溶于水形成溶液的过程中电导率的测定。
第一步:读取室温为 26℃,取 100mL 蒸馏水,加入烧杯中,放入磁力搅拌器磁珠;
第二步:校准传感器,组装仪器,设定搅拌档位;
第三步:用电导率传感器采集数据,迅速将一定质量的氯化钠加入烧杯中。实验数据如图 1所示。
(实验分析 1)请说明 a-b 段曲线呈这种形态的原因:____________。
(实验探究 2)如图 2 所示,将一定质量的某种固体加入盛有水的烧杯中,拿起烧杯,木板掉落,加入的固体可能是___________(填字母)。
A氯化钠 B氢氧化钠 C硝酸铵 D氧化钙
(实验分析 2)上述四种固体中,有一种固体加入水中产生的热量变化是由化学反应引起的,该反应的化学方程式为____________。
(实验探究 3)物质溶于水形成溶液的过程中温度的测定。
第一步:读取室温为 26℃,取 30mL 蒸馏水,加入烧杯中,放入磁力搅拌器磁珠;
第二步:校准传感器,组装仪器,设定搅拌档位;
第三步:用温度传感器采集数据,迅速将 7.5g 氯化钠加入烧杯中,根据实验数据绘制出氯化钠溶解过程中温度随时间变化的曲线简图如图 3 所示。
(实验分析 3)将氯化钠更换为等质量的氢氧化钠或硝酸铵,重新进行上述实验。请在图 3中分别绘制出氢氧化钠和硝酸铵溶解过程中温度随时间变化的曲线简图(趋势合理即可),并在曲线旁边写出对应物质的化学式____________。
2、小红同学通过对化学上册内容的学习,越来越觉得化学有意思。下面是她最近这段时间的两个学习经历,请同学们阅读之后完成下面的问题。
Ⅰ、小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究。
(查阅资料)市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”一元素符号Pt。小红结合化学课上学习的金属活动性顺序,展开了下列实验活动。
(1)鉴别两种白金,她的方法可能是_____。
(2)探究Zn、Ni(镍)、铜的活动性顺序。
(作出假设)对三种金属的活动性顺序提出可能的假设:①Zn>Ni>Cu;②Zn>Cu>Ni你觉得还有其他的可能性吗?请把它们写出来(一种即可)
假设:③_____
(查阅资料)小红同学查阅了部分含镍化合物的溶解性如下表,且得知镍能与酸反应。
| OH- | CI- | ||
Ni2+ | 不 | 溶 | 溶 | 溶 |
(设计实验)同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象。
(记录现象)请帮助小红把实验现象填写完整
金属 | Ni | Zn | Cu |
与盐酸反应的现象 | 气体产生缓慢金属逐渐溶解 | 气体产生激烈金属迅速溶解 | _____ |
(得出结论)原假设中正确的是_____(填序号),写出镍与盐酸反应的化学方程式_____。
(结论应用)
①根据探究结果,请你预测镍与硫酸铜溶液_____(填“能”或“不能”)反应,理由是_____。
②除小红的实验设计外,你能否象小红一样,设计另一组实验,也这样一次验证上述假设的正确与否,你的设计所用的一组物质的化学式是_____(只写出一组即可)。
Ⅱ、小红同学按照下面的操作过程示意图配制50g质量分数为5%的氯化钠溶液:
试回答:
(1)配制该氯化钠溶液的正确的操作顺序是(____)
A ④⑤①②③ B ①②③④⑤ C ③④①②⑤ D ②①④③⑤
(2)⑤操作中应称量氯化钠的质量是_____g。放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是_____。
(3)②操作应选用_____mL的量筒(从10mL、100mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的_____处保持水平。若俯视读数,则所配氯化钠溶液的溶质质量分数会_____(填“偏大”、“偏小”或“不变”)。
(4)③操作的作用是_____。
3、为探究铁的化学性质,某学习小组做了如图甲所示实验。他们观察到试管a中铁粉全部溶解,产生大量气泡,溶液呈① ____ 色,反应的化学方程式为② ____ ;试管b中有③ ______ 色固体生成,该反应的化学方程式为④ _____ 。为进一步确定试管a所得溶液中的溶质成分和试管b所得固体的组成,他们进行了以下实验探究。
(提出猜想)(1)试管a中的溶质成分:猜想一:FeSO4;猜想二:⑤ ______ 。
(2)试管b中固体的组成:猜想三:Cu; 猜想四:Fe和Cu。
(实验探究)甲图所示实验结束后,将试管a、试管b内的物质全部倒入同一烧杯中(如乙图所示),他们惊奇地发现烧杯内溶液中产生大量气泡。
(总结交流)经过讨论,大家一致认为上述猜想中正确的是⑥ _______ 。
(拓展探究)某混合溶液由硫酸铜和硫酸溶液组成。上述小组同学取192.4g该混合溶液于烧杯中,然后往其中加入33.6g铁粉,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
(3)原混合溶液中H2SO4的质量 ______ 。(计算结果保留一位小数)
(4)原混合溶液中CuSO4和H2SO4的质量比 ______ 。
(5)完全反应后所得溶液中溶质的质量分数 _______ 。(计算结果保留一位小数)
4、(1)以下是某研究小组探究影响化学反应速率的一些因素的相关数据(“常温”指20℃;“浓度”指溶质的质量分数)
I.实验①和②的实验目的是_____________________________________________________。
II.实验④中,过氧化氢溶液浓度/%的数值是___________。
Ⅲ.由上述实验可知,实验室用过氧化氢制取氧气最优组合的序号是________________。
IV.配置450克5%的过氧化氢溶液,往一定量30%的过氧化氢溶液中加入_______克水。
(2)下表是氯化钠和碳酸钠在不同温度时的溶解度
①用50mL蒸馏水(密度约为1g/mL)配制40℃的氯化钠饱和溶液。计算需称取氯化钠的质量是_______g。
②碳酸钠溶液中混有少量氯化钠杂质时,采用__________的方法提纯碳酸钠。
2021年度最新人教版九年级化学下册第九单元溶液期末考试卷【可编辑】: 这是一份2021年度最新人教版九年级化学下册第九单元溶液期末考试卷【可编辑】,共15页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2021年度最新人教版九年级化学下册第九单元溶液期末模拟试卷(word可编辑): 这是一份2021年度最新人教版九年级化学下册第九单元溶液期末模拟试卷(word可编辑),共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2021年度最新人教版九年级化学下册第九单元溶液期末考试卷【可打印】: 这是一份2021年度最新人教版九年级化学下册第九单元溶液期末考试卷【可打印】,共11页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。












