



还剩18页未读,
继续阅读
鲁教版九年级下册第一节 酸及其性质评课课件ppt
展开这是一份鲁教版九年级下册第一节 酸及其性质评课课件ppt,共26页。PPT课件主要包含了知识点一酸,知识点二浓盐酸,图7-1-1,知识点三浓硫酸,图7-1-2,图7-1-3,方法点拨,图7-1-4,浓盐酸,常见的酸等内容,欢迎下载使用。
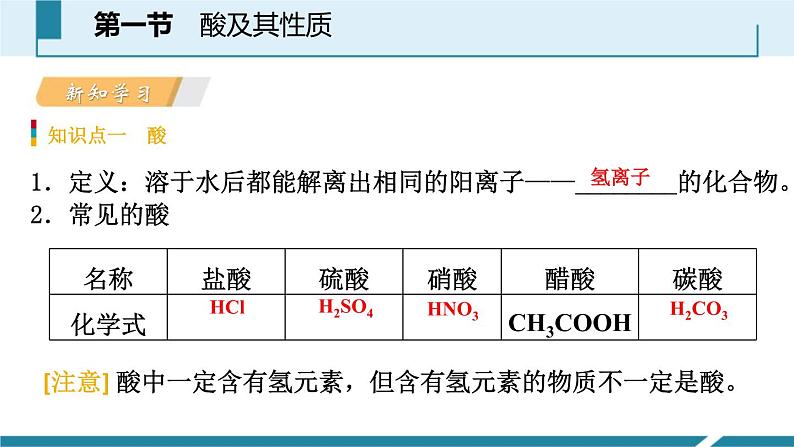
1.定义:溶于水后都能解离出相同的阳离子——________的化合物。2.常见的酸
[注意] 酸中一定含有氢元素,但含有氢元素的物质不一定是酸。
1.物理性质浓盐酸是________色液体,有________气味,易挥发,在空气中会形成________,这是因为浓盐酸挥发出来的________气体跟空气里的________接触,形成______________的缘故。工业用浓盐酸因含有少量杂质而略带________色。
2.闻气味的方法闻气味时不可凑近瓶口,要小心地打开瓶塞,用手在________处轻轻扇动,仅使极少量的气体飘进鼻孔(如图7-1-1所示)。
[注意] “雾”是小液滴,“烟”是固体小颗粒,浓盐酸挥发时形成的是白雾,不是白烟。
1.物理性质纯净的浓硫酸是没有颜色、______、油状的液体,不容易________。浓硫酸具有________和强烈的________,在使用时应十分小心。如果不慎将浓硫酸沾到皮肤上,应立即用大量的________冲洗,然后涂上3%~5%的____________溶液,以防灼伤皮肤。
[注意] ①浓硫酸具有吸水性,常用作干燥剂。②易挥发的浓盐酸和具有吸水性的浓硫酸,都要密封保存。
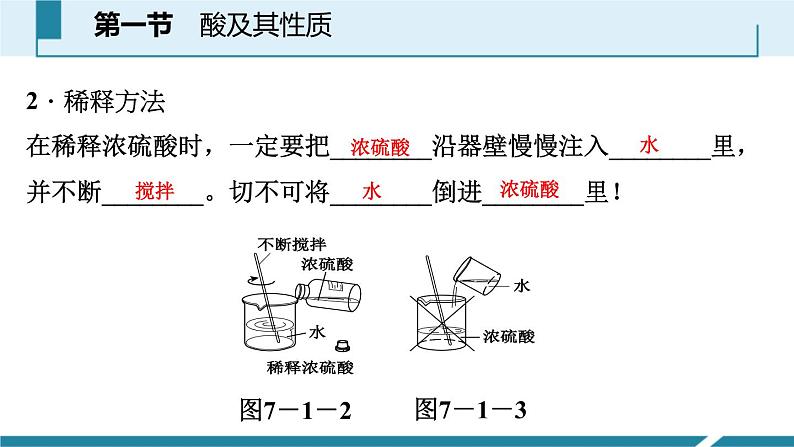
2.稀释方法在稀释浓硫酸时,一定要把________沿器壁慢慢注入________里,并不断________。切不可将________倒进________里!
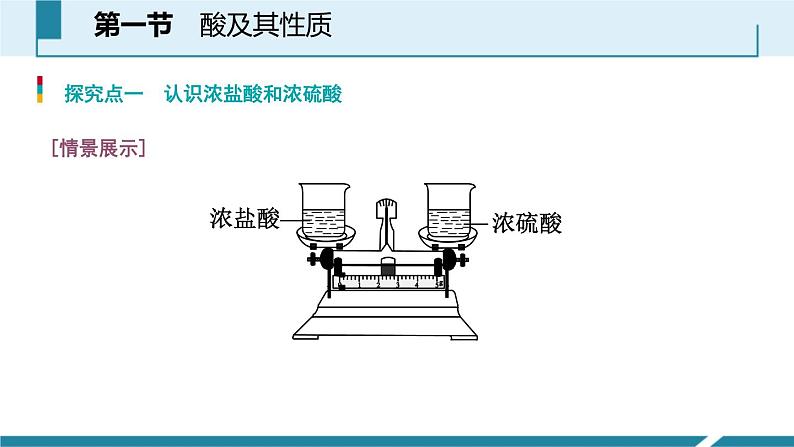
探究点一 认识浓盐酸和浓硫酸
如图所示,在天平的两端分别放入等质量的盛有浓盐酸和浓硫酸的敞口烧杯,,观察会有什么现象,一段时间后,天平是否会失去平衡?
浓盐酸易挥发,会挥发出氯化氢气体,遇到空气中的水蒸气结合形成盐酸小液滴,所以我们看到浓盐酸的烧杯口有白雾出现,敞口放置质量会减小,同时溶质质量分数也会减小;而浓硫酸无挥发性,但是有吸水性,敞口放置质量会增加,但溶质质量分数也会减小。二者保存时都必须密封保存。
核心一 认识浓盐酸和浓硫酸
例1 下列说法正确的是( )A.凑到试剂瓶瓶口去闻浓盐酸和浓硫酸的气味B.打开盛浓盐酸的试剂瓶,瓶口会产生白烟C.浓硫酸露置于空气中,质量和溶质质量分数都会变大D.露置于空气中的浓盐酸和浓硫酸,其溶质质量分数都会发生变化
[解析] 闻药品的气味时,不能凑近瓶口,应用手在瓶口处轻轻扇动,仅使极少量的气体飘进鼻孔;打开盛浓盐酸的试剂瓶,瓶口会产生白雾,而不是白烟;浓硫酸具有吸水性,露置于空气中,质量会变大,溶质质量分数会变小;露置于空气中的浓盐酸能够挥发出氯化氢气体,质量和溶质质量分数都会变小。
探究点二 浓硫酸的稀释
哪种稀释浓硫酸的方法才是正确的?不正确的操作会产生什么样的后果?
浓硫酸的稀释从理论上来说,是指将浓硫酸加水变成稀硫酸的过程,但由于水的密度较小,会浮在浓硫酸上面,而浓硫酸溶于水时会放出大量的热,使水立刻沸腾,造成硫酸液滴向四周飞溅,这是非常危险的。因此,稀释浓硫酸时,一定要将浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌;切不可将水倒进浓硫酸里。可以简记为:“酸入水,沿器壁,慢慢倒,不断搅”。
又由于浓硫酸具有很强的腐蚀性,所以使用时一定要注意安全,如果不慎沾到皮肤上,应立即用布拭去,再用大量水冲洗。
例2 实验室中常需要使用硫酸。(1)用小木棍蘸取少量浓硫酸,放置一会儿后,可观察到___________________________________________________。(2)用温度计的液泡蘸取少量浓硫酸,放置在空气中一会儿,可观察到温度计显示温度升高,其原因是___________________________________________________。
小木棍沾有浓硫酸的部位变黑
浓硫酸具有吸水性,吸收空气中的水蒸气,浓硫酸溶于水放热
[解析] (1)浓硫酸具有腐蚀性,能使木材等物质碳化,所以沾有浓硫酸的小木棍变黑;(2)浓硫酸具有吸水性,可吸收空气中的水蒸气,且浓硫酸溶于水放热,所以温度计显示温度升高;
(3)如果不慎将浓硫酸沾到皮肤上,应立即用______________,然后涂上3%~5%的碳酸氢钠溶液。(4)实验室用98%的浓硫酸(密度1.84 g/cm3)配制100 g溶质质量分数为20%的稀硫酸。浓硫酸稀释过程如图7-1-4所示,b中盛放的物质是________,a的作用是________________。
[解析] (3)浓硫酸具有强腐蚀性,使用时应特别小心,一旦将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液;(4)稀释浓硫酸时一定要将浓硫酸倒入水中,并不断搅拌,使热量迅速散失。
【方法点拨】稀释浓硫酸时一定不能将水倒入浓硫酸中,因为水的密度比浓硫酸小,会浮在浓硫酸上。若将水倒进浓硫酸中,稀释时放出大量的热会使表面的水迅速沸腾,混和着浓硫酸向外飞溅液滴,十分危险。所以稀释浓硫酸必须要“注酸入水”,并不断搅拌,使热量迅速散失。
无色透明液体,易挥发,有刺激性气味
无色粘稠的油状液体,有吸水性和强烈的腐蚀性
1.化学上常对物质进行分类和研究,以下物质中属于酸的是( )A.HNO3 B.MgOC.O2 D.NaCl
知识点2 认识浓盐酸和浓硫酸
2.实验室常用浓硫酸作某些气体的干燥剂,这是因为( )A.浓硫酸溶于水能放出热量 B.浓硫酸具有挥发性C.浓硫酸具有腐蚀性 D.浓硫酸具有吸水性3.盐酸是________气体的水溶液。纯净的盐酸________颜色,有________气味,工业盐酸常因含有铁离子而呈黄色。浓盐酸具有________性,在空气中会形成“白雾”,这是因为从浓盐酸里挥发出来的____________跟空气中的________接触,形成____________的缘故。
相关课件
初中化学鲁教版九年级下册第一节 酸及其性质精品ppt课件:
这是一份初中化学鲁教版九年级下册第一节 酸及其性质精品ppt课件
初中化学鲁教版九年级下册第一节 酸及其性质精品ppt课件:
这是一份初中化学鲁教版九年级下册第一节 酸及其性质精品ppt课件,文件包含第七单元第一节第1课时pptx、71酸及其性质第一课时教案docx、71酸及其性质第一课时练习docx等3份课件配套教学资源,其中PPT共18页, 欢迎下载使用。
初中化学鲁教版九年级下册第一节 酸及其性质教学演示课件ppt:
这是一份初中化学鲁教版九年级下册第一节 酸及其性质教学演示课件ppt,共22页。PPT课件主要包含了产生气泡,产生白色沉淀,无明显变化,FeCl3,Fe2SO43,MgCl2,MgSO4,FeCl2,FeSO4,NaCl等内容,欢迎下载使用。









