




化学九年级下册课题2 酸和碱的中和反应集体备课ppt课件
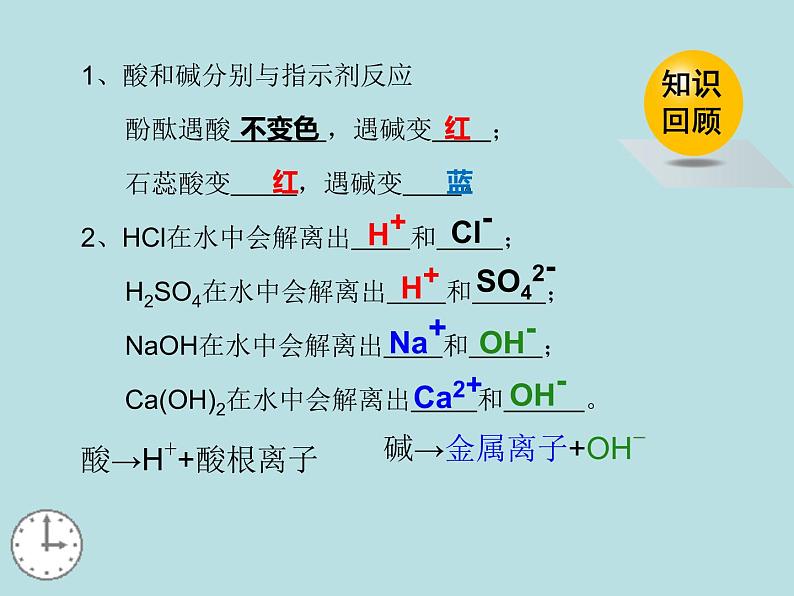
展开1、酸和碱分别与指示剂反应 酚酞遇酸 ,遇碱变 ; 石蕊酸变 ,遇碱变 。2、HCl在水中会解离出 和 ; H2SO4在水中会解离出 和 ; NaOH在水中会解离出 和 ; Ca(OH)2在水中会解离出 和 。
酸和碱混合在一起,会发生化学反应吗?
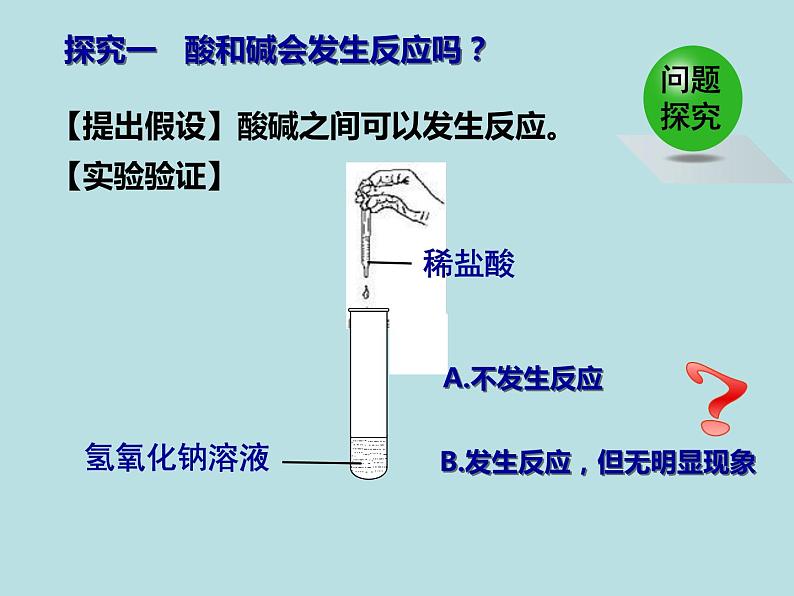
【提出假设】酸碱之间可以发生反应。
B.发生反应,但无明显现象
探究一 酸和碱会发生反应吗?
【实验验证】 重新设计实验方案...
活动与探究中和反应.flv:
溶液由红色逐渐变为无色
1.为什么要加入酚酞指示剂? 借以判断反应有无发生 2. 什么时候酸和碱恰好完全反应? 溶液刚好由红色变为无 色 3.能否换成紫色的石蕊作指示剂?现象? 可以, 溶液由蓝色变成紫色,继续加酸又变成红色
【实验验证】 根据实验方案进行实验...
提示:滴加液体时速度要慢。
【实验验证】 反应后生成物是什么...
由金属离子和酸根离子构成的化合物。
2HCl + Ca(OH)2=CaCl2 + 2H2O H2SO4 + 2NaOH=Na2SO4 + 2H2O
1.定义:酸与碱作用生成盐和水的反应。
【及时练习】以下的反应均生成盐和水,它们是不是中和反应呢? CO2+2NaOH=Na2CO3 + H2O Fe2O3+6HCl = 2FeCl3 +3H2O
探究二 中和反应的本质
水分子在溶液中不易电离。反应后,溶液中减少的离子是 。
酸中的H+和碱中的OH-反应生成水。
探究二 中和反应的实质
二、中和反应在实际中的应用
阅读P61页的相关内容。
1.为什么向酸性土壤中加入熟石灰,而不可以加入氢 氧化钠粉末? 2.写出用熟石灰处理含硫酸的工厂污水时所发生反应 的化学方程式: 3.用于治疗胃酸过多的药物中常含有Al(OH)3和 Mg(OH)2 等物质,请写出胃酸(HCl)与这两种成分反应的化学 方程式:
答:因为氢氧化钠有强烈的腐蚀性。
H2SO4 + Ca(OH)2=CaSO4 + 2H2O
3HCl + Al(OH)3= AlCl3 + 3H2O
2HCl + Mg(OH)2= MgCl2 + 2H2O
思考:可不可以用NaOH来中和胃酸、蚁酸?为什么?
可涂抹一些含有碱性物质(如氨水NH3·H2O和肥皂水)的药水。
答:不可以。因为NaOH的碱性太强,具有强的腐蚀性。
课题2 酸和碱的中和反应
2.盐:由金属离子和酸根离子 构成的化合物。
1、改变土壤的酸碱性(常用熟石灰)
3、医药(中和胃酸3HCl + Al(OH)3= AlCl3 + 3H2O )
制成含碱性物质的药水,防蚊虫叮咬
考点一:酸碱中和反应的考查。1.下列有关中和反应的说法,不正确的是 ( )A.中和反应一定是酸和碱的反应 B.凡是生成盐和水的化学反应都是中和反应C.中和反应的实质是H+和OH-结合生成水 D.中和反应一定生成盐和水
解析:有盐和水生成的反应不一定是中和反应。例如:金属氧化物+酸——盐+水 非金属氧化物+碱——盐+水
考点二:考查中和反应在实际中的应用2.某同学不小心被黄蜂蛰了(黄蜂毒液呈碱性),为了减 轻疼痛,可以涂抹下列哪种物质( ) A.浓硫酸 B.食醋 C.食盐水 D.苏打水或肥皂水(呈碱性)3.酸与碱作用生成盐和水的反应,叫作中和反应,它在工 农业生产和日常生活中有广泛的用途,下列应用一定与 中和反应原理无关的是( ) A.服用含Al(OH)3的药物治疗胃酸过量 B.使用熟石灰改良酸性土壤 C.用熟石灰和硫酸铜配制波尔多液 D.用NaOH溶液洗涤石油产品中的残余硫酸
初中化学人教版九年级下册第十单元 酸和碱课题2 酸和碱的中和反应评课课件ppt: 这是一份初中化学人教版九年级下册第十单元 酸和碱课题2 酸和碱的中和反应评课课件ppt,共60页。PPT课件主要包含了关注生活,知识点一中和反应,H2O,处理突发事件,课堂练习,反思提升,综合练习等内容,欢迎下载使用。
人教版九年级下册课题2 酸和碱的中和反应评课ppt课件: 这是一份人教版九年级下册课题2 酸和碱的中和反应评课ppt课件,共36页。PPT课件主要包含了教学目标,教学策略,教学环节,新问题,收获感悟,思维拓展,调查研究,板书设计,教学反思等内容,欢迎下载使用。
人教版第十单元 酸和碱课题2 酸和碱的中和反应课前预习课件ppt: 这是一份人教版第十单元 酸和碱课题2 酸和碱的中和反应课前预习课件ppt,共18页。PPT课件主要包含了活动与探究,你明白了没有,试试身手吧,复分解反应,改变土壤的酸碱性,用熟石灰中和,处理工厂的废水,用于医药,胃乐胶囊的主要成分,氢氧化铝等内容,欢迎下载使用。













