
2022届高三化学一轮高考复习常考题型:14流程情景中方程式的书写专题
展开www.ks5u.com
2022届高三化学一轮高考复习常考题型14流程情景中方程式的书写专题
一、单选题(共15题)
1.硼氢化钠(NaBH4)是常用的还原剂之一,与水反应可放出氢气,可用如下所示转化合成。已知硼氢化钠中B为+3价。下列有关说法错误的是
A.该合成反应在隔绝空气的条件下进行
B.该合成反应中Na和H2作还原剂
C.NaBH4与水反应时,每生成1molH2转移1mole-
D.该反应的化学方程式为NaBO2+2SiO2+4Na+2H22Na2SiO3+NaBH4
2.利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的,制取石膏()的过程如下:
下列说法正确的是
A.属于盐类和纯净物
B.过程II中反应的离子方程式为
C.过程I后溶液pH增大
D.将10L上清液中的(浓度为)转化为,理论上共需要
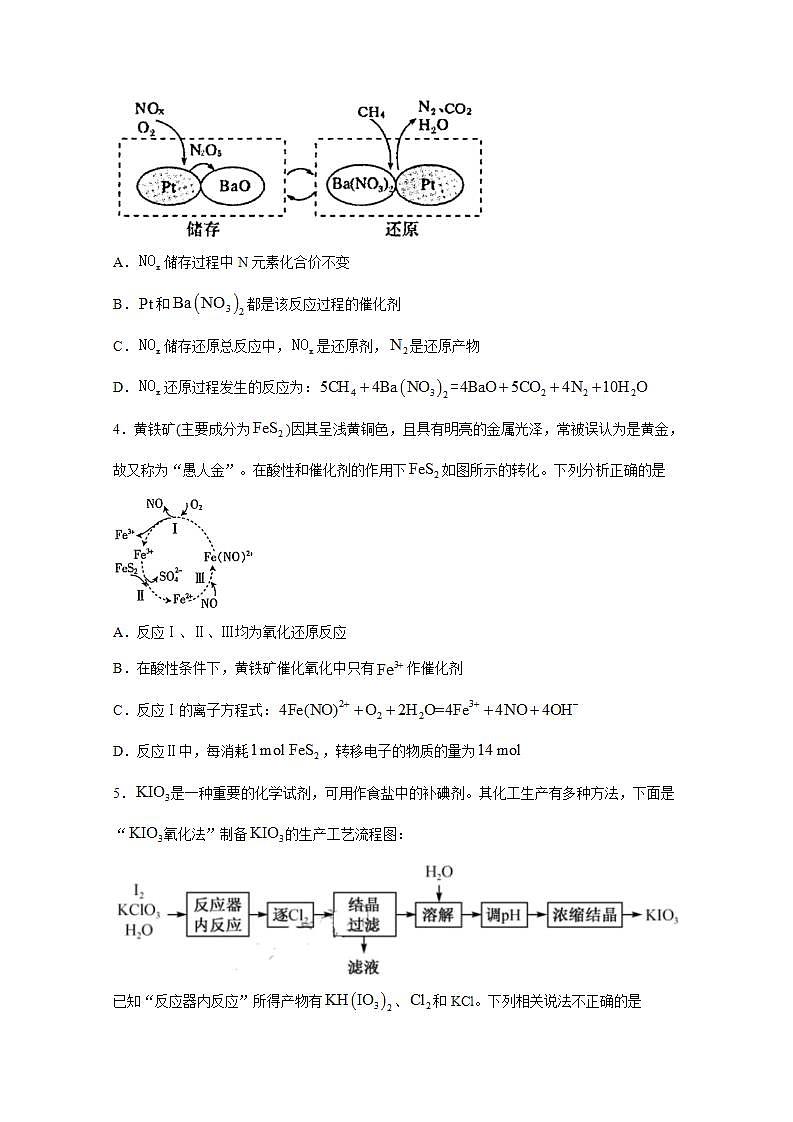
3.(储存还原)技术可有效降低柴油发动机中的排放,的储存和还原在不同时段交替进行,工作原理如图所示。下列说法正确的是
A.储存过程中N元素化合价不变
B.和都是该反应过程的催化剂
C.储存还原总反应中,是还原剂,是还原产物
D.还原过程发生的反应为:
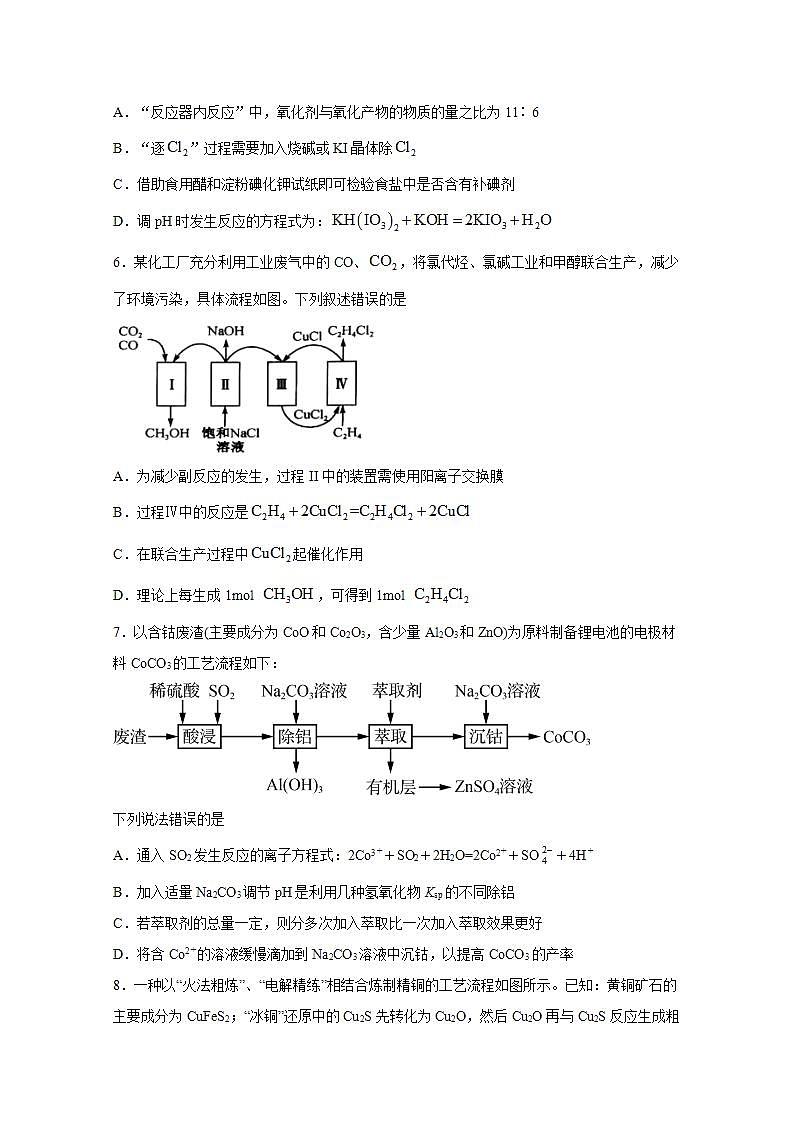
4.黄铁矿(主要成分为)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性和催化剂的作用下如图所示的转化。下列分析正确的是
A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.在酸性条件下,黄铁矿催化氧化中只有作催化剂
C.反应Ⅰ的离子方程式:
D.反应Ⅱ中,每消耗,转移电子的物质的量为
5.是一种重要的化学试剂,可用作食盐中的补碘剂。其化工生产有多种方法,下面是“氧化法”制备的生产工艺流程图:
已知“反应器内反应”所得产物有、和KCl。下列相关说法不正确的是
A.“反应器内反应”中,氧化剂与氧化产物的物质的量之比为11∶6
B.“逐”过程需要加入烧碱或KI晶体除
C.借助食用醋和淀粉碘化钾试纸即可检验食盐中是否含有补碘剂
D.调pH时发生反应的方程式为:
6.某化工厂充分利用工业废气中的CO、,将氯代烃、氯碱工业和甲醇联合生产,减少了环境污染,具体流程如图。下列叙述错误的是
A.为减少副反应的发生,过程II中的装置需使用阳离子交换膜
B.过程Ⅳ中的反应是
C.在联合生产过程中起催化作用
D.理论上每生成1mol ,可得到1mol
7.以含钴废渣(主要成分为CoO和Co2O3,含少量Al2O3和ZnO)为原料制备锂电池的电极材料CoCO3的工艺流程如下:
下列说法错误的是
A.通入SO2发生反应的离子方程式:2Co3++SO2+2H2O=2Co2++SO+4H+
B.加入适量Na2CO3调节pH是利用几种氢氧化物Ksp的不同除铝
C.若萃取剂的总量一定,则分多次加入萃取比一次加入萃取效果更好
D.将含Co2+的溶液缓慢滴加到Na2CO3溶液中沉钴,以提高CoCO3的产率
8.一种以“火法粗炼”、“电解精练”相结合炼制精铜的工艺流程如图所示。已知:黄铜矿石的主要成分为CuFeS2;“冰铜”还原中的Cu2S先转化为Cu2O,然后Cu2O再与Cu2S反应生成粗铜。下列叙述正确的是
A.“焙烧”过程中,CuFeS2既是氧化剂又是还原剂
B.在Cu2S“还原”为Cu的总反应中,Cu2O作催化剂
C.“电解”过程中阴极增重6.4g的同时,粗铜质量减少6.4g
D.该炼铜工艺零污染,对环境友好
9.NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
下列说法错误的是:
A.NaClO2中Cl的化合价为+3价
B.“电解”所用食盐水是由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为NaOH溶液、Na2CO3溶液。
C.“电解”中阴极反应的主要产物是NaClO2。
D.“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应中,氧化剂与还原剂的物质的量之比为1∶2,
10.碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图,下列说法不正确的是
A.该工艺中I2和HI的相互转化体现了“碘循环”
B.反应器中,控制温度为20-100℃,温度过低速率慢,温度过高水气化且增大碘的流失,反应速率也慢
C.分离器中的物质分离操作为过滤
D.碘循环工艺的总反应为SO2+2H2O=H2+H2SO4
11.下图是一种综合处理SO2废气的工艺流程。下列说法正确的是
A.操作Ⅱ发生反应的离子方程式为:2Fe2++4H++O2=2Fe3++2H2O
B.溶液b中阳离子只有Fe2+
C.溶液a转化为溶液b的反应中,SO2被氧化
D.加入FeO可以使溶液c转化为溶液a
12.为减轻环境污染,提高资源的利用率,可将钛厂、氯碱厂和甲醇厂联合进行生产。生产工艺流程如下:
已知:“氯化”过程在高温下进行,且该过程中元素的化合价没有变化。下列叙述错误的是
A.中为+4价
B.“合成”过程中原子利用率为
C.“氯化”时发生反应的化学方程式为
D.上述流程中生成钛时可用代替
13. 2020年突发而至的“新冠肺炎”疫情打断了人们以往平静的生活,社会对消毒剂的需求急剧增加。NaClO2 和ClO2 是两种比较常见的含氯消毒剂,其生产流程如图所示。下列有关说法错误的是
A. 粗盐水中常含有 、Ca2+ 、Mg2+ 等杂质离子,可向其中先后加入过量的Na2CO3溶液和Ba(OH)2溶液,然后过滤除去难溶物,即可得到精制食盐水
B.该生产流程可与硫酸厂联合生产,可以有效利用硫酸厂废气,保护环境,减少污染
C.产物A是
D.电解槽中电解的总反应式为2ClO2+2NaCl2NaClO2+Cl2
14.如图为从光盘中提取Ag(其它金属微量忽略不计)对废旧资源进行回收利用的工艺流程,下列说法错误的是
A.“氧化"阶段需在80 ℃条件下进行,则适宜的加热方式为水浴加热
B.“氧化“过程还生成O2,则反应方程式为4Ag+4NaClO+2H2O=4AgCl+ 4NaOH+O2↑
C.“还原”过程中N2H4·H2O转化为无害气体N2,则理论上消耗1molN2H4·H2O可提取到43.2g的单质Ag
D.10%的氨水溶解AgCl固体,可生成Cl-和[Ag(NH3)2]+
15.铋与氮同主族,在中性及碱性环境下常以的形式存在,铋及其化合物广泛应用于电子、医药等领域。以辉铋矿(主要成分为,含少量杂质等)为原料,采用湿法冶金制备精铋工艺流程如下,下列说法错误的是
A.“浸出”产生S的主要离子反应为
B.“浸出”时盐酸可以还原杂质PbO2
C.“浸出、置换、再生、电解精炼”工序中不全是氧化还原反应
D.再生液可以加入“浸出”操作中循环利用
二、填空题(共10题)
16.(根据实验流程书写陌生化学(离子)方程式)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
写出“反应”步骤中生成ClO2的化学方程式:___________。
17.Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
回答下列问题:
“酸浸”后,钛主要以TiOCl形式存在,写出相应反应的离子方程式:___________。
18.工业上制取硝酸铵的流程图如图,回答下列问题:
(1)设备Ⅱ发生反应的化学方程式为___。
(2)设备Ⅲ中生成HNO3化学方程式为____。
(3)设备Ⅳ中的尾气主要为NO,可以用NaClO溶液吸收,其他条件相同,NO转化为NO的转化率随NaClO溶液初始pH的变化如图所示。
在酸NaClO性溶液中,HClO氧化NO生成Cl-和NO,其离子方程式为__。
19.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:
(1)写出实验室制备黄绿色气体乙的化学方程式:_______,
(2)反应③中的离子方程式是_______
(3)反应⑤的离子方程式是_______
20.结合所学内容,回答下列问题。
(1)氮元素及其化合物的转化关系如图。
①写出X的化学式___________,Y的化学式___________。
②图中所示,关于转化为的反应过程,下列说法正确的是
a.氮元素的化合价不发生变化
b.若用与反应制取,另一种生成物是NO
c.该转化过程中,既是氧化剂又是还原剂
(2)催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氧化物脱除技术,反应原理如图。
①SCR技术中的氧化剂为___________。
②当与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为___________。
(3)某同学利用如图装置,进行氨气的喷泉实验。回答下列问题:
①仪器A的名称是___________。
②写出实验室用和制取氨气的化学方程式___________。
21.(1)是一种新型自来水消毒剂,具有强氧化性。其一种生产工艺如图甲所示:
①电解反应的化学方程式为_______。
②具有强氧化性,制取反应的化学方程式为_______。
③饮用水中残留的可用适量溶液去除,该反应的离子方程式为_______。
(2)某制备高纯碳酸锰的核心工艺如图乙,该沉锰过程的离子方程式为_______。
(3)在酸性条件下,黄铁矿催化氧化的流程如图丙,反应Ⅱ的离子方程式为:_______。
22.根据信息书写指定反应的方程式。
(1)请从下列试剂中选择合适的完成指定转化(试剂可重复选用)。
试剂:稀盐酸、溶液、溶液、溶液、浓硫酸、溶液
①的化学方程式:_______;
②的离子方程式:_______。
(2)钛铁矿(FeTiO3)在高温下经氯化得到四氯化钛,再制取金属钛的流程如图。写出“氯化”的化学方程式:_______。
23.2020年世界环境日的宣传主题为“关爱自然。刻不容慢”。防治大气污染、水体污染等是世界各国保护环境的最重要课题。
(1)氮的氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理更有助于消除大气污染。
C2H4催化还原NO是重要的烟气脱硝技术,研究发现在Cu+上可能发生的反应过程如图。写出该脱硝过程的总反应的化学方程式: ___________。
(2)烟气中的氮氧化物经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中氮氧化物的含量。
①室温下,固定进入反应器的NO的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)和n(NO2)随反应前n(O3):n(NO)的变化见下图。
当n(O3):n(NO)≤1时,发生反应的化学方程式为 ___________;
当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是___________;
②当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(弱碱性)中SO将NO2转化为NO,其离子方程式为___________。
(3)可综合利用上述吸收烟气后的溶液处理含NH废水,每产生1 mol无污染气体转移电子数为_______。
24.实验室以锌灰(含ZnO、PbO、CuO、FeO、Fe2O3、SiO2等)为原料制备Zn3(PO4)2·4H2O的流程如图。
滴加KMnO4溶液后有MnO2生成,该反应的离子方程式为___。
25.(1)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___。
(2)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为___。
(3)实验室中可用次氯酸钠溶液与氨反应制备联氨(N2H4),反应的化学方程式为___。
(4)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如表。
离子
SO
SO
NO
c/(mol·L-1)
8.35×10-4
6.87×10-6
1.5×10-4
离子
NO
Cl-
c/(mol·L-1)
1.2×10-5
3.4×10-3
写出NaClO2溶液脱硝过程中主要反应的离子方程式___。
26.用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如图:
回答下列问题:MnO2与BaS溶液反应转化为MnO的化学方程式为___。
27.化学还原法是处理含Cr2O的工业废水常用的方法,主要分为“还原”和“沉淀”两步:
Cr2OCr3+Cr(OH)3
已知:①Na2S2O5+H2O=2NaHSO3
②“COD”是指化学需氧量,反映了水样中较强还原性物质含量的多少。水中还原性物质越少,则COD越低,表明水质污染程度越小。
(1)取含Cr2O的工业废水,分别在不同pH条件下,向每个水样中分别加一定量的FeSO4、NaHSO3,搅拌,充分反应,然后滴加Ca(OH)2悬浊液,静置沉淀,测定+6价Cr的去除率,实验结果如图-1所示。
①在酸性条件下,请写出NaHSO3与Cr2O反应的离子方程式:___。
②分析比较亚铁盐和亚硫酸盐去除+6价Cr的效果。
Ⅰ.亚铁盐在中性和碱性条件下,对+6价Cr的去除效果优于酸性条件下的去除效果,亚硫酸盐则相反;
Ⅱ.___。
(2)用焦亚硫酸钠(Na2S2O5)处理废水后,可能会使废水中的COD增大。在焦亚硫酸钠与废水中铬元素不同质量比的情况下,加H2SO4与未加H2SO4处理含铬废水后其COD对比变化如图-2所示。
①未加H2SO4时,随着Na2S2O5质量增大,废水COD增大的原因是___。
②在焦亚硫酸钠与废水质量比相同的情况下,加H2SO4时,与未加H2SO4相比,废水COD均有所下降,原因可能是___。
(3)三价铬[Cr(Ⅲ)]在水溶液中的存在形态随pH的变化如图-3所示,为尽可能除去铬元素实现达标排放,沉淀过程中pH要控制在___;若pH过高,溶液中残留铬量增大,其原因为___。
28.已知溶液中,还原性为HSO>I-,氧化性为IO>I2>SO。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量(mol)的关系如图所示,请回答下列问题
下列问题:
(1) a点处的氧化产物是_________(填化学式,下同),还原产物是_______,a点对应的离子方程式为______________。
(2)当n(I2)达到最大值时,n(IO)对应的最小值为_____________mol,此时反应的离子方程式是_____________。
(3)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为_____
参考答案
1.B
【详解】
A.该反应产生氢气,反应条件是加热,为防止氢气燃烧,需要隔绝空气进行反应,A正确;
B.NaBO2、NaBH4中B均为+3价,H为-1价,则Na和H2生成NaBH4,Na化合价升高做还原剂,H2化合价降低做氧化剂,B错误;
C.NaBH4与水反应放出氢气,H2中H变价来源于NaBH4从-1升到0价,H2O从+1降至0价,则每生成1molH2转移1mole-,C正确;
D.由反应物和生成物可知,该反应的化学方程式为NaBO2+2SiO2+4Na+2H22Na2SiO3+NaBH4,D正确;
故选:B。
2.A
【分析】
由流程可知,CaO与硫酸锰反应生成,通入氧气生成,涉及反应为2+O2+4OH-=2+4H2O,与S2-反应生成,进而与氧气反应生成SO,可用于制备CaSO4•2H2O。
【详解】
A.俗名生石膏,属于结晶水合物,具有固定的组成和性质,属于纯净物里的盐类,A正确;
B.根据转化关系图,过程Ⅱ中与生成和,根据氧化还原反应得失电子守恒和物料守恒,反应的离子方程式为:,B错误;
C.由分析可知过程Ⅰ中发生反应:,溶液的pH减小,C错误;
D.10L上清液中的的物质的量,根据物质转化过程可知,转化为过程中需要消耗氧气,转化为也需要消耗氧气,在的过程中,硫元素的化合价由-2价变成+6价,共失去电子,在反应中得到4mol电子,所以将10L上清液中的转化为,理论上共需要的物质的量,D错误。
故选A。
3.D
【详解】
A.储存过程中被氧气氧化,N元素化合价发生改变,A错误;
B.在反应前后不发生改变,但是参与了反应历程,属于催化剂,是储存时生成的物质,是中间产物,不是催化剂,B错误;
C.储存还原总反应中生成,化合价降低,所以是氧化剂,是还原产物,C错误;
D.根据示意图可知还原过程发生的反应为甲烷和硝酸钡反应生成氧化钡、二氧化碳、氮气和水,配平得出方程式为:,D正确;
答案选D。
4.D
【分析】
由图可知,反应物为Fe3+、FeS2,生成物为Fe2+和,离子反应为14Fe3++FeS2+8H2O=15Fe2++2+16H+,S元素的化合价升高,则FeS2作还原剂,NO为该反应的催化剂,总反应为2FeS2+7O2+2H2O4+2Fe2++4H+,以此解答该题。
【详解】
A.反应III是Fe2+结合NO生成配合物Fe(NO)2+,化合价不变,不属于氧化还原反应,A错误;
B.反应前后NO的不变,起催化剂作用,B错误;
C.反应Ⅰ中Fe3+、FeS2反应生成Fe2+和,离子反应为14Fe3++FeS2+8H2O=15Fe2++2+16H+,C错误;;
D.反应Ⅱ的FeS2中S硫元素化合价从-1价升高到+6价,每消耗,转移电子的物质的量为1mol×2×7=14mol,D正确;
故选:D。
5.B
【详解】
A.根据题干提示,该反应方程式为:11KClO3+6I2 =6KH(IO3)2+3Cl2+5KCl,其中氧化剂是KClO3,氧化产物为KH(IO3)2,故氧化剂与氧化产物的物质的量之比为11∶6,A项正确;
B.加热可以促进溶解在溶液中气体的逸出,故“逐”过程只需要采用加热溶液即可,不用加入烧碱或KI晶体除Cl2,B项错误;
C.由于反应:5I-++6H+=3I2+3H2O,碘单质能使淀粉溶液变蓝色,故借助食用醋和淀粉碘化钾试纸即可检验是否含有补碘剂,C项正确;
D.调pH的目的是让,转化为,故应该加入KOH调节pH,发生反应的方程式为:,D项正确;
答案选B。
6.D
【分析】
由联合生产流程图可知,过程II中发生反应2NaCl +2H2O2NaOH + Cl2↑+H2↑,生成的H2参与过程I,与CO2、CO反应生成CH3OH,Cl2参与过程Ⅲ,发生反应2CuCl +Cl2= =2CuCl2,CuCl2进入过程IV中发生反应 2CuCl2 +C2H4 = C2H4Cl2 +2CuCl。
【详解】
A. 过程II为电解饱和NaCl溶液的过程,根据上述分析,电解过程中阳极发生氧化反应生成Cl2,阴极发生还原反应生成OH-,使用阳离子交换膜可防止Cl2和阴离子OH-通过,减少副反应,A正确;
B. 过程Ⅳ中的反应是,B正确;
C. CuCl2进入过程IV反应,过程Ⅲ发生的反应主要为过程IV产生的CuCl与过程Ⅱ产生的Cl2反应生成CuCl2,实现了CuCl2的再生,故在联合生产过程中起催化作用,C正确;
D. 过程I为H2与CO2、CO反应生成CH3OH,过程中H元素的化合价由0 价升高为+1价,则每生成1 mol CH3OH转移4 mol电子,过程Ⅲ发生反应 2CuCl+Cl2 = 2CuCl2,过程IV中发生反应,每生成1 mol C2H4Cl2转移2 mol电子,结合过程II中发生的反应,则理论上每生成1 mol CH3OH,可得到2 mol C2H4Cl2,D错误;
故选D。
7.D
【分析】
钴废渣主要成分为CoO、Co2O3,还含有Al2O3、ZnO等杂质,加入硫酸酸浸并通入二氧化硫,纵观整个流程最后得到CoCO3,说明该过程中二氧化硫会还原Co2O3,发生反应:Co2O3+SO2+H2SO4=2CoSO4+H2O,硫酸与CoO、氧化铝、氧化锌反应,所得溶液中还含有硫酸铝、硫酸锌等,加入碳酸钠调节溶液的pH,使铝离子转化为氢氧化铝沉淀,过滤除去,然后加入萃取剂,萃取锌离子,在有机层中加入稀硫酸,可得到硫酸锌。在水相中加入碳酸钠生成CoCO3固体。
【详解】
A.根据分析可知酸浸过程中二氧化硫会还原Co2O3,根据电子守恒和元素守恒得到离子方程式为2Co3++SO2+2H2O=2Co2++SO+4H+,A正确;
B.氢氧化物Ksp不同,则开始沉淀时所需的pH值不同,加入适量Na2CO3调节相应的pH可以只沉淀Al3+,B正确;
C.萃取过程中,每一次萃取都是按照一定比例进行的溶质分配,多次萃取相当于不断降低物质的浓度,提取效率就高,C正确;
D.将含Co2+的溶液缓慢滴加到Na2CO3溶液中,碳酸钠过量,碱性过程,会生成Co(OH)2沉淀,降低CoCO3的产率,D错误;
综上所述答案为D。
8.A
【分析】
黄铜矿石经选矿富集CuFeS2得铜精矿砂,铜精矿砂焙烧得含Cu2S、FeS的冰铜,冰铜还原得粗铜(含Fe等杂质),电解得精铜。
【详解】
A.CuFeS2中铜为+2价,铁为+2价,硫为−2价,“焙烧”过程中,,Cu元素化合价降低,部分S元素化合价升高,则CuFeS2既是氧化剂又是还原剂,A正确;
B.在Cu2S“还原”为Cu的反应中,Cu2S先转化为Cu2O,然后Cu2O再与Cu2S反应生成Cu铜单质,Cu2O得电子被还原,做氧化剂,B错误;
C.电解精炼铜时,精铜作阴极,铜离子得电子变为铜,粗铜作阳极,失电子变为金属阳离子, 粗铜中活性比Cu强的金属在Cu之前失电子,故阴极增重6.4g的同时,阳极减少质量不为6.4g,C错误;
D.该炼铜工艺会放出二氧化硫,影响环境,对环境不友好,D错误;
答案选A。
9.D
【分析】
由流程知,NaClO3和SO2、HSO4反应生成NHSO4和ClO2;“电解”时阴极发生还原反应,通过电解,由ClO2制取NaClO2;吸收ClO2用NaOH和H2O2,反应方程式为:2ClO2+H2O2+2NaOH=2NaClO2+2H2O+O2↑,据此分析解答。
【详解】
A.根据NaClO2中化合价代数和为零,Na为+1价,O为-2价,则Cl的化合价为+3价,故A正确;
B.食盐水精制中除Mg2+用NaOH溶液,除Ca2+用Na2CO3溶液,因而要加入的试剂分别为NaOH溶液、Na2CO3溶液,故B正确;
C.“电解”时阴极发生还原反应,根据流程图可知通过电解,可以由ClO2制取NaClO2,故阴极的反应为:ClO2+e-=Cl,阴极的主要产物是NaClO2,故C正确;
D.由流程知,吸收ClO2用NaOH和H2O2,反应方程式为:2ClO2+H2O2+2NaOH=2NaClO2+2H2O+O2↑,其中氧化剂为ClO2,还原剂为H2O2,二者的物质的量之比为2:1,故D错误;
答案选D。
10.C
【分析】
从流程图可知,在反应器中,I2氧化SO2,生成硫酸和HI,在分离器中分离硫酸和HI,在膜反应器中HI发生分解反应产生H2和I2。
【详解】
A.在反应器中I2反应转换为HI,在膜反应器中HI分解转化为H2和I2,从而实现了碘循环,A说法正确;
B.在反应器中,控制温度为20-100℃,根据温度对化学反应速率的影响,若反应温度过低速率慢,但温度过高,水气化,会使碘单质升华,增大碘的流失,也会导致反应速率比较慢,B说法正确;
C.H2SO4、HI都溶于水,所以分离器中的物质分离操作不可能是过滤,C说法错误;
D.在反应器中发生反应:SO2+I2+2H2O=H2SO4+2HI,在膜反应器中发生反应:2HI=H2+I2,所以碘循环工艺总反应为SO2+2H2O=H2+H2SO4,D说法正确;
答案为C。
11.C
【分析】
Fe3+有氧化性,SO2有还原性,Fe2(SO4)3被SO2还原为FeSO4,溶液b主要溶质为FeSO4、H2SO4,可能含Fe2(SO4)3或SO2,空气中氧气将FeSO4及可能存在的SO2氧化得溶液a循环使用。
【详解】
A.电荷不守恒,操作Ⅱ发生反应的离子方程式为:4Fe2++4H++O2= 4Fe3++2H2O,A错误;
B.操作I中发生反应的离子方程式为:2Fe3++SO2+2H2O = 2Fe2+++4H+,溶液中阳离子有Fe2+、H+,若SO2少量,则还有Fe3+,B错误;
C.溶液a转化为溶液b的反应中,SO2被Fe3+氧化,C正确;
D.溶液c中含有 Fe2(SO4)3、H2SO4等物质,加入FeO后会生成FeSO4,D错误。
答案选C。
12.D
【详解】
A.由题干信息知,Ti元素化合价没有变化,TiCl4中Ti为+4价,则中为+4价,故A正确;
B.“合成”反应中CO与H2反应生成CH3OH,反应方程式为CO+2H2CH3OH,由此可见原子利用率为100%,故B正确;
C.根据流程图知,“氯化”过程中,C转化为CO,FeTiO3转化为FeCl3和TiCl4,反应为2FeTiO3+6C+7Cl2= 2FeCl3+2TiCl4+6CO,故C正确;
D.Ar与Mg不反应,所以Ar可以用作保护气,Mg与反应生成氧化镁和碳,所以不能用代替Ar,故D错误;
故答案选D。
13.A
【分析】
NaClO3被SO2在反应器中还原得到ClO2,SO2被氧化成硫酸根,发生的反应,2NaClO3+SO2=Na2SO4+2ClO2,所以产物A为Na2SO4;将ClO2与饱和食盐水混合电解得到Cl2和NaClO2,根据氯元素的价态变化可得总反应方程式应为2NaCl+2ClO22NaClO2+Cl2。
【详解】
A.由于过量的钡离子还需要碳酸钠除去,所以要先加Ba(OH)2,再加Na2CO3,过滤后滴加盐酸除去氢氧根和碳酸根,故A错误;
B.硫酸厂的废气中含有大量二氧化硫,二氧化硫会污染空气,将该流程与硫酸厂联合,可以有效利用废气中的二氧化硫,减少污染,故B正确;
C.反应器中反应为2NaClO3+SO2=Na2SO4+2ClO2,所以产物A为Na2SO4,故C正确;
D.将ClO2与饱和食盐水混合电解得到Cl2和NaClO2,根据氯元素的价态变化和元素守恒可得总反应方程式应为2NaCl+2ClO22NaClO2+Cl2,故D正确;
综上所述答案为A。
14.C
【分析】
回收一种光盘金属层中的少量Ag,由流程可知,氧化时发生4Ag+4NaClO+2H2O=4AgCl+4NaOH+O2↑,为控制80°C,可水浴加热,过滤分离出AgCl、可能含Ag,再加10%的氨水溶解AgCl,发生AgCl+2NH3·H2O=[Ag(NH3)2] ++Cl-+2H2O,过滤分离出的滤渣为Ag,对过滤得到的滤液用N2H4·H2O (水合肼)在碱性条件下能还原[Ag(NH3)2] +得到Ag,以此解答该题。
【详解】
A.控制80°C的反应条件,可选择水浴加热,以提供恒定的温度,A正确;
B.NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,发生反应的化学方程式为:4Ag+4NaClO+2H2O=4AgCl+4NaOH+O2↑,B正确;
C.氮气存在的条件未知,不能确定是否标准状况下,则不能确定物质的量,C错误;
D.AgCl与NH3·H2O按1:2反应,反应的离子方程式AgCl+2NH3·H2O=[Ag(NH3)2] ++Cl-+2H2O,生成Cl-和[Ag(NH3)2] +,D正确;
故选C。
15.C
【分析】
辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等)加入足量的FeCl3溶液和盐酸浸取,Fe3+将S氧化成S单质沉淀,盐酸将PbO2还原,由于溶液中有大量氯离子,所以得到PbCl2沉淀;此时溶液中主要含有Fe2+、Bi3+、Fe3+以及H+,加入适量铁粉将H+、Fe3+还原,同时置换出Bi单质,过滤得到粗铋以及主要含有FeCl2的滤液,粗铋经电解精炼得到精铋,氯化亚铁溶液中通入氯气得到氯化铁再生液。
【详解】
A.浸出时S单质的生成主要是由于Fe3+将-2价的S元素氧化,结合电子守恒和元素守恒可以得到离子方程式为,故A正确;
B.盐酸可以提供氢离子和氯离子,酸性环境中PbO2可以将氯离子氧化,故B正确;
C.根据A、B分析可知浸出过程全部为氧化还原反应,置换过程中Fe与H+、Fe3+和Bi3+的反应是氧化还原反应,再生过程氯气将亚铁离子氧化,电解精炼也是发生氧化还原反应,故C错误;
D.根据分析可知再生液为氯化铁溶液,可以加入浸出操作中循环利用,故D正确;
综上所述答案为C。
16.2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4
【分析】
由制备流程可知,NaClO3和SO2在H2SO4酸化条件下生成ClO2,其中NaClO3是氧化剂,回收产物为NaHSO4,说明生成硫酸氢钠,据此分析书写反应的方程式。
【详解】
“反应”步骤中NaClO3和SO2在H2SO4酸化条件下生成ClO2和硫酸氢钠,反应的化学方程式为2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2,故答案为:2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2。
17.FeTiO3+4H++4Cl-=Fe2++TiOCl+2H2O
【详解】
用盐酸溶解FeTiO3,反应后钛主要以TiOCl形式存在,则FeTiO3→TiOCl。依据得失电子守恒、质量守恒和电荷守恒完成方程式FeTiO3+4H++4Cl-→Fe2++TiOCl+2H2O。
18.4NH3+5O24NO+6H2O 4NO+3O2+2H2O=4HNO3或2NO+O2=2NO2、3NO2+H2O=2HNO3+NO 3HClO+2NO+H2O=3Cl-+2NO+5H+或3ClO-+2NO+H2O=3Cl-+2NO+2H+
【详解】
(1)由流程图可知:设备Ⅱ是氨气和氧气在Pt—Rh合金网作催化剂的条件下发生反应生成一氧化氮和水,反应的化学方程式为4NH3+5O24NO+6H2O 。
(2) 由流程图可知:设备Ⅲ中是一氧化氮和氧气反应生成二氧化氮,二氧化氮和水反应生成一氧化氮和HNO3,设备Ⅲ在工作时不断通入空气的目的是使NO循环利用,最终全部转化成HNO3,反应的化学方程式为2NO+O2=2NO2、3NO2+H2O=2HNO3+NO或4NO+3O2+2H2O=4HNO3。
(3)在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO,Cl元素的化合价由+1价降至-1价,N元素的化合价由+2价升至+5价,根据得失电子守恒、电荷守恒和原子守恒,反应的离子方程式为3HClO+2NO+H2O=3Cl-+2NO+5H+或3ClO-+2NO+H2O=3Cl-+2NO+2H+。
19.4HCl(浓)+MnO2Cl2↑+MnCl2+2H2O 2Al+2OH-+2H2O=2AlO+3H2↑ 2Fe2++Cl2=2Fe3++2Cl-
【分析】
金属单质A焰色反应呈黄色,则A是Na,Na与H2O反应产生气体甲是H2,D溶液为NaOH,金属B和氢氧化钠溶液反应,说明B为Al,黄绿色气体乙为Cl2,气体甲和氯气反应生成丙为HCl,物质E为盐酸溶液,物质D是氢氧化钠,D和物质G反应生成红褐色沉淀H为Fe(OH)3,盐酸与金属C反应产生金属氯化物,该氯化物与NaOH溶液反应产生Fe(OH)3,则C是Fe,F为FeCl2、G为FeCl3。
【详解】
(1)气体乙为氯气,实验室利用二氧化锰和浓盐酸共热制取氯气,化学方程式为4HCl(浓)+MnO2Cl2↑+MnCl2+2H2O;
(2)反应③为铝和NaOH溶液的反应,生成偏铝酸钠、氢气,离子方程式为2Al+2OH-+2H2O=+3H2↑;
(3)结合分析可知,反应⑤为FeCl2与Cl2反应生成FeCl3,其离子方程式是2Fe2++Cl2=2Fe3++2Cl-。
20.NH3 N2O5 bc NO、NO2 NO2+NO+2NH32N2 + 3H2O 2+CaCl2+ 2NH3+ 2H2O
【详解】
(1)①根据价类二维图可知,X为N元素的-3价的氢化物,所以X为氨气,化学式为NH3;Y为N元素的+ 5的氧化物,所以Y为五氧化二氮,化学式为: N2O5,故答案为: NH3; N2O5;
②a.由图可知,NO2转化为HNO3的反应过程中,氮元素的化合价发生了变化,由+4价升高到了+5价,故a错误;
b. NO2与H2O反应制取HNO3,方程式为:3NO2 + H2O= 2HNO3 + NO,即一种生成物是NO,故b正确;
c.由b分析可知,该转化过程中,N元素既有升高又有降低,所以NO2既是氧化剂,又是还原剂,故c正确;
故答案: bc;
(2)①由图可知,在NH3催化还原氮氧化物(SCR)技术中,氧化剂为NO、NO2,还原剂为NH3,相互之间发生归中反应生成了N2和H2O,故答案: NO、NO2;
②当NO2与NO的物质的量之比为1 : 1时,与足量氨气在一定条件下发生反应,根据得失电子守恒可得反应的化学方程式为:NO2+NO+2NH3 2N2 + 3H2O,故答案为: NO2+NO+2NH32N2 + 3H2O;
(3) ①由装置图可知:仪器A的名称是圆底烧瓶,故答案:圆底烧瓶;
②实验室用和反应生成氯化钙、氨气和水,其反应的化学方程式2+CaCl2+ 2NH3+ 2H2O,故答案:2+CaCl2+ 2NH3+ 2H2O。
21.NH4Cl+2HClNCl3+3H2↑ 6NaClO2+NCl3+3H2O=6ClO2↑+3NaCl+NH3↑+3NaOH 5Fe2++ClO2+4H+=Cl-+5Fe3++2H2O Mn2++2HCO=MnCO3↓+CO2↑+H2O 14Fe3++FeS2+8H2O=15Fe2++2SO+16H+
【详解】
(1)①由工艺流程图可知,NH4Cl与HCl发生电解产生NCl3和H2,N由-3价变到+3价,H由+1价变到0价,通过得失电子守恒,得到反应的化学方程式为:NH4Cl+2HClNCl3+3H2↑,故答案为:NH4Cl+2HClNCl3+3H2↑;
②由工艺流程图可知,NaClO2与NCl3在碱性条件下发生氧化还原反应生成ClO2和NH3,NaClO2中Cl由+3价变到+4价,NCl3中N由+3价变到-3价,通过得失电子守恒和原子守恒,得到反应的化学方程式为:6NaClO2+NCl3+3H2O=6ClO2↑+3NaCl+NH3↑+3NaOH,故答案为:6NaClO2+NCl3+3H2O=6ClO2↑+3NaCl+NH3↑+3NaOH;
③采用溶液,其电离出的Fe2+可将ClO2还原为Cl-,达到除去水中残留的的目的,该反应的离子方程式为5Fe2++ClO2+4H+=Cl-+5Fe3++2H2O,故答案为:5Fe2++ClO2+4H+=Cl-+5Fe3++2H2O;
(2)由流程知“沉锰”反应物为MnSO4和NH4HCO3,产物之一为MnCO3,MnCO3中C来自 HCO的电离(HCO C+H+),由于Mn2+结合C使HCO电离平衡正向移动,溶液中c(H+)增大,与另一部分HCO发生反应:HCO+ H+= CO2↑+H2O,故反应的离子方程式为:Mn2++2HCO=MnCO3↓+CO2↑+H2O,故答案为:Mn2++2HCO=MnCO3↓+CO2↑+H2O;
(3)由物质转化图示可知,反应Ⅱ中Fe3+为氧化剂,FeS2为还原剂,反应生成了Fe2+和SO,通过得失电子守恒和电荷守恒,得到反应的离子方程式为:14Fe3++FeS2+8H2O=15Fe2++2SO+16H+,故答案为:14Fe3++FeS2+8H2O=15Fe2++2SO+16H+。
22.Cl2+2NaOH=NaCl+NaClO+H2O 4H++NO+3Fe2+=NO↑+3Fe3++2H2O 2FeTiO3+6C+7Cl22FeCl3+6CO+2TiCl4
【详解】
(1)①Cl2与NaOH反应生成NaCl、NaClO和H2O,方程式为Cl2+2NaOH=NaCl+NaClO+H2O;
②HNO3有强氧化性,与Fe2+反应可得到NO,离子方程式为4H++NO+3Fe2+=NO↑+3Fe3++2H2O;
(2)根据流程图可知,反应物为FeTiO3、C和Cl2,产物为FeCl3、CO和TiCl4,方程式为2FeTiO3+6C+7Cl22FeCl3+6CO+2TiCl4。
23.6NO+C2H43N2+2CO2+2H2O 3NO+O3=3NO2 O3将NO2氧化为更高价态氮氧化合物 SO+2NO2+2OH-=SO+2NO+H2O 3NA
【详解】
(1)由图可知,C2H4催化还原NO中生成物为N2、H2O、CO2,反应中N元素化合价由+2降低至0,C元素化合价由-2升高至+4,根据氧化还原反应化合价升降守恒以及原子守恒可知反应方程式为6NO+C2H43N2+2CO2+2H2O;
(2)①当n(O3):n(NO)≤1时,NO与O3反应的产物为NO2,反应过程中N元素化合价由+2升高至+4,O3中O元素化合价由0降低至-2,根据氧化还原反应化合价升降守恒及原子守恒可知反应方程式为3NO+O3=3NO2;当n(O3):n(NO)>1时,O3具有强氧化性,能够将NO2氧化为更高价态氮氧化合物,导致NO2的物质的量减小,故答案为:3NO+O3=3NO2;O3将NO2氧化为更高价态氮氧化合物;
②SO将NO2转化为NO的反应中,N元素化合价由+4降低至+3,则S元素化合价由+4升高至+6,根据氧化还原反应化合价升降守恒、电荷守恒以及溶液呈弱碱性可知反应的离子方程式为SO+2NO2+2OH-=SO+2NO+H2O;
(3)吸收烟气后的溶液中含有大量NO,NO与NH反应时生成无污染的N2,根据化合价升降守恒可知反应物质的关系式为NH~NO~N2,则每产生1 mol N2时转移电子数为3NA。
24.+3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+
【详解】
锌灰被稀硫酸“浸取”后,溶液中有Fe2+,KMnO4溶液氧化Fe2+生成Fe3+,自身被还原为MnO2,反应的离子方程式为MnO+3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+。
25.2Fe2++H2O2+2H+=2Fe3++2H2O 2+6H++5H2O2=2Mn2++8H2O+5O2↑ NaClO+2NH3=N2H4+NaCl+H2O 4NO+3+4OH-=4+2H2O+3Cl-
【详解】
(1)H2O2是强氧化剂,能将Fe2+氧化成Fe3+,则有2Fe2++H2O2+2H+=2Fe3++2H2O;
(2)双氧水可以被酸性高锰酸钾溶液氧化生成水和氧气,离子方程式为2+6H++5H2O2=2Mn2++8H2O+5O2↑;
(3)由题意可知,次氯酸钠是强氧化剂,氨是还原剂,氮元素由-3价升高到-2价,失去1个电子,生成联氨,氯元素由+1价降低到-1价,得到2个电子,生成稳定的氯化钠,则反应的化学方程式为2NH3+NaClO=N2H4+NaCl+H2O;
(4)NaClO2溶液脱硝过程,转化为Cl-,NO主要转化为,则有4NO+3+4OH-=4+2H2O+3Cl-。
26.MnO2+BaS+H2O=Ba(OH)2+MnO+S
【详解】
由流程图所给信息可知,MnO2与BaS溶液反应转化为MnO、S和Ba(OH)2,反应的化学方程式为MnO2+BaS+H2O=Ba(OH)2+MnO+S,故答案为:MnO2+BaS+H2O=Ba(OH)2+MnO+S。
27.3HSO+Cr2O+5H+=2Cr3++3SO+4H2O 中性和碱性条件下,亚铁盐对+6价Cr的去除效果明显优于亚硫酸盐的去除效果,在酸性条件下则相反 Na2S2O5质量增大,反应后废水中剩余的HSO(或S2O)的量就越多,HSO(或S2O)具有较强的还原性,所以废水的COD增大 废水酸性增强,促进HSO(或S2O)与Cr2O充分反应,还原性的HSO(或S2O)转化更完全,含量减少。(或废水酸性增强,HSO转化为SO2气体逸出) 7~11 Cr(OH)3转化为可溶性的Cr(OH)
【详解】
(1)①Cr2O具有较强氧化性,酸性环境下可将HSO氧化成SO,根据电子守恒和元素守恒可得离子方程式为3HSO+Cr2O+5H+=2Cr3++3SO+4H2O;
②Ⅱ.据图可知中性和碱性条件下,亚铁盐对+6价Cr的去除效果明显优于亚硫酸盐的去除效果,在酸性条件下则相反;
(2)①未加H2SO4时,Na2S2O5质量增大,反应后废水中剩余的HSO(或S2O)的量就越多,HSO(或S2O)具有较强的还原性,消耗的氧气增多,所以废水的COD增大;
②加H2SO4后,废水酸性增强,促进HSO(或S2O)与Cr2O充分反应,还原性的HSO(或S2O)转化更完全,含量减少,(或废水酸性增强,HSO转化为SO2气体逸出),所以废水COD均有所下降;
(3)据图可知pH为7~11时,以Cr(OH)3沉淀形式存在的Cr元素含量最高;pH过高Cr(OH)3转化为可溶性的Cr(OH),溶液中残留铬量增大。
28. I- 2+6═2I-+6+6H+ 1.2 +6H++5I-=3H2O+3I2 2+5=I2+5+3H++H2O
【分析】
(1)还原性>I-,首先发生反应:2+6═2I-+6+6H+,反应完毕,继续加入KIO3,由于氧化性>I2,再发生反应:+6H++5I-=3H2O+3I2,结合图中a点碘的量判断发生的反应,据此解答;
(2)由图可知,c点时I-完全反应,n(I2)达到最大值时,此时共加入1.2molKIO3,由于生成I2,发生反应:+6H++5I-=3H2O+3I2;
(3)向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,被氧化为,KIO3过量,由于氧化性>I2,KIO3会氧化I-,反应不能生成I-,而是生成I2,据此书写。
【详解】
(1)还原性>I-,首先发生反应:2+6═2I-+6+6H+,反应完毕,继续加入KIO3,由于氧化性>I2,再发生反应:+6H++5I-=3H2O+3I2,由图可知,a点没有生成碘,故发生反应2+6═2I-+6+6H+,氧化产物是,还原产物是I-,故答案为:;I-;2+6═2I-+6+6H+;
(2)由图可知,c点时I-完全反应,n(I2)达到最大值时,此时共加入1.2molKIO3,生成I2的离子方程式为:+6H++5I-=3H2O+3I2,故答案为:1.2;+6H++5I-=3H2O+3I2;
(3)向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,被氧化为,KIO3过量,由于氧化性>I2,KIO3会氧化I-,反应不能生成I-,而是生成I2,反应离子方程式为:2+5=I2+5+3H++H2O,故答案为:2+5=I2+5+3H++H2O。
2023年高考化学二轮复习(新高考版) 专题5 题型专攻1 “陌生情景下”方程式的书写: 这是一份2023年高考化学二轮复习(新高考版) 专题5 题型专攻1 “陌生情景下”方程式的书写,文件包含2023年高考化学二轮复习新高考版专题5题型专攻1“陌生情景下”方程式的书写docx、专题5题型专攻1“陌生情景下”方程式的书写docx等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
2022届高考化学一轮复习常考题型05离子方程式的书写规范含解析: 这是一份2022届高考化学一轮复习常考题型05离子方程式的书写规范含解析,共20页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
2022届高考化学一轮复习常考题型14流程情景中方程式的书写专题含解析: 这是一份2022届高考化学一轮复习常考题型14流程情景中方程式的书写专题含解析,共29页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。













