


2021高考化学专题讲解 专题十九 物质的检验、分离与提纯(讲解部分)课件
展开考点一 物质的分离与提纯
基础知识1.物质分离与提纯的区别(1)物质的分离:将混合物中的各组分分离开来,获得几种纯净物的过程。(2)物质的提纯:将混合物中的杂质除去而得到目标物质的过程。
2.物质分离与提纯的基本原则(1)“四原则”:不增(提纯过程中不增加新的杂质);不减(不减少被提纯的 物质);易分离(被提纯物质与杂质容易分离);易复原(被提纯物质转化后要 易复原)。(2)“四必须”:除杂试剂必须过量;过量试剂必须除尽(因为过量试剂引入 新的杂质);必须选最佳除杂途径;除去多种杂质时必须考虑加入试剂的顺 序。
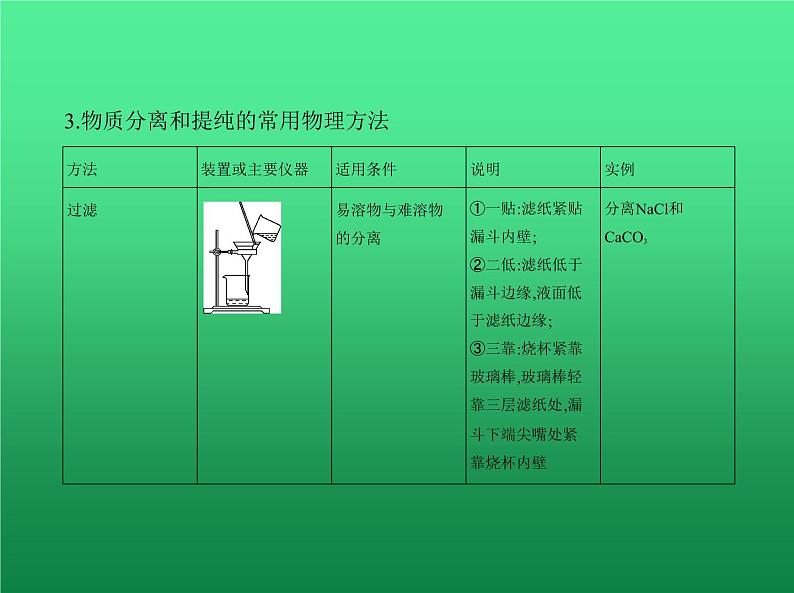
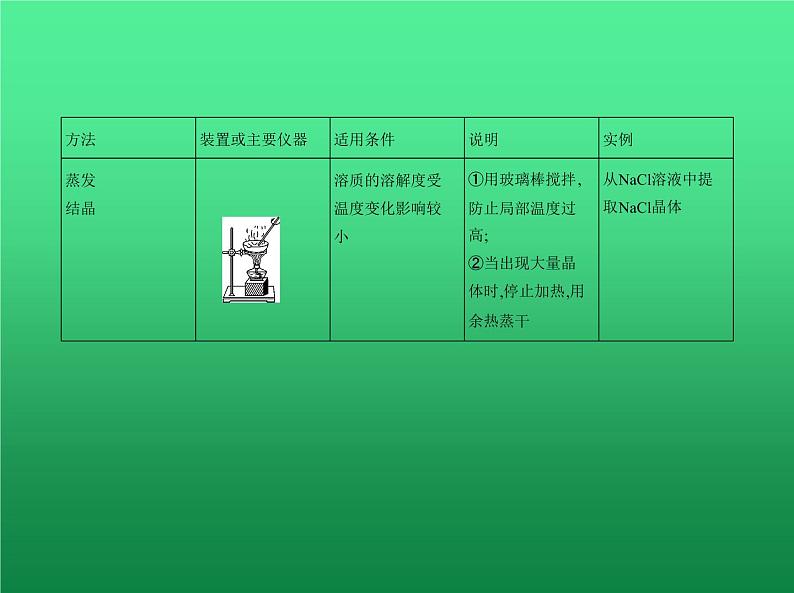
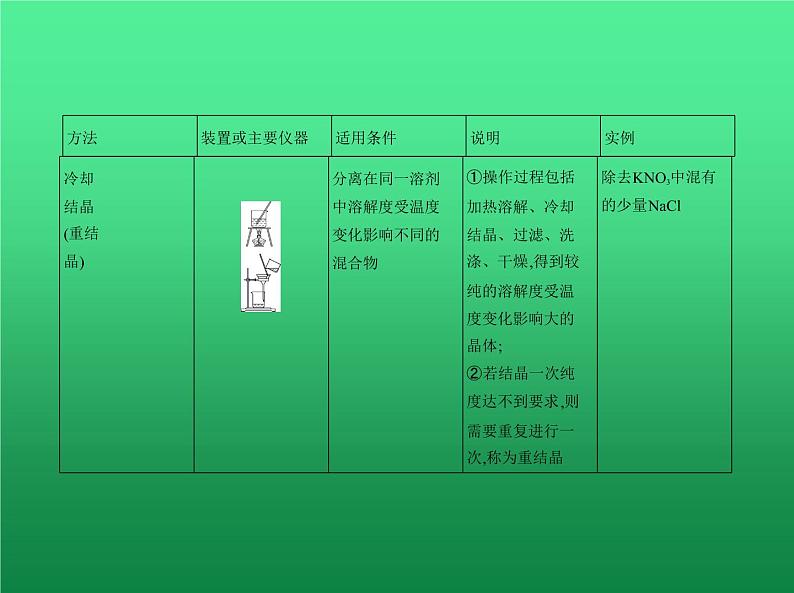
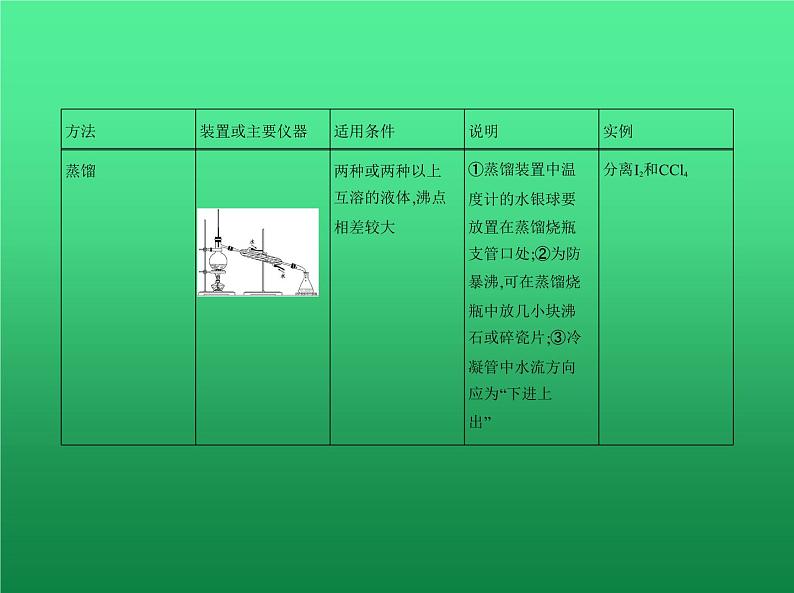
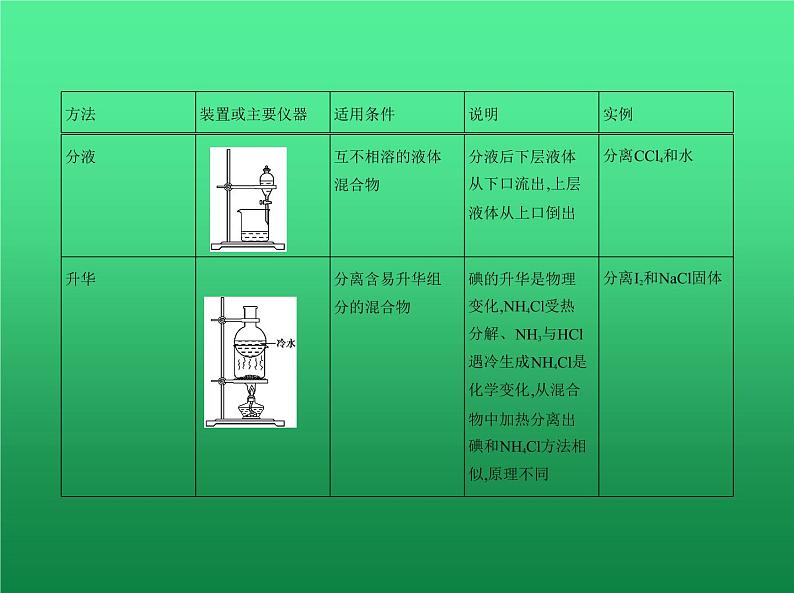
3.物质分离和提纯的常用物理方法
4.物质分离与提纯的化学方法
核心精讲沉淀洗涤题的解题思路1.常用洗涤剂(1)蒸馏水:主要适用于除去沉淀吸附的可溶性杂质。(2)冷水:除去沉淀的可溶性杂质,降低沉淀在水中的溶解度而减少沉淀损 失。(3)沉淀的饱和溶液:减少沉淀的溶解。(4)有机溶剂(酒精、丙酮等):适用于易溶于水的固体,既减少了固体溶解, 又利用有机溶剂的挥发性,除去固体表面的水分,产品易干燥。
2.沉淀洗涤的解题思路注洗涤液(沿玻璃棒向漏斗中注入洗涤液)↓标准(使洗涤液完全浸没沉淀或晶体)↓重复(待洗涤液流尽后,重复操作2~3次)3.沉淀是否洗净的解题思路取样(取少量最后一次洗涤液于一洁净的试管中)↓加试剂[加入××试剂(必要时加热,如检验N )]↓现象(不产生××沉淀、溶液不变××色或不产生××气体)↓结论(说明沉淀已经洗涤干净)
考点二 物质的检验与鉴别
基础知识1.物质检验的三原则一看(颜色、状态);二嗅(气味);三实验(加试剂)。2.物质检验的一般步骤观察外观 取少量样品 加入试剂 观察现象 得出结论
1.抽滤由于水流的作用,使图1装置a、b中气体压强减小,过滤速率加快。 图1
图2中,双耳球上端球形容器的容积较大,既能除去气体中的气态杂质,又能 防止倒吸。 图2例 (2019湖南、湖北八市十二校一调,20节选)某研究小组在实验室以含 铁的铜屑为原料制备Cu(NO3)2·3H2O晶体,并进一步探究用SOCl2制备少量 无水Cu(NO3)2。设计的合成路线如下:Cu屑(含Fe) Cu(NO3)2溶液 Cu(NO3)2·3H2O晶
2.洗气装置——双耳球吸收法
体 无水Cu(NO3)2已知:Cu(NO3)2·3H2O Cu(NO3)2·Cu(OH)2 CuO;SOCl2的熔点为-105 ℃、沸点为76 ℃,遇水剧烈水解生成两种酸性气体。请回答:(1)第②步调pH适合的物质是 (填化学式)。(2)第③步包括蒸发浓缩、冷却结晶、抽滤等步骤,其中蒸发浓缩的具体操 作是 。为得到较大颗粒的Cu(NO3)2·3H2O晶体,可采用的方法是 (填一种)。(3)第④步中发生反应的化学方程式是 。(4)第④步,某同学设计的实验装置示意图(夹持及控温装置省略)有一处不
合理,请提出改进方案并说明理由: 。 装置改进后,向仪器A中缓慢滴加SOCl2时,需打开活塞 (填“a” “b”或“a和b”)。
解题导引 为提高铜的浸取率,所用硝酸必然是足量的,此时铁也溶解转化 为硝酸铁,调pH的目的是除去铁离子。然后蒸发浓缩、降温结晶得到Cu(NO3)2·3H2O晶体,最后在SOCl2的保护下脱去结晶水得到无水硝酸铜,据此 解答。
解析 (1)调节pH使铁离子形成沉淀,不引入新杂质,同时不能沉淀铜离子, 因此第②步调pH适合的物质是CuO或Cu(OH)2或Cu2(OH)2CO3。(2)根据题意,温度不能高于170 ℃,否则Cu(NO3)2·3H2O变质,故蒸发浓缩应 将溶液转移至蒸发皿中,控制温度(不高于170 ℃),加热至溶液表面形成一 层晶膜;减慢冷却结晶的速度,可得到较大颗粒的Cu(NO3)2·3H2O晶体。(3)根据已知信息可知第④步中发生反应的化学方程式是Cu(NO3)2·3H2O+3SOCl2 Cu(NO3)2+3SO2↑+6HCl↑。(4)第④步,某同学设计的实验装置有一处不合理,根据装置图可知氢氧化 钠溶液中的水蒸气可以进入A中影响三水合硝酸铜晶体的脱水反应。改 进的方法是在A、B之间增加干燥装置;装置改进后,向仪器A中缓慢滴加 SOCl2时,需打开活塞b。
答案 (1)CuO或Cu(OH)2或Cu2(OH)2CO3(2)将溶液转移至蒸发皿中,控制温度(不高于170 ℃,防止硝酸铜水解),加热 至溶液表面形成一层晶膜 减慢冷却结晶的速度或冷却后静置较长时间(3)Cu(NO3)2·3H2O+3SOCl2 Cu(NO3)2+3SO2↑+6HCl↑(4)在A、B之间增加干燥装置,防止B中水蒸气进入A中 b
实现物质的分离、提纯,需要对物质的物理性质及化学性质的相同点、差 异点熟练掌握并应用。如固液分离、分离互不相溶的液体、分离互溶的 液体等的物理方法;如沉淀法、气体法、氧化还原法等化学方法。
例1 (2019广东深圳二模,10)NiSO4·6H2O易溶于水,其溶解度随温度升高 明显增大。以电镀废渣(主要成分是NiO,还有CuO、FeO等少量杂质)为原 料制备该晶体的流程如下,下列说法错误的是 ( ) A.溶解废渣时不能用稀盐酸代替稀H2SO4B.除去Cu2+可采用FeSC.流程中a→b的目的是富集NiSO4D.“操作Ⅰ”为蒸发浓缩、冷却结晶
解析 A项,在除去Cu2+和Fe2+后加入Na2CO3溶液,Ni2+与C 生成NiCO3沉淀,所以溶解废渣时若用稀盐酸代替稀H2SO4对制备不会有影响,故错误;B 项,CuS比FeS更难溶,向含有Cu2+的溶液中加入FeS发生沉淀的转化生成 CuS,故正确;C项,NiSO4与Na2CO3反应生成NiCO3沉淀,而后过滤,再加适量 稀硫酸溶解又生成NiSO4,这样可提高NiSO4的浓度,所以流程中a→b的目的 是富集NiSO4,故正确;D项,NiSO4·6H2O为结晶水合物,从溶液中得到NiSO4·6H2O的实验操作为蒸发浓缩、冷却结晶,故正确。
题目价值 本题考查物质除杂的方法选择,涉及元素及其化合物的性质及 实验基本操作,体现科学探究与创新意识的学科核心素养。
例2 (2019天津河西二模)下列实验操作、现象与对应的结论或解释正确 的是 ( )
山东专用高考化学一轮复习专题十九物质的检验分离与提纯专题综合检测含解析: 这是一份山东专用高考化学一轮复习专题十九物质的检验分离与提纯专题综合检测含解析,共20页。
山东专用高考化学一轮复习专题十九物质的检验分离与提纯_基础集训含解析: 这是一份山东专用高考化学一轮复习专题十九物质的检验分离与提纯_基础集训含解析,共6页。
山东专用高考化学一轮复习专题十九物质的检验分离与提纯_模拟集训含解析: 这是一份山东专用高考化学一轮复习专题十九物质的检验分离与提纯_模拟集训含解析,共58页。












