

高中第一节 铁及其化合物课堂检测
展开一、选择题(本题包括2小题,每小题5分,共10分)
1.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是( )
2.下列除杂的操作不正确的是( )
A.MgCl2溶液中混有少量FeCl3:加入足量镁充分反应后过滤
B.FeCl2溶液中混有少量FeCl3:加入过量铁粉充分反应后过滤
C.CuCl2溶液中混有少量FeCl3:加入NaOH溶液充分反应后过滤
D.CuCl2溶液中混有少量FeCl2:先加入H2O2将Fe2+氧化成Fe3+,再加入CuO充分反应后过滤
【补偿训练】
将1.12 g铁粉加入25 mL 2 ml·L-1的氯化铁溶液中,充分反应后,其结果是
( )
A.铁粉剩余,溶液呈浅绿色,Cl-基本不变
B.向溶液中滴入无色KSCN溶液,不显红色
C.溶液中Fe2+与Fe3+物质的量之比为6∶1
D.氧化产物与还原产物的物质的量之比为2∶5
二、非选择题(本题包括1小题,共20分)
3. (2019·哈尔滨高一检测)同学们用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 ml·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是 __。
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为 __。
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是
__。
(4)丙同学取10 mL 0.1 ml·L-1 KI溶液,加入6 mL 0.1 ml·L-1FeCl3溶液混合。取2 mL此溶液于试管中,加入1 mL CCl4充分振荡、静置,CCl4层显紫色,发生反应的离子方程式为 __。
(5)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为 __。
非选择题(本题包括1小题,共20分)
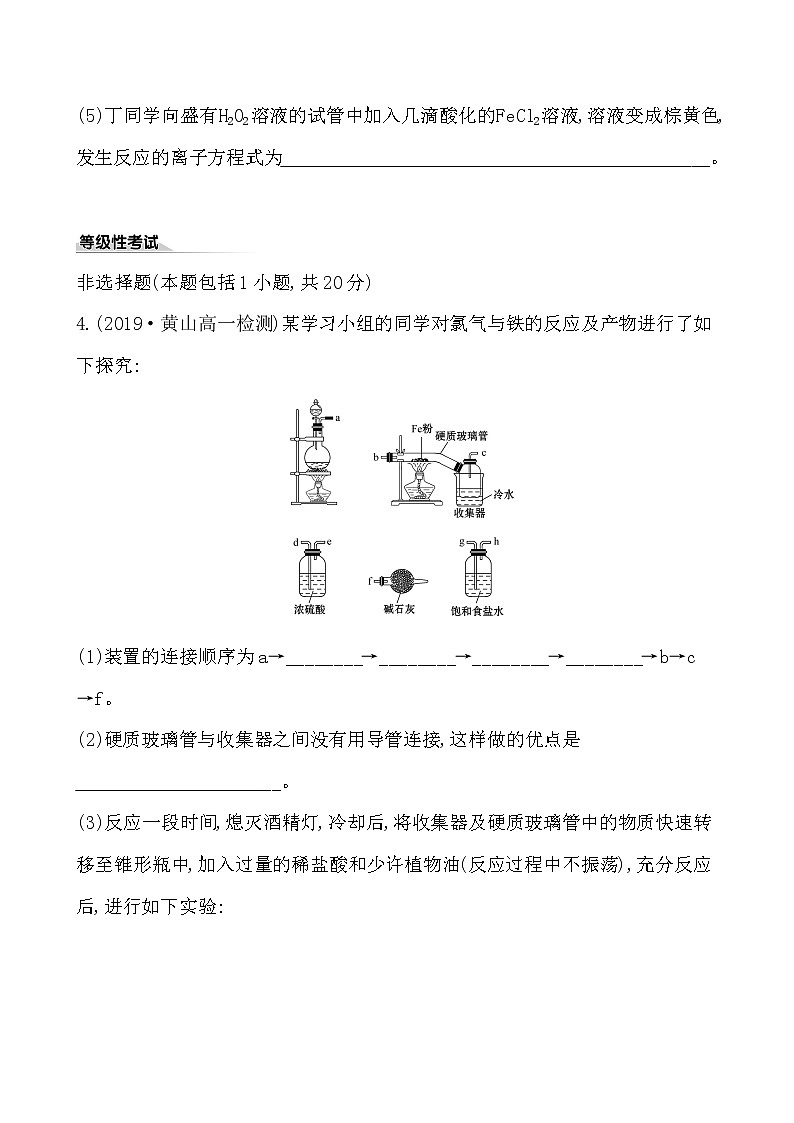
4.(2019·黄山高一检测)某学习小组的同学对氯气与铁的反应及产物进行了如下探究:
(1)装置的连接顺序为a→________→________→________→________→b→c
→f。
(2)硬质玻璃管与收集器之间没有用导管连接,这样做的优点是 __。
(3)反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
试剂X中溶质的化学式为________;固体产物的成分可能为________(填字母)。
A.Fe和FeCl3
B.FeCl2和FeCl3
C.Fe、FeCl2和FeCl3
D.Fe和FeCl2
(4)加入少许植物油的作用是 __, 加入新制氯水后溶液红色加深的原因: __(用离子方程式表示)。
(5)现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe)∶n(Cl)
=1∶2.1,则该样品中FeCl3的物质的量分数为________。(计算结果保留两位有效数字)
铁盐和亚铁盐
(30分钟 50分)
一、选择题(本题包括2小题,每小题5分,共10分)
1.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是( )
【解析】选D。A项中Fe3+将I-氧化为I2,淀粉遇碘单质变蓝;B项中红棕色斑点是Fe2O3;C项中铁与盐酸反应生成Fe2+。
2.下列除杂的操作不正确的是( )
A.MgCl2溶液中混有少量FeCl3:加入足量镁充分反应后过滤
B.FeCl2溶液中混有少量FeCl3:加入过量铁粉充分反应后过滤
C.CuCl2溶液中混有少量FeCl3:加入NaOH溶液充分反应后过滤
D.CuCl2溶液中混有少量FeCl2:先加入H2O2将Fe2+氧化成Fe3+,再加入CuO充分反应后过滤
【解析】选C。FeCl3溶液中加入足量Mg,能除去Fe3+,A正确;加入过量铁粉,FeCl3与Fe反应生成FeCl2而达到除杂的目的,B正确;先用H2O2将Fe2+氧化成Fe3+,再利用FeCl3的水解,加入的CuO与H+反应将Fe3+转化成Fe(OH)3而除去,D正确;C项中加入NaOH溶液,Cu2+、Fe3+均转化成氢氧化物沉淀,不符合除杂要求。
【补偿训练】
将1.12 g铁粉加入25 mL 2 ml·L-1的氯化铁溶液中,充分反应后,其结果是
( )
A.铁粉剩余,溶液呈浅绿色,Cl-基本不变
B.向溶液中滴入无色KSCN溶液,不显红色
C.溶液中Fe2+与Fe3+物质的量之比为6∶1
D.氧化产物与还原产物的物质的量之比为2∶5
【解析】选C。n(Fe)=0.02 ml,n(FeCl3)=0.05 ml,由Fe+2Fe3+3Fe2+知,Fe3+过量0.01 ml,铁粉全部溶解,反应生成Fe2+ 0.06 ml,故A错误、C正确;Fe3+过量,滴入无色KSCN溶液,溶液显红色,故B错误;氧化生成的Fe2+和还原生成的Fe2+的物质的量之比为1∶2,故D错误。
二、非选择题(本题包括1小题,共20分)
3. (2019·哈尔滨高一检测)同学们用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 ml·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是 __。
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为 __。
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是
__。
(4)丙同学取10 mL 0.1 ml·L-1 KI溶液,加入6 mL 0.1 ml·L-1FeCl3溶液混合。取2 mL此溶液于试管中,加入1 mL CCl4充分振荡、静置,CCl4层显紫色,发生反应的离子方程式为 __。
(5)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为 __。
【解析】(1)铁和氯化铁反应生成氯化亚铁,在FeCl2溶液中需加入少量铁屑,其目的是防止氯化亚铁被氧化。
(2)氯气具有氧化性,能氧化氯化亚铁为氯化铁,反应的离子方程式为2Fe2++Cl2
2Fe3++2Cl-。
(3)煤油不溶于水,密度比水小,分层后可以隔离溶液与空气接触,排除氧气对实验的影响。
(4)CCl4层显紫色说明有单质碘生成,这是由于铁离子氧化碘化钾,发生反应的离子方程式为2Fe3++2I-2Fe2++I2。
(5)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,说明过氧化氢氧化亚铁离子为铁离子,反应的离子方程式为H2O2+2Fe2++2H+2Fe3++2H2O。
答案:(1)防止Fe2+被氧化
(2)2Fe2++Cl22Fe3++2Cl-
(3)隔绝空气(排除氧气对实验的影响)
(4)2Fe3++2I-2Fe2++I2
(5)H2O2+2Fe2++2H+2Fe3++2H2O
【易错警示】警惕Fe2+的还原性、Fe3+的氧化性
设置实验情境考查Fe2+的还原性,Fe3+的氧化性及其检验方法,是一种常见的题型。需要注意的是:
(1)Fe2+的还原性大于Br-的,但比I-的弱。亚铁盐在溶液中遇到强氧化剂(如氯气、硝酸、酸性高锰酸钾溶液、溴水、双氧水等)时,一般能被氧化成铁盐。
(2)Fe3+具有较强的氧化性,可跟Fe、Cu及SO2、H2S、HI等还原性物质反应,还原产物为Fe2+。
非选择题(本题包括1小题,共20分)
4.(2019·黄山高一检测)某学习小组的同学对氯气与铁的反应及产物进行了如下探究:
(1)装置的连接顺序为a→________→________→________→________→b→c
→f。
(2)硬质玻璃管与收集器之间没有用导管连接,这样做的优点是 __。
(3)反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
试剂X中溶质的化学式为________;固体产物的成分可能为________(填字母)。
A.Fe和FeCl3
B.FeCl2和FeCl3
C.Fe、FeCl2和FeCl3
D.Fe和FeCl2
(4)加入少许植物油的作用是 __, 加入新制氯水后溶液红色加深的原因: __(用离子方程式表示)。
(5)现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe)∶n(Cl)
=1∶2.1,则该样品中FeCl3的物质的量分数为________。(计算结果保留两位有效数字)
【解析】 (1)浓硫酸具有吸水性,能作氯气的干燥剂,碱石灰具有碱性而吸收氯气,饱和食盐水吸收氯化氢而抑制氯气溶解。装置的排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理。
(2)Fe在氯气中燃烧生成棕褐色烟,冷却易生成固体,导气管口较细,易堵塞,所以硬质玻璃管与收集器之间没有用导管连接。
(3) Fe3+用KSCN溶液检验,Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈红色,所以试剂X为KSCN溶液;固体和氯气反应时可能没有完全反应,剩余的Fe和稀盐酸、氯化铁反应生成氯化亚铁,固体中成分可能为Fe和FeCl3,A选项正确。
(4) Fe2+不稳定易被氧化,所以植物油的作用是隔绝空气,防止Fe2+被氧化;Fe2+被氯气氧化生成Fe3+,从而增大了Fe3+的浓度,Fe3+、SCN-反应生成Fe(SCN)3,从而增大了络合物浓度,溶液颜色加深,离子方程式为2Fe2++Cl22Fe3++2C1- 。
(5)FeCl2和FeCl3的混合物的样品中FeCl2物质的量为x,FeCl3的物质的量为y,则(x+y)∶(2x+3y)=1∶2.1,得到x∶y=9∶1,则样品中氯化铁的物质的量分数=×100%=10%。
答案:(1)g h d e (2) 防止堵塞
(3)KSCN(或NH4SCN) A
(4)隔绝空气,防止Fe2+被氧化
2Fe2++Cl22Fe3++2C1-
(5) 0.10或10%
选项
操作、现象
解释
A
向KI-淀粉溶液中加入FeCl3溶液,溶液变蓝
Fe3+能与淀粉发生显色反应
B
把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点
铁在潮湿的空气中易生成
Fe(OH)3
C
向盐酸中加入少量铁粉,有气泡产生
说明Fe被氧化为Fe3+
D
新制Fe(OH)2露置于空气中一段时间,白色物质变成了红褐色
说明Fe(OH)2易被O2氧化成Fe(OH)3
选项
操作、现象
解释
A
向KI-淀粉溶液中加入FeCl3溶液,溶液变蓝
Fe3+能与淀粉发生显色反应
B
把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点
铁在潮湿的空气中易生成
Fe(OH)3
C
向盐酸中加入少量铁粉,有气泡产生
说明Fe被氧化为Fe3+
D
新制Fe(OH)2露置于空气中一段时间,白色物质变成了红褐色
说明Fe(OH)2易被O2氧化成Fe(OH)3
人教版 (2019)必修 第一册第一节 铁及其化合物课时练习: 这是一份人教版 (2019)必修 第一册第一节 铁及其化合物课时练习,文件包含新教材精创312铁的氢氧化物铁盐和亚铁盐练习2解析版docx、新教材精创312铁的氢氧化物铁盐和亚铁盐练习2原卷版docx等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
高中化学人教版 (2019)必修 第一册第一节 铁及其化合物同步测试题: 这是一份高中化学人教版 (2019)必修 第一册第一节 铁及其化合物同步测试题,文件包含新教材精创312铁的氢氧化物铁盐和亚铁盐练习1解析版docx、新教材精创312铁的氢氧化物铁盐和亚铁盐练习1原卷版docx等2份试卷配套教学资源,其中试卷共13页, 欢迎下载使用。
鲁科版 (2019)必修 第一册第1节 铁的多样性一课一练: 这是一份鲁科版 (2019)必修 第一册第1节 铁的多样性一课一练,共3页。试卷主要包含了将1,下列离子方程式中,正确的是等内容,欢迎下载使用。














