


化学九年级下册课题2 酸和碱的中和反应多媒体教学课件ppt
展开[主要成分] 每粒含氢氧化铝140mg,维生素U50mg,颠茄提取物l0mg。 [药理作用]用于胃酸过多、慢性胃炎 胃痉挛等。
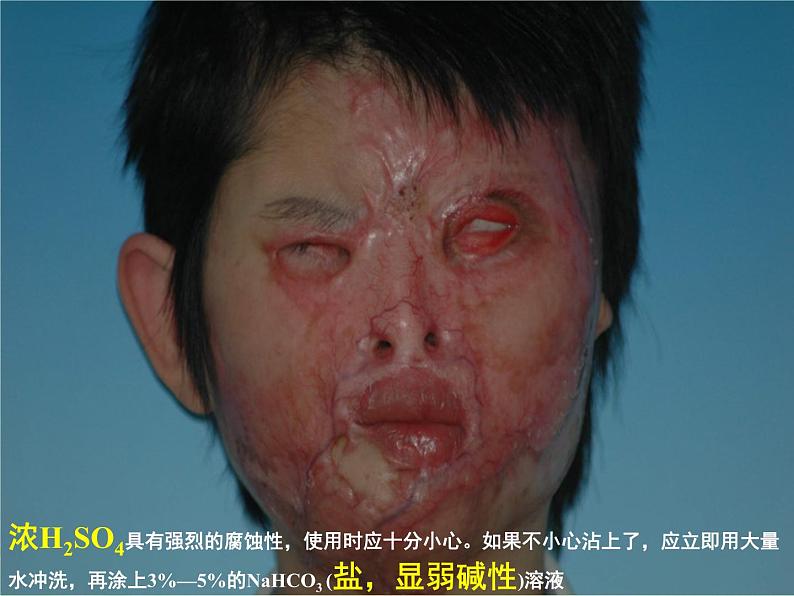
浓H2SO4具有强烈的腐蚀性,使用时应十分小心。如果不小心沾上了,应立即用大量水冲洗,再涂上3%—5%的NaHCO3 (盐,显弱碱性)溶液
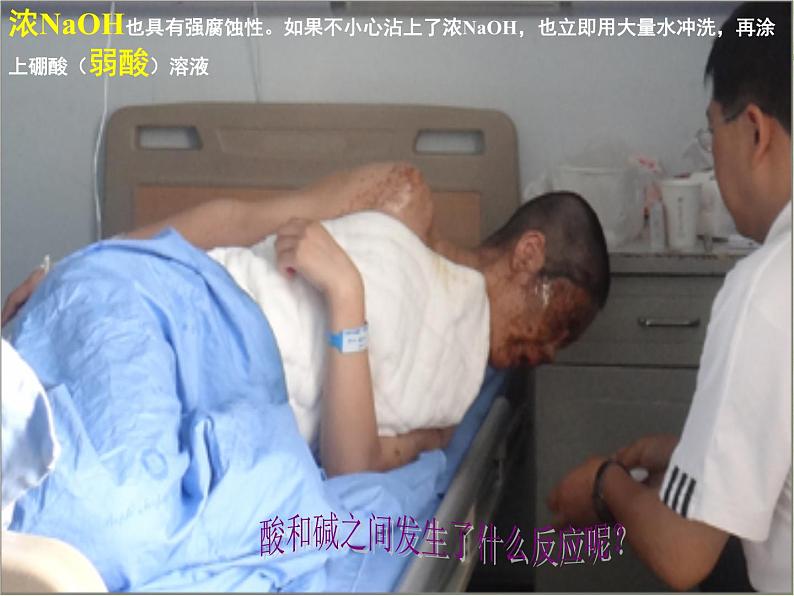
浓NaOH也具有强腐蚀性。如果不小心沾上了浓NaOH,也立即用大量水冲洗,再涂上硼酸(弱酸)溶液
酸和碱之间发生了什么反应呢?
第十单元 课题2 酸和碱的中和反应
学习目标: 1、了解中和反应的特征,知道酸和碱发生中和反应,生成盐和水; 2、学会书写中和反应的化学方程式; 3、了解中和反应在生活实际中的应用;学习重点: 1、什么是中和反应; 2、中和反应在生活实际中的应用;完成预习导学(课前完成)
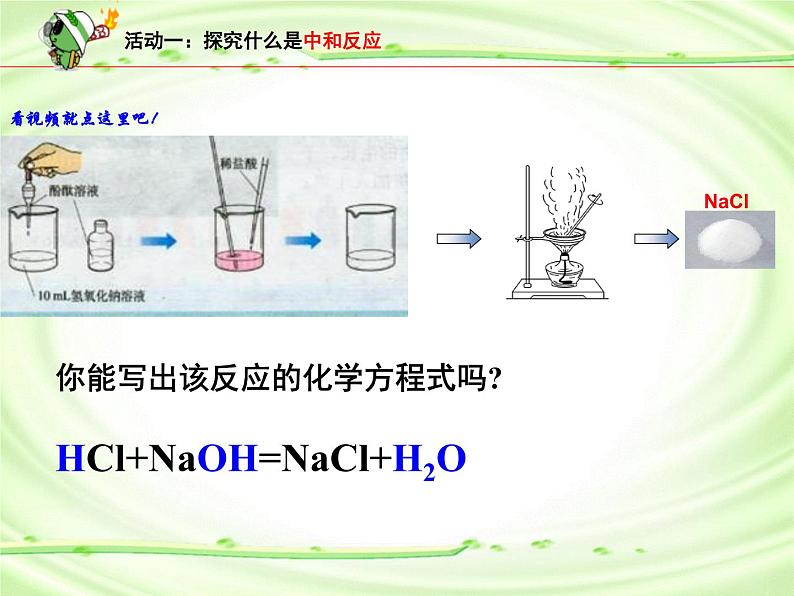
活动一:探究什么是中和反应
你能写出该反应的化学方程式吗?HCl+NaOH=NaCl+H2O
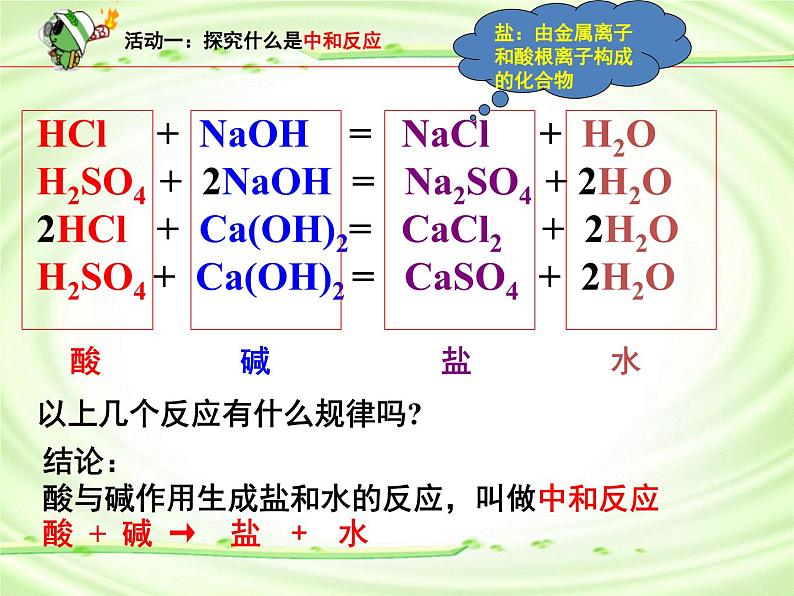
HCl + NaOH = NaCl + H2OH2SO4 + 2NaOH = Na2SO4 + 2H2O2HCl + Ca(OH)2= CaCl2 + 2H2OH2SO4 + Ca(OH)2 = CaSO4 + 2H2O以上几个反应有什么规律吗?
酸 碱 盐 水
盐:由金属离子和酸根离子构成的化合物
结论:酸与碱作用生成盐和水的反应,叫做中和反应酸 + 碱 → 盐 + 水
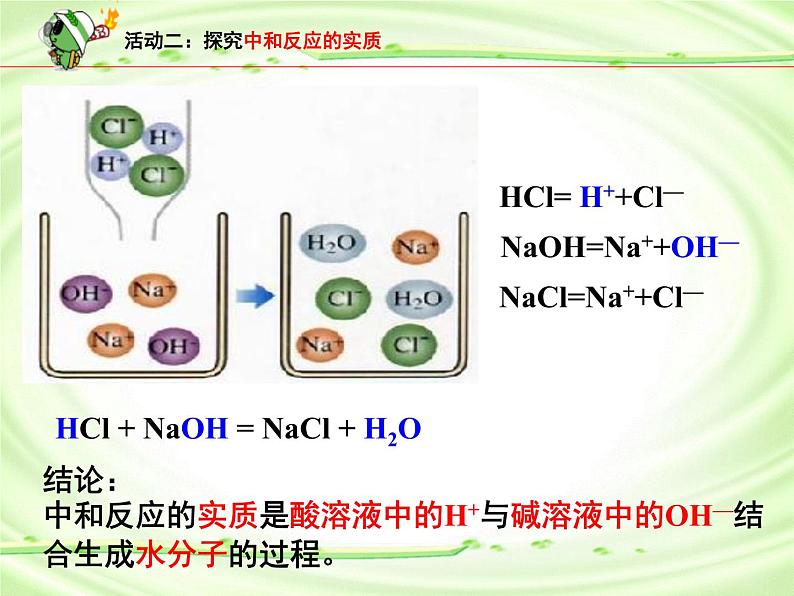
活动二:探究中和反应的实质
HCl= H++Cl—
NaOH=Na++OH—
HCl + NaOH = NaCl + H2O
结论:中和反应的实质是酸溶液中的H+与碱溶液中的OH—结合生成水分子的过程。
NaCl=Na++Cl—
1、改变土壤的酸碱性植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长。
思考:应怎样去改变酸性土壤?
交流:能用生石灰代替熟石灰吗?为什么?
当然可以。因为 CaO + H2O = Ca(OH)2
活动三:探究中和反应在实际中的应用
某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢?
应在排放前用碱性物质(例如熟石灰)进行中和处理。
Ca(OH)2 + H2 SO4 = CaSO4 + 2H2O
Al(OH)3 + 3HCl = AlCl3 + 3H2O
3、用于医药胃酸的主要成分是:斯达舒胶囊的主要成分:氢氧化铝能中和胃酸,试写出其化学方程式:
斯达舒说明书[药品名称]斯达舒胶囊[性状]本品为胶囊剂, 内容物为白色粉末[主要成分] 每粒含氢氧化铝140mg,维生素U50mg,颠茄提取物l0mg。 [药理作用]中和胃酸过多、慢性胃炎 胃痉挛等。 [用法与用量]口服,一次1粒,一日3次
轻松一下:新版泰囧正在上演……
我的健康树快死了,怎么办呀?
王宝宝为妈妈种的健康树被酸雨腐蚀了……
Ca(OH)2 +H2SO4 = CaSO4 +2H2O
王宝宝正在河边洗头,上游印染厂的碱性废水没有处理就排放了。
你印染厂的水为什么不处理,看我的头发成什么颜色了!
第一次去泰国的王宝宝,觉得的泰国菜太好吃了,不知不觉就吃多了,吐酸水。
胃酸过多的病人可服用胃舒平:Al(OH)3+3HCl=AlCl3+3H2O
我的胃好痛呀!妈呀!娘呀!苍天呀!大地呀!
王宝宝正与一“白富美”合影,蚊子(蚊子咬人会分泌蚁酸)又来捣乱。
我的收获: 1、中和反应:酸与碱作用生成盐和水的反应叫中和反应 酸 + 碱 → 盐 + 水 (盐:由金属离子和酸根离子构成的化合物叫做盐。盐在水溶液中能解离出金属离子和酸根离子 ) 2、中和反应的实质:中和反应就是酸溶液中的H+与碱溶液中的OH—结合生成水分子的过程。 3、中和反应在实际中的应用: ①农业上:调节土壤的酸碱性 ②工业上:处理生产污水 ③医药上:中和胃酸,制成含碱性药水,防蚊虫叮咬课外延伸: 1、皮蛋味涩,如何做可除去涩味?亲自动手做做看。 2、醋可以将热水瓶胆壁上的水垢(主要成份是CaCO3、Mg(OH)2)除掉,原理是什么? 3、找找身边还有哪些应用中和反应的事例?
注:CaSO4微溶于水,BaSO4不溶于水。(详见P114附录部分酸、碱和盐的溶解性表)
酸 + 碱 → 盐 + H2O
人教版九年级下册课题2 酸和碱的中和反应课堂教学课件ppt: 这是一份人教版九年级下册课题2 酸和碱的中和反应课堂教学课件ppt,共23页。PPT课件主要包含了酸碱之间可以发生反应,怎样处理呢等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 酸和碱的中和反应示范课课件ppt: 这是一份初中化学人教版九年级下册课题2 酸和碱的中和反应示范课课件ppt,共19页。PPT课件主要包含了一实验探究,中和反应,课堂练习一,改变土壤的酸碱性,处理工厂的废水,课堂练习二等内容,欢迎下载使用。
人教版九年级下册课题2 酸和碱的中和反应教案配套课件ppt: 这是一份人教版九年级下册课题2 酸和碱的中和反应教案配套课件ppt,共20页。PPT课件主要包含了酸和碱能反应,微观世界,或铵根离子,中和反应,●改良酸性土壤,●处理工厂废水,●生活中用于医药,◆中和胃酸,◆防蚊虫叮咬,改良酸性土壤等内容,欢迎下载使用。














