





2026年中考化学备考复习课件:第一部分 考点大梳理 第五讲 金属与金属材料
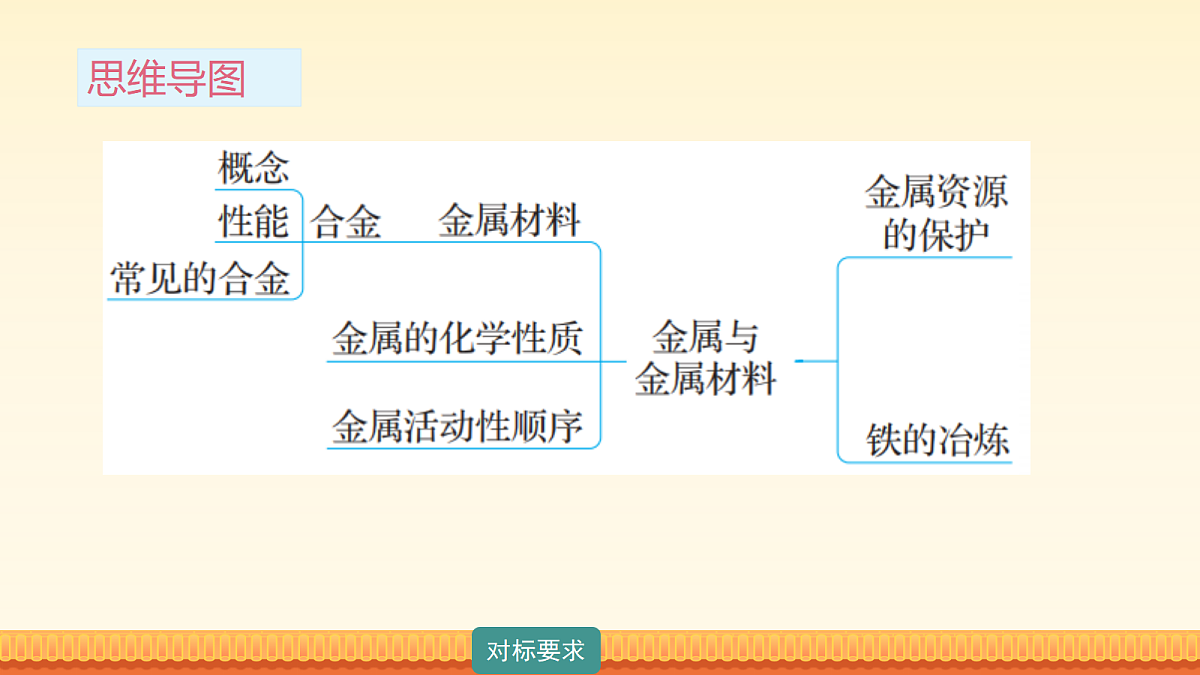
展开 这是一份2026年中考化学备考复习课件:第一部分 考点大梳理 第五讲 金属与金属材料,共48页。PPT课件主要包含了思维导图,知识归纳,化学方程式归纳,知识点1金属材料,纯金属,4合金,非金属,人造骨骼,MgO,Al2O3等内容,欢迎下载使用。
1.知道金属的物理性质,认识常见金属的主要化学性质及金属活动性顺序。 2.了解常见合金,知道金属材料在生产生活和社会发展中的重要作用。 3.了解高炉炼铁,知道铁生锈条件 ,了解防止金属腐蚀的常用方法及废弃金属对环境的影响。
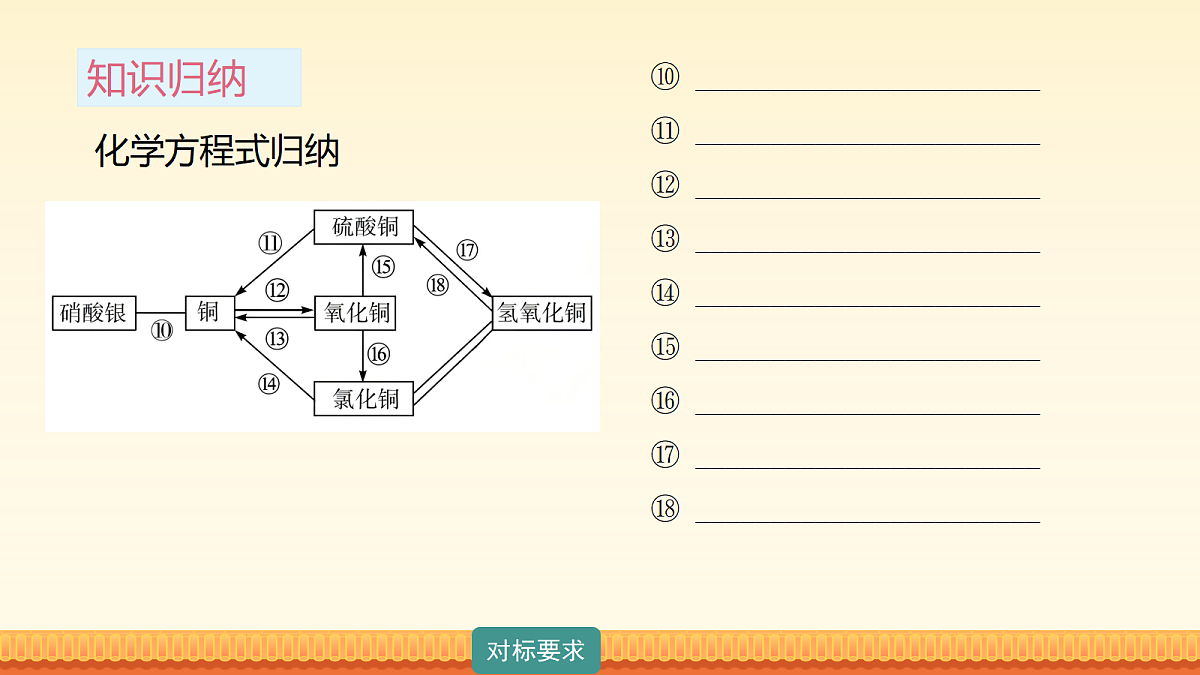
① _______________________② _______________________③ _______________________④ _______________________⑤ _______________________⑥ _______________________⑦ _______________________⑧ _______________________⑨ _______________________
⑩ _______________________⑪ _______________________⑫ _______________________⑬ _______________________⑭ _______________________⑮ _______________________⑯ _______________________⑰ _______________________⑱ _______________________
1.金属材料:包括______以及它们的______。2.金属的物理性质及用途(1)金属的物理性质:有金属光泽,密度较____,硬度较____,熔点较____,具有____性、____性、____性。(2)金属的用途:在生活与生产中用途广泛,如用作电线、钻头等。(3)金属特性:大多数金属呈银白色,铜呈____色,金呈____色;常温下,大多金属都是固体,但汞 (俗称:水银)为____。
3.金属之最(1)地壳中含量最高的金属元素是____。(2)目前世界年产量最高的金属是____。(3)人体中含量最高的金属元素是____。(4)导电、导热性最好的金属是____。(5)熔点最高的金属是____(常用作灯丝)。(6)熔点最低的金属是____。
知识点2 金属的化学性质
2AlCl3+3H2↑
3Cu+Al2(SO4)3
Cu(NO3)2+2Ag
知识点3 金属活动性顺序
知识点4 铁的锈蚀、冶炼与防护1.铁的锈蚀与防护。
实验 铁制品锈蚀条件的探究
【实验方法】控制变量法:通过对比的方法寻找变量,在研究单一变量时,控制其他变量不变。如实验装置图中提供锈蚀所需的一个条件而控制另一个条件不变,观察铁钉是否锈蚀。【实验现象及分析】 【实验装置】
A中铁钉生锈,B中无变化
【实验结论】铁制品生锈的条件是与_____、_____同时接触。【注意事项】(1)实验前,为除去铁钉表面的污物,需进行的操作是_________________。(2)实验B中植物油的作用是______________________________________。【创新装置】(1)实验装置一体化:增强了实验的对比性,实验现象更明显(图1)。(2)实验原理创新(图2)。
防止空气中的氧气溶于蒸馏水,导致铁钉生锈
例1 (2025·辽宁)下列制品主要利用金属导热性的是( )A.铁锅 B.铜导线C.金饰品D.铝制易拉罐
命题点2 金属的化学性质
例2 金属有重要的化学性质。(1)“真金不怕火炼”说明金的化学性质______。(2)实验室用锌粒与稀硫酸反应的制取氢气的化学方程式是__________________________________。该反应的基本反应类型是___________。(3)把打磨过的铜丝放入硝酸银溶液中,观察到__________________________________________________。
有银白色固体析出,溶液由无色变为蓝色
命题点3 金属活动性顺序
例3 (2024·株洲)现有X、Y 、Z三种金属,为探究其金属活动性顺序,进行了如下实验:①将X和Z分别放入稀硫酸中,X溶解并产生氢气,Z不反应;②将Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。则有关X、Y、Z的金属活动性顺序正确的是( )
A.X>Y>Z B.X>Z>YC.Y>X>Z D.Z>X>Y
例4 我国有着悠久的钢铁冶炼史,《天工开物》中记载的“炒钢法”,该方法的生产过程可用下图表示。
根据图文回答下列问题。(资料:①潮泥灰主要成分是石灰石;②铁的熔点是1535℃) (1)常见的铁矿石有赤铁矿和(填一种)_________________。 (2)不断鼓入空气的目的是____________。
(3)炼铁炉中生成铁的化学方程式为___________________________________________________________________。(4)撒入潮泥灰主要作用是______。不断翻炒液态生铁,是为了降低______元素的含量。(5)钢的性能优良,如钢的熔点比纯铁_______,易于加工。
命题点5 铁的锈蚀与防护
例5 (2025·陕西)某学习小组同学探究铁钉锈蚀的条件时做了如图所示的实验。(1)一段时间后,实验①中铁钉锈蚀最严重的部位是___(填“a”“b”或“c”)。(2)上述实验能证明铁钉锈蚀与____________有关。(3)用稀盐酸或稀硫酸清除上述实验后锈蚀铁钉表面的铁锈时,发生反应的化学方程式为______________________________________________________________________________________________________(任写一个)。
Fe2O3十3H2SO4══Fe2(SO4)3十3H2O (或 Fe2O3十6HCl══2FeCl3十3H2O)
1.(2025·广东)古丝绸之路贸易中的下列商品,主要成分属于金属材料的是( )A.丝绸 B.瓷器 C.玉器 D.铁器2.(2025·广西)下列对铁片的处理方式中,容易导致其生锈的是( )A.在表面喷漆 B.制成不锈钢C.在表面涂油 D.泡在海水中
3.(2025·苏州)白炽灯泡的结构如下图所示,通电后钨丝在高温下发光。生产时灯泡内可能会混入少量氧气。下列说法正确的是( )A.钨丝的熔点低B.两侧的金属丝不导电C.灯泡内填充氮气是因为其化学性质活泼D.白炽灯工作时,红磷能消耗残留氧气
4.(2025·河南)金属在改善人类生活方面发挥着巨大作用。下列相关叙述不正确的是( )A.纯铜的硬度比黄铜的大B.钛合金具有良好的抗腐蚀性能C.铁制品刷漆可防止生锈D.回收废旧金属可实现资源再利用
5.(2025·云南)云南斑铜“妙在有斑,贵在浑厚”,其制作技艺是国家非物质文化遗产。(1)《滇南闻见录》记载:“自来铜(铜基合金),不可经火,须生锤成器”,通过捶打将斑铜塑成不同形状,体现了金属的_________性。斑铜的熔点比纯铜_________(填“高”或“低”)
(2)斑铜主要含有铜、锌、锡、铁等。用下图所示装置及药品,通过一次实验验证锌、铁、铜的金属活动性,回答下列问题。① 组装好装置,装入药品前,应先_______________________________。②集气瓶中金属B和溶液X可能的组合为______________________(任填一组)。
Fe与稀硫酸(合理即可)
6.(2024·云南)铜是重要的金属资源,它对于改善人类生活、促进人类文明起着重要作用。(1)铜的认识:生活中常用铜作为导线,体现了铜良好的延展性和______性。(2)铜的冶炼:黄铜矿的主要成分是CuFeS2,根据其主要成分的组成元素,推断用黄铜矿炼铜过程中产生形成酸雨的空气污染物是______(填化学式)。
(3)铜的加工:青铜是金属冶铸史上最早的合金,其主要成分是铜和锡。表中的A和B分别表示铜和青铜中的一种。《吕氏春秋》记载:“金(铜)柔锡柔,合两柔则刚”,据此判断A是_____。注:硬度以金刚石的硬度为10作为标准,1表示很软,10表示很硬。(4)铜的锈蚀:铜在潮湿的空气中锈蚀的反应为:X的化学式为_________。
(5)铜的回收:某工厂的废水经预处理后得到含FeSO4和CuSO4的溶液。为了减少污染并促进废物利用,工厂设计以下流程回收Cu和FeSO4。①步骤Ⅰ中发生反应的化学方程式为_______________________________。②溶液C中的溶质是___________。
Fe+CuSO4══FeSO4 +Cu
1.防雷击要远离金属制品。因为金属具有( )A.导热性 B.导电性 C.延展性 D.光泽
2.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材 料制成。下列金属防护措施不正确的是( )A.在金属制品表面镀保护层B.改变金属结构制成合金使用C.在金属制品表面涂油漆D.用稀盐酸定期清洗金属制品
3.(2025·吉林)1956年,在吉林省诞生了新中国第一辆解放牌汽车。生产汽车的材料中,属于金属材料的是( )A.合金 B.橡胶C.塑料 D.玻璃
4.下列各项比较中,正确的是( )A.含碳量:生铁>钢B.耐腐蚀性:铁>铝C.地壳中元素含量:铁>铝D.熔点:青铜>铜5.可通过金属与稀盐酸反应直接得到的物质是( )A.氯化锌 B.氯化银C.氯化铜 D.氯化铁
6.如图是炼铁高炉示意图,下列说法正确的是( )A.焦炭的主要作用是提供热量、产生二氧化碳B.石灰石的作用是与铁矿石中的杂质反应形成炉渣C.生铁出口位置低于炉渣出口的原因是生铁密度小于炉渣D.产生的废气无须处理,因为它不会污染空气
7.现有一定质量的由两种金属组成的混合物。加入过量的稀盐酸,充分反应,测得生成H2 0.2g,将反应后的溶液蒸发,得到11.1g固体。则金属混合物的组成不可能是( )A.Mg Fe B.Fe ZnC.Zn Mg D.Al Fe
8.A是目前世界年产量最高的金属,据图回答下列问题。(1)B的名称是____________。(2)溶液C中溶质的化学式为_______。(3)D可用于制_____,③可证明铁的金属活动性比铜____(填“强”或“弱”)。(4)②的基本反应类型是__________。(5)④的化学方程式为_________________________________。
9.(2024·天津)金属材料在生产、生活中具有广泛的用途。(1)“天津之眼”摩天轮的轿厢使用铝合金材料,利用铝合金的性质是____(填字母)。A.良好的导电、导热性B.密度小且抗腐蚀性强(2)工业上炼铁原理是利用一氧化碳与氧化铁在高温下反应,化学方程式为_________________________________________。
(3)“乌铜走银”是我国特有的铜制工艺技术,迄今已有300余年的历史。该工艺的废料经初步处理后可得到硝酸银和硝酸铜的混合溶液,向其中加入一定量的金属锌,充分反应后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,有气泡产生,则滤液中含有的溶质为___________(填化学式)。(4)我国神舟载人飞船上的天线使用了钛镍合金,其中镍(Ni)和铁的金属活动性相近,该元素常见的化合价为+2价。将8g镍加入一定量的硫酸铜溶液中,充分反应后过滤,得到金属混合物8.5g,则该混合物中铜的质量为 _______g。
10.(2024·济宁)某一工厂的金属废料中含有铜、铁、金等金属单质,为回收铜和金并得到氧化铁。工作人员设计了如下图所示的工艺流程。请回答下列问题。(1)滤液A的溶质为__________。(填化学式)(2)固体A与空气加热发生化学反应,写出反应后的生成物与适量稀硫酸反应的化学方程式:__________________________________
CuO+H2SO4══CuSO4+H2O
(3)操作1和操作2为同一操作,两操作中用到的玻璃仪器有玻璃棒、烧杯和_____________。(4)往滤液B中加入的物质X是___________。
11.(2024·湖南)铁制品经常有锈蚀现象,于是某兴趣小组围绕“锈”进行一系列研究。(1)探锈现有洁净无锈的铁钉、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙,还可以选用其他物品。为探究铁制品锈蚀的条件,设计如下实验。①A中玻璃仪器的名称是_________。②一周后,观察A、B、C中的铁钉,只有A中的铁钉出现明显锈蚀现象,由此得出铁钉锈蚀需要与_________________接触的结论。
(2)除锈取出生锈的铁钉,将其放置在稀盐酸中,一段时间后发现溶液变黄,铁钉表面有少量气泡产生。产生气泡的原因是________________________(用化学方程式表示)。稀盐酸可用于除锈,但铁制品不可长时间浸泡其中。(3)防锈防止铁制品锈蚀,可以破坏其锈蚀的条件,常用的防锈方法有____________________(写一种即可)。兴趣小组继续通过文献研究、调研访谈,发现如何防止金属锈蚀已成为科学研究和技术领域中的重要科研课题。
Fe+2HCl══FeCl2 +H2 ↑
表面刷漆、涂油等 (合理即可)
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




