
【化学】河北省廊坊市多校2025-2026学年高一上学期期末考试
展开 这是一份【化学】河北省廊坊市多校2025-2026学年高一上学期期末考试,共8页。试卷主要包含了单选题,填空题,解答题等内容,欢迎下载使用。
1.合金的应用促进了人类社会的发展。下列物品的主要成分不属于合金的是
A.三星堆青铜面具B.“蛟龙”号潜水器耐压外壳
C.不锈钢锅D.塑料管材
【答案】D
2.下列与实验有关的图标和名称不相符的是
【答案】C
3.下列叙述不正确的是
A.金刚石、石墨和C60互为同素异形体
B.丁达尔效应是胶体和溶液的本质区别
C.根据交叉分类法可知,碳酸钠属于钠盐、碳酸盐
D.云和雾属于分散系中的气溶胶
【答案】B
4.在溶液中能大量共存的离子组是
A.CO32-、Na+、ClO-、H+B.NH4+、Na+、HCO3-、OH-
C.H+、Mg2+、CH3COO-、Cl-D.K+、Na+、SO42-、MnO4-
【答案】D
5.下列变化过程中,加入氧化剂才能实现的是
A.Cl2→Cl-B.Cu→CuNO32C.SO2→SO32-D.CuO→Cu
【答案】B
6.下列过程的相关方程式书写正确的是
A.Cl2通入水中制氯水:Cl2+H2O=2H++Cl-+ClO-
B.铁粉与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
C.向氢氧化钡溶液中加入硫酸镁溶液:Ba2++SO42-=BaSO4↓
D.澄清石灰水中Ca(OH)2的电离:Ca(OH)2=Ca2++2OH-
【答案】D
7.下列有关铁、铝及其化合物的叙述正确的是
A.高温下用CO还原铁的氧化物制铁B.FeO在空气中受热,能迅速被氧化为Fe2O3
C.Fe(OH)2不稳定,具有较强的氧化性D.Al2O3与NaOH溶液不反应
【答案】A
8.已知某反应的反应物与生成物为KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O和未知物X,其中Na2SO3是反应物之一,下列说法错误的是
A.未知物X为Na2SO4B.该反应的氧化剂是KIO3
C.还原性:Na2SO3>I2D.该反应中,KIO3发生氧化反应
【答案】D
9.某化学兴趣小组的同学,在学习了钠的性质后,用小刀切割了一小块钠,然后放入盛有空气的集气瓶中,充分燃烧后发现瓶壁上有黑色固体附着,下面是该兴趣小组的几点推测,你认为不合理的是
A.黑色固体是碳
B.钠在燃烧时只发生了一个反应
C.钠在金属活动性顺序中排在镁前面,所以钠能与二氧化碳反应(已知:2Mg+CO22MgO+C)
D.钠保存在煤油中,可能滤纸没有完全吸干煤油,煤油不完全燃烧产生碳
【答案】B
10.下列实验过程不能达到实验目的的是
【答案】A
11.设NA表示阿伏加德罗常数的值。下列说法中正确的是
A.过氧化钠与水反应生成0.1 ml氧气,则转移电子的数目为0.2NA
B.11.2 L O2与CO2的混合气体中所含氧原子的数目为NA
C.1 ml⋅L-1 Na2CO3溶液中所含Na+的数目为2NA
D.100 g质量分数为46%的乙醇(C2H6O)水溶液中所含氧原子的数目为NA
【答案】A
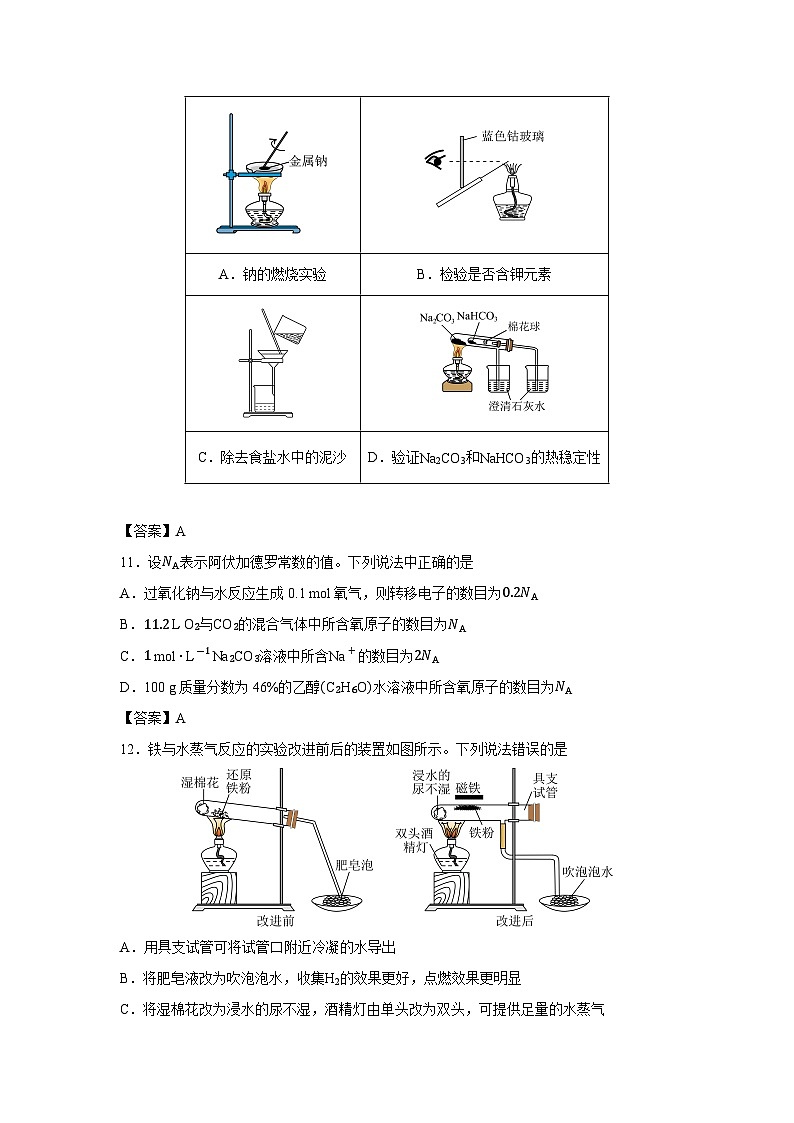
12.铁与水蒸气反应的实验改进前后的装置如图所示。下列说法错误的是
A.用具支试管可将试管口附近冷凝的水导出
B.将肥皂液改为吹泡泡水,收集H2的效果更好,点燃效果更明显
C.将湿棉花改为浸水的尿不湿,酒精灯由单头改为双头,可提供足量的水蒸气
D.改进后,悬挂的磁铁能吸引铁粉,实验过程中,能看到具支试管中有黑色固体不断落下
【答案】D
13.“价—类”二维图是一种学习化学的重要工具,氯的部分“价—类”二维图如下图所示。下列说法错误的是
A.物质a可与水反应生成物质b和cB.物质a和b均能与碱溶液反应生成物质d
C.光照下物质c易分解D.物质e的钙盐是漂白粉的有效成分
【答案】D
14.根据实验目的,下列实验操作及现象和结论都正确的是
【答案】D
二、填空题
15.某同学按下列步骤配制250 mL 0.4 ml⋅L-1 Na2CO3溶液,请回答下列问题。
Ⅰ.(1)配制过程
Ⅱ.误差分析
(2)若配制过程中缺少洗涤步骤,则使所配制溶液的浓度 (填“偏低”“偏高”或“无影响”)。
(3)配制一定体积、一定物质的量浓度的溶液时,下列操作可能使溶液浓度偏高的是___________(填字母)。
A.容量瓶中存留少量蒸馏水
B.在转移溶液的过程中,不慎有少量液体洒在容量瓶外
C.定容时俯视刻度线
D.定容时,发现凹液面超过了刻度线,随即用滴管将多余的溶液吸出
【答案】(1)10.6 天平(或托盘天平)、药匙 加速溶解 防止液体溅出 改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
(2)偏低
(3)C
三、解答题
16.实验室用如图装置制取氯气,并用氯气进行实验。回答下列问题:
(1)仪器B的名称是 。仪器A中盛放浓盐酸,仪器B中盛放MnO2,则反应的离子方程式为 。
(2)装置E中有红色干布条,装置F中有红色湿布条,对比E装置和F装置中产生现象的差异,可得出的结论是 。
(3)装置C和D中盛装的试剂分别为 、 。
(4)装置G中发生反应后的现象为 。
(5)用离子方程式表示试剂X的作用: 。
(6)家庭中常用“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生,但是二者不能同时使用的原因是 (用离子方程式表示)。
【答案】(1)圆底烧瓶 MnO2+4H++2Cl-ΔMn2++Cl2↑+2H2O
(2)Cl2没有漂白性,而HClO(或Cl2与H2O反应生成的HClO)有漂白性
(3)饱和食盐水(或饱和NaCl溶液) 浓硫酸
(4)棉花团变成蓝色
(5)Cl2+2OH-=Cl-+ClO-+H2O
(6)ClO-+Cl-+2H+=Cl2↑+H2O
17.某小组同学依据性质差异,采用比较的方法设计实验鉴别Na2CO3和NaHCO3。
依据上述实验回答问题(在常温下进行实验)。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,试管A中温度计的示数略有降低,试管B中温度计的示数升高。说明固体b溶解于水的过程中 (填“放出”或“吸收”)热量,可判断固体b为 (填化学式)。
(2)实验Ⅱ中,向试管C和D中分别加入5 mL水,充分振荡,试管C中的固体有剩余,试管D中的固体几乎完全溶解。
①判断固体c为 (填化学式)。
②分别向两支试管中滴加2滴酚酞溶液,试管 (填字母)中液体的红色较深。
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,试管F中开始滴加就可以观察到气泡;试管E中开始无气泡产生,一段时间后才产生气泡。用离子方程式解释试管E中开始无气泡产生的原因: 。
(4)写出NaHCO3在水中的电离方程式: 。
(5)下列实验方案中,能测出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是 (填序号)。
①取m g该混合物充分加热,固体质量减少n g
②取m g该混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到n g固体
③取m g该混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加n g
④取m g该混合物与足量NaOH溶液充分反应,得到n g溶液
⑤取m g该混合物与足量CaOH2溶液充分反应,过滤、洗涤、干燥,得到n g固体
⑥取m g该混合物与足量稀硫酸充分反应,逸出气体经无水氯化钙干燥后,用碱石灰充分吸收,碱石灰的质量增加n g
(6)若配制的Na2CO3溶液中混有部分NaHCO3,为确定其纯度,现在取适量溶液,向该溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成CO2的体积和消耗盐酸的体积并绘制成图像如图所示,则V(盐酸)的体积为“4~9”阶段,其反应的离子方程式为 。根据图计算可知,样品中纯碱和小苏打的物质的量之比为 。
【答案】(1)放出 Na2CO3
(2)NaHCO3 D
(3)CO32-+H+=HCO3-
(4)NaHCO3=Na++HCO3-
(5)①②⑤⑥
(6)HCO3-+H+=CO2↑+H2O 4:1
18.明矾[化学式为KAlSO42⋅12H2O]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为Al和Fe)为原料制备明矾的工艺流程如图所示。
已知:pH约为3.7时,铁元素在溶液中主要以FeOH3形式存在。
回答下列问题:
(1)“酸溶”后溶液中主要的金属离子有 、Fe3+。
(2)加入H2O2的目的是 。
(3)“调pH”约为3.7,滤渣②的主要成分是 (填化学式)。
(4)“沉铝”中加入NaHCO3的目的是将Al3+转化为Al(OH)3沉淀同时生成CO2气体,该反应的离子方程式为 。
(5)“操作”包括蒸发浓缩、冷却结晶、 、洗涤、 ,可得到明矾晶体。
(6)在绿色发展理念下,某工厂用a kg废易拉罐(含Al5.4%)制备KAlSO42⋅12H2O[已知KAlSO42⋅12H2O的相对分子质量为474],最终得到产品的质量为b kg,则该产品的产率为 (用分数表示)。(已知:产率=实际产量理论产量×100%)
【答案】(1)Fe2+、Al3+
(2)将“酸溶”后溶液中的Fe2+氧化为Fe3+
(3)Fe(OH)3
(4)Al3++3HCO3-=Al(OH)3↓+3CO2↑
(5)过滤 干燥
(6)250b237a×100%A.护目镜
B.用电
C.热烫
D.锐器
A.钠的燃烧实验
B.检验是否含钾元素
C.除去食盐水中的泥沙
D.验证Na2CO3和NaHCO3的热稳定性
选项
实验目的
实验操作及现象
结论
A
检验FeCl3溶液中是否混有Fe2+
将待测溶液滴入酸性KMnO4溶液中,紫色褪去
溶液中存在Fe2+
B
检验溶液中是否含有CO32-
向待测溶液中滴加稀盐酸,产生无色、无味且能使澄清石灰水变浑浊的气体
该溶液中一定含有CO32-
C
检验某盐中是否含有Cl-
向某盐的溶液中滴入适量稀盐酸,无现象,再滴入AgNO3溶液产生白色沉淀
该盐中一定含有Cl-
D
探究Na2O与水反应的产物
将1~2 mL水滴入盛有1~2 g Na2O固体的试管中,再滴入2滴酚酞溶液,溶液变红
反应生成了NaOH
实验步骤
有关问题
计算所需Na2CO3固体的质量
需要Na2CO3固体的质量为 g。
称量Na2CO3固体
称量过程中用到的主要仪器有 。
将Na2CO3放入100 mL烧杯中加水溶解
溶解时用玻璃棒不断搅拌的目的是 。
将烧杯中的溶液转移至250 mL容量瓶中
转移时用玻璃棒引流的作用是 。
向容量瓶中加蒸馏水至刻度线
当加入蒸馏水至液面距离刻度线1~2 cm时, 。(补全操作)
实验Ⅰ
实验Ⅱ
实验Ⅲ
相关试卷
这是一份【化学】河北省廊坊市多校2025-2026学年高一上学期期末考试,共8页。试卷主要包含了单选题,填空题,解答题等内容,欢迎下载使用。
这是一份2025-2026学年河北省廊坊市多校高一上学期期末考试化学试卷,共8页。试卷主要包含了单选题,填空题,解答题等内容,欢迎下载使用。
这是一份河北廊坊市2025-2026学年高一上学期期末考试 化学试题,共3页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 









