

上海市嘉定区第一中学2025-2026学年高二上学期期末化学试题(原卷版+解析版)
展开 这是一份上海市嘉定区第一中学2025-2026学年高二上学期期末化学试题(原卷版+解析版),共29页。试卷主要包含了有机物的结构与性质,阿司匹林的前世今生,含酚废水处理,白花丹酸的合成,对甲苯磺酸的制备等内容,欢迎下载使用。
说明:本试题的选择题,没有特别注明,为单选题,只有一个正确选项;若注明不定项,有1-2个正确选项,多选、错选不得分,漏选得一半分数。
可能用到的相对原子质量:
一、有机物的结构与性质
有机化合物的结构和性质之间有着密不可分的关系
1. 下列有机物的命名正确的是__________。
A. 1,3,4-三甲苯
B. 3-甲基戊烯
C. 2,3,4-三甲基-2-乙基戊烷
D. 2-溴戊烷
2. 会分类使化学学习事半功倍。下列关于有机化合物的分类正确的是__________。
A. 属于脂环化合物B. 属于芳香烃
C. 属于环烷烃D. 属于醛类
3. 一种由乙烯合成乙二醇的路线如下图所示,下列说法正确的是__________。
A. 乙二醇可以发生酯化、还原反应
B. 环氧乙烷的分子式为
C. 环氧乙烷与乙二醇互为同系物
D. 已知反应②原子利用率为,则物质X是
4. 如图是常见四种有机物的空间填充模型示意图。下列说法正确的是__________。
A. 甲能使酸性高锰酸钾溶液褪色
B. 乙可与溴水发生取代反应使溴水褪色
C. 丙在铁作催化剂下与溴水发生取代反应
D. 丁在浓硫酸作用下可与乙酸发生取代反应
5. 我国科研人员发现中药成分黄芩素能明显抑制新冠病毒的活性。下列关于黄芩素的说法不正确的是__________。
A. 分子中有3种官能团
B. 能与溶液反应
C. 空气中可发生氧化反应
D. 能和发生取代反应和加成反应
6. 我国首个自主研发的胆固醇吸收抑制剂海博麦布的结构简式如图。下列说法不正确的是__________。(不定项)
A. 该分子不存在顺反异构体
B. 该分子中含有1个手性碳原子
C. 该物质既能与HCl反应,也能与NaOH反应
D. 该物质既能发生氧化反应,也能发生还原反应
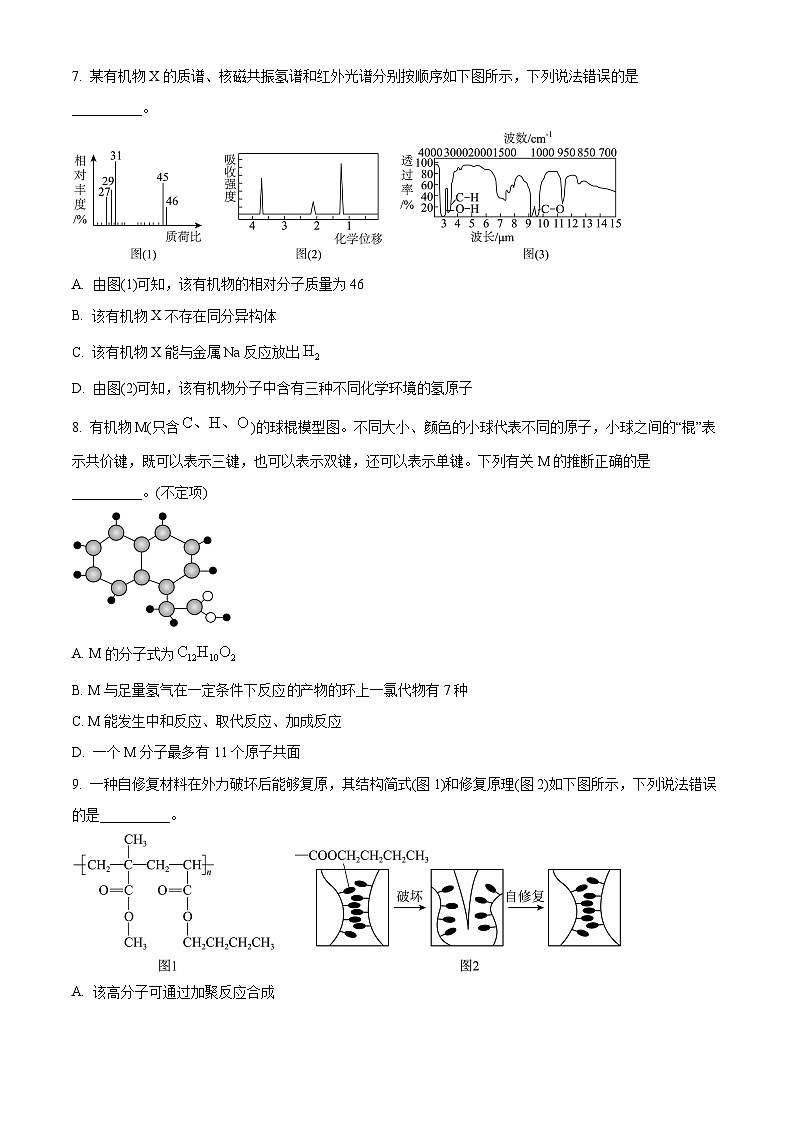
7. 某有机物X的质谱、核磁共振氢谱和红外光谱分别按顺序如下图所示,下列说法错误的是__________。
A. 由图(1)可知,该有机物的相对分子质量为46
B. 该有机物X不存在同分异构体
C. 该有机物X能与金属Na反应放出
D. 由图(2)可知,该有机物分子中含有三种不同化学环境的氢原子
8. 有机物M(只含)的球棍模型图。不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键。下列有关M的推断正确的是__________。(不定项)
A. M的分子式为
B. M与足量氢气在一定条件下反应产物的环上一氯代物有7种
C. M能发生中和反应、取代反应、加成反应
D. 一个M分子最多有11个原子共面
9. 一种自修复材料在外力破坏后能够复原,其结构简式(图1)和修复原理(图2)如下图所示,下列说法错误的是__________。
A. 该高分子可通过加聚反应合成
B. 合成该高分子的两种单体含有相同的官能团
C. 自修复过程中“”基团之间形成了化学键
D. 使用该材料时应避免接触强酸或强碱
10. X为有机物同分异构体,同时满足如下三个条件的X的结构简式有__________。(写出1个即可)
①含有苯环;
②有三种不同化学环境的氢,个数比为6:2:1;
③1 ml X与足量金属Na反应可生成2g H2。
二、阿司匹林的前世今生
在阿司匹林之前,人们用水杨酸作为止痛药,但它有较强的酸性,能引起胃出血。时。水杨酸结构如图所示
11. 下列关于水杨酸的叙述正确的是__________。
A.水杨酸与互为同系物
B.水杨酸分子中所有原子一定都在同一平面上
C.水杨酸既可以看成是酚类物质,也可以看成是羧酸类物质
12. 将水杨酸与__________溶液作用(填化学式),可以生成。
13. 写出水杨酸的第一步电离的电离方程式__________。
水杨酸钠()易溶于水,可用作食品防腐剂,其水溶液呈碱性。
14. 常温时,将0.1 ml的水杨酸钠溶于水配成1升溶液,该溶液中OH-的浓度__________ml/L。
15. 若向上述水杨酸钠溶液中加0.001mlFeCl3(忽略体积变化),是否会有Fe(OH)3沉淀产生?通过计算说明__________(已知:25℃时,Fe(OH)3的)。
由于水杨酸的酸性较强,对胃肠道刺激大,目前只供外用。把水杨酸乙酰化后成为阿司匹林,副作用较低,阿司匹林成了现在主流的解热镇痛药。
16. 阿司匹林可用水杨酸与乙酸酐(乙酸酐结构见下图)在催化剂、加热的条件下制得,写出该反应的化学方程式:___________________
17. 当1 ml阿司匹林和足量氢氧化钠溶液反应时最多需氢氧化钠__________。
A 2 mlB. 3 mlC. 4 mlD. 5 ml
18. 胃溃疡患者服用阿司匹林片时,为何需同时服用氢氧化铝片__________?
一种缓释阿司匹林的结构式如下图,可缓慢释放药物,减少胃肠道刺激,维持稳定的血药浓度,减少不良反应,适合长期需要用药的慢性病患者。
19. 该物质在酸性条件下水解生成阿司匹林、__________和一种聚合物、这种聚合物的单体的结构简式是__________。
三、含酚废水处理
含酚废水对环境和人类都有极大的毒性,需严格处理。电解法是其中的一种处理方法。
20. 某污水处理厂处理含酚废水并制氢,工作原理如图所示。下列说法正确的是__________。
A. X为电源的正极,a极发生还原反应
B. a极电极反应式为:C6H5OH+11H2O-28e-=6CO2↑+28H+
C. 产生标准状况下4.48L CO2,则有1.4ml H+通过质子交换膜
D. 电解后将两极区溶液混合,与原废水相比较,溶液的pH保持不变
光解法是处理酚类废水的另一种方法。例如:BMO(Bi2MO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示
21. 下列说法不正确的是__________。
A. 该过程的总反应:
B. 该过程中BMO表现较强氧化性
C. 降解产物的分子中只含有极性共价键
D. ①和②中被降解的苯酚的物质的量之比为3:1
某工厂含酚废水处理流程如图
22. 流程图设备Ⅰ中进行的是________________操作(填写操作名称)。
23. 在设备Ⅱ中发生反应的化学方程式为______________。
24. 设备Ⅲ进入设备Ⅳ的物质B是__________。
25. 在设备Ⅳ中,物质B的水溶液和CaO反应,产物是__________、__________和水(填化学式)可通过__________操作(填写操作名称)分离出产物,并进入设备Ⅴ从而重新获得CaO;
26. 图中,能循环使用的物质是:苯、CaO、__________、__________。(填化学式)
27. 为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是________________。
28. 为测定废水中苯酚的含量,取此废水100 mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331 g,此废水中苯酚的含量为__________mg·L-1。
四、白花丹酸的合成
白花丹酸具有镇咳祛痰的作用,其合成路线流程图如下:
29. 写出A中官能团的结构简式:__________。
30. 写出的化学方程式:__________。
31. 的名称__________,它在整个合成路径中的作用是____________。
32. 的反应类型为__________。
A. 取代反应B. 加成反应C. 还原反应D. 氧化反应
33. E的结构简式__________。
34. 以下对于白花丹酸的分析错误的是__________。
A. 分子式为
B. 分子中所有碳原子可能共平面
C. 0.5 ml白花丹酸最多与1.5 ml NaOH反应
D. 苯环上的二氯代物有3种
35. 白花丹酸分子中混有,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:__________。
①分子中有四种不同化学环境的氢原子;
②与溶液能发生显色反应,且1 ml该物质最多能与3 ml NaOH反应。
36. 已知:,根据已有知识并结合题中流程图中信息写出以苯酚和乙醛为原料制备的合成路线图________(合成路线参考本题题干,其他无机试剂任选)。
五、对甲苯磺酸的制备
对甲苯磺酸是一种白色晶体,熔点,易溶于醇、醚和水,是用途广泛的化工原料。
实验室利用磺化反应制备对甲苯磺酸(实验装置如图所示),装置中有分水器,其作用是使回流的水蒸气冷凝进入分水器,有机溶剂进入烧瓶,增大反应物的转化率。
37. 写出该反应的化学方程式__________。
38. 下列说法错误是__________。
A. 当分水器中的水量不再增加时,停止加热
B. 分水器可将反应体系中的甲苯移除
C. 烧瓶中不需要添加沸石
D. 冷凝水从x口进入
根据对甲苯磺酸的结构,有同学推测对甲苯磺酸的性质和硫酸相似,进行了一系列的探究。
39. 对甲苯磺酸可能是强酸,电离方程式:
请设计简单实验证明猜想_______________。
40. 对甲苯磺酸的电离常数,苯磺酸的电离常数,据此判断酸性:对甲苯磺酸__________苯磺酸(填“>”或“ 碳酸 > 苯酚。水杨酸中的羧基酸性强于碳酸,可以与NaHCO3反应;而酚羟基酸性弱于碳酸,不与NaHCO3反应,因此选用NaHCO3溶液可以只让羧基反应,故答案为:NaHCO3;
【13题详解】
由于羧基的酸性强于酚羟基,故水杨酸的第一步电离的电离方程式为:+H+;
【14题详解】
常温时,将0.1 ml的水杨酸钠溶于水配成1升溶液,此时水杨酸钠溶液的浓度为:0.1ml/L,根据+H2O+OH-的Kh===10-11,即有=10-11,水解程度较小,故有:=10-11,解得c(OH-)==10-6ml/L,即该溶液中OH-的浓度10-6ml/L;
【15题详解】
由上述(4)分析可知,该溶液中OH-的浓度10-6ml/L,若向上述水杨酸钠溶液中加0.001mlFeCl3,即c(FeCl3)=0.001ml/L,此时c(Fe3+)c3(OH-)=0.001×(10-6)3=10-21>2.8×10-39=Ksp[Fe(OH)3],即会有Fe(OH)3沉淀产生;
【16题详解】
由题干水杨酸、阿司匹林、乙酸酐的结构简式可知,阿司匹林可用水杨酸与乙酸酐在催化剂、加热的条件下制得,该反应的化学方程式为:+(CH3CO)2O+CH3COOH;
【17题详解】
由题干阿司匹林的结构简式可知,1ml分子中含有1ml羧基需消耗1mlNaOH,1ml酚酯基需消耗2mlNaOH,故当1 ml阿司匹林和足量氢氧化钠溶液反应时最多需氢氧化钠3ml,故答案为:B;
【18题详解】
由题干阿司匹林的结构简式可知,阿司匹林分子中含有羧基,将刺激胃壁,同时服用氢氧化铝片可知中和胃酸和羧基,减少药物对胃溃疡患者胃壁的刺激作用,同时在溃疡面形成保护膜,隔绝阿司匹林和胃酸对溃疡处的刺激;
【19题详解】
由题干高聚物的结构简式可知,该物质中含有酯基在酸性条件下水解生成阿司匹林、乙二醇和一种聚合物即聚2-甲基丙烯酸,这种聚合物的单体即2-甲基丙烯酸,其结构简式是CH2=C(CH3)COOH,故答案为:乙二醇(或HOCH2CH2OH);CH2=C(CH3)COOH。
三、含酚废水处理
含酚废水对环境和人类都有极大的毒性,需严格处理。电解法是其中的一种处理方法。
20. 某污水处理厂处理含酚废水并制氢,工作原理如图所示。下列说法正确的是__________。
A. X为电源的正极,a极发生还原反应
B. a极电极反应式为:C6H5OH+11H2O-28e-=6CO2↑+28H+
C. 产生标准状况下4.48L CO2,则有1.4ml H+通过质子交换膜
D. 电解后将两极区溶液混合,与原废水相比较,溶液的pH保持不变
光解法是处理酚类废水的另一种方法。例如:BMO(Bi2MO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示
21. 下列说法不正确的是__________。
A. 该过程的总反应:
B. 该过程中BMO表现较强氧化性
C. 降解产物的分子中只含有极性共价键
D. ①和②中被降解的苯酚的物质的量之比为3:1
某工厂含酚废水处理流程如图
22. 流程图设备Ⅰ中进行的是________________操作(填写操作名称)。
23. 在设备Ⅱ中发生反应的化学方程式为______________。
24. 设备Ⅲ进入设备Ⅳ的物质B是__________。
25. 在设备Ⅳ中,物质B的水溶液和CaO反应,产物是__________、__________和水(填化学式)可通过__________操作(填写操作名称)分离出产物,并进入设备Ⅴ从而重新获得CaO;
26. 图中,能循环使用的物质是:苯、CaO、__________、__________。(填化学式)
27. 为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是________________。
28. 为测定废水中苯酚的含量,取此废水100 mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331 g,此废水中苯酚的含量为__________mg·L-1。
【答案】20. B 21. B
22. 萃取、分液 23. +NaOH→+H2O
24. NaHCO3 25. ①. CaCO3 ②. NaOH ③. 过滤
26 ①. NaOH ②. CO2
27. 取废水,向其中加FeCl3溶液,溶液变成紫色,说明含有苯酚
28. 940
【解析】
【分析】根据电解池原理,苯酚在a极发生氧化反应,生成二氧化碳和氢离子,氢离子穿过质子交换膜在b极发生还原反应,生成氢气;含苯酚的废水和苯一同进设备Ⅰ,出来的是被分离开的水、苯和苯酚,设备Ⅰ中进行的操作是萃取和分液、下层为水,上层为苯和苯酚的混合液;苯和苯酚的混合液进入设备Ⅱ,在设备Ⅱ中苯酚和物质A即NaOH溶液发生反应生成易溶于水的苯酚钠,进入设备Ⅲ,分离出的苯可返回设备Ⅰ重复利用;在设备Ⅲ中通入的二氧化碳与苯酚钠发生如下反应:+ H2O +CO2→+NaHCO3,生成的NaHCO3即物质B进入设备Ⅳ与CaO反应生成CaCO3、NaOH和H2O,过滤分离出CaCO3进入设备V进行高温煅烧得到CaO和CO2,据此分析解题。
【20题详解】
A.X为电源的正极,a极连电源正极作阳极,发生氧化反应,A错误;
B.a极发生氧化反应,电极反应式为:C6H5OH+11H2O-28e-=6CO2↑+28H+,B正确;
C.产生标准状况下4.48L 二氧化碳,即=0.2ml CO2,根据a极反应式:C6H5OH+11H2O-28e-=6CO2↑+28H+,可知有ml H+通过质子交换膜,C错误;
D.电解后将两极区溶液混合,与原废水相比较,原废液为苯酚,显弱酸性,电解总反应消耗了弱酸性的苯酚,但生成了CO2,其溶于水形成酸性比苯酚强的碳酸,故溶液的pH发生改变,D错误;
故答案为:B;
【21题详解】
A.反应物是C6H6O和氧气,生成物是二氧化碳和水,该过程的总反应:C6H6O+7O26CO2+3H2O,A正确;
B.该反应中BMO化合价升高,失电子发生氧化反应,作还原剂,体现较强的还原性,B错误;
C.降解产物的分子为二氧化碳,其中只含有极性共价键,C正确;
D.1个转为-2价的氧需得到3个电子,1个BMO+转化为BMO过程中需得到1个电子,根据转移电子守恒知,①和②中被降解的苯酚的物质的量之比为3:1,D正确;
故答案为:B;
【22题详解】
据分析,设备Ⅰ中进行的操作名称是萃取、分液,故答案为:萃取、分液;
【23题详解】
据分析,设备Ⅱ中发生反应的化学方程式为+NaOH→+H2O;
【24题详解】
已知苯酚钠与H2O、CO2反应生成苯酚和NaHCO3,结合分析可知,设备Ⅲ进入设备Ⅳ的物质B是NaHCO3;
【25题详解】
由分析可知,在设备Ⅳ中,物质B的水溶液即NaHCO3水溶液和CaO反应,产物是CaCO3、NaOH和水,可通过过滤操作分离出产物CaCO3,并进入设备Ⅴ进行高温煅烧,从而重新获得CaO,故答案为:CaCO3;NaOH;过滤;
【26题详解】
由分析可知,图中,能循环使用的物质是:苯、CaO、NaOH、CO2,故答案为:NaOH;CO2;
【27题详解】
苯酚遇三价铁离子显紫色,检验某工厂排放的污水中有无苯酚,此方法是取废水,向其中加FeCl3溶液,溶液变成紫色,说明含有苯酚;
【28题详解】
根据苯酚与足量的浓溴水反应得到2,4,6-三溴苯酚,则为测定废水中苯酚的含量,取此废水100 mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331 g,即有:n(苯酚)=n(2,4,6-三溴苯酚)==0.001ml,此废水中苯酚的含量为=940mg·L-1,故答案为:940。
四、白花丹酸的合成
白花丹酸具有镇咳祛痰的作用,其合成路线流程图如下:
29. 写出A中官能团的结构简式:__________。
30. 写出的化学方程式:__________。
31. 的名称__________,它在整个合成路径中的作用是____________。
32. 的反应类型为__________。
A. 取代反应B. 加成反应C. 还原反应D. 氧化反应
33. E的结构简式__________。
34. 以下对于白花丹酸的分析错误的是__________。
A. 分子式为
B. 分子中所有碳原子可能共平面
C. 0.5 ml白花丹酸最多与1.5 ml NaOH反应
D. 苯环上的二氯代物有3种
35. 白花丹酸分子中混有,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:__________。
①分子中有四种不同化学环境的氢原子;
②与溶液能发生显色反应,且1 ml该物质最多能与3 ml NaOH反应。
36. 已知:,根据已有知识并结合题中流程图中信息写出以苯酚和乙醛为原料制备的合成路线图________(合成路线参考本题题干,其他无机试剂任选)。
【答案】29. -OH、-CHO
30. 31. ①. 环己酮 ②. 保护羟基 32. D
33. 34. B
35. 或 36. 或者。
【解析】
【分析】D与BrCH2COOC2H5发生取代反应生成E,E水解生成F,由D、F的结构简式可知,E是。
【29题详解】
A中官能团为羟基、醛基,官能团的结构简式分别为-OH、-CHO;
【30题详解】
是A和反应生成B和水,反应的化学方程式为;
【31题详解】
含有酮羰基,名称为环己酮,在整个合成路径中, 先与A中酚羟基反应,最后一步又得到酚羟基,所以的作用是保护2个酚羟基。
【32题详解】
是C中的羟基变为羰基,反应类型为氧化反应,选D;
【33题详解】
D与BrCH2COOC2H5发生取代反应生成E,E水解生成F,由D、F的结构简式可知E是。
【34题详解】
A.白花丹酸的结构简式,可知分子式为,故A正确;
B.中*标出的碳原子通过单键连接3个碳原子,不可能所有碳原子共平面,故B错误;
C.酚羟基、羧基都能与氢氧化钠反应,所以0.5 ml白花丹酸最多与1.5 ml NaOH反应,故C正确;
D.苯环上的二氯代物有、、,共3种,故D正确;
选B。
【35题详解】
①分子中有四种不同化学环境氢原子,说明结构对称,②与溶液能发生显色反应,且1 ml该物质最多能与3 ml NaOH反应,含有酚羟基、且含有1个酚酯基(酯基水解后生成羧基和酚羟基);同时满足所有条件的的同分异构体有或。
【36题详解】
苯酚和氢气发生加成反应生成环己醇,环己醇发生消去反应生成环己烯,环己烯与溴化氢发生加成反应生成,与Mg反应生成,和乙醛在酸性条件下生成,合成路线为。或者流程为:。
五、对甲苯磺酸的制备
对甲苯磺酸是一种白色晶体,熔点,易溶于醇、醚和水,是用途广泛的化工原料。
实验室利用磺化反应制备对甲苯磺酸(实验装置如图所示),装置中有分水器,其作用是使回流的水蒸气冷凝进入分水器,有机溶剂进入烧瓶,增大反应物的转化率。
37. 写出该反应的化学方程式__________。
38. 下列说法错误的是__________。
A. 当分水器中的水量不再增加时,停止加热
B. 分水器可将反应体系中的甲苯移除
C. 烧瓶中不需要添加沸石
D. 冷凝水从x口进入
根据对甲苯磺酸的结构,有同学推测对甲苯磺酸的性质和硫酸相似,进行了一系列的探究。
39. 对甲苯磺酸可能是强酸,电离方程式:
请设计简单实验证明猜想_______________。
40. 对甲苯磺酸的电离常数,苯磺酸的电离常数,据此判断酸性:对甲苯磺酸__________苯磺酸(填“>”或“
相关试卷
这是一份上海市嘉定区第一中学2025-2026学年高二上学期期末化学试题(原卷版+解析版),共29页。试卷主要包含了有机物的结构与性质,阿司匹林的前世今生,含酚废水处理,白花丹酸的合成,对甲苯磺酸的制备等内容,欢迎下载使用。
这是一份2025-2026学年上海市嘉定区第一中学高二上学期期末化学试题,共29页。
这是一份上海市嘉定区第一中学2025-2026学年高一上册期中考试化学试卷(含解析),共14页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
![上海市嘉定区第一中学2025~2026学年高一上册期中考试化学试题[附解析]](http://img-preview.51jiaoxi.com/3/7/17811111/0-1768516657573/0.jpg?x-oss-process=image/resize,w_202)



.png)




