

四川省绵阳中学2026届高三上学期期中考试 化学试卷(含答案)
展开 这是一份四川省绵阳中学2026届高三上学期期中考试 化学试卷(含答案),共10页。试卷主要包含了5mm黑色墨迹签字笔书写,已知等内容,欢迎下载使用。
注意事项:
开始作答前,请先将自己的姓名、准考证号、座位号填涂到答题卡对应位置上。
选择题部分用2B铅笔填涂,非选择题部分用0.5mm黑色墨迹签字笔书写。
考试结束后,将答题卡交回,
一、单选题:本大题共15小题,共45分。
1.纪录片《我在故宫修文物》表现了文物修复者穿越古今与百年之前的人进行对话的职业体验,让我们领略到历史与文化的传承。下列文物修复和保护的过程中涉及化学变化的是( )
A. AB. BC. CD. D
2.氟气通过碎冰表面,发生反应①F2+H2O -40 ∘C HOF+HF,生成的HOF遇水发生反应②HOF+H2O=HF+H2O2。下列说法正确的是( )
A. HOF的电子式为B. H2O2为非极性分子
C. 反应①中有非极性键的断裂和形成D. 反应②中HF为还原产物
3.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 100g质量分数为17%的H2O2溶液中极性键数目为NA
B. 标准状况下,11.2LO2参与反应转移的电子数一定为2NA
C. 标准状况下,11.2L一氯甲烷中含有的氯原子数为0.5 NA
D. 常温下,1L0.1ml⋅L-1Na2C2O4溶液中含C2O42-数目为0.1NA
4.K2FeO4是优良的饮用水处理剂,一种制备方法是将Fe2O3、KNO3、KOH混合共熔,反应为Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O。下列说法不正确的是( )
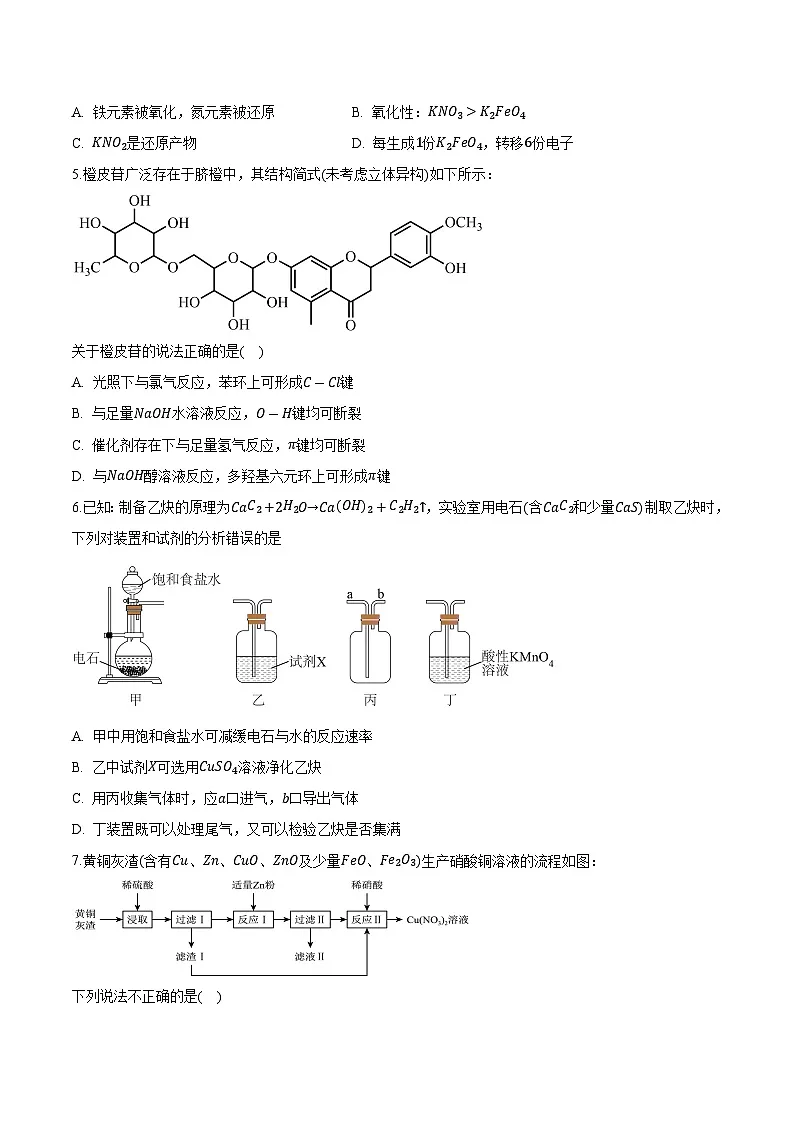
A. 铁元素被氧化,氮元素被还原B. 氧化性:KNO3>K2FeO4
C. KNO2是还原产物D. 每生成1份K2FeO4,转移6份电子
5.橙皮苷广泛存在于脐橙中,其结构简式(未考虑立体异构)如下所示:
关于橙皮苷的说法正确的是( )
A. 光照下与氯气反应,苯环上可形成C-Cl键
B. 与足量NaOH水溶液反应,O-H键均可断裂
C. 催化剂存在下与足量氢气反应,π键均可断裂
D. 与NaOH醇溶液反应,多羟基六元环上可形成π键
6.已知:制备乙炔的原理为CaC2+2H2O→CaOH2+C2H2↑,实验室用电石(含CaC2和少量CaS)制取乙炔时,下列对装置和试剂的分析错误的是
A. 甲中用饱和食盐水可减缓电石与水的反应速率
B. 乙中试剂X可选用CuSO4溶液净化乙炔
C. 用丙收集气体时,应a口进气,b口导出气体
D. 丁装置既可以处理尾气,又可以检验乙炔是否集满
7.黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量FeO、Fe2O3)生产硝酸铜溶液的流程如图:
下列说法不正确的是( )
A. “浸取”时适当提高硫酸浓度可加快反应速率
B. 若反应中所加Zn过量,所得Cu(NO3)2溶液中含Zn(NO3)2杂质
C. 滤液Ⅱ一定含Zn2+、Fe2+、Fe3+、SO42-等离子
D. Cu(NO3)2溶液在稀硝酸中蒸发浓缩、冷却结晶、过滤得到Cu(NO3)2⋅3H2O
8.现有短周期元素W、X、Y、Z和R在周期表中的位置如图所示,其中Y原子的核外电子数是X原子核外电子数的两倍,下列说法正确的是( )
A. R的气态氢化物比Y的气态氢化物稳定
B. 原子半径(r):r(Y)>r(Z)>r(W)
C. X元素的最高化合价为+6价
D. R氧化物对应水化物的酸性一定比Y氧化物对应水化物的酸性强
9.已知Mg、Al、O三种元素可形成尖晶石型晶体,如图所示该晶体的晶胞由4个A型小晶格和4个B型小晶格构成,其中Al3+和O2-都在小晶格内部,部分Mg2+在小晶格内部,部分Mg2+在小晶格顶点,下列分析错误的是( )
A. 该晶体为离子晶体
B. 该物质的化学式为Mg2Al2O5
C. 该晶胞中所含离子总数为56
D. 2个Mg2+之间的最短核间距是 3a4pm
10.高分子N可用于制备聚合物离子导体,其合成路线如图。下列说法不正确的是( )
A. 苯乙烯不存在顺反异构体B. 试剂a为
C. 试剂b为HO(CH2CH2O)mCH3D. 反应1为加聚反应,反应2为缩聚反应
11.实验小组利用传感器探究Na2CO3和NaHCO3的性质。下列分析不正确的是( )
A. ①与②的实验数据基本相同,说明②中的OH-未参与该反应
B. 加入试剂体积相同时,②所得沉淀质量大于③所得沉淀质量
C. 从起始到a点过程中反应的离子方程式为:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-
D. b点对应溶液中水的电离程度小于c点对应溶液中水的电离程度
12.某同学设计以下实验,探究简单配合物的形成和转化。
下列说法错误的是( )
A. ②中沉淀与④中沉淀不是同一种物质
B. ③中现象说明配体与Cu2+的结合能力:NH3>H2O
C. ④中深蓝色物质在乙醇中的溶解度比在水中小
D. 若向⑤中加入稀硫酸,同样可以得到黄绿色溶液
13.某温度时,反应X (g)4Y (g)+Z(g) ΔH=-Q kJ⋅ml-1在2L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法正确的是( )
A. 2min内,X的平均反应速率为0.5ml⋅L-1⋅min-1
B. 5min内,反应放出的热量为0.8Q kJ
C. 第5 min后,X的生成速率与Y的生成速率相等且保持不变
D. 第t1min时,该反应未达到平衡状态
14.某医用超声清洗器带有臭氧消毒功能,其臭氧电解发生器的原理示意图如图。下列叙述正确的是( )
A. 阳极可能的副产物有O2、NO
B. 阴极电极反应是O2+4e-+4HR=2H2O+4R-
C. 装置所用的离子交换膜是阴离子交换膜
D. 容器内壁可用不锈钢、陶瓷、橡胶等材质
15.室温下,某二元碱X(OH)2水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示,下列说法正确的是( )
A. 室温下,Kb2的数量级为10-5
B. X(OH)NO3水溶液显酸性
C. 等物质的量的X(NO3)2和X(OH)NO3混合溶液中:c(X2+)>c[X(OH)+]
D. 在X(OH)NO3水溶液中:c[X(OH)2]+c(OH-)=c(X2+)+c(H+)
二、非选择题。(共55分)
16.(13分)Fe3O4是一种用途广泛的磁性材料,以FeCl2为原料制备Fe3O4并获得副产物CaCl2水合物的工艺如下。
25℃时各物质溶度积见下表:
回答下列问题:
(1)Fe3O4中Fe元素的化合价是+2和_______。O2-的核外电子排布式为_______。
(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是_______。
(3)反应釜2中,加入CaO和分散剂的同时通入空气。
①反应的离子方程式为_______。
②为加快反应速率,可采取的措施有_______。(写出两项即可)。
(4)①反应釜3中,25℃时,Ca2+浓度为5.0ml/L,理论上pH不超过_______。
②称取CaCl2水合物1.000g,加水溶解,加入过量Na2C2O4,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用0.1000ml/L KMnO4标准溶液滴定,消耗24.00mL。滴定达到终点的现象为_______,该副产物中CaCl2的质量分数为_______。
17.(14分)侯氏制碱法为国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备少量NaHCO3,得到副产品Na2CO3和NH4Cl,流程如下图:
按要求回答下列问题。
(1)写出上图制备NaHCO3总反应的化学方程式:__________________________。
(2)制取CO2时为使下图A装置中分液漏斗内的稀盐酸顺利滴下,可将玻璃塞上的凹槽对准漏斗颈部的小孔或者______________________。
(3)制备NaHCO3时,需将A装置产生的气体,与B、C装置导管进行连接,其接口顺序是a__________(按气流方向,用小写字母表示)。“雾化装置”的优点是______________________。
(4)反应完成后,将装置B中混合物处理得到固体NaHCO3和母液。
①将固体NaHCO3加热充分,并将产生的气体先通过足量的试剂X吸收水分,再通过足量Na2O2,Na2O2增重0.14g。试剂X为__________,产品Na2CO3的质量为__________g。
②已知NaCls+NH4Claq⇀↽NaClaq+NH4Cls;NaCl和NH4Cl溶解度曲线(如图)。
i.为使NH4Cl沉淀从母液中充分析出,需向母液中加入的试剂Y为__________;
ii.得到副产品NH4Cl所需的操作有__________、__________、过滤、洗涤、干燥。
(5)题干实验流程中可以回收再利用的物质有_______________。
(6)称量吸收了一定量水分的NaHCO3粉末,配制成NaHCO3标准溶液,用于滴定未知浓度盐酸的浓度。预测该标准液对滴定结果造成的影响是__________(填“偏高”、“偏低”或“无影响”)。
18.(14分)一氧化氮可用作人造丝的漂白剂及丙烯和二甲醚的安定剂。
(1)工业上在钯或铂催化加热作用下,氨气与氧气制备一氧化氮的反应为4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H。
已知:①N2g+O2g=2NOg ΔH1=akJ⋅ml-1
②2H2g+O2g=2H2Og ΔH2=bkJ⋅ml-1
③N2g+3H2g⇌2NH3g ΔH3=ckJ⋅ml-1
则△H= kJ/ml(用含a、b、c的代数式表示)。
(2)1073 K时,在容积不变的密闭容器中发生反应2NOg+2H2g⇌N2g+2H2Og,测得反应速率与NO、H2浓度的变化如下表。
该反应的速率方程为v=kcmNO⋅cnH2,则m= ,n= ,k= (保留两位有效数字)L2⋅ml-2⋅s-1。
(3)T℃时,在2 L恒容密闭容器中充入1 ml NO、1 ml H2,发生反应2NOg+2H2g⇌N2g+2H2Og,起始时体系压强为p MPa,t min时反应达到平衡,此时测得N2的物质的量分数为25%。
①平衡时,体系压强p= MPa。
②平衡时,c(N2)= 。
③T℃时,该反应的压强平衡常数Kp= MPa-1(用含p的代数式表示,Kp为以分压表示的平衡常数,分压=总压×气体的物质的量分数)。
19.(14分)水仙花所含的挥发油中含有某些物质。它们的结构简式如下:
请回答下列问题:
(1)①有机物C的名称__________;从结构上看,上述四种有机物中与互为同系物的是__________ (填序号)。
②有机物C经__________ (填反应类型)反应可得到B。
(2)有机物A中含氧官能团的名称是__________,可能具有的性质是__________(填字母)。
A.能与NaOH发生反应
B. 1ml该物质最多与4ml溴水发生反应
C.既可燃烧,也可使酸性KMnO4溶液褪色
D.可与NaHCO3溶液反应放出CO2气体
(3)写出C和银氨溶液发生反应的化学方程式为__________。
(4)有机物A转化为丙的过程为(已略去无关产物)
A→I一定条件下→ΔO2/Cu甲→Ⅱ一定条件下乙→III一定条件下丙
如果反应Ⅱ为消去反应,则反应Ⅱ的试剂及条件是__________,反应Ⅲ为加聚反应,则高聚物丙的结构简式为__________。
2025-2026绵阳中学高2023级高三上期中考试化学试题参考答案
1.A 2.A 3.C 4.D 5.C 6.C 7.C 8.A 9.B 10.D 11.C 12.D 13.D 14.D 15.D
解答题答案说明:出于年级组的要求,我们将暂时不公布解答题每个小问的具体分值,谢谢考生们的理解与支持!
16. (1)+3;1s22s22p6
(2)防止二价铁被空气中氧气氧化为三价铁
(3)①4CaO+6H2O+4Fe2++O2=4FeOH3+4Ca2+
②适当升高温度、搅拌
(4)①11
②最后半滴标准液加入后,溶液变为红色,且半分钟内不变色;66.6%
17. (1)NH3⋅H2O+NaCl+CO2=NH4Cl+NaHCO↓↓
(2)将分液漏斗上部的玻璃塞打开
(3)efb;可增大与二氧化碳的接触面积,从而提高产率
(4)①浓硫酸;0.53
②NaCl粉末;加热浓缩;冷却结晶
(5)滤液M即食盐水、气体Z即CO2
(6)偏高
18.(1)2a+3b-2c
(2)m=2 n=1 4003
(3) 0.8p 0.2 ml/L 256p
19. (1)①苯甲醛 B ②加成或还原
(2)(酚)羟基、醚键 AC
(3) +2Ag(NH3)2OH →Δ +2Ag↓+3NH3+H2O
(4)NaOH醇溶液,加热 A
B
C
D
银器用除锈剂见新
变形的金属香炉复原
古画水洗除尘
木器表面擦拭烫蜡
W
X
Z
Y
R
实验操作
实验数据
测量下述实验过程的pH变化
物质
Fe(OH)2
Fe(OH)3
Ca(OH)2
溶度积Ksp
4.9×1017
2.8×10-39
5.0×10-6
实验序号
cH2/ml⋅L-1
cNO/ml⋅L-1
v/ml-1⋅L-1⋅s-1
1
0.0060
0.0010
8.0×10-7
2
0.0060
0.0020
3.2×10-6
3
0.0030
0.0040
6.4×10-6
4
0.0015
0.0040
3.2×10-6
相关试卷
这是一份四川省绵阳中学2026届高三上学期第二次模拟考试化学试卷(含答案),文件包含四川省绵阳中学2026届高三第二次模拟考试化学试题docx、四川省绵阳中学2026届高三第二次模拟考试化学试题docx等2份试卷配套教学资源,其中试卷共7页, 欢迎下载使用。
这是一份四川绵阳中学2026届高三第二次模拟考试化学试题(含答案),共7页。
这是一份四川省绵阳中学2026届高三上学期1月第二次模拟考试化学试卷(Word版附答案),文件包含四川省绵阳中学2026届高三第二次模拟考试化学试题docx、四川省绵阳中学2026届高三第二次模拟考试化学答案docx等2份试卷配套教学资源,其中试卷共7页, 欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 











