

河南省南阳市镇平县2025-2026学年九年级上学期期中考试化学试卷(有答案和解析)
展开 这是一份河南省南阳市镇平县2025-2026学年九年级上学期期中考试化学试卷(有答案和解析),共15页。试卷主要包含了选择题,填空题,简答题,综合应用题等内容,欢迎下载使用。
可能用到的相对原子质量:H-1 C-12 N-14 O-16
一、选择题(每题只有一个选项符合题意,每小题1分,共14分)
1. 如图所述物质用途中,主要利用其化学性质的是
A. 用金属制作奥运奖牌
B. 用钢材铸造体育场“鸟巢”
C. 用羊绒作“福娃”的外层材料
D. 用丙烷做“祥云”火炬的燃料
【答案】D
【解析】
【详解】A、用金属制作奥运奖牌,是利用金属具有良好的延展性,不需要通过化学变化就能表现出来,属于物理性质。
B、用钢材铸造体育场“鸟巢”,是利用钢铁的硬度大,不需要通过化学变化就能表现出来,属于物理性质。
C、用羊绒作“福娃”的外层材料,是利用羊绒柔软,不需要通过化学变化就能表现出来,属于物理性质。
D、用丙烷做“祥云”火炬的燃料,是利用丙烷具有可燃性,需要通过化学变化才能表现出来,属于化学性质。
故选D。
2. 《美丽中国建设评估指标体系及实施方案》中对市级及以上城市空气质量优良天数比例作出了具体规定。下列属于空气质量日报中需要监测的污染物是
A 二氧化氮B. 氧气C. 氮气D. 二氧化碳
【答案】A
【解析】
【详解】目前计入空气质量评价的主要污染物有:二氧化硫(SO2)、一氧化碳(CO)、二氧化氮(NO2)、可吸入颗粒物(PM10)、细颗粒物(PM2.5)和臭氧(O3)等,二氧化碳、氧气、氮气均属于空气的成分,不属于空气污染物,故属于空气质量日报中需要监测的污染物为二氧化氮;
故选:A。
3. 下列做法符合“建设美丽家园”主题是
A. 使用一次性筷子B. 提倡使用光伏发电
C. 废旧电池深埋处理D. 生活污水直接排放
【答案】B
【解析】
【详解】A、使用一次性筷子浪费资源,增加污染,A选项不符合题意;
B、提倡光伏发电,利用太阳能可再生能源,减少污染,符合主题,B选项符合题意;
C、废旧电池深埋会污染土壤和地下水,C选项不符合题意;
D、生活污水直接排放造成水污染,D选项不符合题意。
故选:B。
4. 科学无止境,精神永流传。测定了“铟、锑”等相对原子质量科学家是
A. 张青莲B. 拉瓦锡C. 闵恩泽D. 门捷列夫
【答案】A
【解析】
【详解】A、张青莲是我国著名化学家,主持测定了铟、锑等元素的相对原子质量,并被国际原子量委员会采用,A选项符合题意;
B、拉瓦锡首先通过实验得出空气是由氮气和氧气组成的结论,B选项不符合题意;
C、闵恩泽研发了多种用于石油化工生产的催化剂,C选项不符合题意;
D、门捷列夫发现了元素周期律,D选项不符合题意。
故选:A。
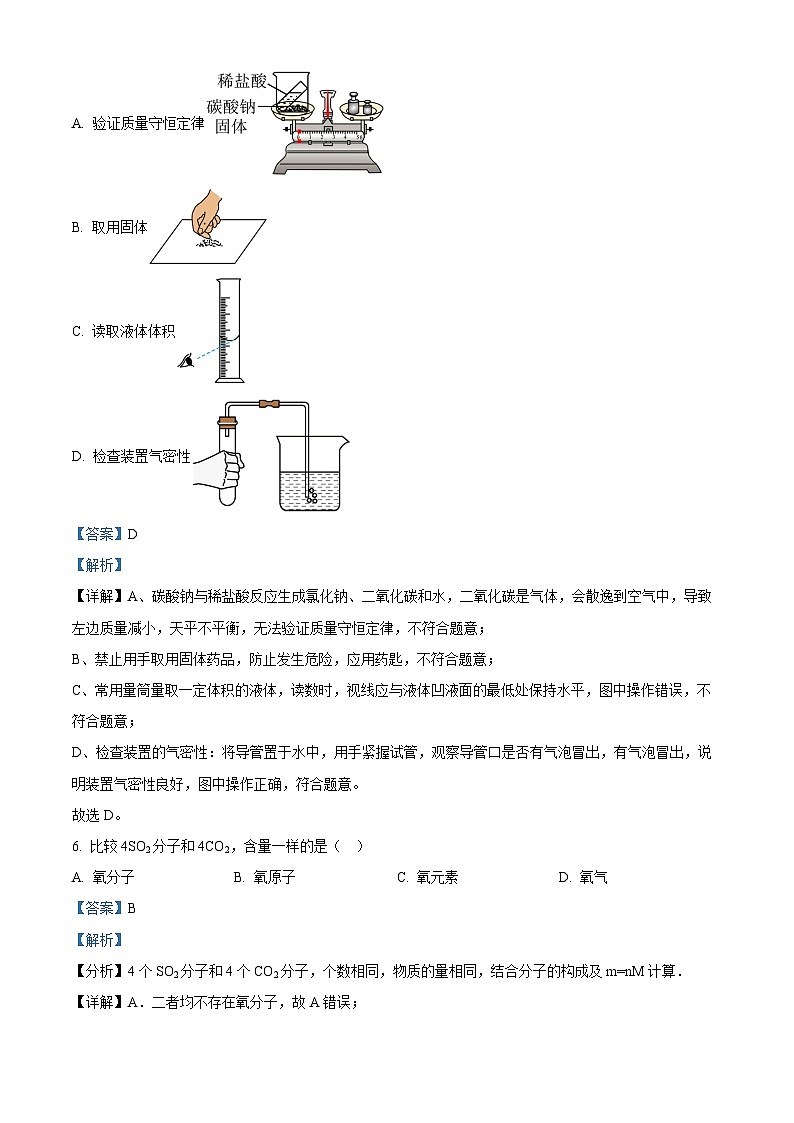
5. 化学是以实验为基础的科学。下列实验操作正确的是
A. 验证质量守恒定律
B. 取用固体
C. 读取液体体积
D. 检查装置气密性
【答案】D
【解析】
【详解】A、碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,二氧化碳是气体,会散逸到空气中,导致左边质量减小,天平不平衡,无法验证质量守恒定律,不符合题意;
B、禁止用手取用固体药品,防止发生危险,应用药匙,不符合题意;
C、常用量筒量取一定体积的液体,读数时,视线应与液体凹液面的最低处保持水平,图中操作错误,不符合题意;
D、检查装置的气密性:将导管置于水中,用手紧握试管,观察导管口是否有气泡冒出,有气泡冒出,说明装置气密性良好,图中操作正确,符合题意。
故选D。
6. 比较4SO2分子和4CO2,含量一样的是( )
A. 氧分子B. 氧原子C. 氧元素D. 氧气
【答案】B
【解析】
【分析】4个SO2分子和4个CO2分子,个数相同,物质的量相同,结合分子的构成及m=nM计算.
【详解】A.二者均不存在氧分子,故A错误;
B.由分子构成可知,4个分子中均含8个氧原子,故B正确;
C.由B可知,氧原子个数相同,物质的量相同,由m=nM可知,氧元素的质量相同,但元素只论种类不论个数,故C错误;
D.均不含氧气,则氧气含量无意义,故D错误;
故选B。
7. 如图是某元素在元素周期表中的有关信息和其原子结构示意图,下列有关说法正确的是
A. 该元素为金属元素
B. 该元素的相对原子质量为35.453 g
C. 该元素位于元素周期表的第三周期
D. 该元素在化学反应中容易失去电子
【答案】C
【解析】
【详解】A、根据元素周期表的信息可知,该元素原子序数为17,即原子的质子数为17,为氯元素,元素名称带“气”字旁,属于非金属元素,故选项说法不正确。
B、根据元素周期表的信息可知,元素名称下方的数字表示相对原子质量,则氯的相对原子质量为35.453,单位是“1”,不是“g”,故选项说法不正确。
C、周期数=原子的核外电子层数,氯原子核外有三个电子层,因此该元素位于元素周期表的第三周期,故选项说法正确。
D、由氯原子的结构示意图可知,最外层电子数为7,大于4,在化学反应中容易得到电子,故选项说法不正确。
故选C。
8. 据报道,俄罗斯科学家最近合成了一种新的原子,经测定该原子的核电荷数为114,相对原子质量为289,其中子数为( )
A. 175
B. 114
C. 61
D. 289
【答案】A
【解析】
【详解】因为原子中:核电荷数=核内质子数=核外电子数,由题意科学家最近合成了核电荷数为114的元素原子,故其核内质子数为114;根据相对原子质量≈质子数+中子数,由题意该原子的相对原子质量为289,则中子数=289-114=175。
故选A。
【点睛】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数、相对原子质量≈质子数+中子数。
9. 金属钠的化学性质非常活泼,将一小块金属钠放入冷水中,钠能与水剧烈反应,生成一种化合物和一种气体,这种气体可能是
A. SO2B. CO2C. N2D. H2
【答案】D
【解析】
【详解】化学反应前后元素种类不变;将一小块金属钠放入冷水中,钠能与水剧烈反应,生成一种化合物和一种气体,反应物中元素为钠、氢、氧,则生成的气体中含有以上元素;
反应物中不含硫、碳、氮元素,故ABC错误;反应物中含有氢元素,则这种气体可能是氢气;
故选D。
10. 下列各组物质中,按单质、化合物、混合物的顺序排列的一组是
A. 冰、液氧、空气B. 水、高锰酸钾、稀有气体
C. 铜、氧化铁、冰水混合物D. 水银、蒸馏水、海水
【答案】D
【解析】
【分析】由同种物质组成的是纯净物,由不同种物质组成的是混合物。由同种元素组成的纯净物是单质,由不同种元素组成的纯净物是化合物。
【详解】A. 冰与水是同种物质,冰属于化合物,液氧属于单质,空气属于混合物,此选项不符合题意;
B. 水属于化合物,高锰酸钾属于化合物,稀有气体包括氦气、氖气、氩气等,则稀有气体属于混合物,此选项不符合题意;
C. 铜属于单质,氧化铁属于化合物,冰、水是同种物质,则冰水混合物属于化合物,此选项不符合题意;
D. 水银是汞的俗称,水银属于单质,蒸馏水属于化合物,海水属于混合物,此选项符合题意。
故选D。
11. 剧烈运动时肌肉里产生乳酸(C3H6O3),会导致肌肉酸痛。下列说法错误的是
A. 乳酸的相对分子质量为90B. 乳酸由碳、氢、氧三种元素组成
C. 乳酸中氧元素的质量分数最大D. 乳酸中碳、氢、氧元素质量之比为1:2:1
【答案】D
【解析】
【详解】A、乳酸的相对分子质量为:12×3+1×6+16×3=90,故A正确;
B、由乳酸的化学式可知,乳酸是由碳、氢、氧三种元素组成的,故B正确;
C、乳酸中碳、氢、氧三种元素的质量比为(12×3):(1×6):(16×3)=36:6:48,可见其中氧元素的质量分数最大,故C正确;
D、乳酸中碳、氢、氧三种元素的质量比为(12×3):(1×6):(16×3)=36:6:48=6:1:8,故D错误。故选D。
12. 推理是学习化学的一种重要方法,但推理必须科学、严谨。下列推理正确的是
A. 木炭能在氧气中燃烧,所以氧气具有可燃性
B. 化合物中含不同种元素,所以由不同种元素组成的纯净物是化合物
C. 原子核是由质子和中子构成的,因此所有原子核中都一定含有质子和中子
D. 催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
【答案】B
【解析】
【详解】A、木炭在氧气中能燃烧,说明氧气能够支持燃烧,但是不具有可燃性,该选项说法不正确;
B、化合物中含不同种元素,所以由不同种元素组成的纯净物是化合物,该选项说法正确;
C、原子核中都一定含有质子,但是不一定含有中子,例如氢原子的原子核中不含有中子,该选项说法不正确;
D、反应前后质量不变的物质不一定是催化剂,例如铜锌合金和稀盐酸混合时,反应前后铜质量不变,但是铜不是催化剂,该选项说法不正确。
故选B。
13. 一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如表:则下列说法不正确的是
A. 物质乙可能是催化剂
B. 丙和丁两种物质变化的质量比为8︰2
C. 该反应的基本反应类型是化合反应
D. 物质丙一定是化合物
【答案】C
【解析】
【分析】根据质量守恒定律,化学反应前后物质的总质量不变,则2g+1g+12g+4g=8g+xg+4g+6g,x=1,反应后,甲的质量增加,甲是生成物,乙的质量不变,乙可能是催化剂,也可能是不参与反应的杂质,丙的质量减小,丙是反应物,丁的质量增加,丁是生成物。
【详解】A、化学反应前后乙的质量不变,乙可能是催化剂,也可能是不参与反应的杂质,不符合题意;
B、该反应中,丙和丁两种物质变化的质量比为:(12g-4g):(6g-4g)=8:2,不符合题意;
C、由分析可知,该反应中,丙是反应物,甲、丁是生成物,该反应符合“一变多”的特点,属于分解反应,符合题意;
D、由分析可知,该反应中,丙是反应物,甲、丁是生成物,分解反应的反应物是化合物,不符合题意。
故选C。
14. 现有C2H4O、C3H6O、C4H8O组成的混合物,经测定其中氧元素的质量分数为30%,则混合物中氢元素的质量分数为
A. 6.7%B. 10%C. 15%D. 16.7%
【答案】B
【解析】
【详解】现有C2H4O、C3H6O、C4H8O组成的混合物,经测定其中氧元素的质量分数为30%,则碳、氢元素质量分数的和=1-30%=70%,在三种化合物中碳、氢原子个数比都为1:2,故碳元素和氢元素的质量比=12:(1×2)=6:1,故氢元素的质量分数=。 故选B。
二、填空题(每空1分,共16分)
15. 请用合适的化学用语填空:空气中含量较高且化学性质不活泼的气体是______;地壳中含量最高的金属元素形成的氧化物为______;3个碳酸根离子______。
【答案】 ①. ②. ③.
【解析】
【详解】空气中含量高且化学性质不活泼的气体是氮气;地壳中含量最高的金属元素是铝,铝的氧化物由铝(+3价)和氧(-2价)组成,两者形成的化合物为氧化铝,正负化合价代数和为零,其化学式为;由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,3个碳酸根离子表示为,故填:;;。
16. 在化学王国里,数字被赋予了丰富的内涵。对下列化学用语中数字“2”的表示意义,把对应的序号填在横线上。
①2H ②2NH3 ③SO2 ④ ⑤Mg2+ ⑥2OH- ⑦H2O
(1)表示离子所带电荷数的是______。
(2)表示分子中原子个数的是______。
【答案】(1)⑤ (2)③⑦
【解析】
【分析】①2H中的2表示氢原子的个数为2个;②中的2表示氨分子的个数为2个;③中的2表示一个二氧化硫分子中含有2个氧原子;④中的2表示氧化铜中铜元素的化合价为+2;⑤中的2表示一个镁离子带有2个单位的正电荷;⑥中的2表示氢氧根离子的个数为2个;⑦中的2表示一个水分子中含有2个氢原子。
【小问1详解】
由分析可知,表示离子所带电荷数的是⑤,故填:⑤;
【小问2详解】
由分析可知,表示分子中原子个数的是③⑦,故填:③⑦。
17. 下列各图中和分别表示不同元素的原子,其中表示混合物的是______,表示化合物的是______。
A. B. C. D.
【答案】 ①. A ②. B
【解析】
【详解】A、图示中含有三种分子,即含有三种物质,属于混合物。
B、图示中只含有一种分子,且该分子是由不同种原子构成,属于化合物。
C、图示中只含有一种分子,且该分子是由同种原子构成,属于单质。
D、图示中只含有一种分子,且该分子是由同种原子构成,属于单质。
由上述分析可知,表示混合物的是A;表示化合物的是B。
18. 我们的星球因水而美丽,水是人类不可缺少的宝贵资源。
(1)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:②对应的作用是______。(填字母序号)
a.杀菌作用 b.吸附作用 c.沉淀过滤 d.蒸馏
(2)实验I中水从A转移到C的过程中,水分子本身______(填“有”或“没有”)发生变化,水分子间的间隙发生变化。
(3)实验室用图II装置来探究水组成,则a端产生的气体是______;用化学方程式表示该实验原理______。
(4)图III的操作名称是______,缺少的一种仪器,其作用是______。
【答案】(1)c (2)没有
(3) ①. 氢气##H2 ②.
(4) ①. 过滤 ②. 引流
【解析】
【小问1详解】
②处的超滤膜可起到过滤的作用,除去水中的难溶性杂质,故对应的作用是c;
【小问2详解】
实验I中水从A转移到C的过程中,只是水的状态的改变,无新物质生成,故水分子本身没有发生变化,只是水分子之间的间隔发生变化;
【小问3详解】
在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,试管a与负极相连,产生的是氢气;
水通电分解生成氢气和氧气,该反应的化学方程式为:;
【小问4详解】
图III的操作名称是过滤;
过滤所需的仪器是:烧杯、漏斗、玻璃棒、铁架台(带铁圈),故缺少的仪器是玻璃棒,过滤时,玻璃棒的作用是:引流。
19. X、Y、Z是中学化学常见的物质,三种物质均含有同一种元素,它们之间有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。X、Y是组成元素完全相同的两种液体;Z是气体单质。则X转化为Y的化学方程式为______;从微观角度解释X和Y性质有差异的原因是______。
【答案】 ①. 2H2O22H2O+O2↑ ②. 分子构成不同
【解析】
【分析】X、Y、Z是中学化学常见的物质,三种物质均含有同一种元素,X、Y是组成元素完全相同的两种液体;Z是气体单质;过氧化氢在二氧化锰催化作用下生成水和氧气,水通电分解生成氢气和氧气,氢气在氧气中燃烧生成水,则X为过氧化氢、Y为水、Z为氧气。
【详解】根据分析可知,X转化为Y的反应为过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O22H2O+O2↑;
从微观角度解释(过氧化氢)和(水)都是由分子构成,它们的化学性质不同的原因是分子构成不同。
20. 在化学反应中,X的化学式为_________。
【答案】NO
【解析】
【详解】根据质量守恒定律,化学反应前后原子的种类和数目不变,反应物中有3个铜原子、8个氢原子、8个氮原子、24个氧原子,生成物中有3个铜原子、8个氢原子6个氮原子、22个氧原子,故X中有2个氮原子和1个氧原子,故X为NO。
三、简答题(本题包括4个小题)
21. 请从分子角度分析并解释下列问题。
(1)香水要密封保存。
(2)化学变化和物理变化的区别是什么?
【答案】(1)分子在不断运动
(2)是否生成新分子
【解析】
【小问1详解】
香水中的液体分子(如香料分子、酒精分子)在不断运动。若未密封,这些分子会扩散到空气中,导致香水挥发、浓度降低甚至失效。密封保存可减少分子逸出,保持香水成分稳定,故填:分子在不断运动;
【小问2详解】
化学变化的本质是生成新分子,物理变化中分子种类不变,是否生成新分子是两者的本质区别,故填:是否生成新分子。
22. 请按要求写出下列反应的化学方程式。
(1)氢气在氯气中燃烧生成氯化氢。
(2)铁丝在氧气中剧烈燃烧。
【答案】(1)
(2)
【解析】
【小问1详解】
氢气和氯气在点燃条件下生成氯化氢,该反应的化学方程式为,故填:;
【小问2详解】
在点燃的条件下,铁与氧气反应生成四氧化三铁,反应的化学方程式为,故填:。
23. 如图,请根据要求回答相关问题。
(1)用图中装置测定空气中氧气的含量,若结果偏小,试分析可能导致的原因。(试写一条)
(2)写出图中实验发生反应的化学方程式。
(3)为什么不能用硫替代红磷?
【答案】(1)红磷的量不足(合理即可)
(2)
(3)硫在空气中燃烧生成二氧化硫,二氧化硫是气体,化学反应前后压强变化不大,无法测定空气中氧气的含量
【解析】
【小问1详解】
用图中装置测定空气中氧气的含量,若结果偏小,可能是红磷的量不足,不能将装置内氧气耗尽,也可能是装置漏气,在冷却至室温的过程中外界空气进入,占据了一定的体积,也可能是未冷却至室温就打开弹簧夹,气体受热膨胀占据了一定的体积;
【小问2详解】
图中实验发生反应为红磷燃烧生成五氧化二磷,该反应的化学方程式为:;
【小问3详解】
硫在空气中燃烧生成二氧化硫,二氧化硫是气体,化学反应前后压强变化不大,无法测定空气中氧气的含量,故不能用硫替代红磷。
24. 如图是某化学反应的微观示意图:
(1)A中碳、氢元素的质量比为_____。
(2)该反应的化学方程式为______。
(3)请从微观角度解释化学反应遵守质量守恒定律的原因:______。
【答案】(1)3:1 (2)CH4+2O22H2O+CO2
(3)化学反应中,原子的种类、数目、质量都没有发生改变
【解析】
【小问1详解】
由微粒的构成可知,A为化学式为CH4,其中碳、氢元素的质量比为(12×1):(1×4)= 3:1;故填:3:1。
【小问2详解】
由反应的微观示意图可知,甲烷在氧气中燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O22H2O+CO2;故填:CH4+2O22H2O+CO2。
【小问3详解】
从微观角度来看,化学反应遵守质量守恒定律的原因是化学反应中,原子的种类、数目、质量都没有发生改变;故填:化学反应中,原子的种类、数目、质量都没有发生改变。
四、综合应用题(共10分)
25. 如图是实验室制取气体的常用装置。
(1)图中仪器a的名称为______。
(2)高锰酸钾制氧气的化学反应方程式______,为了获得较为纯净的氧气,应选用的收集装置为______,若选取F装置,采用排水法收集氧气,氧气应从______(填“a”或“b”)端通入。
(3)某同学用过氧化氢溶液和二氧化锰混合制取氧气,二氧化锰起______作用,若用C装置收集氧气,验证氧气已收集满的方法是:______。
(4)和装置A相比,B装置制取氧气的优点______。
(5)氢能源智轨电车是通过液态氢与空气中的氧气结合而发电。完全燃烧4 kg氢气,理论上需要消耗氧气的质量是多少?
【答案】(1)分液漏斗
(2) ①. 2KMnO4K2MnO4+MnO2+O2↑ ②. E ③. b
(3) ①. 催化 ②. 将带火星的木条放到集气瓶口,木条复燃,则证明氧气已收集满
(4)安全、环保、节能##可以控制反应速率
(5)32 kg
解:设理论上需要消耗氧气的质量为x。
答:理论上需要消耗氧气的质量为32 kg。
【解析】
【小问1详解】
由图可知,仪器a的名称为分液漏斗;故填:分液漏斗。
【小问2详解】
高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO4K2MnO4+MnO2+O2↑;
氧气的密度比空气大,不易溶于水,可采用向上排空气法或排水法收集,采用排水法收集气体较纯净,选择的收集装置为E;
氧气的密度比水小,若选取F装置,采用排水法收集氧气,氧气应从b端通入;
故填:2KMnO4K2MnO4+MnO2+O2↑;E;b。
【小问3详解】
某同学用过氧化氢溶液和二氧化锰混合制取氧气,二氧化锰是该反应的催化剂,在反应中起催化作用;
氧气具有助燃性,若用C装置收集氧气,验证氧气已收集满的方法是将带火星的木条放到集气瓶口,木条复燃,则证明氧气已收集满;
故填:催化;将带火星的木条放到集气瓶口,木条复燃,则证明氧气已收集满。
【小问4详解】
和装置A相比,B装置制取氧气反应不需要加热,可以节约能源,产物是水,无污染,且可以通过分液漏斗控制液体的滴加速率,来控制反应速率;故填:安全、环保、节能或可以控制反应速率。
物质
甲
乙
丙
丁
反应前的质量/g
2
1
12
4
反应后的质量/g
8
x
4
6
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

(1).png)



