

天津市第二十一中学2025-2026学年高三上学期10月月考化学试题(含答案)
展开 这是一份天津市第二十一中学2025-2026学年高三上学期10月月考化学试题(含答案),共11页。试卷主要包含了 下列关于0,6 g, 下列装置或操作与说法正确的是等内容,欢迎下载使用。
一、选择题(共12题,每题只有一个正确答案)
1. 大国重器彰显中国实力,化学材料助力科技成果转化运用。下列说法正确的是
A. “蛟龙号”载人潜水器使用的钛合金是金属材料
B. “C919”大飞机使用的氮化硅陶瓷是传统硅酸盐材料
C. “玉兔二号”月球车使用的太阳能电池板材料是二氧化硅
D. “山东舰”航母使用的碳纤维是一种新型有机高分子材料
2. 德国著名行业杂志《应用化学》上曾刊登介绍:某中德联合研究小组设计制造了一种“水瓶”,用富勒烯 (C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。下列说法正确的是
A. “水瓶”、 都是混合物
B. 熔点:金刚石
C. 一定条件下,石墨转化为是物理变化
D. 磷酸钙是强电解质,其组成元素均为短周期元素
3. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 澄清透明的溶液:、、、
B. 水电离出的溶液:、、、
C. 的溶液:、、、
D. 使甲基橙变黄的溶液:、、、
4. 下列关于0.1 ml·L-1Na2CO3溶液的叙述错误的是
A. 该溶液中含有Na2CO3的质量为10.6 g
B. 1 L该溶液中Na+的物质的量浓度为0.2 ml·L-1
C. 从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为0.1 ml·L-1
D. 取该溶液10 mL,加水稀释至100 mL后所得溶液中Na2CO3的物质的量浓度为0.01 ml·L-1
5. 在标准状况下,将V L A气体(摩尔质量为M g·ml-1)溶于0.1L水中,所得溶液的密度为dg·cm-3,则溶液的物质的量浓度为
A. ml·L-1B. ml·L-1
C. ml·L-1D. ml·L-1
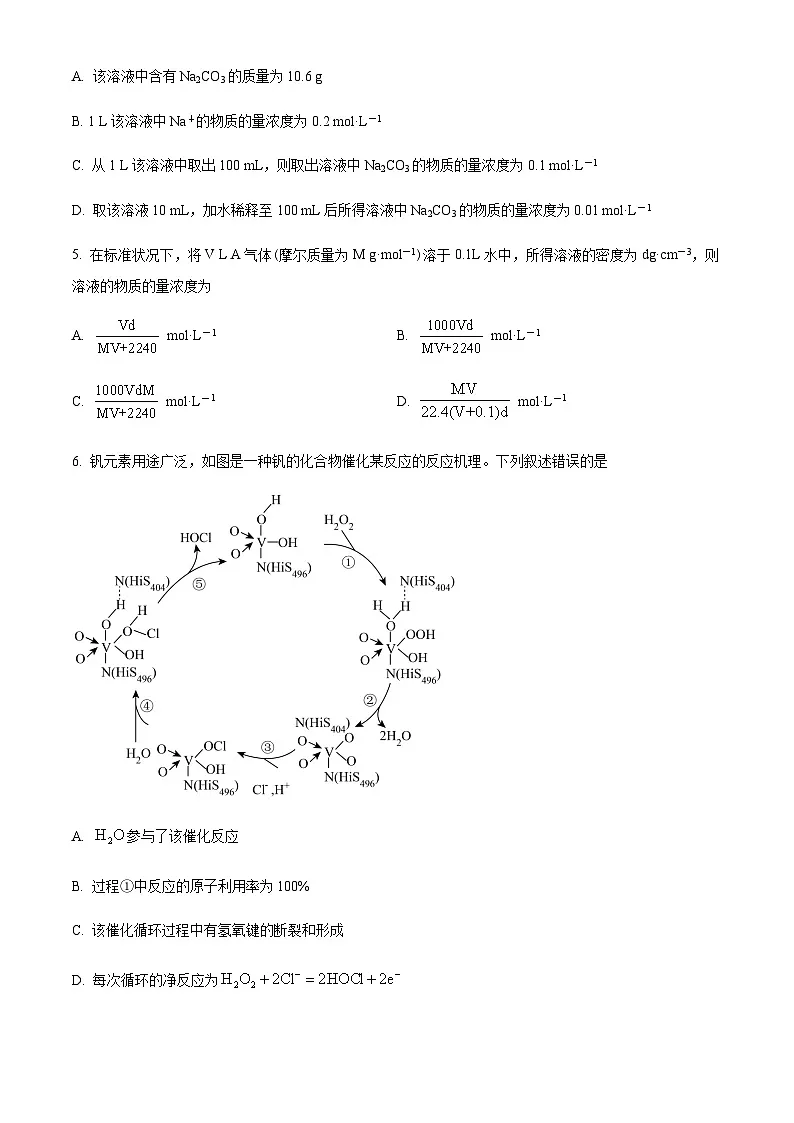
6. 钒元素用途广泛,如图是一种钒的化合物催化某反应的反应机理。下列叙述错误的是
A. 参与了该催化反应
B. 过程①中反应的原子利用率为100%
C. 该催化循环过程中有氢氧键的断裂和形成
D. 每次循环的净反应为
7. 某同学在实验室进行了如图所示的实验,下列说法中错误的是
A. 利用过滤的方法,可将Z中固体与液体分离
B. X、Z烧杯中分散质相同
C. Y中反应的离子方程式为
D. Z中分散系能产生丁达尔效应
8. 设NA为阿伏加德罗常数的值,下列说法正确的是
A. 25℃,pH=13的1.0LBa(OH)2溶液中含有OH-的数目为0.2NA
B. 60gSiO2晶体中Si—O键数目为2NA
C. 在K37ClO3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应中,若有212g氯气生成,则反应中转移电子的数目为5NA
D. 加热条件下,20mL10ml•L-1浓硝酸与足量铜反应转移电子数为0.1NA
9. 下列装置或操作与说法正确的是( )
A. 实验室制乙烯
B. 实验室制乙炔并验证乙炔能发生氧化反应
C 实验室中分馏石油
D. 若甲为醋酸,乙为贝壳(粉状),丙为苯酚钠溶液,则该装置不可以验证醋酸、碳酸、苯酚酸性的强弱
10. 钛有非常广泛应用,有“生物金属”、“未来金属”之称。下列关于钛及其化合物的说法不正确的是
A. Ti位于周期表中第四周期ⅣB族,基态原子的核外电子中,两种自旋状态的电子数之比为5:6
B. 高温下可用金属钠还原溶液来制备金属
C. 可用于提炼钛和制造钛白粉,常用水解法制备:
D. 钛铁矿()与硫酸反应的离子方程式为:
11. 下列离子方程式书写正确的是
A. CaCO3与稀硝酸反应:
B FeSO4溶液与溴水反应:
C. NaOH溶液与过量H2C2O4溶液反应:
D. C6H5ONa溶液中通入少量CO2:
12. 高铁酸钾是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通入氯气,然后再加入溶液的方法制备,发生反应:
①(未配平);
②。
下列说法正确的是
A. 反应①中每消耗,会吸收
B. 氧化性:
C. 若反应①中:1,则氧化剂与还原剂的物质的量之比为2:1
D. 若反应①的氧化产物只有KClO,则得到时消耗
二、非选择题(共四题)
13. 某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1ml·L-1。
某同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
②取少量溶液,加入KSCN溶液无明显变化。
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶依然澄清,且溶液中阴离子种类不变。
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由①、②、③判断,溶液中一定不含有的阳离子是__,一定不含有的阴离子是__(写离子符号)。
(2)③中加入少量盐酸生成无色气体的离子方程式是__,④中生成白色沉淀的离子方程式是_。
(3)将③中所得红棕色气体通入水中,气体变无色,所发生反应的化学方程式为__。
(4)该同学最终确定原溶液中所含阳离子是__,阴离子是__。
14. 新冠肺炎疫情期间,环境消毒是极其关键的,常常喷洒“84”消毒液,其有效成分为NaClO。
(1)某实验需用的消毒液,现用NaClO固体配制,用托盘天平称量NaClO的固体质量为___________g。
(2)实验中必须用到的玻璃仪器有烧杯、量筒、玻璃棒、___________。
(3)以下有关配制该溶液的说法正确的是___________(填字母)。
A.溶解NaClO固体的操作如图①所示
B.定容时的操作如图②所示
C.定容时的操作可用图③表示
D.定容时向容量瓶内加蒸馏水至接近刻度线1—2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
E.定容摇匀后,若发现凹液面低于刻度线,此时不需要用胶头滴管补加蒸馏水至刻度线
(4)下列操作可能使配制溶液浓度偏低的是___________(填字母)。
A.移液时,未洗涤烧杯内壁和玻璃棒 B.溶解后未经冷却就移液且马上定容
C.移液时,有少量液体溅出 D.定容时,仰视刻度线
E.容量瓶内有少量水
(5)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分盐酸)与“84”消毒液而发生氯气中毒事件。请用离子方程式解释其原因:___________。
(6)含氯消毒剂的消毒能力可以用“有效氯”来表示,“有效氯”是指与含氯消毒剂氧化能力相当的氯气的质量。某溶液中含有1mlNaClO,该溶液的“有效氯”是___________g。
15. 氯酸锶白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
(1)仪器b的名称是___________。
(2)A中发生反应的离子方程式为___________。
(3)装置B中所装试剂名称为:___________,其作用是___________。
(4)装置C中搅拌的目的是___________;发生反应的化学方程式为___________。
(5)装置D的作用___________;反应一段时间后,可观察到装置D中红色逐渐褪去,某实验小组的同学对红色突然褪去的原因进行猜想:
猜想一:氯水中的酸或氯分子与NaOH发生反应,将NaOH消耗所致
猜想二:氯水中次氯酸的强氧化性,使红色褪去所致。
假如猜想一成立,请设计实验证明该猜想红色褪去的原因:___________。
16. 氧化还原反应在工业生产、环保及科研中有广泛的应用,请根据以下信息,结合所掌握的化学知识,回答下列问题:
I.酸性KMnO4在生活、卫生医疗中常用作消毒剂。
(1)取300mL0.2ml·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是___________ml。
(2)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,配平上述反应的离子方程式________:++=+ +。
II.钒性能优良,用途广泛,有金属“维生素”之称。
(3)将废钒催化剂(主要成分为V2O5)与稀硫酸、K2SO3溶液混合,充分反应后生成VO2+,该反应中氧化剂和还原剂的物质的量之比为___________。
(4)V2O5能与盐酸反应生成VO2+和一种黄绿色气体,该黄绿色气体能与Na2SO3溶液反应而被吸收,则SO、Cl-、VO2+还原性由强到弱的顺序是___________。
(5)偏钒酸铵在加热条件下反应会生成V2O5、NH3和H2O。V2O5在氮气氛围中,碳高温条件下还原氮气制备VN,还生成一种具有还原性的气体,则该反应的化学方程式为___________。生成标况下22.4L该还原性气体时,反应转移电子数为___________。
高三年级 化学学科 阶段练习(10月)
相对原子质量:H:1 O:16 Si:28 Na:23 C1:35.5
一、选择题(共12题,每题只有一个正确答案)
【1题答案】
【答案】A
【2题答案】
【答案】B
【3题答案】
【答案】A
【4题答案】
【答案】A
【5题答案】
【答案】B
【6题答案】
【答案】D
【7题答案】
【答案】B
【8题答案】
【答案】C
【9题答案】
【答案】D
【10题答案】
【答案】B
【11题答案】
【答案】B
【12题答案】
【答案】D
二、非选择题(共四题)
【13题答案】
【答案】 ①. K+、Fe3+ ②. CO、SiO ③. 3Fe2++NO+4H+=3Fe3++NO↑+2H2O ④. Ba2++SO=BaSO4↓ ⑤. 3NO2+H2O=2HNO3+NO ⑥. Fe2+、Mg2+ ⑦. Cl-、NO、SO
【14题答案】
【答案】(1)74.5
(2)500mL容量瓶、胶头滴管
(3)DE (4)ACD
(5)ClO-+Cl-+2H+=Cl2↑+H2O
(6)71
【15题答案】
【答案】(1)分液漏斗
(2)
(3) ①. 饱和食盐水 ②. 吸收Cl2中混有的HCl
(4) ①. 增大反应物接触面积,促进反应完全,增大反应速率 ②.
(5) ①. 吸收多余的Cl2,防止其污染环境 ②. 取褪色后的溶液于试管中,继续滴加足量的NaOH溶液,若溶液恢复红色,说明猜想一正确;反之,猜想二正确。
【16题答案】
【答案】(1)
(2)
(3)
(4)
(5) ① ②. 阳离子
K+、Mg2+、Fe3+、Al3+、Fe2+
阴离子
Cl-、CO、NO、SO、SiO
①
②
③
相关试卷
这是一份天津市第二十一中学2025-2026学年高三上学期10月月考化学试题(含答案),共11页。试卷主要包含了 下列关于0,6 g, 下列装置或操作与说法正确的是等内容,欢迎下载使用。
这是一份天津中学2025-2026学年高二上学期10月月考化学试题(含答案),共11页。试卷主要包含了选择题,解答题等内容,欢迎下载使用。
这是一份天津市第十四中学2025-2026学年高三上学期10月月考化学试题(无答案),共8页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





