

安徽省合肥市七中2025-2026学年高二上学期10月考试化学试卷
展开 这是一份安徽省合肥市七中2025-2026学年高二上学期10月考试化学试卷,共8页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
可能用到的相对原子质量:H 1C 12N 14O 16Na 23
一、选择题:本题共 20 个小题,每小题 3 分,共 60 分。在每小题给出的四个选项中,只有一项是符合题目要求的。
下列科技成果中蕴含的化学知识叙述正确的是() A.高效光解水催化剂能降低化学反应的焓变
B.建造“福厦高铁”跨海大桥所采用的免涂装耐候钢属于合金 C.运载火箭所采用的“液氢液氧”推进剂可把化学能全部转化为热能 D.利用海洋真菌可降解聚乙烯等多种塑料,且温度越高降解速率越快
下列反应中,生成物的总焓大于反应物总焓的是() A.硫在氧气中燃烧B.氢氧化钡晶体与氯化铵混合
C.NaOH 溶液与 H2SO4 溶液混合D.Al 在高温条件下与 Fe2O3 反应
下列事实中,不能用勒夏特列原理解释的是() A.夏天,打开啤酒瓶时会从瓶口逸出气泡 B.使用催化剂可加快 SO2 转化为 SO3 的速率
C.将盛有二氧化氮和四氧化二氮混合气体的密闭容器置于冷水中,混合气体颜色变浅 D.用饱和食盐水除去氯气中的氯化氢气体
已知:25℃、101kPa 时,0.5ml H2 完全燃烧生成液态水放出 142.9kJ 的热量,下列能表达H2 燃烧热
的热化学方程式中书写正确的是()
2H2 O2 2H2O H 142.9kJ ml1
H2
g 1 O
2
2 g H2Ol
H 285.8kJ ml1
2H2 g O2 g 2H2O g H 571.6kJ ml1
H2
g 1 O
2
2 g H2Og
H 285.8kJ ml1
以 N2O5 为新型硝化剂的硝化反应具有反应条件温和、选择性高、无副反应发生、过程无污染等优点。 N2O5 可通过 N2O4 臭氧化法制备。
已知:①N2O4(g)===2NO2(g)ΔH1
②2O3(g)===3O2(g)ΔH2
③2N2O5(s)===4NO2(g)+O2(g)ΔH3
则 N2O4(g)+O3(g)===N2O5(s)+O2(g)的 ΔH 为()
A.ΔH1+ΔH2-1ΔH3B.2ΔH1-ΔH2+ΔH3
2
C.ΔH1+1ΔH2-1ΔH3D.2ΔH1+1ΔH2+1ΔH3
2222
反应 A(g)+3B(g)⇌2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是() A.v(A)=0.15ml•L-1•min-1B.v(B)=0.01ml•L-1•s-1
C.v(C)=0.0075ml•L-1•s-1D.v(D)=0.40ml•L-1•min-1
已知化学反应 A2(g)+B2(g)‡ˆ ˆ†ˆ 2AB(l)的能量变化如图所示,判断下列叙述中正确的是()
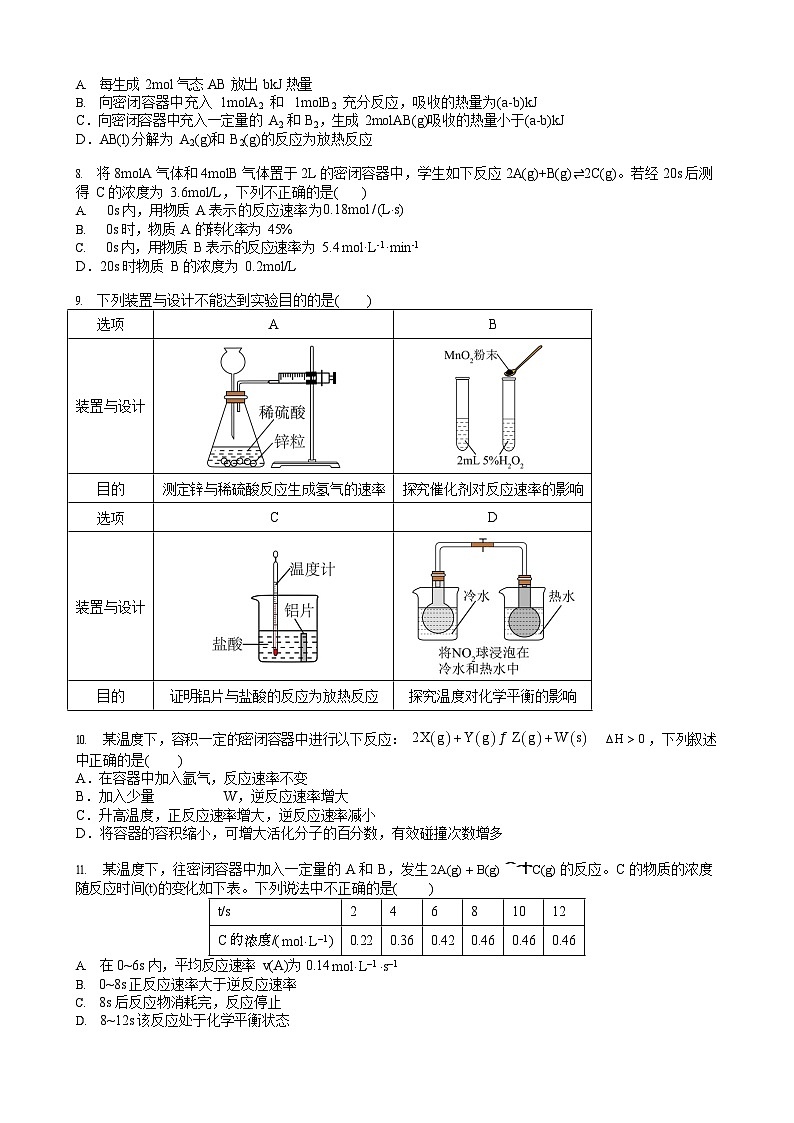
每生成 2ml 气态 AB 放出 bkJ 热量
向密闭容器中充入 1mlA2 和 1mlB2 充分反应,吸收的热量为(a-b)kJ C.向密闭容器中充入一定量的 A2 和 B2,生成 2mlAB(g)吸收的热量小于(a-b)kJ D.AB(l)分解为 A2(g)和 B2(g)的反应为放热反应
将 8mlA 气体和 4mlB 气体置于 2L 的密闭容器中,学生如下反应 2A(g)+B(g)⇌2C(g)。若经 20s 后测得 C 的浓度为 3.6ml/L,下列不正确的是()
0s 内,用物质 A 表示的反应速率为0.18ml / (Ls)
0s 时,物质 A 的转化率为 45%
0s 内,用物质 B 表示的反应速率为 5.4 ml·L-1·min-l D.20s 时物质 B 的浓度为 0.2ml/L
下列装置与设计不能达到实验目的的是()
选项
A
B
装置与设计
目的
测定锌与稀硫酸反应生成氢气的速率
探究催化剂对反应速率的影响
选项
C
D
装置与设计
目的
证明铝片与盐酸的反应为放热反应
探究温度对化学平衡的影响
某温度下,容积一定的密闭容器中进行以下反应: 2Xg Yg ƒ Zg W s
中正确的是() A.在容器中加入氩气,反应速率不变 B.加入少量 W,逆反应速率增大 C.升高温度,正反应速率增大,逆反应速率减小
D.将容器的容积缩小,可增大活化分子的百分数,有效碰撞次数增多
H 0 ,下列叙述
某温度下,往密闭容器中加入一定量的 A 和 B,发生2A(g) B(g) ‡ˆˆ†ˆ C(g) 的反应。C 的物质的浓度随反应时间(t)的变化如下表。下列说法中不正确的是()
在 0~6s 内,平均反应速率 v(A)为 0.14 ml L1 s1
0~8s 正反应速率大于逆反应速率
8s 后反应物消耗完,反应停止
8~12s 该反应处于化学平衡状态
t/s
2
4
6
8
10
12
C 的浓度/( ml L1 )
0.22
0.36
0.42
0.46
0.46
0.46
下列关于各图像的解释或得出的结论不正确的是()
由甲图可知,反应在t1 时刻可能改变了压强或使用了催化剂
由乙图可知,反应在 m 点可能达到了平衡状态
由丙图可知,C 点: v正 v逆
由丁图可知,交点 A 表示反应一定处于平衡状态,此时v正 v逆
N2O 和 CO 是环境污染性气体,可在 Pt2O+表面转化为无害气体,有关化学反应的物质变化过程及能量变化过程分别如图甲、乙所示。下列说法不正确的是()
总反应为 N2O(g)+CO(g)=CO2(g)+N2(g) ΔH=ΔH1+ΔH2
2
为了实现转化,需不断向反应器中补充 Pt2O+和 Pt2O
该反应正反应的活化能小于逆反应的活化能 D.总反应的 ΔH=-226 kJ·ml-1
工业可通过甲醇羰基化法制取甲酸甲酯HCOOCH3 : CH3OHg COg ƒ HCOOCH3 g ,在容积固定的密闭容器中,投入等物质的量CH3OH 和CO ,测得相同时间内CO 的转化率随温度变化如下图所示。下列说法不正确的是( )
A.b 点反应速率v正 v逆 B.升高温度,甲醇转化率会减小 C.生产时反应温度控制在80 85℃ 为宜 D.平衡常数 K75℃ K85℃ ,反应速率vb vd
某课题小组设计一种常温脱除烟气中 NO 的方法,其反应原理如图所示。下列说法错误的是()
催化剂
整个过程的总反应方程式为4NH3 4NO O2 4N2 6H2O
V5 O 在整个反应中起到催化作用 C.反应过程中有极性键的断裂与形成 D.该反应原理涉及的总反应的ΔS>0
恒温恒压下,对于反应:A(g)+3B(g) 3C(g),达到平衡状态的标志是()
A.v 正(A)=3v 逆(C) B.密闭容器内气体的密度不再改变
C.单位时间内消耗 3n mlC 的同时,生成 3n mlB
D.密闭容器内 A、B、C 气体的浓度之比为 1:3:2
下列反应低温有利于自发进行的是()
2KClO3 s 2KCls 3O2 g;ΔH 0
2COg 2Cs,石墨 O2 g;ΔH 0
4Fe(OH)2 s 2H2Ol O2 g 4Fe(OH)3 s;ΔH 0
CaCO3 s CaOg CO2 g;ΔH 0
下列有关实验操作、现象和解释或结论都正确的组合是()
A.AB.BC.CD.D
乙烯直接水合法生产乙醇的反应为 H2Og C2H4 g ƒ CH3CH2OHg 。在容积为 3L 的密闭容器中,
n C2H4
2
投料比 1:1时,乙烯的平衡转化率与温度、压强的关系如图。下列说法正确的是()n H O
选项
实验操作
现象
解释或结论
A
取 0.1ml·L-1 Na2S2O3 溶液,向其中加入 0.1ml·L-1 的硫酸,再分别在 20℃、30℃下,发生反应
2H S O2 =S SO H O
2 322
30℃下先出现浑浊
温度越高,反应速率越快
B
向FeCl3 和KSCN 的混合溶液中加入少量铁粉
血红色溶液颜色变浅
铁粉与Fe3 反应,降低了Fe3 的浓 度,使得平衡正向移动
C
两支试管中各盛有 2mL0.1ml·L-1 酸性高锰酸钾溶液,分别加入 5mL0.1ml·L-1 草酸溶液和 5mL0.2 ml·L-1 草酸溶液
加入 0.2ml·L-1 草酸溶液的试管中,高锰酸钾溶液褪色更快
反应物浓度越大,反应速率越快
D
向紫色石蕊溶液中通入SO2
溶液紫色逐渐变浅
SO2 具有漂白性
2 4
c H2O
当 c C H 不变时,反应达到平衡
该反应的H 0 ,且压强 p1 p2 p3
a、b、c 三点的平衡状态相比, K b K a K c
2
n C2H4
其他条件不变,增大起始投料比 n H O ,一定能提高乙烯的平衡转化率
相关数据实验编号
①
②
③
④
⑤
c(NO)/ml·L-1
0.006
0.001
0.006
0.002
0.003
c(H2)/ml·L-1
0.001
0.006
0.002
0.006
0.006
v 初始/ml·L-1·s-1
3.2×10-3
4.8×10-4
6.4×10-3
1.92×10-3
4.32×10-3
探究反应 2NO(g)+2H2(g) ƒ N2(g)+2H2O(g)△H”“
(2)50%0.025ml·L-1·min-1BC
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




