


第二节 化学反应的表示(教学课件)-2025-2026学年八年级化学全一册(鲁教版五四学制2024)
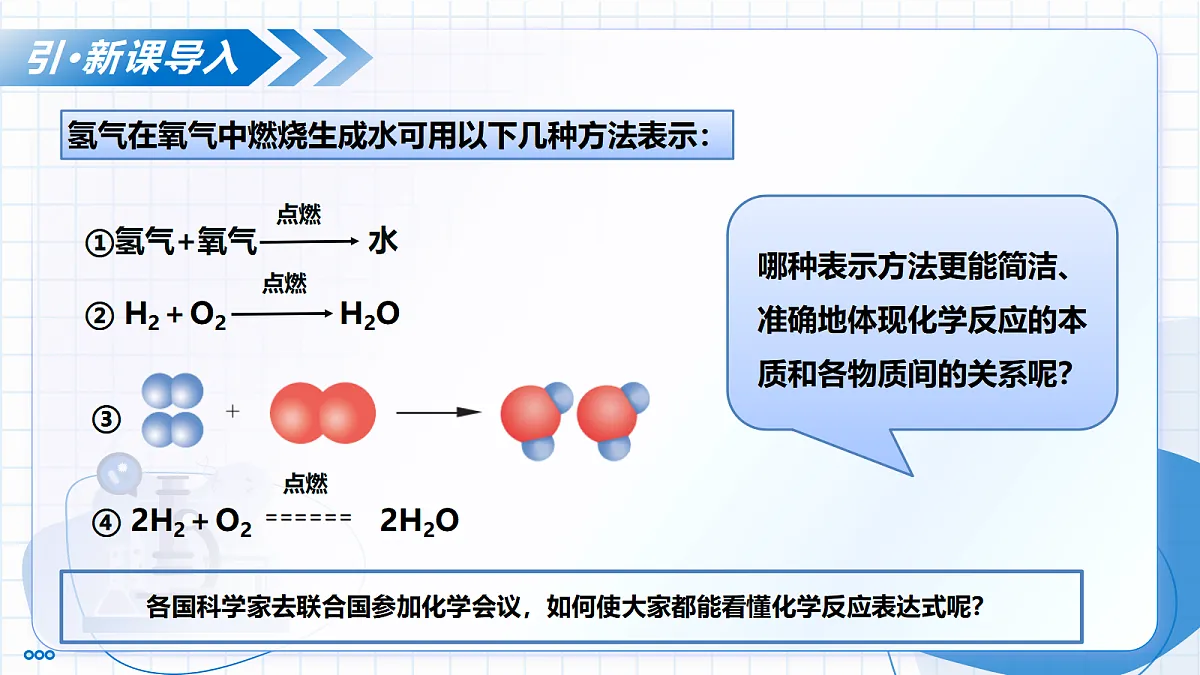
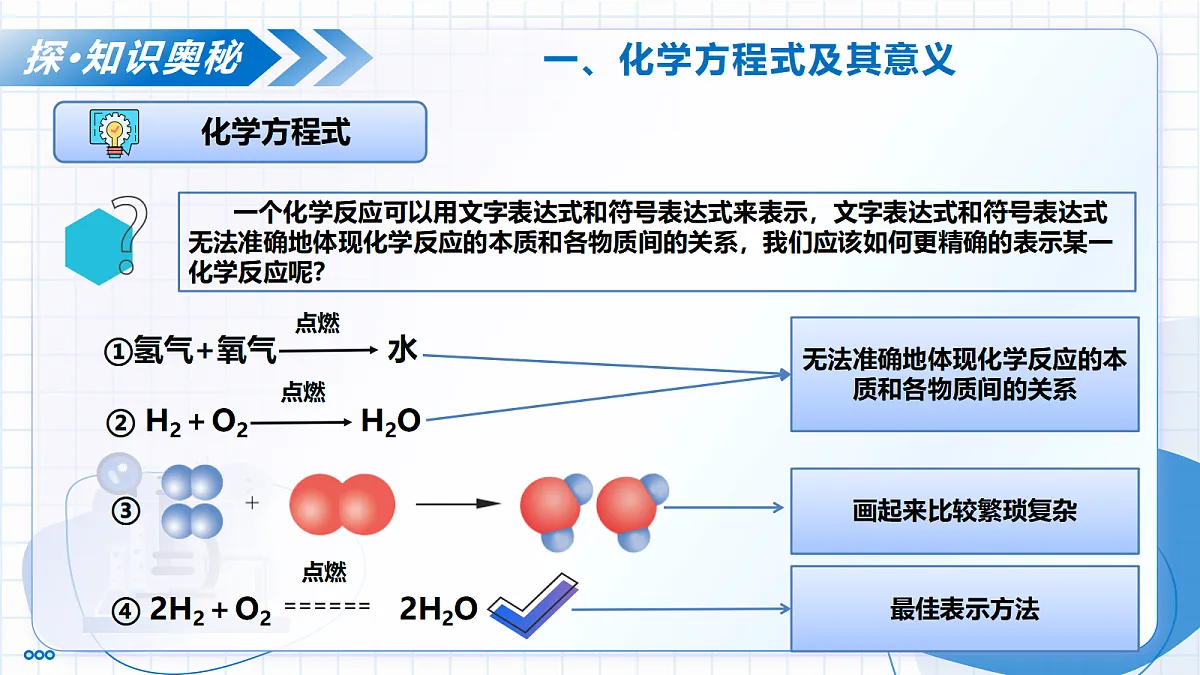
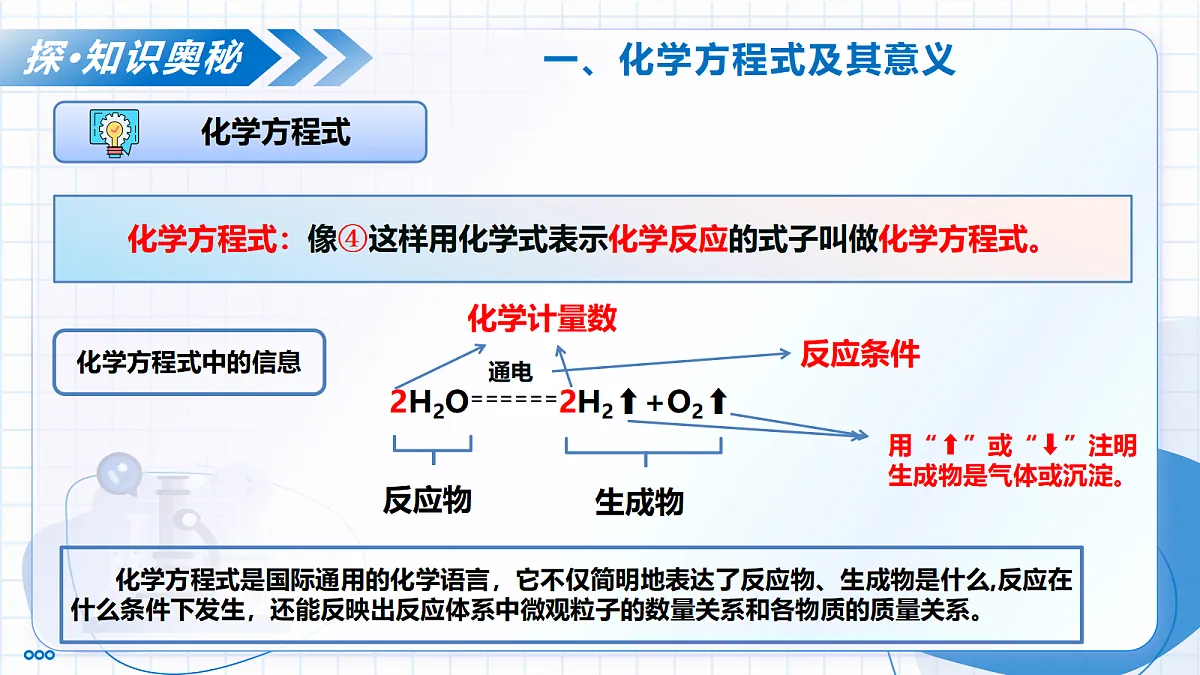
展开第五单元 定量研究化学反应第二节 化学反应的表示 八年级化学 全一册·鲁教版五四学制2024学习内容导览明·学习目标 1.理解化学方程式的含义,包括表示反应物、生成物、反应条件,以及各物质之间的质量比、粒子数目比等。2.掌握化学方程式的书写原则和步骤,能正确书写简单的化学方程式。在化学方程式书写的探究过程中,提高学生的逻辑思维和动手实践能力。3.体会化学方程式作为国际通用化学语言的简洁性和重要性,培养学生严谨、规范的科学态度,以及遵循客观规律的科学精神。② H2+O2 H2O引·新课导入各国科学家去联合国参加化学会议,如何使大家都能看懂化学反应表达式呢?氢气在氧气中燃烧生成水可用以下几种方法表示:①氢气+氧气 ④ 2H2+O2 ====== 2H2O点燃③点燃哪种表示方法更能简洁、准确地体现化学反应的本质和各物质间的关系呢?探·知识奥秘一、化学方程式及其意义一个化学反应可以用文字表达式和符号表达式来表示,文字表达式和符号表达式无法准确地体现化学反应的本质和各物质间的关系,我们应该如何更精确的表示某一化学反应呢?①氢气+氧气 ④ 2H2+O2 ====== 2H2O点燃③点燃② H2+O2 H2O无法准确地体现化学反应的本质和各物质间的关系画起来比较繁琐复杂最佳表示方法探·知识奥秘一、化学方程式及其意义化学方程式:像④这样用化学式表示化学反应的式子叫做化学方程式。 2H2O======2H2⬆+O2⬆通电化学方程式中的信息反应物生成物反应条件化学计量数化学方程式是国际通用的化学语言,它不仅简明地表达了反应物、生成物是什么,反应在什么条件下发生,还能反映出反应体系中微观粒子的数量关系和各物质的质量关系。用“⬆”或“⬇”注明生成物是气体或沉淀。2H2 + O2 ==== 2H2O探·知识奥秘一、化学方程式及其意义观察氢气燃烧的化学方程式:点燃思考下列问题该反应中的反应物、生成物及反应条件是什么?在该反应中氢分子、氧分子和水分子的个数比是多少?你能求出在该反应中氢气、氧气和水的质量比是多少吗?2H2 + O2 ———— 2H2O探·知识奥秘一、化学方程式及其意义点燃粒子数目之比 质量关系: 相对质量之比 物质的质量之比 2(1×2) :16×2 : 2(1×2+16)4 ︰ 32 ︰ 362 : 1 : 2观察氢气燃烧的化学方程式及微观示意图根据质量守恒定律可知:化学反应前后,原子种类不变,原子数目不变相对原子质量:H-1 C-12 O-16从各物质粒子及质量关系中,你还能发现哪些规律?探·知识奥秘一、化学方程式及其意义2H2 + O2 ———— 2H2O点燃氢气和氧气在点燃的条件下反应生成水宏观每2个氢分子和1个氧分子在点燃的条件下反应生成2个水分子微观每4份质量的氢气和32份质量的氧气在点燃的条件下反应生成36份质量的水质量关系化学方程式中,化学计量数之比等于粒子个数之比探·知识奥秘一、化学方程式及其意义化学方程式相比其他表示方法,有什么优点?化学方程式等号两边各原子的种类和数目相等,能清晰地反映出化学反应前后物质的质量关系。体现质量守恒定律化学方程式不仅写出了反应物和生成物的化学式,还用等号连接,同时注明了反应条件,对于有气体或沉淀生成的反应,还会标注气体符号或沉淀符号。 信息完整性化学式和符号简洁地表示了反应,且国际通用,不受语言文字差异的限制 。表达简洁性化学方程式能清晰地展现出反应物和生成物之间的粒子数目比、质量比等定量关系,为化学研究和实际生产中的定量计算提供了依据。定量分析优势化学方程式使用化学式和特定的符号,更符合化学学科的专业表达方式,能深入体现化学反应的本质,如原子的重新组合等微观过程。体现化学学科特点理·核心要点化学方程式及其意义化学方程式的表示方法化学方程式的意义 2H2O======2H2⬆+O2⬆通电反应物生成物反应条件化学计量数用“⬆”或“⬇”注明生成物是气体或沉淀。宏观表示了反应物、生成物及反应条件。用化学式表示化学反应的式子叫做化学方程式。微观化学方程式中,化学计量数之比等于粒子个数之比质量各物质的微粒的质量比1.依据化学方程式 ,下列信息不正确的是( )A.该反应是化合反应B.该反应是在点燃的条件下进行的C.该反应中三种物质的质量比为2:1:1D.该反应中参加反应的氧气与生成的二氧化碳的分子个数比为1:2析·典型范例C2.液氢、液氧可作为火箭发动机的推进剂,其反应的微观示意图如下所示。下列说法正确的是( )A.乙为氧化物 B.该反应为化合反应C.反应前后分子的个数不变D.反应前后氧元素的化合价不变析·典型范例B探·知识奥秘二、化学方程式的书写H2+O2===H2O点燃P+O2===PO2点燃反应前后原子数目不相等,不遵循质量守恒定律。生成物应为P2O5,不遵循客观事实。书写化学方程式的两大原则:必须以客观事实为基础必须遵循质量守恒定律探·知识奥秘二、化学方程式的书写首先在短线的左边写出参加反应的物质(反应物)的化学式,然后在短线的上方注明反应条件,最后在短线的右边写出反应所生成的物质(生成物)的化学式,同时注明生成物的状态(气体⬆沉淀⬇符号)。第一步:描述反应事实01根据质量守恒定律,在相应的化学式前配上适当的数字(称为化学计量数),使反应前后各种元素的原子个数相等。第二步:配平02探·知识奥秘二、化学方程式的书写写出水通电分解生成氢气和氧气的反应方程式在等号左右两边写出反应物和生成物的化学式化学式的书写要遵循客观事实。添加反应条件常见的反应条件:加热(△)、点燃、通电、高温、催化剂等探·知识奥秘二、化学方程式的书写观察是否需要标注气体⬆和沉淀下箭头符号表示反应生成了气体或沉淀如果反应物和生成物中都有气体,气体生成物就不需要标注“⬆”。反应物中没有气体,反应后生成了气体,需要标注“⬆”。同样,对于溶液中的反应,如果反应物和生成物中都有固体,固体生成物也不需要标注“⬇”。反应物中没有固体,反应后生成了固体,需要标注“⬇” 化学方程式的书写步骤探·知识奥秘二、化学方程式的书写现在反应前后同种元素原子个数并不相等,如何使其相等符合质量守恒定律?OOH氢原子O氧原子HHOHH添加化学计量数:这一过程我们称为化学方程式的配平探·知识奥秘二、化学方程式的书写22化学方程式的配平:根据质量守恒定律,就是在式子两边的化学式前配上适当的化学计量数,使式子两边每一种元素原子的数目相等。H氢原子O氧原子探·知识奥秘二、化学方程式的书写22化学方程式的配平:根据质量守恒定律,就是在式子两边的化学式前配上适当的化学计量数,使式子两边每一种元素原子的数目相等。H氢原子O氧原子探·知识奥秘二、化学方程式的书写 最小公倍数法:选择左右只出现一次且个数最多的原子作起点,求其最小公倍数,再以最小公倍数分别除以该原子在不同化学式中的个数作为该化学式的化学计量数,并由此推出其它化学计量数。2和3的最小公倍数是66÷336÷22右边铝原子的总数是44检查反应前后原子个数是否相等探·知识奥秘二、化学方程式的书写注意事项:1、配平时不得随意更改化学式右下角的角码2、化学计量数必须化成最简整数比实战演练:配平下列化学方程式高温点燃点燃高温点燃点燃二、化学方程式的书写(以 “ 氯酸钾 氯化钾+氧气” 为例)加热左反右生一横线箭号标气或沉淀等号上下注条件配平以后加一线 KClO3 KCl+ O2 KClO3 KCl+ O2 KClO3 KCl+ O2 2 KClO3 2KCl+ 3 O2MnO2MnO2△理·核心要点△化学方程式的书写反应物中没有气体,反应后生成了气体,需要标注“⬆”化学式的书写要遵循客观事实。配平后检查反应前后原子个数是否相等注意事项:1、配平时不得随意更改化学式右下角的角码2、化学计量数必须化成最简整数比1.下列有关反应的化学方程式正确的是( )A.过氧化氢在二氧化锰的催化作用下分解:B.实验室用高锰酸钾制取氧气:C.碳在氧气中燃烧生成二氧化碳:D.磷在氧气中燃烧生成五氧化二磷:析·典型范例D2.电解水的简易实验装置如下图所示。下列相关说法不正确的是( ) 析·典型范例B理·核心要点化学反应的表示化学方程式的意义化学方程式的书写宏观表示了反应物、生成物及反应条件。微观化学方程式中,化学计量数之比等于粒子个数之比质量各物质的微粒的质量比步骤:左反右生一横线➡箭号标气或沉淀➡等号上下注条件➡配平以后加一线书写化学方程式的两大原则:1、必须以客观事实为基础2、必须遵循质量守恒定律注意事项:1、配平时不得随意更改化学式右下角的角码2、化学计量数必须化成最简整数比3、反应物中没有气体,反应后生成了气体,需要标注“⬆”4、反应物中没有固体,反应后生成了固体,需要标注“⬇”5、常见的反应条件:加热(△)、点燃、通电、高温、催化剂等1.利用化学方法可消除家居装修过程中的甲醛,其反应的微观示意图如下。下列说法不正确的是( )A.图中的单质为氧气B.反应的产物均为无毒物质C.反应前后元素的化合价均无变化D.反应的化学方程式为练·技能实战C2.中国芯片蚀刻技术国际领先。用NF3进行硅芯片蚀刻时,产物均为气体,在蚀刻物表面不留任何残留物。该反应的微观示意图如下图所示。下列说法错误的( )A.丁物质由分子构成B.反应中甲和丙的分子个数之比为3:4C.反应中硅元素的化合价升高D.反应前后元素的种类和质量均不变练·技能实战BTHANKS!谢谢观看八年级化学 全一册·鲁教版五四学制2024
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)




