








2026年高考化学第一轮总复习导学案--第13讲 铁及其化合物(含答案)
展开 这是一份2026年高考化学第一轮总复习导学案--第13讲 铁及其化合物(含答案),文件包含模块2主题4第13讲铁及其化合物pptx、2026年高考化学第一轮总复习导学案--第13讲铁及其化合物含答案doc等2份学案配套教学资源,其中学案共11页, 欢迎下载使用。
1. 了解铁及其重要化合物的主要物理性质。2. 了解铁分别与氧气、水、酸、盐等物质反应的情况。3. 认识Fe3+和Fe2+之间的相互转化,了解Fe3+的检验方法。4. 了解氧化铁与酸反应的情况。5. 了解氢氧化铁、氢氧化亚铁的制备方法,了解氢氧化铁的受热分解。
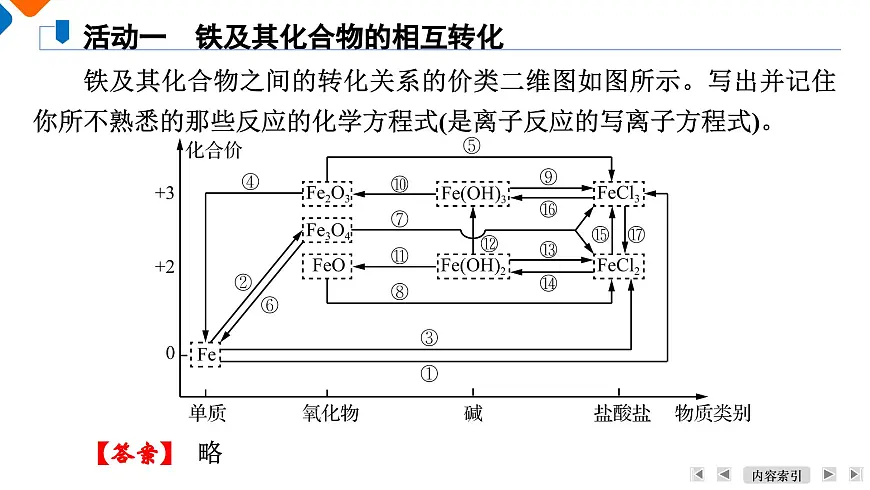
铁及其化合物之间的转化关系的价类二维图如图所示。写出并记住你所不熟悉的那些反应的化学方程式(是离子反应的写离子方程式)。
活动一 铁及其化合物的相互转化
1. 铁与酸的反应。(1) 铁除了能与盐酸反应外,还能与硫酸、硝酸发生反应。请写出铁与稀硫酸、过量稀硝酸、少量稀硝酸发生反应的离子方程式。
活动二 铁的重要性质
(2) 常温下,将铁投入浓硫酸或浓硝酸中,铁表面均看不到明显变化。请设计简单的实验证明铁发生了钝化。提供的实验试剂有:铁、浓硝酸、浓硫酸、硫酸铜溶液。【答案】 将铁从浓硫酸或浓硝酸中取出,小心投入硫酸铜溶液中,没有明显现象,说明铁表面发生了钝化。
2. 铁与水的反应。下图所示的装置可实现铁和水蒸气的反应。
(1) 加热湿棉花的目的是什么? 【答案】 提供水蒸气,使之与还原铁粉在高温下发生反应。(2) B处酒精灯上网罩的作用是什么?实验开始时,应先点燃哪个酒精灯?【答案】 集中火焰,产生高温;A。
(3) 将产生的气体导入肥皂液中的目的是什么?【答案】 将产生的气体导入肥皂液中是为了产生气泡,便于点燃验证产物中的气体。
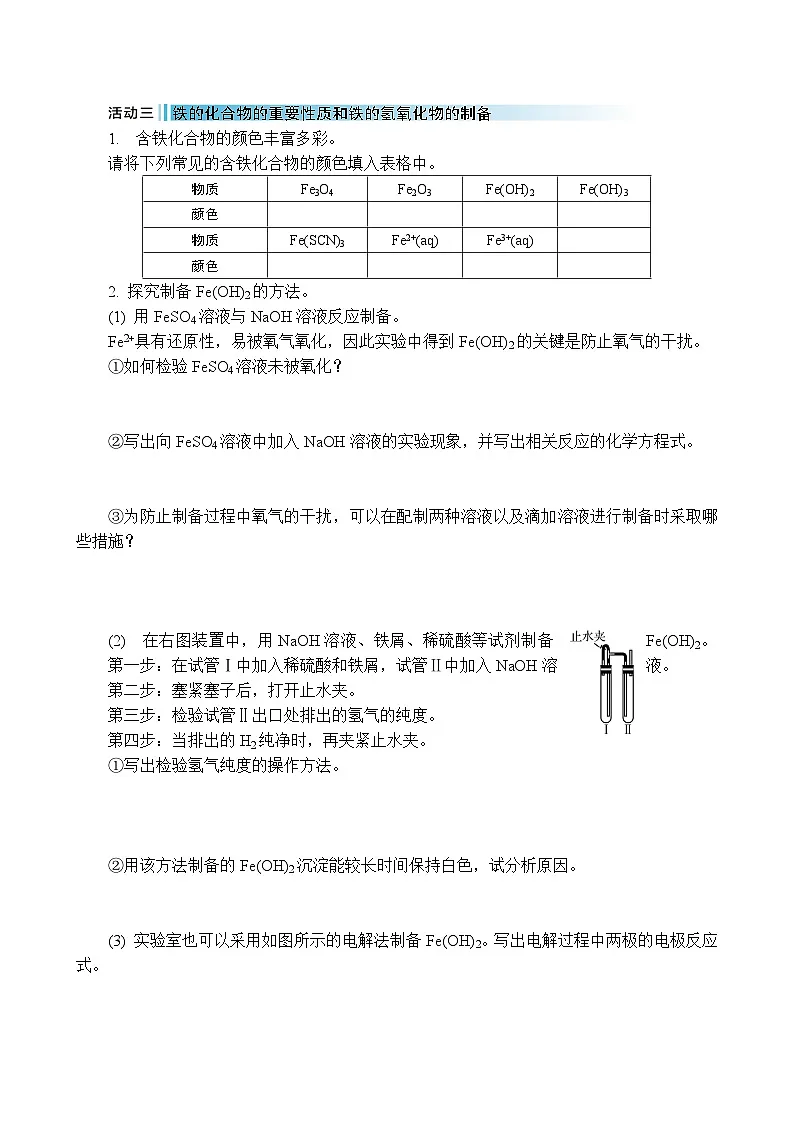
1. 含铁化合物的颜色丰富多彩。请将下列常见的含铁化合物的颜色填入表格中。
活动三 铁的化合物的重要性质和铁的氢氧化物的制备
2. 探究制备Fe(OH)2的方法。(1) 用FeSO4溶液与NaOH溶液反应制备。Fe2+具有还原性,易被氧气氧化,因此实验中得到Fe(OH)2的关键是防止氧气的干扰。①如何检验FeSO4溶液未被氧化?【答案】 取少量FeSO4溶液于一支洁净的试管中,加入KSCN溶液,观察是否有红色物质生成。
②写出向FeSO4溶液中加入NaOH溶液的实验现象,并写出相关反应的化学方程式。【答案】 产生的白色沉淀迅速成灰绿色,最终变为红褐色。FeSO4+2NaOH===Fe(OH)2↓+Na2SO44Fe(OH)2+O2+2H2O===4Fe(OH)3③为防止制备过程中氧气的干扰,可以在配制两种溶液以及滴加溶液进行制备时采取哪些措施?【答案】 在新制的FeSO4溶液中加入少量铁粉;用煮沸过的蒸馏水配制NaOH溶液或将NaOH溶液煮沸以减少溶解在溶液中的氧气含量;将胶头滴管伸入液面以下滴加溶液。
(2) 在右图装置中,用NaOH溶液、铁屑、稀硫酸等试剂制备Fe(OH)2。第一步:在试管Ⅰ中加入稀硫酸和铁屑,试管Ⅱ中加入NaOH溶液。第二步:塞紧塞子后,打开止水夹。第三步:检验试管Ⅱ出口处排出的氢气的纯度。第四步:当排出的H2纯净时,再夹紧止水夹。①写出检验氢气纯度的操作方法。【答案】 用一支干燥洁净的试管收集试管Ⅱ出口处排出的气体,用拇指堵住试管口,靠近酒精灯火焰,松开拇指,若听到尖锐的爆鸣声,说明氢气不纯,若听到“噗”声,说明氢气已经纯净。
②用该方法制备的Fe(OH)2沉淀能较长时间保持白色,试分析原因。【答案】 试管Ⅰ中反应生成的H2将试管Ⅰ和试管Ⅱ中的空气排出,且外界O2不易进入,Fe(OH)2不易被氧化。
(3) 实验室也可以采用如图所示的电解法制备Fe(OH)2。写出电解过程中两极的电极反应式。
【答案】 阳极:Fe-2e-===Fe2+阴极:2H2O+2e-===H2↑+2OH-
3. 氢氧化铁的获得与分解。(1) 写出向FeCl3溶液中滴加NaOH溶液时发生反应的离子方程式。【答案】 Fe3++3OH-===Fe(OH)3↓(2) 将FeCl3溶液加热蒸干,继续加强热,至固体质量不再发生变化,最终所得固体残渣是什么?如果加热的是FeCl2溶液呢?【答案】 氧化铁。加热FeCl2溶液得到的也是氧化铁。
4. Fe3+和Fe2+之间的相互转化。利用FeCl3溶液腐蚀电路铜板的废液回收Cu和FeCl3,流程如下:(1) 通过实验确定溶液A中既含Fe2+又含Fe3+。【答案】 取少许溶液A,滴加K3[Fe(CN)6]溶液,出现蓝色沉淀,说明含有Fe2+;另取少许溶液A,滴加KSCN溶液,溶液显红色,说明含有Fe3+。
(2) 试剂X最适宜选择_________(填字母,下同),试剂Y可以选择__________。A. Zn B. Fe C. SO2 D. NaI E. Cl2 F. HNO3G. H2O2 H. 酸性KMnO4溶液
1 [2024苏锡常镇一调]实验室由硫铁矿烧渣(含FeO、Fe2O3、SiO2等)制取无水氯化铁的实验原理和装置不能达到实验目的的是( )
A. 用装置甲溶解硫铁矿烧渣B. 用装置乙过滤得到含Fe2+、Fe3+混合溶液C. 用装置丙氧化得到FeCl3溶液D. 用装置丁蒸干溶液获得无水FeCl3
【解析】 由于加热会促进Fe3+的水解和HCl的挥发,故欲制得无水FeCl3,应该在HCl气氛中蒸发浓缩、冷却结晶、脱水,装置丁不能达到实验目的,D符合题意。
2 [2023江苏卷]室温下,探究0.1 ml/L FeSO4溶液的性质,下列实验方案能达到探究目的的是( )
3 [2024江苏卷]实验室进行铁钉镀锌实验。下列相关原理、装置及操作不正确的是( )
【解析】 不能在容量瓶中溶解固体,A错误。
A. 配制NaOH溶液 B. 铁钉除油污 C. 铁钉除锈 D. 铁钉镀锌
4 [2024无锡期末节选]FeCO3晶体细微多孔,能集纳和释放Li+,可作为Li+电池的负极材料。以FeSO4·7H2O为原料制备FeCO3的实验流程如图所示。
已知:产品FeCO3中含Fe(HCO3)2。当温度超过60 ℃时,FeCO3和Fe(HCO3)2开始分解。(1) 制备。①“反应”控温160 ℃。发生反应的离子方程式是_______________ ___________________________________________________。
②沉淀剂不使用Na2CO3的原因是______________________________ ________________________________________________________________________________________。(2) 检测。检测产品中的碳酸亚铁的质量分数。①热分解。称量0.800 0 g的样品,在500 ℃加热2 h,转移至干燥器中冷却,称量,重复操作至恒重,质量为0.506 0 g。(假定样品中杂质不含铁,且杂质在500 ℃时不分解)②测Fe(Ⅱ)。称取热解后的试样0.253 0 g放入锥形瓶中,加入5 mL 6 ml/L盐酸、10 mL 1 ml/L硫酸—磷酸混合酸,滴入4滴二苯胺磺酸钠指示剂,用0.010 00 ml/L K2Cr2O7标准溶液滴定至紫色稳定半分钟,消耗标准液16.67 mL。
Na2CO3溶液为碱性,易生成Fe(OH)2,碱性条件下,Fe(OH)2易被氧化产生Fe(OH)3沉淀等杂质[答到生成Fe(OH)2也可]
③测Fe(Ⅲ)。另取热解后的试样0.253 0 g放入锥形瓶中,_________ __________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________,消耗0.100 0 ml/L Na2S2O3标准溶液20.00 mL。(供选药品:5 g/L淀粉溶液,6 ml/L盐酸,KI固体,0.100 0 ml/L Na2S2O3标准溶液,蒸馏水。已知:2Na2S2O3+I2===Na2S4O6+2NaI)④数据处理。综合上述数据计算产品中碳酸亚铁的质量分数(写出计算过程)。
溶铁:边搅拌边加入6 ml/L盐酸大于1.6 mL(或至固体不再溶解);生碘:加入KI固体0.6 g(或大于0.53 g),再加入适量蒸馏水,充分搅拌;滴定:用0.100 0 ml/L Na2S2O3标准溶液滴定至溶液变为淡黄色,滴入2~3滴5 g/L淀粉溶液,继续滴定至溶液恰好由蓝色变为无色且半分钟内不恢复
【答案】 0.253 0 g热解后的试样中Fe3+、Fe2+的物质的量:n(Fe3+)=n(Na2S2O3)=0.100 0 ml/L×20.00×10-3 L=2.000×10-3 mln(Fe2+)=6n(K2Cr2O7)=6×0.010 00 ml/L×16.67×10-3 L≈ 1.000×10-3 ml0.253 0 g热解后的试样中杂质的质量:
0.800 0 g原样品中:m(FeCO3)+m[Fe(HCO3)2]=n(FeCO3)×116 g/ml+n[Fe(HCO3)2]× 178 g/ml=0.800 0 g-0.021 00 g×2=0.758 0 gn(FeCO3)+n[Fe(HCO3)2]=2×(2.000×10-3+1.000×10-3)ml=6.000×10-3ml联立以上两式,可得:n(FeCO3)=5.000×10-3 ml,n[Fe(HCO3)2]=1.000×10-3 ml
5 [2024南通二模]实验室以FeS2为原料制备磷酸亚铁晶体[Fe3(PO4)2·8H2O],其部分实验过程如下:
(1) 将一定体积98%的浓硫酸稀释为200 mL 30%的硫酸,除量筒外,还必须使用的玻璃仪器有_______________。(2) 检验“还原”已完全的实验操作为_________________________ _____________________________________________________________________________________________。
取少量还原后的溶液于试管中,滴加KSCN溶液(或亚铁氰化钾),溶液不变为红色(无特征蓝色沉淀),则“还原”已完全
(3) 向过滤后的滤液中加入Na2HPO4,并用氨水或CH3COONa调节溶液pH,“共沉淀”生成 Fe3(PO4)2·8H2O。①若使用CH3COONa调节溶液pH,“共沉淀”反应的离子方程式为_____________________________________________________________ _____________________。②不使用NaOH调节溶液pH的原因是___________________________ _____________________________________。
NaOH碱性强,容易造成局部pH过高,生成Fe(OH)2等杂质
③补充完整利用如图所示装置(夹持装置已略去)制取Fe3(PO4)2·8H2O的实验方案:向三颈烧瓶中加入抗坏血酸溶液,_____________________ ______________________________至混合液pH≈4,_________________ ________________________________________________________________________,充分搅拌一段时间,过滤,洗涤固体,真空干燥。(已知:所用抗坏血酸溶液pH=2.8,当溶液pH控制在4~6之间时,所得晶体质量最好。恒压滴液漏斗a、b中分别盛放FeSO4溶液和CH3COONa-Na2HPO4混合液)
向三颈烧瓶中滴加CH3COONa-Na2HPO4混合溶液
再向三颈烧瓶中滴加FeSO4溶液,通过调节恒压滴液漏斗a、b的活塞,控制溶液pH为4~6
(4) 测定样品中Fe3(PO4)2·8H2O(M=502 g/ml)的纯度(质量分数)。取0.627 5 g样品完全溶解后配制成250 mL溶液,取出25.00 mL于锥形瓶中,加入一定量的H2O2将铁元素完全氧化,以磺基水杨酸为指示剂,用0.020 00 ml/L EDTA标准溶液进行滴定至终点(Fe3+与EDTA按物质的量之比为1∶1发生反应),消耗EDTA溶液15.00 mL。计算该磷酸亚铁晶体样品的纯度:_____________(写出计算过程)。
【答案】 每25.00 mL溶液中n(Fe2+)=0.020 00 ml/L×15.00×10-3 L=3.000×10-4 mln[Fe3(PO4)2·8H2O]=1.000×10-4 ml
相关学案
这是一份2026年高考化学第一轮总复习导学案--第13讲 铁及其化合物(含答案),文件包含模块2主题4第13讲铁及其化合物pptx、2026年高考化学第一轮总复习导学案--第13讲铁及其化合物含答案doc等2份学案配套教学资源,其中学案共11页, 欢迎下载使用。
这是一份第8讲 铁及其化合物 学案(含答案)2026届高三化学一轮总复习,共10页。学案主要包含了 铁的概述, 铁的性质, 氢氧化亚铁的制备, 溶液中Fe2+等内容,欢迎下载使用。
这是一份2024年高考化学一轮复习 第15讲 铁及其氧化物和氢氧化物 学案(含答案),共11页。
相关学案 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




