

甘肃省兰州市2025届高三诊断考试(一模) 化学试卷(解析版)
展开 这是一份甘肃省兰州市2025届高三诊断考试(一模) 化学试卷(解析版),共22页。试卷主要包含了 下列离子方程式的书写正确的是等内容,欢迎下载使用。
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号框涂黑。如需改动,用橡皮擦干净后,再选涂其它答案标号框。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 K-39 Cu-64 I-127 Pb-207
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1. 文物承载着人类的文明与智慧。下列有关文物的叙述不正确的是
A. 武威出土的铜奔马属于合金材料
B. 马家窑出土的陶器属于硅酸盐产品
C. 甘肃简牍博物馆珍藏的竹简主要成分属于多糖
D. 敦煌壁画绘制用到的红色颜料为
【答案】D
【解析】A.铜奔马属于铜合金,为合金材料,A正确;
B.陶器的主要原料是粘土和陶土,其化学成分以硅酸盐为主,属于硅酸盐,B正确;
C.竹简主要成分是纤维素,属于多糖,C正确;
D.敦煌壁画绘制用到的红色颜料为,为黑色,D错误;
故选D。
2. 化学用语是描述化学物质组成及变化的专业语言符号。下列有关表述不正确的是
A. 用电子云轮廓图示意键的形成:
B. 的价层电子轨道表示式为:
C. 的价层电子对互斥(VSEPR)模型:
D. 的形成过程:
【答案】B
【解析】A.键电子云以肩并肩方式重叠形成,图示正确,故A正确;
B.的价层电子轨道表示式为:,故B错误;
C.中心O原子的价层电子对数为2+=3,含一对孤对电子,VSEPR模型为平面三角形,故C正确;
D.离子化合物,用电子式形成过程表示为,故D正确;
故选:B。
3. 科技工作者研究、利用化学知识造福人类,彰显了劳动者的智慧与精神。下列有关说法不正确的是
A. 酿酒师酿造葡萄酒添加目的是起杀菌和抗氧化等作用
B. 医生做“钡餐”透视时病人吞服的钡餐主要成分是
C. 材料科学家研制的包装材料聚乳酸()是由加聚而成
D. 环境保护工程师利用除去废水中的
【答案】C
【解析】A.SO2有杀菌作用,且有还原性,加在葡萄酒中可起到杀菌和抗氧化的作用,A正确;
B.做“钡餐”透视时所使用的主要成分是BaSO4,因其难溶于水且对X射线有良好阻挡作用,B正确;
C.聚乳酸一般由乳酸[HOCH(CH3)COOH]过缩聚方式生成,不是加聚反应,C错误;
D.Na2S能与Hg2+生成难溶于水的HgS,从而去除废水中的Hg2+,D正确;
故选C。
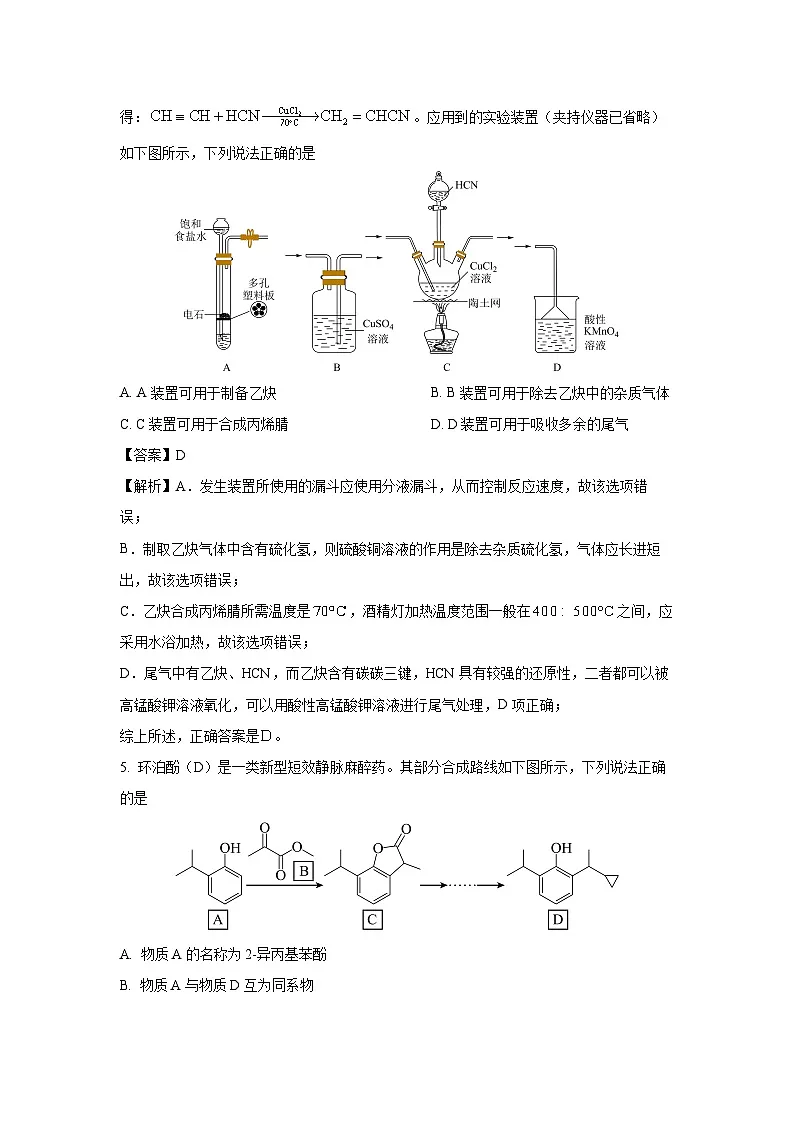
4. 丙烯腈是合成纤维、橡胶和树脂的重要材料,由乙炔与HCN反应制得:。应用到的实验装置(夹持仪器已省略)如下图所示,下列说法正确的是
A. A装置可用于制备乙炔B. B装置可用于除去乙炔中的杂质气体
C. C装置可用于合成丙烯腈D. D装置可用于吸收多余的尾气
【答案】D
【解析】A.发生装置所使用的漏斗应使用分液漏斗,从而控制反应速度,故该选项错误;
B.制取乙炔气体中含有硫化氢,则硫酸铜溶液的作用是除去杂质硫化氢,气体应长进短出,故该选项错误;
C.乙炔合成丙烯腈所需温度是,酒精灯加热温度范围一般在之间,应采用水浴加热,故该选项错误;
D.尾气中有乙炔、HCN,而乙炔含有碳碳三键,HCN具有较强的还原性,二者都可以被高锰酸钾溶液氧化,可以用酸性高锰酸钾溶液进行尾气处理,D项正确;
综上所述,正确答案是D。
5. 环泊酚(D)是一类新型短效静脉麻醉药。其部分合成路线如下图所示,下列说法正确的是
A. 物质A的名称为2-异丙基苯酚
B. 物质A与物质D互为同系物
C. 可用溶液检验D中是否存在未反应的A
D. 1mlB和C分别与足量的溶液反应均消耗
【答案】A
【解析】A.根据A的结构,母体为苯酚,异丙基在2号位上,故名称为2-异丙基苯酚,故A正确;
B.D的支链含有环状结构,与A的结构不相似,不是同系物,故B错误;
C.A和D中都含有酚羟基,都能使溶液显色,不能用溶液检验D中是否存在未反应的A,故C错误;
D.B中只含有1个酯基,1mlB只能消耗1mlNaOH,C含有酚酯基,1mlC消耗2mlNaOH,故D错误;
答案选A。
6. 下列离子方程式的书写正确的是
A. 用三氯化铁溶液刻蚀覆铜电路板:
B. 海水提溴过程中将溴吹入吸收塔:
C. 向中加入:
D. 电解水溶液的离子方程式:
【答案】B
【解析】A.反应中Fe元素化合价+3→+2,铜元素化合价0→+2,根据得失电子守恒,离子方程式应为:,A错误;
B.反应中Br元素化合价降低,0→-1,S元素化合价升高,+4→+6,根据得失电子守恒、电荷守恒、元素守恒可得离子方程式为:,B正确;
C.Na2O2既做氧化剂又做还原剂,所以离子方程式为:2H218O+2Na2O2=4Na++218OH-+2OH-+O2↑,C错误;
D.电解产生的氢氧根会和镁离子生成沉淀,正确的离子方程式为,D错误;
故选D;
7. 物质结构决定性质,性质决定用途。下列有关事实解释不正确的是
A. AB. BC. CD. D
【答案】D
【解析】A.无水乙醇极性较小,加入溶液后,降低溶剂的极性,导致该离子化合物的溶解度下降,析出深蓝色晶体,A正确;
B.石墨导电是由于每个碳原子以杂化形成平面结构,未杂化的p轨道垂直于平面,重叠形成离域大π键,电子可在平面内自由移动,B正确;
C.的酸性强于,因F的电负性比Cl大,吸电子效应更强,使羧基中的羟基极性更大,更易解离,C正确;
D.的熔点低于,主要原因是乙基的引入增大了阳离子体积,导致的半径大于,的离子键强度小于,所以熔点,而非改变晶体类型(仍为离子晶体),D错误;
故选D。
8. 离子化合物水解可用于制备石墨,其反应原理为(石墨,s,表示阿伏加德罗常数的值。下列说法正确的是
A. 2.7g中含有的离子总数为
B. 常温下,的溶液中含的数目为
C. 7.2g单层石墨中含有六元环的数目为
D. 每生成3.36L,转移电子的数目为
【答案】C
【解析】A.由K+、构成,2.7g物质的量为0.02ml,含有的离子总数为,A错误;
B.溶液体积未知,无法计算离子数目,B错误;
C.石墨中每个碳原子被3个六元环共用,故每个六元环实际占有2个碳原子,7.2克单层石墨含有0.6ml碳原子,石墨中含有的六元环的个数为0.3 NA,C正确;
D.氢气的温度、压强未知,无法计算转移电子数目,D错误;
故选C。
9. 钙钛矿太阳能电池材料中含有前四周期X、Y、Z、W四种元素。基态X原子s能级上的电子数是p能级上电子数的2倍,Y的第一电离能在同周期中仅小于两种元素,Z元素形成的单质为淡黄色固体,X、Z的质子数之和等于W的质子数。下列说法中正确的是
A. 基态原子中未成对电子数:
B. 简单氢化物的沸点:
C. 只有Z的最高价氧化物对应水化物为强酸
D. W位于第四周期、第ⅡB族
【答案】A
【解析】基态X原子s能级上的电子数是p能级上电子数的2倍,则其电子排布式为:1s22s22p2,则X为C元素,Y的第一电离能在同周期中仅小于两种元素,且原子序数比C大,则Y为N元素,Z元素形成的单质为淡黄色固体,则Z为S元素,X、Z的质子数之和等于W的质子数,则W为Ti元素,以此解题。
A.X为C元素,Y为N元素,Z为S元素,其价层电子排布式分别为:2s22p2,2s22p3,3s23p4,未成对电子数分别为:2、3、2,即:基态原子中未成对电子数:,A正确;
B.X为C元素,Y为N元素,Z为S元素,其简单氢化物分别为:CH4,NH3,H2S,其中氨气可形成分子间氢键,沸点较高,硫化氢分子量较大,其沸点比甲烷大,故简单氢化物的沸点:,B错误;
C.Y为N元素,其最高价氧化物对应的水化物为硝酸,是强酸,C错误;
D.W为Ti元素,是22号元素,位于第四周期、第ⅣB族,D错误;
故选A。
10. 下列设计的实验方案不能达到实验目的的是
A. AB. BC. CD. D
【答案】B
【解析】A.CuCl2溶液中存在的平衡Cu2+(蓝色)+4Cl-(黄色),通过改变温度观察溶液颜色变化,能有效探究温度对化学平衡的影响,方案可行,A不符合题意;
B.溴乙烷在NaOH乙醇溶液中加热生成乙烯,但实验中未对挥发的乙醇进行除杂处理,乙醇蒸气可能被酸性高锰酸钾氧化,导致溶液褪色,干扰实验结果,无法准确验证消去反应,方案存在缺陷,B符合题意;
C.向NaCl溶液中先加少量生成AgCl沉淀,再滴加KI溶液,若生成黄色AgI沉淀,说明AgI的溶度积更小,实验中用量少,优先与Cl⁻反应,后续加入KI时,生成黄色AgI沉淀,涉及沉淀的转化,可正确比较,方案合理,C不符合题意;
D.麦芽糖是还原性糖,直接与新制悬浊液共热生成砖红色沉淀;蔗糖无还原性,无法反应,该方案可有效鉴别两者,方法正确,D不符合题意;
故选B。
11. 某研究所设计以软锰矿(主要成分为,含少量、等的氧化物)为原料制备,其实验流程如下:
已知:固体和溶液均为墨绿色。
下列说法正确的是
A. “熔融煅烧”过程中使用到的仪器主要有蒸发皿,三脚架和酒精灯
B. “滤渣1”的成分是
C. “调pH2”过程中反应离子方程式为
D. “结晶”过程中获得晶体可采用降温结晶法
【答案】D
【解析】软锰矿(主要成分为,含少量、等的氧化物)与KOH在空气中熔融煅烧生成、和,浸取液通入过量得到的滤渣1有和,滤液加入冰醋酸 “调pH2”生成和,据此解答。
A.“熔融煅烧”需要高温,应该用坩埚而不是蒸发皿,A错误;
B.由分析知“滤渣1”的成分是和, B错误;
C.“调pH2”过程中加入冰醋酸,冰醋酸为弱电解质不拆,反应的离子方程式为,C错误;
D.的溶解度受温度影响变化较大,可以采用降温结晶的方法得到,D正确;
故选D。
12. 科学家为消除酸性工业废水中甲醛的危害,利用驱动耦合电催化实现了与转化为高附加值的产品。下图是耦合电催化反应系统原理图示。下列有关说法不正确的是
A. 管负载纳米绒电极为阴极
B. 反应过程中从左极室向右极室移动
C. 电路中通过2ml电子时,在装置中可生成1ml
D. 阳极的电极反应式为
【答案】C
【解析】b连接的左侧中加入HCHO,生成HCOOH,C元素化合价升高,此电极为阳极,连接正极(b),电极反应为:,则右侧为阴极,连接电源负极(a),电极反应,据此分析;
A.根据分析可知,管负载纳米绒电极为阴极,A正确;
B.反应过程中阳离子从阳极向阴极移动,即从左极室向右极室移动,B正确;
C.电路中通过2ml电子时,在装置中可生成2ml,C错误;
D.根据分析可知,阳极的电极反应式为,D正确;
故选C;
13. 某太阳能电池材料的化学式为,其晶胞结构如下图所示,其中代表,表示阿伏加德罗常数。下列说法中不正确的是
A. N的杂化方式为B. 图中代表
C. 晶体密度为D. 的配位数为8
【答案】D
【解析】A.中N的价电子对数是4,为杂化,A正确;
B.由图可知,1个位于体内,位于面心,个数为6×=3个,位于顶点,个数为8×=1,根据甲胺铅碘的化学式(CH3NH3)PbI3可知,面心的代表,顶点的代表,B正确;
C.1个晶胞中含有1个(CH3NH3)PbI3,则晶胞的质量为,晶胞的体积为,则晶胞的体积为,C正确;
D.位于晶胞的顶点,与其距离最近的位于3个面的面心,顶点被8个晶胞共用,面心被两个晶胞共用,则的配位数为个,D错误;
故选D。
14. 室温下,的某二元酸溶液中,溶液中可能存在的含A粒子(、、等)物质的量分数(x)随pH变化的关系如下图所示。下列说法不正确的是
A. 的电离方程式为,
B. 室温下,
C. 将相同物质的量的和固体溶于水所得混合溶液,离子浓度大小关系为
D. 时,溶液中存在
【答案】C
【解析】A.溶液中不存在分子,说明第一步完全电离,则电离方程式为,,A正确;
B.,由图可知,与浓度相等时pH=3,,,B正确;
C.将相同物质的量的和固体溶于水所得混合溶液,由,可知的电离大于的水解,故,C错误;
D.时,溶液中阳离子除外还有调pH加入的物质中的阳离子,根据电荷守恒可知时,溶液中存在,D正确;
故选C。
二、非选择题:本题共4小题,共58分。
15. 海洋锰结核是一种富含多种金属元素的矿物资源,从中提取的金属在钢铁、电子、航天领域有着广泛的用途。其主要成分为锰、镍、铜、钴、铁等金属的氧化物。从锰结核中回收金属的工艺流程如下:
已知:①“还原熔炼”后得到富锰渣和粗合金。
②“加压酸浸”后、、元素均以二价盐的形式存在。
③常温下,相关金属离子()生成氢氧化物沉淀的pH如下表:
(1)“加压酸浸”过程中加压的目的是________。
(2)滤渣的主要成分是________,“调pH”操作中pH的控制范围为________,该过程中发生反应的离子方程式为________。
(3)“电解沉积镍”的过程中使用石墨电极,阳极的电极反应式为________。
(4)萃取剂Ⅰ为,“萃取铜”后铜元素的存在形式为,其中铜元素的配位数为________。萃取后通过________操作将其分离出来。请解释萃取剂Ⅰ能萃取分离铜元素的原因________。
【答案】(1)提高反应速率,增大浸取率
(2) ①. ②. 3~4.2 ③.
(3)
(4) ①. 2 ②. 分液 ③. 萃取剂Ⅰ难溶于水,且能与形成配位键
【解析】锰结核和焦炭“还原熔炼”后得到富锰渣和粗合金,加入S和水硫化熔炼除氧,加压酸浸,、、元素均以二价盐的形式存在,浸出液加过氧化氢氧化亚铁离子,加氨水调pH值,得到氢氧化铁滤渣,加萃取剂1萃取铜,经反萃取并电解沉积铜,萃取剂1循环利用;加萃取2萃取镍,经反萃取并电解沉积镍,萃取剂2循环利用;最后回收钴,据此分析;
(1)“加压酸浸”过程中加压的目的是增加气体浓度,提高反应速率,增大浸取率;
(2)据分析可知,滤渣的主要成分是,“调pH”使铁离子沉淀完全,铜离子、钴离子、镍离子不沉淀,操作中pH的控制范围为3~4.2,过氧化氢氧化亚铁离子,加氨水调pH值,得到氢氧化铁滤渣,离子方程式为;
(3)使用石墨电极,阳极失电子,电极反应式为;
(4),其中铜与N形成配位键,铜元素的配位数为2;萃取后通过分液操作将其分离出来;萃取剂Ⅰ难溶于水,且能与形成配位键,形成的络合物在有机相和水相中的溶解度差异,使得铜离子能够被有效地从水相转移到有机相中;
16. 二草酸合铜(Ⅱ)酸钾是一种重要的配合物,具有特殊的结构和性质,制备流程如下:
已知:1.
2.二草酸合铜(Ⅱ)酸钾微溶于冷水,可溶于热水,难溶于乙醇。
实验步骤:
步骤1:制备:称取2.5g硫酸铜晶体(),溶于水,滴入过量的溶液,加热煮沸,冷却,用下图所示的装置抽滤,然后用蒸馏水洗涤,得到氧化铜。
步骤2:制取:将晶体加入蒸馏水中,微热,溶解过程中温度不能超过85℃,待充分溶解后分次加入,反应生成。
步骤3:制备二草酸合铜(Ⅱ)酸钾:将与混合液在50℃加热至反应充分,得到二草酸合铜(Ⅱ)酸钾。反应结束后将溶液冷却至室温,再置于冰水浴中冷却,析出晶体,过滤并用乙醇洗涤晶体。
请回答:
(1)步骤1称取2.5g硫酸铜晶体,需要用到的仪器有________。抽滤时将仪器接在水龙头上,其作用是________。用蒸馏水洗涤氧化铜时,证明已洗涤干净的方法:________。
(2)步骤2溶解过程中温度不能超过85℃的原因是________。
(3)步骤3制备二草酸合铜(Ⅱ)酸钾反应的化学方程式为________。加热温度控制在50℃可以采取的加热措施是________,用乙醇洗涤晶体的目的是________。
(4)将制得的进行热重分析,结果如下图所示,由图可知在C点剩余固体为和________。
【答案】(1) ①. 托盘天平、药匙 ②. 抽气,减小吸滤瓶、安全瓶中的压强,加快过滤速度 ③. 取最后一次洗涤滤液于洁净的试管中,加入盐酸酸化的氯化钡溶液,若无白色沉淀生成,则说明已洗涤干净(其他合理答案也可)
(2)防止草酸分解 (3) ①. ②. 水浴加热 ③. 洗去晶体表面杂质和水分,减少洗涤中晶体溶解造成的产物损失,加速晶体干燥
(4)
【解析】胆矾溶于水,加氢氧化钠溶液生成氢氧化铜,加热煮沸氢氧化铜分解生成氧化铜;草酸晶体加水微热,然后加入碳酸钾固体,可生成草酸氢钾;二者混合在50℃水浴加热,反应结束后将溶液冷却至室温,再置于冰水浴中冷却,析出晶体,过滤并用乙醇洗涤晶体,得到二草酸合铜(Ⅱ)酸钾晶体。
(1)步骤1称取2.5g硫酸铜晶体,称量固体药品,需要用到的仪器有托盘天平、药匙;抽滤时将仪器接在水龙头上,其作用是通过水流动起到抽气作用,减小吸滤瓶、安全瓶中的压强,加快过滤速度;用蒸馏水洗涤氧化铜时,证明已洗涤干净只要证明最后的洗涤液中不含,方法为:取最后一次洗涤滤液于洁净的试管中,加入盐酸酸化的氯化钡溶液,若无白色沉淀生成,则说明已洗涤干净(其他合理答案也可);
(2)草酸受热易分解,步骤2溶解过程中温度不能超过85℃的原因是防止草酸分解;
(3)将与混合液在50℃加热至反应充分,得到二草酸合铜(Ⅱ)酸钾,反应方程式为;加热温度控制在50℃可以采取的加热措施是水浴加热;二草酸合铜(Ⅱ)酸钾微溶于冷水,可溶于热水,难溶于乙醇,用乙醇洗涤晶体可以洗去晶体表面杂质和水分,减少洗涤中晶体溶解造成的产物损失,加速晶体干燥;
(4)进行热重分析,加热至恒重,应得到剩余固体为和铜的氧化物,1ml质量为354g,根据原子守恒,可得到1ml,1ml的质量为138g,C点剩余质量59.3%×354g≈210g,则铜的氧化物质量为210g-138g=72g,根据铜原子守恒,该固体含有64g铜原子,余下应为O原子质量8g,该氧化物为。
17. 煤制甲醇工业对国家能源安全和化工产业发展意义重大。其主要流程分为煤气化和合成甲醇:
Ⅰ.煤气化的主要反应:
反应1:
反应2:
请回答:
(1)反应的________,在________(选填“低温”、“高温”或“任意温度”)条件下有利于该反应自发进行。
(2)在恒温恒容容器内进行反应1和反应2,下列说法正确的有________(填序号)。
A. 混合气体的密度保持不变时,说明反应体系已达到平衡
B. 平衡时的体积分数可能大于
C. 平衡时向容器中充入惰性气体,平衡体系中的体积分数不变
D. 平衡时缩小容器体积,平衡体系中减小
(3)研究人员结合实验与计算机模拟结果揭示了在金催化剂表面上反应2的反应历程(如下图所示),其中吸附在金催化剂表面上的物质用*标注。该历程中决定反应2速率的步骤方程式为________。
(4)在一定温度下,向体积固定的密闭容器中加入足量的和同时发生反应1和反应2,起始压强为0.1MPa,平衡时的转化率为50%,的物质的量是为0.1ml,则反应1的平衡常数________。(已知为分压平衡常数,分压=总压物质的是分数)
Ⅱ.合成甲醇的主要反应为 。
(5)在其他条件一定时,甲醇的产量随温度和压强的变化趋势如上图所示,其中压强最大的是________(选填)。
(6)在550K、条件下,M点所示的反应状态中甲醇的生成速率________甲醇的消耗速率(选填“>”“
相关试卷
这是一份甘肃省兰州市2025届高三诊断考试(一模) 化学试卷(解析版),共22页。试卷主要包含了 下列离子方程式的书写正确的是等内容,欢迎下载使用。
这是一份甘肃省兰州市2025届高三下学期诊断考试(一模)化学试卷(含答案),共9页。
这是一份甘肃省兰州市2025届高三下学期诊断考试(一模)化学(含答案),共9页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




