

安徽省亳州市第二完全中学2024-2025学年高二下学期第一次月考 化学试题(原卷版+解析版)
展开 这是一份安徽省亳州市第二完全中学2024-2025学年高二下学期第一次月考 化学试题(原卷版+解析版),共7页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。
一、单选题
1. 下列各组微粒具有相同质子数和电子数的是( )
A. OH-和NH4+B. H2O和NH3C. F和OH-D. O2-和NH4+
2. 氮化硅可通过在高温下由石英与炭在氮气流中制备:,关于该反应中相关微粒的说法正确的是
A. 和共价键极性和分子极性相同
B. 五种微粒固态时,属于原子晶体的可能有三种
C. 基态硅原子的价电子轨道表示式为
D. 二氧化硅的空间填充模型是
3. 下列说法正确的是
A. 的电子排布式,违反了泡利不相容原理
B. 因硫元素核电荷数比磷元素大,故硫元素比磷元素大
C. 电子排布式违反了洪特规则
D. 电子的能量一般低于电子的能量
4. 下列化学用语表达正确的是
A. 的电子式为:
B. 联氨分子的结构式为:
C. 的共价键类型:键
D. 激发态原子的轨道表示式:
5. 下列有关σ键和π键的说法错误的是
A. π键是原子轨道“肩并肩”方式重叠形成的共价键
B 当原子形成分子时,首先形成σ键,可能形成π键
C. σ键较π键稳定
D. 苯分子中含有12个σ键和3个π键
6. 以下说法正确的是
A. 从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道
B. p能级能量一定比s能级能量高
C. 2p、3p、4p能级的轨道数依次增多
D. 轨道相互垂直,且能量各不相等
7. Q、W、X、Y、Z是元素周期表中原子序数依次增大的前四周期元素,Q是宇宙中含量最多的元素;W与X同周期,W基态原子有3个未成对电子,X元素原子的价层电子排布为;Y元素的原子半径在同周期中最大(稀有气体除外);Z元素最高能层只有1个电子,其余能层均充满电子。下列说法错误的是
A. 电负性:B. 第一电离能:
C. Z原子核外有7种能量不同的电子D. 是含有极性键和非极性键的非极性分子
8. 2023年11月24日消息,据国家知识产权局公告,荣耀终端有限公司申请一种新型锂离子电池。其电解质的阴离子结构如图,其由同一短周期的X、Y、Z、W四种元素组成,且W的原子序数为Y、Z最外层电子数之和,下列说法一定正确的是
A. 氢化物的沸点:W>X
B. 电负性:Z>X>Y>W
C. ZW3分子构型为三角锥形
D. Z的最高价氧化物对应水化物为一元酸
9. 下列有关物质性质、结构特点表述均正确,且存在因果关系的是
A. AB. BC. CD. D
10. 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。氧化镍原子分数坐标参数A为(0,0,0),B为(1,1,1),则C的坐标参数为
A. ( ,,)B. (1,1, )C. (,1, )D. (1,,)
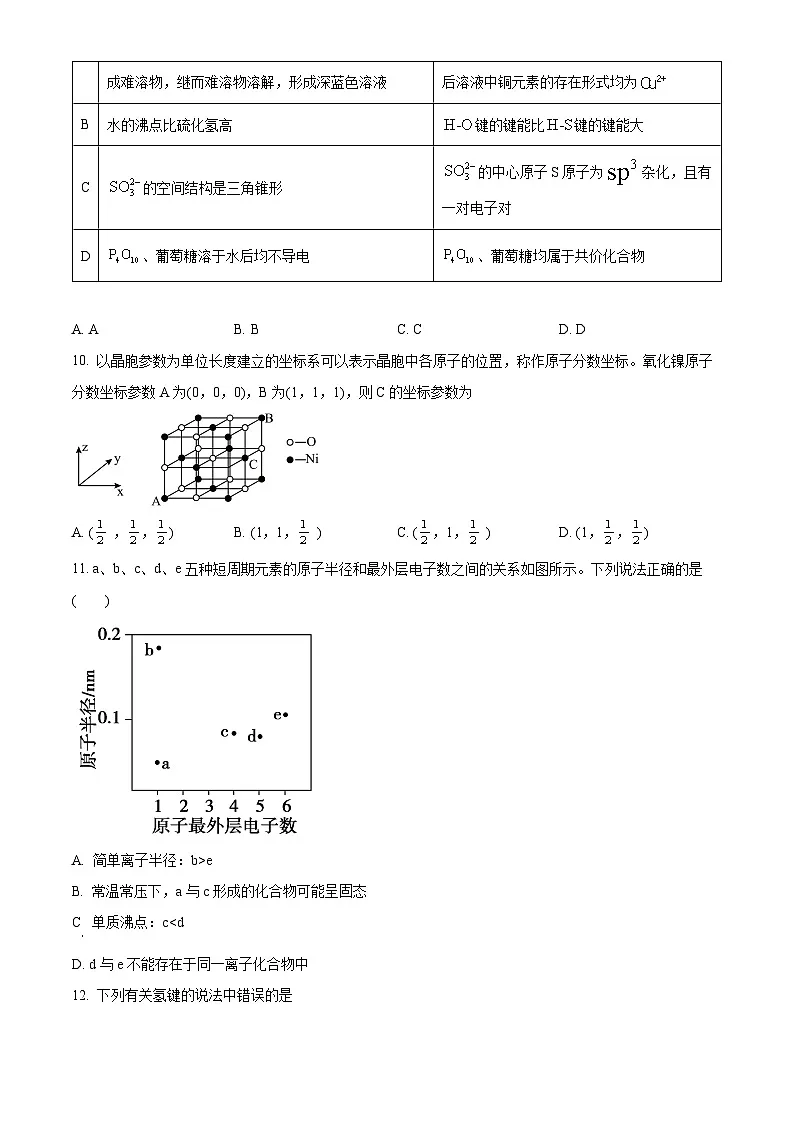
11. a、b、c、d、e五种短周期元素的原子半径和最外层电子数之间的关系如图所示。下列说法正确的是( )
A. 简单离子半径:b>e
B. 常温常压下,a与c形成的化合物可能呈固态
C 单质沸点:cC>Zn
C. Zn、C、O的第一电离能:Zn>C>O
D. 中的化学键有离子键、非极性键和极性键
14. 已知X、Y为第三周期元素,且电负性X>Y,下列说法正确的是
A. 第一电离能Y一定小于X
B. 简单气态氢化物的稳定性:X>Y
C. 最高价含氧酸的酸性:Y>X
D. X和Y形成化合物时,X显正价,Y显负价
15. 下列说法正确的是
A. 若把分子写成分子,违背了共价键的饱和性
B. s轨道和p轨道重叠可以形成π键
C. 所有共价键都有方向性
D. 2个原子形成共价键时,可形成多个键
16. 甲烷晶体的晶胞结构如图所示,下列说法正确的是
A. 甲烷晶胞中的球只代表1个C原子
B. 晶体中1个CH4分子中有12个紧邻的CH4分子
C. 甲烷晶体熔化时需克服共价键
D. 1个CH4晶胞中含有8个CH4分子
二、填空题
17. 回答下列问题
(1)基态Cu原子的价层电子排布式为______;位于元素周期表______区。
(2)已知电负性H 2.1、Si 1.8,则SiH4中Si的化合价为______。
(3)基态Ge原子有______种不同能量的电子。
(4)基态原子核外电子填充在5个轨道中元素有______(填元素符号)。
18. 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:(已知:在溶液中为橙色,在溶液中为黄色)
(1)下列反应曾用于检测司机是否酒后驾驶:2+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
①基态Cr原子外围电子排布图为__________________;配合物[Cr(H2O)6]3+中与Cr3+形成配位键的原子是__________________(填元素符号)。
②CH3CH2OH与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为__________________。
(2)有下列实验:
①呈天蓝色的离子的化学式为____,溶剂X可以是____(填名称),继续添加氨水,沉淀溶解的离子方程式为__________________。
②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是__________________。
③下列有关化学实验的“操作→现象→解释”均正确的是__________________。
19. 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)2SO3(g) △H=-190kJ•ml-1。
(1)基态O原子核外电子排布式是_______。
(2)根据价电子对互斥理论可预测SO2的空间结构是_______,中心原子S杂化轨道的类型是_______。
(3)该反应的平衡常数表达式K=________,温度升高后,平衡常数将_______(选填“增大”、“减小”或“不变”)。
(4)在一个固定容积为5L的密闭容器中充入0.20mlSO2和0.10mlO2,10分钟后达到平衡,测得容器中含SO30.18ml,则v(O2)=_______。
(5)假设该反应在恒容密闭容器中进行,一定能说明该反应达到平衡状态的是_______。
A. 混合气体的密度不再变化
B. v(SO2)=2v(O2)
C. 混合气体的平均相对分子质量不再变化
D. 混合气体中氧元素的质量分数不再变化
三、计算题
20. 现有甲、乙、丙三种晶体的晶胞(甲中X处于晶胞的中心,乙中A处于晶胞的中心),可推知:甲晶体中X与Y的个数比是___________,乙中A与B的个数比是___________,丙晶胞中有___________个C离子,有___________个D离子。
甲晶体化学式是___________(X为阳离子)。丙晶胞中距离C离子等距离且最近的D离子有___________个。
表述1
表述2
A
向盛有硫酸铜溶液的试管里滴加氨水至过量,先形成难溶物,继而难溶物溶解,形成深蓝色溶液
反应后溶液中不存在任何沉淀,所以反应前后溶液中铜元素的存在形式均为
B
水的沸点比硫化氢高
键的键能比键的键能大
C
的空间结构是三角锥形
的中心原子S原子为杂化,且有一对电子对
D
、葡萄糖溶于水后均不导电
、葡萄糖均属于共价化合物
选项
操作
现象
解释
A
向某溶液中滴加KSCN溶液
产生红色沉淀
Fe3++3SCN-=Fe(SCN)3↓
B
向由0.1mlCrCl3·6H2O配成的溶液加入足量AgNO3溶液
产生0.2ml沉淀
已知Cr3+的配位数为6,则
CrCl3·6H2O的化学式可表示为[Cr(H2O)5Cl]Cl2·H2O
C
向溶液K2Cr2O7溶液中先滴加3滴浓硫酸,再改加10滴浓NaOH
溶液先橙色加深,后变为黄
色
溶液中存在+H2O2+2H+
D
向AgCl悬浊液中滴加氨水
沉淀溶解
AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl-
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




