

2024届福建省厦门市高三下学期联考模拟预测化学试题(解析版)
展开 这是一份2024届福建省厦门市高三下学期联考模拟预测化学试题(解析版),共18页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
本试卷共6页。总分100分。考试时间75分钟。
可能用到的相对原子质量:O16 V51 Fe56 Zn65
一、选择题:本题共10小题,每小题4分,共40分。每小题只有一个选项符合题目要求。
1. 我国明代李时珍《本草纲目》中记载豆腐制作过程:“凡黑豆…皆可为之。水浸,硙碎。滤去渣,煎成。以卤汁或山鞋叶或酸浆醋淀,就釜收之”。制作过程不涉及的操作及现象是
A. 溶解B. 过滤C. 聚沉D. 蒸馏
【答案】D
【解析】
【详解】A.“水浸”涉及到的操作是溶解,A不符合题意;
B.“滤去渣”涉及到的操作是过滤,B不符合题意;
C.“以卤汁或山鞋叶或酸浆醋淀” 涉及到的现象是聚沉,豆浆是胶体分散系,加入电解质发生聚沉,形成豆腐,C不符合题意;
D.蒸馏操作未涉及,D符合题意;
故选D。
2. 花椒中的椒麻味主要是由羟基-γ-山椒素(M)产生的,其结构如图。下列说法错误的是
A. M的不饱和度为6
B. M中所有碳原子共平面
C. 可消耗
D. M无对映异构体
【答案】B
【解析】
【分析】有机物M含有官能团碳碳双键和酰胺基、羟基,酰胺基能够与NaOH反应,羟基不与NaOH反应,据此回答。
【详解】A.由结构式可知,有5个碳碳双键和一个碳氧双键,所以不饱和度为6,A正确;
B.M中出现结构“”,则所有碳原子不可能共平面,B错误;
C.酰胺基能够与NaOH发生反应,1mlM可消耗1mlNaOH,C正确;
D.从结构可知,M无手性碳,无对映异构体,D正确;
故选B。
3. 加热溶液,发生反应:(粉红色)(蓝色),溶液颜色由粉红色变为蓝色。下列说法错误的是
A. 基态原子的价电子排布式为
B. 该反应为吸热反应
C. 向冷溶液中加入固体,溶液变蓝
D. 加水稀释,平衡正移
【答案】D
【解析】
【详解】A.C为27号元素,基态C原子的价电子排布式为3d74s2,A正确;
B.加热CCl2溶液,溶液颜色由粉红色变为蓝色,说明升高温度,平衡正向移动,该反应为吸热反应,B正确;
C.向冷CCl2溶液中加入NaCl固体,Cl-浓度增大,平衡正向移动,溶液变蓝,C正确;
D.加水稀释,反应物浓度减少程度更大,平衡逆向移动,D错误;
故选D。
4. 晶体为体心立方晶胞结构。与在一定条件下发生如下反应:。是阿伏加德罗常数的值。下列说法错误的是
A. 的溶液中数目为
B. 中配位键数为
C. 生成(标准状况),转移电子数为
D. 1个晶胞质量为
【答案】A
【解析】
【详解】A.的溶液中H+浓度为10-5ml/L,溶液体积未知,无法计算H+数目,故A错误;
B.中Fe2+与6个CN-形成6个配位键,因此中配位键数为,故B正确;
C.(标准状况)物质的量为0.5ml,生成(标准状况),转移电子数为,故C正确;
D.晶体为体心立方晶胞结构,根据均摊法,1个晶胞中Fe的数目为,因此1个晶胞质量为,故D正确;
故选A。
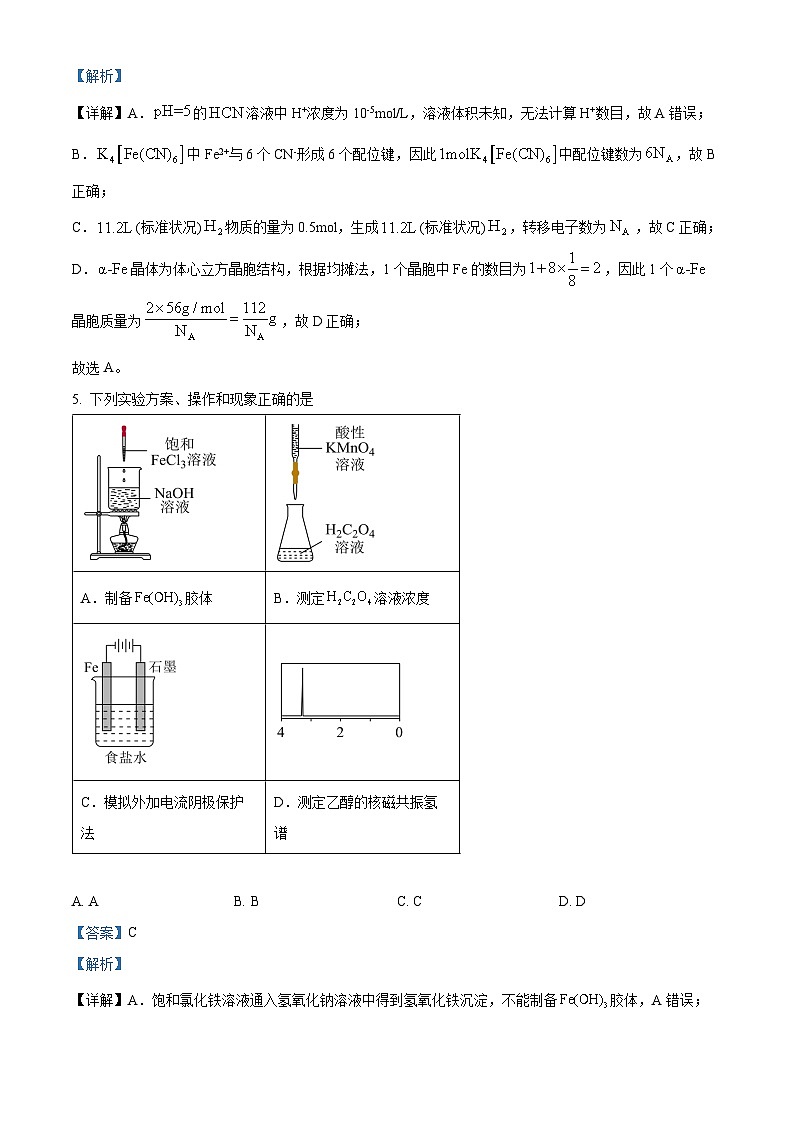
5. 下列实验方案、操作和现象正确的是
A. AB. BC. CD. D
【答案】C
【解析】
【详解】A.饱和氯化铁溶液通入氢氧化钠溶液中得到氢氧化铁沉淀,不能制备胶体,A错误;
B.酸性高锰酸钾溶液应该用酸式滴定管盛放,B错误;
C.铁与电源的负极相连,作阴极被保护,该装置可以模拟外加电流阴极保护法,C正确;
D.乙醇的结构简式为CH3CH2OH,乙醇的核磁共振氢谱应该出现三组峰,且峰面积之比是3:2:1,D错误;
答案选C。
6. 某光敏剂的结构如图。前四周期元素X、Y、Z、W、Q的原子半径依次增大,X、Z、W、Q位于不同周期。下列说法错误的是
A. 第一电离能:
B. Q的单质颜色为深红棕色
C. 沸点:
D. 形成四面体形的VSEPR模型
【答案】C
【解析】
【分析】某光敏剂的结构如图。前四周期元素X、Y、Z、W、Q的原子半径依次增大,X、Z、W、Q位于不同周期,X连接1个共价键,X为H,Y连接3个共价键,Y为N,Z连接4个共价键,Z为C,W连接2个共价键,W为S,Q连接1个共价键,Q为Br。
【详解】A.P的3p轨道处于半充满的稳定状态,其第一电离能大于S,P和N同处于第VA族,N的原子半径小于P,则N的第一电离能大于P,则第一电离能:N>S,A正确;
B.Br2颜色为深红棕色,B正确;
C.N2H4分子间存在氢键,沸点:,C错误;
D.H2S中心原子价层电子对数为2+=4,形成四面体形的VSEPR模型,D正确;
故选C。
7. 在浓硫酸作用下,苯与浓硝酸发生反应的反应历程如图。下列说法错误的是
A. 生成中间体时碳的杂化方式未发生改变
B. 生成中间体的反应为决速步骤
C. 产物1为加成反应的产物
D. 动力学和热力学优势产物均为产物2
【答案】A
【解析】
【详解】A.反应物苯中碳的杂化方式为sp2杂化,生成的中间体中碳的杂化方式既有双键碳的sp2杂化、又有饱和碳原子的sp3杂化,所以碳原子的杂化发生了改变,故A错误;
B.由图可知,生成中间体的反应的活化能最大,化学反应速率最慢,所以生成中间体的反应为决速步骤,故B正确;
C.对比苯和产物1的结构简式可知,反应过程相当于在苯的两个邻位碳上各加一个原子团,其中一个加硝基、另外一个加-OSO3H,即产物1为加成反应的产物,故C正确;
D.由图示可知,生成产物2的反应的活化能更小,化学反应速率更快,即动力学优势产物为产物2,产物2的能量更低、更稳定,即热力学优势产物为产物2,故D正确;
故答案为:A。
8. 利用富磺酸盐修饰锌碘二次电池,总反应为,其装置如下。
下列关于充电过程说法错误的是
A. a为阳极
B. 向b极移动的原因是电场作用
C. 理论上消耗转移电子数目为
D. 富磺酸盐的作用是减缓b电极的腐蚀
【答案】B
【解析】
【分析】充电时,a极为阳极,发生氧化反应,I-失去电子,电极反应式为:,b极为阴极,电极反应式为:。
【详解】A.由分析得,a为阳极,故A正确;
B.充电过程中,在电场作用下,向阳极,即a电极移动,故B错误;
C.由电极反应式可知,理论上消耗转移电子数目为,故C正确;
D.富磺酸盐中含有Zn2+,作用是减缓b电极腐蚀,故D正确;
故选B。
9. 氧化沉淀法回收石油炼制的加氢脱氮催化剂的流程如下。
已知:25℃时,。下列说法正确的是
A. “浸出”时可将替换为
B. “氧化”过程说明氧化性:
C. “沉铁”后溶液中,则
D. “沉淀”中X主要成分为
【答案】C
【解析】
【分析】废催化剂用硫酸溶液浸取,浸出液含有亚铁离子、铝离子、钴离子,向滤液加入H2O2主要是氧化溶液中的Fe2+得Fe3+,后用氢氧化钠调节溶液pH,使Fe3+转化为Fe(OH)3沉淀,通过过滤除去氢氧化铁沉淀达到除铁的目的,过滤后的滤液中加入碳酸钠将钴转化为CCO3沉淀、将铝离子转化为氢氧化铝沉淀,过滤滤液处理得到硫酸钠晶体;
【详解】A.具有强氧化性,会生成污染性气体NO,且会引入硝酸根离子杂质,A错误;
B.“氧化”过程亚铁离子被氧化为铁离子,而C2+没有被氧化为C3+,说明氧化性:,B错误;
C.“沉铁”后溶液中,则,pOH=10.8,则pH=3.2,即,C正确;
D.铝离子和碳酸根离子水解生成氢氧化铝沉淀,“沉淀”中X主要成分为氢氧化铝,D错误;
故选C。
10. 丙氨酸是人体内重要的氨基酸。25℃时,、、的分布分数[如]与关系如图。下列说法错误的是
A. 中电离能力强于
B. 时,丙氨酸微粒无法在电场作用下定向移动
C.
D. 溶液中
【答案】C
【解析】
【分析】NH2CH(CH3)COOH有-NH2,-COOH两种官能团,氨基具有碱性,在酸性较强时会结合H+,羧基具有酸性,在碱性较强时会与OH-反应,则曲线a表示的分布分数,曲线b表示的分布分数,曲线c表示NH2CH(CH3)COO-的分布分数,结合25℃时曲线a、b交点坐标(2.5,0.50),对应c(H+)=10-2.5ml/L且c[]=c[],计算⇌+H+的平衡常数K1==10-2.5,同理再根据b、c曲线交点坐标(9.7,0.50)可得⇌NH2CH(CH3)COO-+H+的电离常数为K2=10-9.7,由此解题。
【详解】A.由溶液中的离子可知,发生电离时是羧基先电离,故中-COOH电离能力强于,A正确;
B.由图知pH≈6.1时,丙氨酸微粒以形式存在,整体不带电荷,无法在电场作用下定向移动,B正确;
C.由分析,K1=10-25>K2=10-9.7,即,可得,C错误;
D.HOOCCH(CH3)NH3Cl溶液中,存在电离平衡⇌+H+,弱电解质是小部分发生电离,氢离子除了该电离平衡产生,还有水电离产生,故c[]>c(H+)>c[],D正确;
本题错误的选C。
二、非选择题:本题共4小题,共60分。
11. 利用某阳极泥(含和单质)回收贵金属并合成高能量密度材料的工艺流程如下。
(1)“溶浸”过程生成的离子方程式为___________。
(2)“还原”过程发生反应的化学方程式为___________。
(3)溶液中含银微粒的物质的量分数随的变化如图。
①“络合”过程为获得,应调节最佳浓度为___________。
②25℃时,的,的,的平衡常数___________。
(4)“电解”过程生成的电极反应式为___________。
(5)“溶解”过程可提高溶解速率的措施有___________(填1条)。
(6)晶体的局部结构如图。
①晶体中存在的微粒间作用力有___________(填标号)。
A.离子键 B.键 C.键 D.金属键 E.氢键
②晶体中的杂化轨道类型___________(填“相同”或“不同”),依据是___________。
【答案】(1)
(2)或
(3) ①. 0.025 ②.
(4)
(5)适当升温 (6) ①. ABCE ②. 不同 ③. 与形成配位键的原子个数不同(或形成的空间构型不同)
【解析】
【分析】阳极泥(含和单质)用氯化钠、氯酸钠和硫酸溶浸生成HAuCl4,滤渣中含氯化银,滤液用一水合肼还原生成金;滤渣中的氯化银与硫代硫酸钠反应生成,电解得到银单质,用硝酸溶解生成硝酸盐,最终得到。
【小问1详解】
“溶浸”过程Au与氯化钠、氯酸钠和硫酸反应生成HAuCl4,生成的离子方程式为;
【小问2详解】
HAuCl4用一水合肼还原生成金,一水合肼中氮元素化合价升高被氧化生成氮气,“还原”过程发生反应的化学方程式为或;
【小问3详解】
①由图可知,的浓度为0.025ml/L时,的物质的量分数最大,所以“络合”过程为获得,应调节最佳浓度为0.025ml/L ;
②25℃时,的,即,的,即的,所以的平衡常数;
【小问4详解】
“电解”生成,其电极反应式为;
【小问5详解】
“溶解”过程可提高溶解速率的措施有适当升温或适当提高硝酸的浓度等;
【小问6详解】
①晶体中存在阴、阳离子,即存在离子键,同时内还存在氮氢键,内存在键,由于氮元素的电负性很强,晶体中还存在氢键,故答案为:ABCE;
②由图可知,和中与Ag+形成配位键的原子个数不同,Ag+的价层电子对数不同(或形成的空间构型不同),则Ag+的杂化轨道类型也不同。
12. 某研究小组对质量分数为的(杂质为)进行分离提纯。
I.将粗品转化为(实验装置如图,夹持及加热装置省略)。
反应原理为
已知:部分物质的熔沸点如下表,是黄色液体且极易水解。
(1)实验操作如下:
a.反应前,称取粗品;
b.通入;
c.停止通入;
d.将无水与粗品加入三颈烧瓶中;
e.加热至160℃并恒温反应;
f.关闭加热装置,待装置冷却至室温。
正确操作顺序为:___________(填标号)。
(2)装置存在的不足之处是___________。
(3)在相同条件下,对上述转化过程进行如下探究。
①实验1中白色固体最可能为___________。
②实验2中反应ⅱ化学方程式是___________。
③从物质结构角度分析熔点较低的原因是___________。
④添加固体可加快化学反应速率并提高利用率的原因是___________。
Ⅱ.由制备并测定提钒率
将加水配成溶液,滴入氨水,在35℃下反应得到,过滤,洗涤,煅烧得到固体。已知:不同下,V(Ⅴ)在溶液中主要的存在形式如下。
(4)滴入氨水生成的原因有___________。
(5)判断沉淀是否洗涤干净,可使用的检验试剂有___________。
(6)称取样品,用稀硫酸溶解配成溶液。取溶液于锥形瓶中,加入溶液,生成,再用,标准液滴定剩余的至终点,消耗标准液。则提钒率为___________。[提钒率]
【答案】(1)
(2)尾气出口未加干燥装置
(3) ①. ②. ③. 为离子晶体,阴离子半径大,阴阳离子电荷低,离子键较弱 ④. 反应生成低熔点的液态,增大反应物接触面积,防止升华
(4)调控为,并生成使V(Ⅴ)转化为沉淀
(5)
(6)
【解析】
【分析】将粗品转化为(实验装置如图,夹持及加热装置省略),反应原理为,操作步骤为:反应前,称取粗品,通入,加热至160℃并恒温反应,关闭加热装置,待装置冷却至室温,停止通入,是黄色液体且极易水解,因此尾气出口应添加干燥装置。
【小问1详解】
操作步骤为:反应前,称取粗品,通入,加热至160℃并恒温反应,关闭加热装置,待装置冷却至室温,停止通入,因此,操作顺序为a→;
【小问2详解】
是黄色液体且极易水解,因此尾气出口应添加干燥装置;
【小问3详解】
①实验1中白色固体最可能为AlCl3,AlCl3加热后升华,进入装置C;
②与V2O5反应,生成、、NaCl,化学方程式为:;
③为离子晶体,阴离子半径大,阴阳离子电荷低,离子键较弱,熔点较低;
④反应生成低熔点的液态,增大反应物接触面积,防止升华,因此添加NaCl固体可加快化学反应速率并提高AlCl3利用率;
【小问4详解】
滴加氨水可调控为,使得V(Ⅴ)以的形式存在,并提供,使V(Ⅴ)转化为沉淀;
【小问5详解】
检验是否洗涤干净,实质是检验最后一次洗涤液中是否含有Cl-,可用来检验Cl-;
【小问6详解】
涉及到的反应有:、可得关系式,滴定的离子方程式为:,参加滴定的Fe2+的物质的量为0.2000ml/L×0.0207mL×5=0.0207ml,与反应得Fe2+的物质的量为:0.5000ml/L×0.05L-0.0207ml=0.0043ml,根据关系式可得,,原料中V2O5物质的量为,提钒率。
13. 可利用干法热分解法和湿法催化氧化法高效脱除沼气中的。
(1)已知:部分键能数据为。
___________。
(2)干法热分解法原理为。向体积为恒容容器中充入,初始压强为,平衡时体系中各物质随温度t的变化如图。
①对应图中的曲线是___________(填字母),结合平衡移动原理说明理由。___________
②t1℃时,的平衡转化率为___________,分压平衡常数___________(以分压表示,分压=总压×物质的量分数,列计算式即可)。
(3)湿法催化氧化法高效脱除的过程如下。
①“沉淀脱硫”中发生反应___________。(已知:25℃时,的的)
②“氧化沉硫”中发生反应的离子方程式有、___________。
③对脱硫效率影响如图。随着增大,脱硫效率趋于平缓的原因是___________。
④该流程中可循环利用的物质有___________(填化学式)。
(4)相比湿法催化氧化法,干法热分解法的优点是___________,缺点是___________。
【答案】(1)+91 (2) ①. c ②. 分解反应为吸热反应,升温平衡正向移动:含量增加,且物质的量比为 ③. 30% ④.
(3) ①. 104 ②. ③. 浓度增大,溶液酸性增强,抑制的电离及促使沉淀脱硫反应逆移 ④.
(4) ①. 操作简单 ②. 耗能较多、脱硫效率低、产物易于分离等
【解析】
【分析】H2S与ZnSO4溶液反应转化为ZnS和H2SO4,沉淀脱硫未反应完的H2S与生成的ZnS与硫酸铁反应转化为S单质、硫酸亚铁、硫酸锌,过滤得到S单质,滤液电解得到H2,据此回答。
【小问1详解】
ΔH=反应物总键能-生成物总键能=4×347-2×436-425=+91kJ⋅ml-1;
【小问2详解】
①H2S分解反应为吸热反应,升温平衡正向移动,S2的含量增大,且物质的量比为2:1,所以S2对应图中的曲线为c;
②由图可知,平衡时H2S的物质的量与起始物质的量之比为70%,起始时H2S为1ml,说明转化的H2S为0.3ml,生成的H2为0.3ml,生成的S2为0.15ml,剩余的H2S为0.7ml,t1℃时,H2S的平衡转化率为,根据压强之比等于物质的量之比有,,则平衡时的压强为1.15kPa,p(H2S)=pkPa,p(S2)=pkPa,p(H2)=pkPa,分压平衡常数Kp=;
【小问3详解】
①“沉淀脱硫”中发生反应Zn2+(aq)+H2S(aq)⇌ZnS(s)+2H+(aq),K==;
②根据分析可知,“氧化沉硫”中发生反应的离子方程式有2Fe3++H2S=2Fe2++S↓+2H+,ZnS+2Fe3+=2Fe2++S+Zn2+;
③c(Fe3+)对脱硫效率影响如图,随着c(Fe3+)增大,脱硫效率趋于平缓的原因是:Fe3+浓度增大,溶液酸性增强,抑制H2S的电离及促使沉淀脱硫反应逆移;
④根据分析可知,该流程中可循环利用的物质有ZnSO4 、Fe2(SO4)3;
【小问4详解】
相比湿法催化氧化法,干法热分解法的优点是操作简单,缺点是耗能较多、脱硫效率低、产物易于分离等。
14. 抗心律失常药物盐酸决奈达隆(Ⅰ)的合成路线如下。
(1)的反应类型为___________。
(2)同时生成。
①D中官能团的名称是___________。
②吸电子能力:1号基团___________2号基团(填“>”或“
相关试卷
这是一份2024届福建省厦门市高三下学期联考模拟预测化学试题(解析版),共18页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份福建省厦门市2024届高三下学期联考模拟预测化学试卷(Word版附解析),文件包含2024届福建省厦门市高三下学期联考模拟预测化学试题原卷版docx、2024届福建省厦门市高三下学期联考模拟预测化学试题解析版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
这是一份2024届福建省厦门市高三下学期联考模拟预测化学试题,共6页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)





