



【精品解析】2025届上海市松江区高三二模质量监控 化学试题(原卷版+解析版)
展开 这是一份【精品解析】2025届上海市松江区高三二模质量监控 化学试题(原卷版+解析版),文件包含2025届上海市松江区高三二模质量监控化学试题原卷版docx、2025届上海市松江区高三二模质量监控化学试题解析版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
(满分100分,完卷时间60分钟)
特别提示:
1.本试卷标注“不定项”的选择题,每小题有1~2个正确选项,只有1个正确选项的,多选不得分;有2个正确选项的,漏选1个得一半分,错选不得分。未特别标注的选择题,每小题只有1个正确选项。
2.除特殊说明外,本卷所用相对原子质量:H-1 B-11 C-12 N-14 O-16 S-32 Fe-56 As-75
一 两种含硼材料
氨硼烷(H3NBH3)是一种高性能化学储氢材料,其结构如下图所示(图中仅标出部分氢原子带电荷情况)。H3NBH3晶体中,分子间存在不寻常的强烈相互作用,为解释这种作用,科学家提出了二氢键的观点,二氢键可以表示为 。
1. 根据上图,判断H3NBH3中N、B、H三种元素的电负性由大到小的顺序为___________。(用元素符号表示)
2. 如要检测H3NBH3的晶体结构,可采用的仪器分析方法为___________。
A. X射线衍射B. 原子发射光谱C. 原子吸收光谱D. 核磁共振波谱
3. H3NBH3中N、B原子的杂化方式分别为___________。
A. sp2 ,sp2B. sp2 ,sp3C. sp3 ,sp2D. sp3 ,sp3
4. H3NBH3中H-N-H的键角___________NH3中H-N-H的键角(填“ > ”或“ < ”),理由是___________。
5. 等电子体是指原子总数相同、价电子总数相同的微观粒子,一般具有相同的结构特征。CH3CH3与H3NBH3是等电子体,但常温下CH3CH3为气态,H3NBH3为固态,原因是___________。
6. 已知H3NBH3在催化剂作用下可发生释氢反应。研究发现,升高温度,H3NBH3释氢反应的速率加快,但平衡产率降低。从化学平衡角度解释产率降低的原因___________。
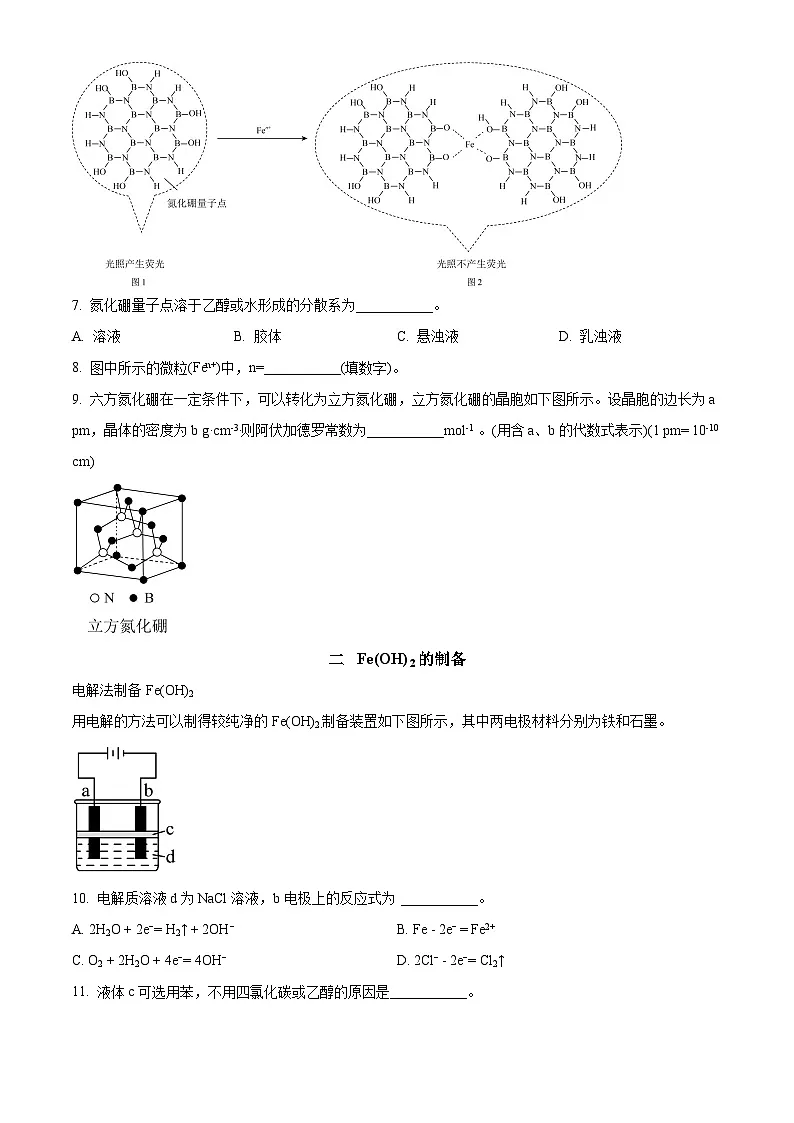
氮化硼量子点(粒径大小为2~10 nm)溶于乙醇或水,可用于Fen+的灵敏检测,检测原理示意图如下:
7. 氮化硼量子点溶于乙醇或水形成的分散系为___________。
A. 溶液B. 胶体C. 悬浊液D. 乳浊液
8. 图中所示的微粒(Fen+)中,n=___________(填数字)。
9. 六方氮化硼在一定条件下,可以转化为立方氮化硼,立方氮化硼的晶胞如下图所示。设晶胞的边长为a pm,晶体的密度为b g·cm-3.则阿伏加德罗常数为___________ml-1 。(用含a、b的代数式表示)(1 pm= 10-10 cm)
二 Fe(OH)2的制备
电解法制备Fe(OH)2
用电解的方法可以制得较纯净的Fe(OH)2.制备装置如下图所示,其中两电极材料分别为铁和石墨。
10. 电解质溶液d为NaCl溶液,b电极上的反应式为 ___________。
A. 2H2O + 2e−= H2↑ + 2OH−B. Fe - 2e− = Fe2+
C. O2 + 2H2O + 4e−= 4OH−D. 2Cl− - 2e−= Cl2↑
11. 液体c可选用苯,不用四氯化碳或乙醇的原因是___________。
12. 用电解的方法制备Fe(OH)2的过程中共转移了0.02 ml的电子,则理论上可产生___________g的Fe(OH)2。
A. 18B. 9C. 1.8D. 0.9
酵母菌法制备Fe(OH)2
实验装置(夹持仪器省略)如图所示:
已知酵母菌常温下可以进行有氧呼吸或无氧呼吸,反应如下:
有氧呼吸 C6H12O6 + 6H2O + 6O2 → 6CO2 + 12H2O
无氧呼吸 C6H12O6 → 2C2H5OH + 2CO2↑
13. 使用绿矾配制FeSO4溶液时,下列做法错误的是___________。
A. 配制时使用新煮沸冷却的蒸馏水B. 可在容量瓶中溶解晶体
C. 配制时加入适量的稀硫酸D. 在溶液中加入适量的铁粉
14. 下列___________试剂可以检验FeSO4溶液中是否含有Fe3+。
A. 酸性高锰酸钾溶液B. 苯酚
C. 硫氰化钾溶液D. 过氧化氢溶液
15. 向橡胶塞中扎入注射器,若观察到___________,即可判断装置内氧气已经被耗尽。再用注射器向内管中分别加入NaOH和FeSO4溶液。
16. 实验后依然发现有少量的灰绿色沉淀出现,可能的原因为___________。
A. 滴加了过量的氢氧化钠
B. 滴加氢氧化钠没有煮沸且密封保存
C. 酵母菌无氧呼吸产生的酒精会和氢氧化亚铁反应
D. 氧气含量低于一定浓度时,酵母菌就开始进行无氧呼吸
为进一步探究灰绿色沉淀的组成,查阅文献得知:为层状结构(如下图所示)。当部分被氧化为时,层状结构不会被破坏,生成灰绿色沉淀——绿锈。夹层内填充有等负离子,化学式可表示为。
取一定质量的绿锈样品,通过以下步骤确定其化学式:
①将样品完全溶于过量稀硫酸,配制成250 mL溶液;
②取25.00 mL上述溶液,用0.0100 ml·L﹣1的酸性KMnO4标准溶液滴定,达到滴定终点时,消耗KMnO4溶液20.00 mL,发生反应的离子方程式为:5Fe2+ + MnO+ 8H+ = 5Fe3+ + Mn2+ + 4H2O;
③另取25.00 mL溶液,依次加入足量的H2O2溶液和NaOH溶液,使其充分反应,将产生的沉淀过滤、洗涤,在空气中充分灼烧至恒重,得到0.24 g固体。
17. 该绿锈样品中Fe2+为___________ml。
18. 已知该绿锈样品中为0.01 ml,则绿锈的化学式为___________。
三 一碳化学
一碳化学研究是从只含有1个碳原子的化合物为原料,生产其他化工原料和产品的方法。用天然气与水蒸气反应可制得H2和CO。主要反应如下:
CH4(g) + H2O(g)CO(g) + 3H2(g) ΔH1= 206 kJ·ml﹣1
19. 提高该反应中CH4的平衡转化率可采取的措施是___________。
A. 降低温度B. 增大压强C. 使用催化剂D. 提升n(H2O)/n(CH4)
20. 该反应的熵变S= 215 J·ml-1·K-1,下列能使反应自发进行的温度是___________。
A. 960 KB. 900 KC. 800 KD. 700 K
21. 反应过程会产生积碳反应:CH4(g)C(s) + 2H2(g) ΔH2 ,会影响催化剂活性。已知:C(s) + H2O(g)CO(g) + H2(g) ΔH3= 131 kJ·ml﹣1,则ΔH2为___________ kJ·ml﹣1。
以CO2和H2为原料合成甲醇。合成过程中发生的反应有:
a.CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH= -49.5 kJ·ml﹣1
b.CO2(g) + H2(g) CO(g) + H2O(g) ΔH= 41.2 kJ·ml﹣1
22. 下列说法正确的是___________。
A. 升高温度,反应a的正反应速率减小,反应b的正反应速率增大
B. 增大H2的浓度,反应a和反应b的平衡均正向移动
C. 增大压强,反应a和反应b的平衡均正向移动
D. 恒温恒容下,向反应体系中充入一定量Ar,反应a和反应b的平衡均发生移动
23. 一定条件下,测得反应容器中n(CH3OH)∶n(CO2)∶n(CO)=1.00∶7.20∶0.11,则该条件下CO2转化率=___________% (精确到小数点后1位)。
其他条件相同时,CO2和H2的初始浓度均为1.00 ml·L-1,反应温度对CO2的转化率和CH3OH的选择性的影响如下图所示:
已知:
①CH3OH选择性=×100%;
②实验值为单位时间内测得。
24. 由图1可知,实验中反应均未达到化学平衡状态的依据是___________。
25. 图2中,CH3OH选择性的平衡值随温度升高而减小的主要原因是___________。
26. 由图2可知,温度相同时CH3OH选择性的实验值略高于平衡值。从化学反应速率的角度解释原因___________。
27. 由图1、图2可知,260℃时,a反应的平衡常数K =___________。(精确到小数点后2位)
四 药物中间体的合成
某药物在医学上具有消炎、镇痛、麻醉等功效,其中间体J合成路线如下:
已知:
28. J中的含氧官能团有硝基和___________。(写出官能团名称)
29. B与足量熔融NaOH反应的方程式为___________。
30. 若在铁粉、液溴条件下,发生A→B的反应,判断正确的是___________。
A. 没有副产物B. 发生加成反应
C. 有颜色较深的油状液体出现D. 反应吸热
31. 在AlCl3作用下生成(物质i)的同时,还会生成(物质ii),但两者沸点差异较大。
①i和ii两者沸点差异较大原因是___________。
②分离两种产物的操作为___________。
A.蒸发 B.萃取 C.过滤 D.蒸馏
32. 检验E完全反应变成F的方法是___________。
A. 浓溴水B. 希夫试剂
C. FeCl3溶液D. 酸性KMnO4溶液
33. 对F→J的过程中,说法正确的是___________。
A. PCC可以选择性氧化羟基
B. I、J两种物质均可发生银镜反应
C. J不存在顺反异构体
D. H→I的过程中会产生挥发性的HCN,所以一般采用低温
34. X是C的同分异构体,符合下列条件的X可能的结构简式为___________。(任写一种)
①核磁共振氢谱有5组峰,且峰面积之比为1∶1∶2∶2∶3。
②含有苯环、硝基,且含有一个手性碳原子。
③能与金属钠反应放出氢气。
35. 请结合题目所给的合成路线,以和上述合成路线中的试剂为原料,设计合成的路线___________。(无机试剂任选)
(路线可表示为:MN目标产物)
五 雄黄和雌黄
雄黄(As4S4),《本草纲目》谓其为“治疮杀毒要药也”,有良好的解毒疗疮作用。砷的另一种硫化物为雌黄(As2S3),也可作为中药治疗一些疾病。
36. 雄黄中没有π键且各原子最外层均达8电子稳定结构。下列为雄黄结构图的是___________。
A. B. C. D.
雄黄和雌黄二者都难溶于水,可以相互转化,如下图所示。
37. 雌黄不溶于水,却可溶于Na2S溶液,生成硫代砷酸钠(Na3AsS3)。请写出相应的离子方程式___________。
38. 上述反应转化历程中属于氧化还原反应的是___________。
A. ①B. ②C. ③D. ④
39. H3AsO3水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如下图所示。
NaH2AsO3溶液中,微粒间关系正确是
A. c(Na+) = c(H3AsO3)+2c(HAsO)+3c(AsO)+c(H2AsO)
B. c(Na+) = 2c(HAsO)+3c(AsO)+c(H2AsO)
C. c(H+)+ c(Na+) = c(OH-)+2c(HAsO)+3c(AsO)+c(H2AsO)
D c(H+)+ c(Na+) = c(OH-)+c(HAsO)+c(AsO)+c(H2AsO)
40. 铁盐混凝剂在溶液中产生Fe(OH)3胶粒,其表面带有正电荷,可吸附含砷化合物。pH=10时,铁盐混凝剂去除水中砷的速率较快,可能的原因是___________。
工业上从雌黄矿(除含As2S3以外,还含少量的PbS、CuS等杂质)提取砷并转化为三氧化二砷(As2O3),工业流程如下图所示。
已知:①Ksp(CuS)=1×10-36;Ksp(PbS)=1×10-26;Ksp(PbSO4)=1×10-8。
②在此条件下,PbS、CuS均不被氧化。
41. 若“转化”时,调节溶液中的浓度为0.1 ml·L﹣1,此时c(S2-)=1×10-28 ml·L﹣1。
①“转化”后,此时Cu2+浓度为___________ml·L﹣1。
②通过计算说明滤渣中铅的存在形式为PbSO4___________。(写出计算过程,附简要文字说明)
42. “溶解”时,HAsO2进一步转化为Na3AsO4。则“溶解”过程中氧化剂与还原剂的物质的量之比为___________。
A. 1:3B. 3:1C. 2:1D. 1:2
43. 为测定反应得到的As2O3,取0.100 g样品于锥形瓶中,加入NaOH溶液,使样品完全溶解。用c ml·L﹣1碘标准溶液(溶质按I2计)滴定,将砷氧化至最高价态+5.到达滴定终点时,消耗碘标准溶液V mL,则样品中砷的质量分数为___________。
相关试卷
这是一份【精品解析】2025届上海市松江区高三二模质量监控 化学试题(原卷版+解析版),文件包含2025届上海市松江区高三二模质量监控化学试题原卷版docx、2025届上海市松江区高三二模质量监控化学试题解析版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
这是一份2021上海松江区高三下学期4月模拟考质量监控(二模)化学试题含答案,共12页。试卷主要包含了04, 关于氨和铵盐的说法错误的是, 石油裂化能得到的物质是, 某化合物X的结构式为等内容,欢迎下载使用。
这是一份上海市松江区2022-2023学年高三上学期期末质量监控(一模)化学试题 附解析,共20页。试卷主要包含了选择题,综合分析题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 



.png)




