




湖北省武汉市第一中学2024-2025学年高二下学期3月月考化学试题(Word版附解析)
展开 这是一份湖北省武汉市第一中学2024-2025学年高二下学期3月月考化学试题(Word版附解析),文件包含湖北省武汉经济技术开发区第一中学2024-2025学年高二下学期3月月考化学试题原卷版docx、湖北省武汉经济技术开发区第一中学2024-2025学年高二下学期3月月考化学试题Word版含解析docx等2份试卷配套教学资源,其中试卷共28页, 欢迎下载使用。
相关相对原子质量:B11 C12 N14 O16 S32 Fe56
一、单选题(共 15 题,每题 3 分,共 45 分)
1. 下列化学用语或图示表达正确的是
A. 电子式: B. 的结构示意图:
C. H2 中共价键的电子云图: D. 的 模型为
2. 交通工具动力系统的演进历程是人类文明进步的生动缩影。下列说法正确的是
A. 畜力时代:给马车的铁制铆钉涂油可防止其生锈
B. 蒸汽时代:蒸汽机中的水汽化时,其化学键被破坏
C. 燃油时代:内燃机中汽油燃烧时,热能转化为化学能
D. 新能源时代:太阳能电池板的主要材质是
3. NA 为阿伏加德罗常数的值。下列说法正确的是
A. 46gCH3CH2OH 中 sp3 杂化的原子数为 2NA
B. 标准状况下,80gSO3 中含有分子数为 NA
C. 4.4g 中含有σ键数目为 0.7NA
D. 向 1L0.1ml/LCH3COOH 溶液通氨气至中性,铵根离子数为 0.1NA
4. 硫化氢可与氧气发生反应: ;生成的硫单质有多种组成形式,如 :
、 : (冠状)等。下列有关说法中正确的是
A. 熔点 B. 键角
C. 、 中 S 原子均为 杂化 D. 生成的硫单质为共价晶体
5. 下列说法正确的是
A. 在沸水中配制明矾饱和溶液,然后快速冷却,可得到较大颗粒明矾晶体
B. 金刚石硬度最大,所以耐锤击能力强
第 1页/共 9页
C. 手性药物分子互为同分异构体
D. 表面活性剂在水中会形成亲水基向内,疏水基向外的胶束
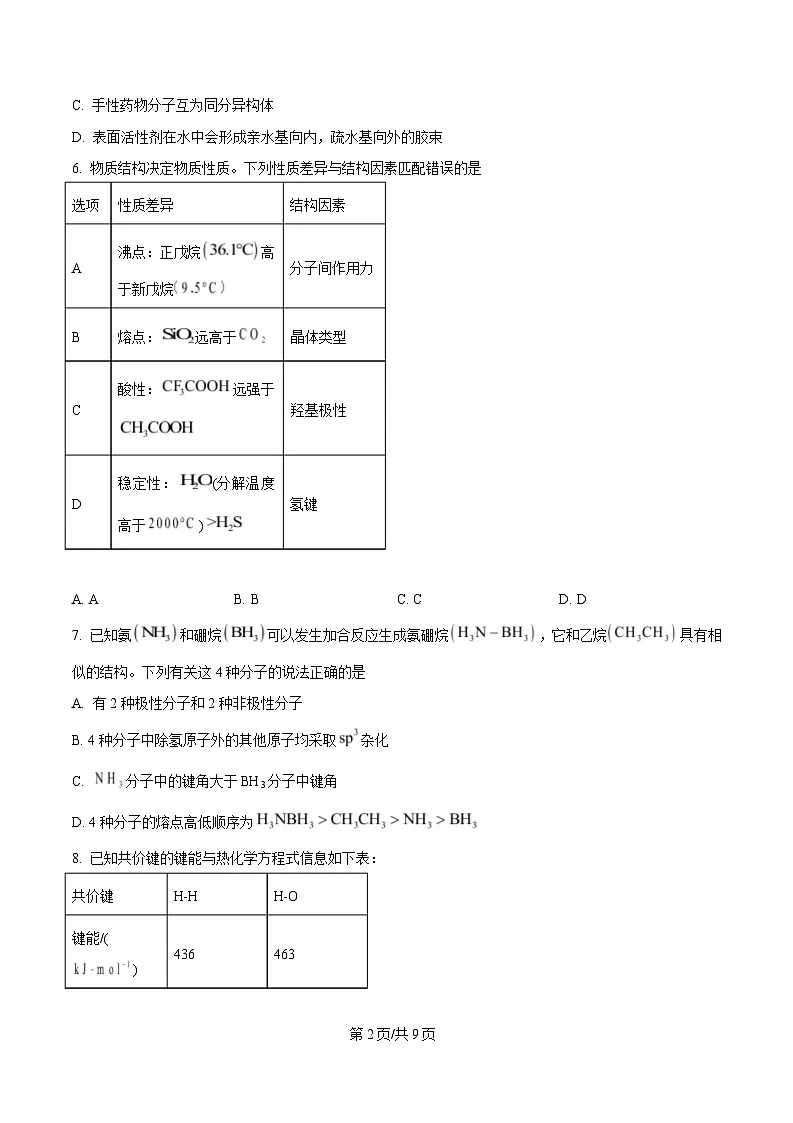
6. 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
沸点:正戊烷 高
A 分子间作用力
于新戊烷
B 熔点: 远高于 晶体类型
酸性: 远强于
C 羟基极性
稳定性: (分解温度
D 氢键
高于 )
A. A B. B C. C D. D
7. 已知氨 和硼烷 可以发生加合反应生成氨硼烷 ,它和乙烷 具有相
似的结构。下列有关这 4 种分子的说法正确的是
A. 有 2 种极性分子和 2 种非极性分子
B. 4 种分子中除氢原子外的其他原子均采取 杂化
C. 分子中的键角大于 BH3 分子中键角
D. 4 种分子的熔点高低顺序为
8. 已知共价键的键能与热化学方程式信息如下表:
共价键 H-H H-O
键能/(
436 463 )
第 2页/共 9页
热化学方程式
则 的 为
A. B. C. D.
9. 化合物 R 具有很强的氧化性,对各种致病性微生物(如病毒、细菌芽孢、真菌等)有很强的杀生作用。R
由 W、X、Y、Z、Q 五种原子序数依次增大的短周期主族元素组成,结构如图所示。W 的一种核素被广泛
用于考古、地质科学的研究中测定年代,Y 是地壳中含量最多的元素。下列说法正确的是
A. 简单离子半径:
B. 工业上电解熔融化合物 ZQ 制备 Z 单质
C. W、X、Y 分别形成的氢化物中,Y 的氢化物的沸点最高
D. Y、Z、Q 三种元素形成的化合物的水溶液均呈碱性
10. 单质硫和氢气在低温高压下可形成一种超导材料,其晶胞如图,晶胞参数为 apm。下列说法错误的是
A. S 位于元素周期表 p 区
B. 该晶体中 H 原子与 S 原子的数目之比为 3:1
C. 该晶体中相邻 S 原子最近距离为 apm
D. S 位于 H 构成的八面体空隙中
11. 某药物结构如图所示。下列有关该药物性质的说法不正确的是
第 3页/共 9页
A. 含有 4 个手性碳原子
B. 分子中碳原子的杂化方式有两种
C. 组成该分子的元素电负性大小排序为 O>N>C>H
D. 该分子中所有氧原子都有两个孤电子对
12. 下列说法错误的是
A. 原子光谱上的特征谱线可以确定组成分子元素
B. 红外光谱法是用高能电子流等轰击样品分子,使分子失去电子变成带正电荷的分子离子和碎片离子等微
粒,通过红外光谱法可以测知有机物所含的官能团
C. 质谱法能快速、微量、精确测定有机物相对分子质量的方法
D. 可用 射线衍射实验来鉴别晶体硅和玻璃
13. 下列物质的有关叙述不正确的是
A. 金刚石晶体中,每个六元环占有的碳原子数为 1/2 个
B. 石墨能导电,因为有可自由移动的电子
C. 等质量的它们充分燃烧会产生等物质的量的气体
D. 分子中仅含 键
14. 磷的常见含氧酸化学式为 ( ),其分子结构和亚磷酸与水形成的部分氢键如下图所示:
第 4页/共 9页
下列说法不正确的是
A. 与足量 NaOH 溶液反应的离子方程式为:
B. 分子中 P 采取 杂化
C. 与水形成如图所示的环,使得羟基难以电离出
D. 相同温度、相同浓度的稀溶液的酸性:
15. 砷化镓是一种高性能半导体材料,被广泛应用于光电子器件等领域。砷化镓立方晶胞(晶胞参数为 )
如图 1。下列说法正确的是
A. 的配位数为 2
B. 该晶胞沿 z 轴方向的平面投影如图 2
C. 原子周围与它距离最近且相等的 原子有 12 个
D. 晶胞中砷原子与镓原子间的最短距离为
二、非选择题 (共 4 题,55 分)
16. 回答下列问题。
Ⅰ.现有七种元素 A、B、C、D、E、F,其中 A、B、C 为三个不同周期的短周期元素,E、F 为第四周期
元素。请根据下列相关信息,回答问题。
A 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素
第 5页/共 9页
B 元素原子的核外 p 电子数与 s 电子数相等
C 基态原子的价电子排布为
D 能层数与 C 相同,且电负性比 C 大
E 元素的主族序数与周期数的差为 1,且第一电离能比同周期相邻两种元素
都大
F 在周期表的第五列
(1)C 基态原子中能量最高的电子所在能层符号___________,C 简单离子核外有___________种运动状态
不同的电子。
(2) 难溶于 ,简要说明理由:___________
(3)F 的一种氧化物常用于工业生产硫酸的催化剂,已知 F 在该氧化物中的化合价等于其价电子数,则该
氧化物的化学式为___________;
Ⅱ.硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根( )可看作是 中的一个 O 原子被 S
原子取代的产物。
(4)比较 S 原子和 O 原子的电负性大小,从原子结构的角度说明理由:___________。
(5) 的空间构型为___________。
(6)已知液态二氧化硫可以发生自电离:2SO2(l) SO2+ + SO 。 中各原子满足 8 电子结构,则其
键和 键数目之比为___________;写出一种与 SO2+空间结构相同的分子___________。
17. 工业上常用软锰矿(主要成分为 ,含少量 )和 合成电极材料
并回收净水剂明矾,其工艺流程如图所示。
第 6页/共 9页
已知:① 在酸性条件下比较稳定, 高于 5.5 时易被 氧化;
②当溶液中某离子浓度 时,可认为该离子沉淀完全;常温下,几种沉淀的
如下表所示:
回答下列问题:
(1) 在元素周期表中的位置为:___________。
(2)“酸浸”时,软锰矿中 成分与 反应的离子方程式:①___________;②___________。
(3)加入 “调 ”时,调节 的范围为 的原因是:___________。
(4)已知滤渣Ⅲ”主要成分为 ,则“氧化”操作中主反应的离子方程式为___________。
(5)为节能减排,整个工艺过程中可循环使用的物质为___________。
(6)蒸发浓缩、冷却结晶、过滤、洗涤即可得到明矾 ,洗涤时若用乙醇洗涤的目的
是___________。(写两点)
18. 我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用
的材料中含有 B、C、N、P、Ni、Fe 等元素。
(1)在第二周期中,第一电离能比 N 高 主族元素有___________种。
(2)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________。
A. B.
C. D.
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地
软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如
图所示。
第 7页/共 9页
①六方相氮化硼晶体结构与石墨相似(如图),晶体中氮原子的杂化方式为___________。
②原子坐标参数,表示晶胞内部各原子的相对位置,其中硼原子 A 坐标参数为 ;则硼原子
B 的坐标参数为___________。
③立方相氮化硼晶体的密度为ρ , 代表阿伏加德罗常数的值,则该晶体中距离最近的氮原子和硼
原子的距离为___________pm。
④氮化硼晶胞沿体对角线方向上的投影图如图所示,请在图中涂黑氮原子___________。
(4) 的结构如下图所示, 中 、 、 由大到小的顺序是___________
。
(5)下列物质不能形成分子间氢键的是___________。
A. CH3CONH2 B. NH4F C. CH3CHO D. 蛋白质分子 E.干冰
19. 材料 发展水平始终是时代进步和人类文明的标志。当前含铁的磁性材料在国防、电子信息等领域中具
有广泛应用。请回答下列问题:
(1)基态铁原子的价电子排布图为___________,基态铁原子核外电子的空间运动状态有___________种。
第 8页/共 9页
(2)一种新研发出的铁磁性材料 M 的分子结构如图 1 所示。
①M 分子中的 Fe2+与上下两个五元碳环相连且 Fe2+共提供了 6 个杂化轨道,则铁原子最可能的杂化方式为
___________(填序号)。
A.sp2 B.sp3 C. dsp2 D.d2sp3
②分子中的大π键可用符号π 表示,其中 m 代表参与形成大π键的原子数,n 代表参与形成大π键的电子数
(如苯分子中的大π键可表示为π ), 则 M 分子中由碳、氧组成的五元环中的大π键应表示为___________。
(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结构如图 2 所示。
① 该化合物的化学式为___________。
② 若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为___________。
③ 已知该铁氮化合物密度为 ,Fe 原子半径为 xpm,N 原子半径为 ypm,阿伏加德罗常数的值为
,则该晶胞中原子的空间利用率(晶胞中原子的体积占晶胞体积的百分率)为___________(列出计算式即
可,不用化简)。
第 9页/共 9页
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




