

2024-2025学年山西省太原市高二下学期开学考试化学检测试题(附答案)
展开 这是一份2024-2025学年山西省太原市高二下学期开学考试化学检测试题(附答案),共11页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
一、单选题
1.现有3种元素的基态原子电子排布式如下:①1s22s22p5;②1s22s22p63s23p3;③1s22s22p63s23p4。下列比较中正确的是
A.第一电离能:①①
C.未成对电子数:②>③>①D.电负性:①>②>③
2.下列有关化学反应与能量变化的叙述正确的是
A.晶体与晶体的反应,为放热反应
B.石墨转化为金刚石需要吸收热量,据此可判断金刚石比石墨稳定
C.放热反应不需要条件即可发生,而吸热反应必须加热才能实现
D.化学反应中的能量变化主要是由化学键变化引起的
3.用下列装置进行实验,不能达到实验目的的是
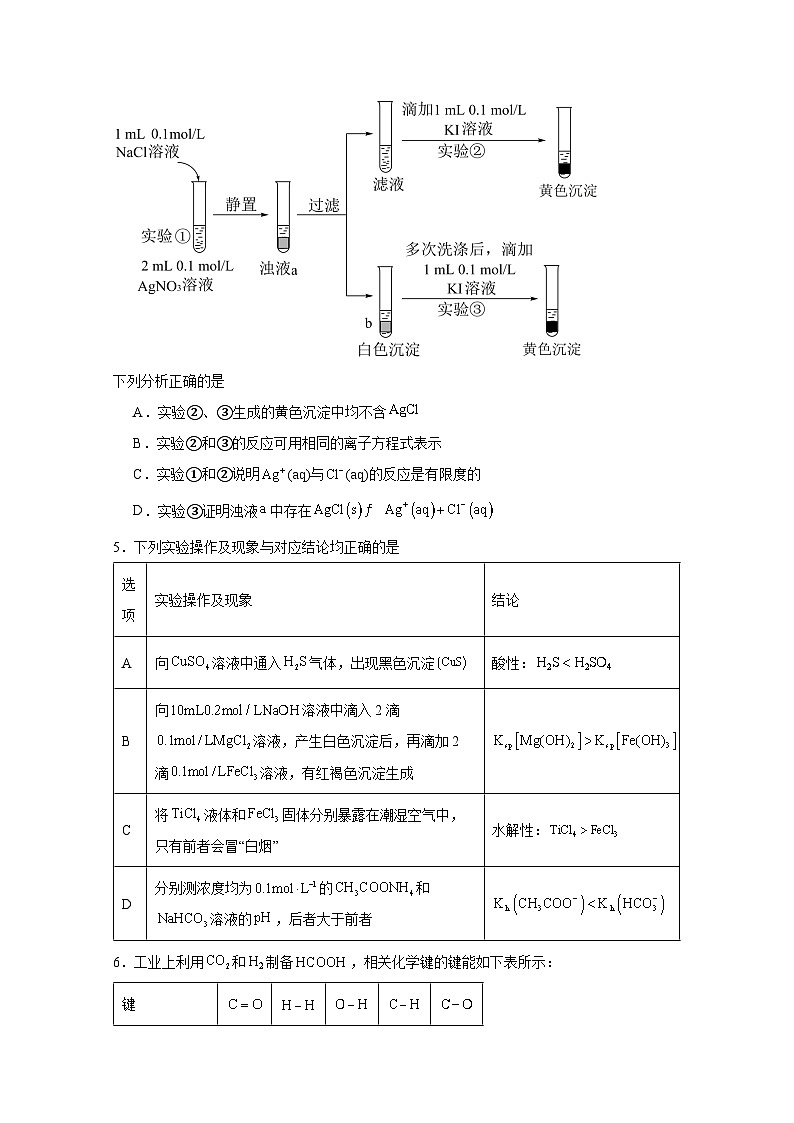
4.某小组同学进行如下实验探究:
下列分析正确的是
A.实验②、③生成的黄色沉淀中均不含
B.实验②和③的反应可用相同的离子方程式表示
C.实验①和②说明(aq)与(aq)的反应是有限度的
D.实验③证明浊液中存在
5.下列实验操作及现象与对应结论均正确的是
6.工业上利用和制备,相关化学键的键能如下表所示:
已知:①温度为时,CO2(g)+H2(g)⇌HCOOH(g)
②实验测得:,,、为速率常数。
下列说法错误的是
A.反应CO2(g)+H2(g)⇌HCOOH(g)
B.时,密闭容器充入浓度均为1ml/L的、,反应至平衡,则体积分数为
C.时,
D.若温度为时,,则
7.中国科学技术大学曾杰教授研究团队通过修饰铜基催化剂,在碳氧化物与有机分子转化的研究中获得多项突破。甲醇与水(均为气态)在铜基催化剂上的反应机理和能量变化如图:
下列说法正确的是
A.反应Ⅱ的热化学方程式为:
B.总反应的快慢由反应I决定,是因为反应I吸热、反应Ⅱ放热
C.选择优良的催化剂可以降低反应I和Ⅱ的活化能,从而减少反应过程中的能耗
D.反应过程涉及极性共价键、非极性共价键的断裂和形成
8.下列事实与盐类水解无关的是
①实验室制氢气时加入可加快反应速率;
②实验室通常使用热的纯碱溶液去除油污;
③溶液中;
④实验室配制溶液时加入少量稀盐酸;
⑤向氯化铁中滴加KSCN,出现红色;
⑥与两种溶液可作泡沫灭火剂;
⑦向中滴加氯水,溶液颜色加深;
⑧明矾、氯化铁晶体常用于净水。
A.①⑤⑦B.①⑤⑧C.⑤⑦⑧D.⑦⑧
9.已知①2H2(g)+O2(g)=2H2O(g) ΔH1=-483.6kJ∙ml-1;
②C(s)+O2(g)=CO(g) ΔH2=-110.5kJ∙ml-1;
③C(s)+O2(g)=CO2(g) ΔH3=-393.5kJ∙ml-1。下列说法不正确的是
A.C的燃烧热ΔH=-393.5kJ/ml
B.2gH2完全燃烧生成液态水放出的热量为241.8kJ
C.反应CO2(g)+H2(g)⇌H2O(g)+CO(g)的反应热为+41.2kJ∙ml-1
D.反应C(s)+H2O(g) ⇌CO (g)+H2(g)在高温下才能自发
10.某同学在学习“金属腐蚀与防护”知识后,设计如图所示装置以减少潮湿地面下钢铁输水管的腐蚀。下列说法正确的是
A.钢铁输水管主要发生化学腐蚀
B.镁极发生还原反应
C.导线中电流由镁流向钢铁输水管
D.该防护方法为牺牲阳极法
11.NA代表阿伏加德罗常数的值,下列说法正确的是
A.精炼铜过程中阴极质量增重64g,溶液中通过的电子数为2NA
B.1L1ml∙L-1Na2CO3溶液中所含阴离子的数目大于NA
C.氯碱工业阳极产生22.4L气体,则阴极产生的OH-的数目为2NA
D.某温度下,1LpH=12的Ba(OH)2溶液中含OH-数目为0.01NA
12.下列表示正确的是
A.基态硅原子价电子的轨道表示式:
B.镁原子最外层电子的电子云轮廓图:
C.基态硫原子核外电子占据的最高能层符号为:M
D.基态氧原子核外电子有8种不同的空间运动状态
13.化学与生活密切相关,下列说法错误的是
A.电动汽车使用的磷酸铁锂电池属于一次电池
B.合成氨工业的原料气必须净化处理以防催化剂“中毒”
C.浑浊的泥水可用适量明矾净化处理
D.可从海水中获取Mg和Cl2等单质
14.25℃时,用的氨水滴定溶液,加入氨水的体积与溶液中的关系如图所示(忽略溶液体积的变化)。下列说法不正确的是
A.点溶液的等于1
B.由图中数据可知,为强酸
C.点水电离出的浓度为
D.点溶液中
二、填空题
15.某温度下,在一个2L的恒容容器中,通入和,发生可逆反应生成,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
(1)该反应的化学方程式为 。
(2)反应1min时,该容器中含有的物质的量 (填“>”“”“
(3) 0.05 > 30%
(4)BCD
16.(1)
(2)
(3) 6.0≤pH<7.6(或6.0~7.6)
(4)10-37.4
(5)分液漏斗、烧杯
(6)2H2O-4e-=4H++O2↑
17.(1) 防止倒吸 防止因pH过大,转化为,使产物不纯
(2) 当滴入最后一滴NaOH溶液时,溶液由无色变为浅红色,且半分钟内不褪色,所以终点的颜色变化为无色变为浅红色 A
(3) 溶液显黄色 产生刺激性气味气体
18.(1) -48.8 kJ∙ml-1 低温
(2)AE
(3) > 减小
(4) 不是 升高温度,化学反应速率加快,甲醇的产率提高 随着温度的升高,平衡逆向移动,催化剂的活性迅速下降
选项
A
B
C
D
实验装置
实验目的
铁电极上镀铜
探究压强对化学平衡的影响
比较的与的的大小
测定盐酸与NaOH反应的中和热
选项
实验操作及现象
结论
A
向溶液中通入气体,出现黑色沉淀
酸性:
B
向溶液中滴入2滴溶液,产生白色沉淀后,再滴加2滴溶液,有红褐色沉淀生成
C
将液体和固体分别暴露在潮湿空气中,只有前者会冒“白烟”
水解性:
D
分别测浓度均为的和溶液的,后者大于前者
键
键能
745
436
462.8
413.4
351
题号
1
2
3
4
5
6
7
8
9
10
答案
C
D
A
D
C
D
C
A
B
D
题号
11
12
13
14
答案
B
C
A
C
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




