








四川省绵阳市绵阳中学2024-2025学年高三上学期12月月考化学试卷(Word版附解析)
展开
这是一份四川省绵阳市绵阳中学2024-2025学年高三上学期12月月考化学试卷(Word版附解析),文件包含四川省绵阳市绵阳中学2024-2025学年高三上学期12月月考化学试题Word版含解析docx、四川省绵阳市绵阳中学2024-2025学年高三上学期12月月考化学试题Word版含解析docx、四川省绵阳市绵阳中学2024-2025学年高三上学期12月月考化学试题Word版无答案docx、四川省绵阳市绵阳中学2024-2025学年高三上学期12月月考化学试题Word版无答案docx等4份试卷配套教学资源,其中试卷共63页, 欢迎下载使用。
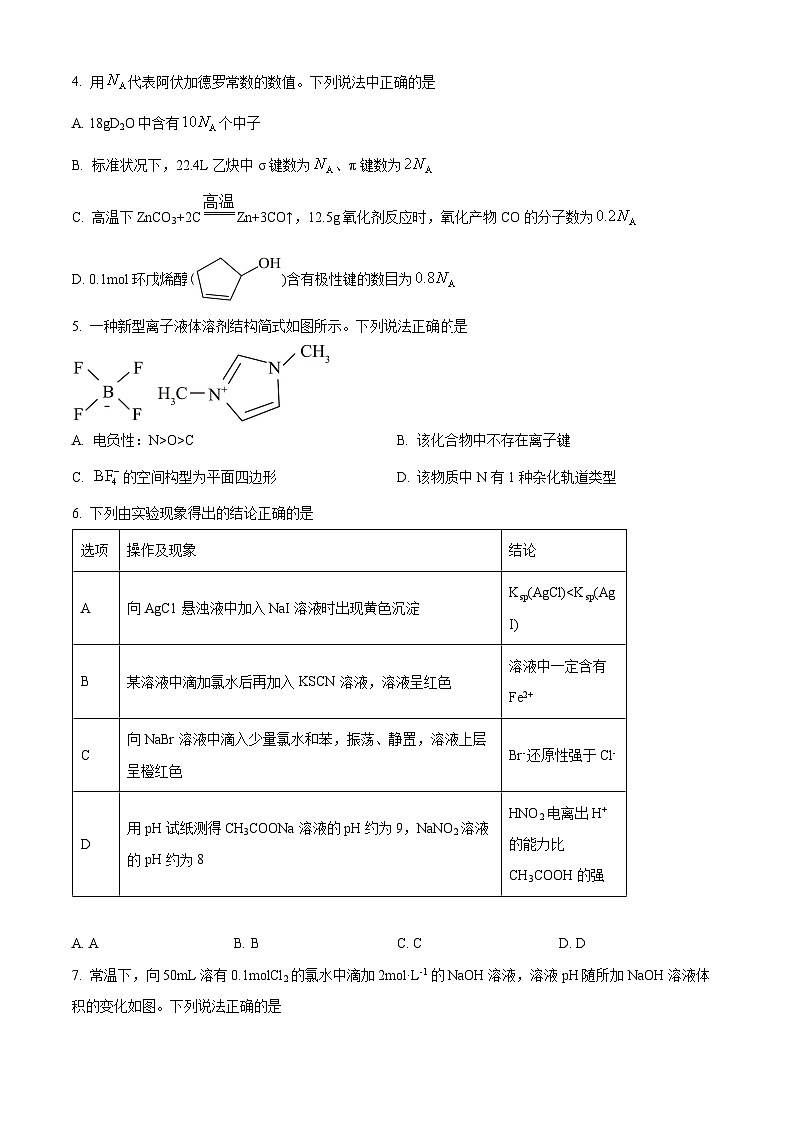
1. 劳动创造美好生活。下列劳动项目所涉及的化学知识错误的是
A. AB. BC. CD. D
2. 下列表示不正确是
A. 中子数为10的氧原子:
B. 的价层电子对互斥(VSEPR)模型:
C. 用电子式表示的形成过程:
D. 的名称:2-甲基-4-乙基戊烷
3. 设为阿伏加德罗常数的值。下列说法错误的是
A. 晶体中含有的共价键数目为
B. 和的固体混合物中所含阴、阳离子的总数目为
C. 1L 1ml/L的溶液中通入适量氨气后呈中性,此时溶液中的数目小于
D. 锌与某浓度的浓硫酸反应,生成混合气体22.4L(标准状况),锌失去电子数目为
4. 下列化学反应与方程式不相符的是
A. 黑火药爆炸:
B. 四氯化钛水解:
C. 硫化钠溶液在空气中氧化变质:
D. 硬脂酸甘油酯在NaOH溶液中皂化:
5. 关于物质的分离、提纯,下列说法错误的是
A. 蒸馏法分离和
B. 过滤法分离苯酚和溶液
C. 萃取和柱色谱法从青蒿中提取分离青蒿素
D. 重结晶法提纯含有少量食盐和泥沙的苯甲酸
6. 为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计和结论都正确的是
A. AB. BC. CD. D
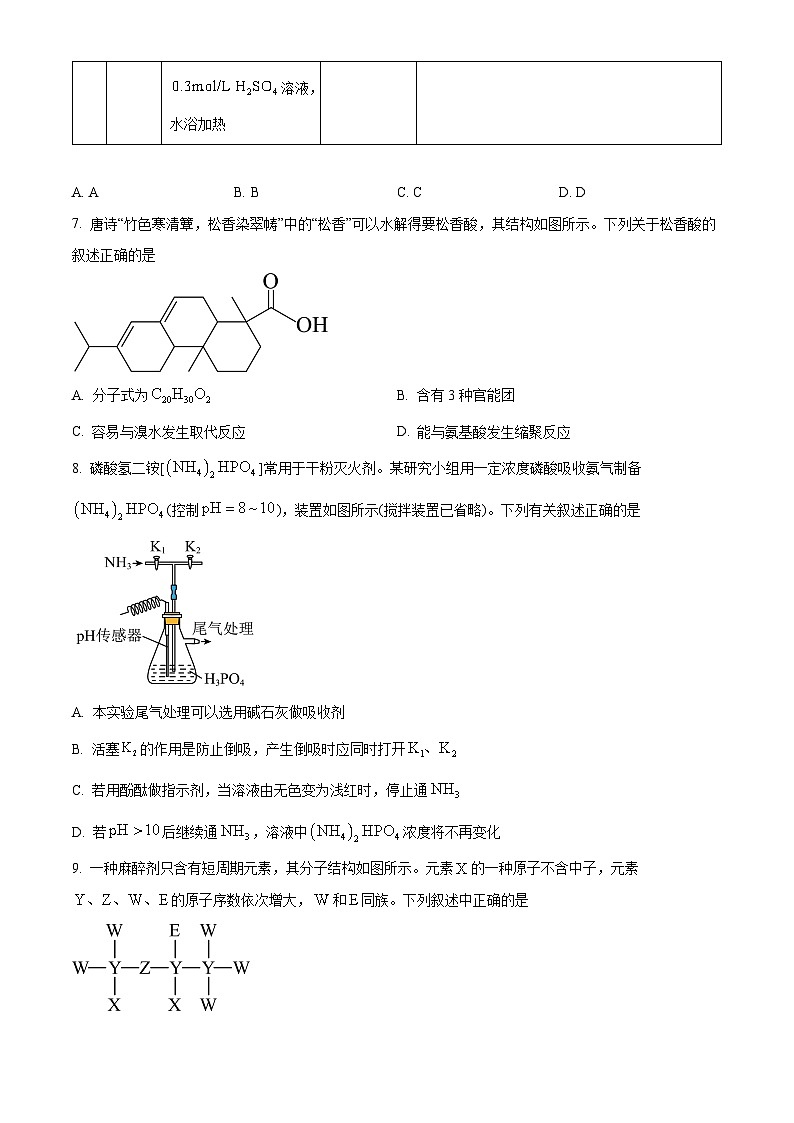
7. 唐诗“竹色寒清簟,松香染翠帱”中的“松香”可以水解得要松香酸,其结构如图所示。下列关于松香酸的叙述正确的是
A. 分子式为B. 含有3种官能团
C. 容易与溴水发生取代反应D. 能与氨基酸发生缩聚反应
8. 磷酸氢二铵[]常用于干粉灭火剂。某研究小组用一定浓度磷酸吸收氨气制备(控制),装置如图所示(搅拌装置已省略)。下列有关叙述正确的是
A. 本实验尾气处理可以选用碱石灰做吸收剂
B. 活塞的作用是防止倒吸,产生倒吸时应同时打开
C. 若用酚酞做指示剂,当溶液由无色变为浅红时,停止通
D. 若后继续通,溶液中浓度将不再变化
9. 一种麻醉剂只含有短周期元素,其分子结构如图所示。元素的一种原子不含中子,元素的原子序数依次增大,和同族。下列叙述中正确的是
A. 简单氢化物的沸点:B. 原子半径大小关系是:
C. 与组成的化合物可能含有非极性键D. 组成的酸一定是弱酸
10. 研究人员制备了一种具有锂离子通道导电氧化物(),其立方晶胞和导电时迁移过程如下图所示。已知该氧化物中为价,为价。下列说法错误的是
A. 导电时,和的价态不变B. 若,与空位的数目相等
C. 与体心最邻近的O原子数为12D. 导电时、空位移动方向与电流方向相反
11. 纳米催化制备甲酸钠的机理如下图所示:
下列说法错误的是
A. 纳米尺寸有利于加快反应速率B. 反应过程中有极性键的断裂与形成
C. 反应过程中不需要持续补充D. 总反应的原子利用率为100%
12. 已知CO2催化加氢的主要反应有:
反应Ⅰ CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH1 ΔS10 ΔS2
在恒温恒压反应器中通入1 ml CO2、3 ml H2气体,CO2的平衡转化率及CH3OH的平衡产率随温度变化关系如下图。已知:CH3OH产率=×100%;CH3OH的选择性=×100%。下列说法不正确的是
A. ΔH1<0,ΔS2>0
B. CH3OH的平衡选择性随温度的升高而减小
C. 525 K后,升高温度对反应Ⅰ的影响大于对反应Ⅱ的影响
D. 525 K时,增大的值或增大压强均能使CO2的平衡转化率达到b点的值
13. 库仑测硫仪可以测定待测气体中的含量,其工作原理如图所示。检测前,溶液中为一定值,电解池不工作。通入待检气体后,电解池开始工作,一段时间后停止。下列说法错误的是
A. 电解池开始工作时,阳极电极反应式:
B. 电解一段时间后停止,是因为已经全部转化为
C. 通入待测气体后发生反应:
D. 测得电解过程转移电子,则待测气体中的含量为
14. 时,向体积相同,浓度均为的、溶液中分别滴加等浓度的盐酸,混合溶液中的离子浓度关系如图所示。下列说法正确的是
A. 的数量级为
B. 相同浓度溶液的
C Q点溶液中:
D. 取等体积的点溶液与点溶液混合,所得混合溶液中:
15. 七水合硫酸镁()在印染、造纸等领域应用广泛。以化工废弃物盐泥(主要成分为,含少量NaCl与含铁化合物)为原料可制取七水合硫酸镁。
回答下列问题:
(1)称取干燥盐泥6.90g于100mL烧杯中,加入蒸馏水,缓慢滴加溶液,不断搅拌,得到酸解浆液,主要反应的化学方程式为______。配制溶液时,用到的实验仪器除烧杯、玻璃棒、量筒外,还必须使用的仪器有______(填标号)。
(2)加热酸解浆液,在搅拌下补加盐泥,调节浆液的pH接近6,加入,继续加热煮沸,趁热过滤。滤渣的主要成分是______、______。继续加热煮沸的目的是______。
(3)要证明铁元素已除尽,实验操作及现象是:______。
(4)向(2)所得滤液中加入溶液至沉淀完全,过滤。该操作的目的是______。将滤渣完全溶于3.0溶液,经如下实验操作:______、过滤、洗涤、干燥,得到七水合硫酸镁。
(5)实验中制得七水合硫酸镁产品的质量为3.69g,则盐泥中的含量为______。将产品加热至,测得固体失重率为,该温度下固体的化学式为______。
(6)室温下,将溶液和溶液)等体积混合,产生灰黑色沉淀,溶液呈黄色。该反应离子方程为______,实验证明该反应为可逆反应,为测定其平衡常数。待反应达到平衡状态时,取25.00mL上层清液,用标准溶液滴定,达到滴定终点记录消耗标准溶液的体积。重复实验3次,平均消耗标准溶液的体积为19.40mL。
①用于盛装标准溶液进行滴定的玻璃仪器名称为______。
②平衡时______,平衡常数______。
③若取混合反应后的含Ag浊液进行实验,会使测得的平衡常数值______。
A.偏大 B.偏小 C.无影响 D.无法判断
16. 重铬酸钠Na2Cr2O7广泛应用于医药和印染行业,用含铬矿渣(主要成分是Cr2O3,还含有少量Fe2O3和Al2O3)制备Na2Cr2O7的流程如下:回答下列问题:
已知:室温下,Al(OH)3+OH-⇌[Al(OH)4]- K=100.63;Kw= 1×10-14。
(1)含铬矿渣“灼烧”过程中,Al2O3将转化为(填化学式)______。而Cr2O3将氧化为Na2CrO4,其化学方程式中氧化剂与还原剂的物质的量之比为______。
(2)“浸取”所得的滤渣中含量最多的金属元素是______。下列措施能显著提高浸取率的方法是______。
A.搅拌 B.增加水量 C.升高温度 D.增大压强
(3)室温下“中和除铝”:[Al(OH)4]-+H+⇌Al(OH)3↓+H2O。控制pH=______,可保证[Al(OH)4]-恰好沉淀完全(溶液中浓度为1×10-5 ml·L-1)。此步骤中H2SO4也可选用“灼烧”步骤产生的(填化学式)______代替。
(4)“酸化”步骤主要发生的离子反应方程式为______。
(5)三氧化铬(CrO3)常用于做鞣革织物媒染剂,可用Na2Cr2O7固体与浓硫酸反应制取,产物中有一种显酸性的盐,写出该化学反应方程式______。
(6)配位化合物六溴硒酸钾是离子晶体,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
晶体中阴离子的化学式为______。若六溴硒酸钾的式量为M,晶胞中相邻K之间的最短距离为dnm,则晶体密度为______g·cm-3,(列出计算式,NA表示阿伏加德罗常数的值)。
17. 燃油汽车尾气中含有CO和氮氧化物,氮氧化物包括、等,研究CO还原氮氧化物及氮氧化物的分解对环境的治理有重要意义。
(1)已知: ;的燃烧热为。写出与催化转化成和的热化学方程式______。
(2)在的催化作用下,还原的反应历程和相对能量变化如图所示(逸出后物质认为状态不发生变化,在图中略去)。
①分析反应历程, ______;分子的中心原子是______,其结构式为______。
②该反应分两步进行:A.;B.______。历程中决定反应速率的变化过程是______。
A.②~③ B.③~④ C.⑤~⑥ D.⑥~⑦
(3)和恒定压强时,在密闭容器中模拟某种废气中直接催化分解过程,分解过程主反应为。反应前后各组分的信息如下表:
分析数据,写出一个分解的副反应的化学方程式:______。
该温度下主反应的______kPa(以分压表示,分压=总压物质的量分数)。若除去废气中的气体,在相同的条件下模拟实验,发现体系中的平衡转化率明显降低,解释其原因:______。
(4)杂环化合物咪唑、呋喃、噻吩均能作为配体形成配合物,三种物质的信息如下表。
①咪唑分子中所有原子共平面,其大键可以表示为______。咪唑中氮原子的杂化方式为______,易形成配位键的氮原子是______(填“a”或“b”)。
②请分析表中数据,解释咪唑、呋喃、噻吩三者沸点差异的原因______。
18. 化合物为某种用于治疗哮喘的药物的中间体,其合成路线如下:
(1)写出B结构简式________,C的化学名称______,D中能发生加成反应的官能团名称_______。
(2)根据化合物G的结构特征,分析预测其可能发生的反应类型有________。
A. 加聚反应B. 取代反应C. 氧化反应D. 消去反应
(3)的转化分两步进行:第一步为加成反应,反应方程式为_______;第二步反应生成的小分子为______。
(4)的同分异构体是醇类化合物,其核磁共振氢谱显示有3组峰,峰面积之比为,写出所有可能的结构简式为_______。
(5)利用的反应原理,设计以化合物和为原料制备聚酯高分子的合成路线为:,回答下列问题:
①的结构简式是_______。
②写出一个单体可能的化学方程式是_______。选项
劳动项目
化学知识
A
水质检验员检测自来水中余氯含量
使用氯气消毒自来水会产生余氯
B
技术员采用阳极氧化增强铝材抗腐蚀性
铝能形成致密氧化膜,增强抗腐蚀性
C
测试工程师测定钢和生铁中的碳含量
钢含碳量比生铁高,硬度比生铁大
D
环保工程师用熟石灰处理酸性废水
熟石灰具有碱性,可调控废水
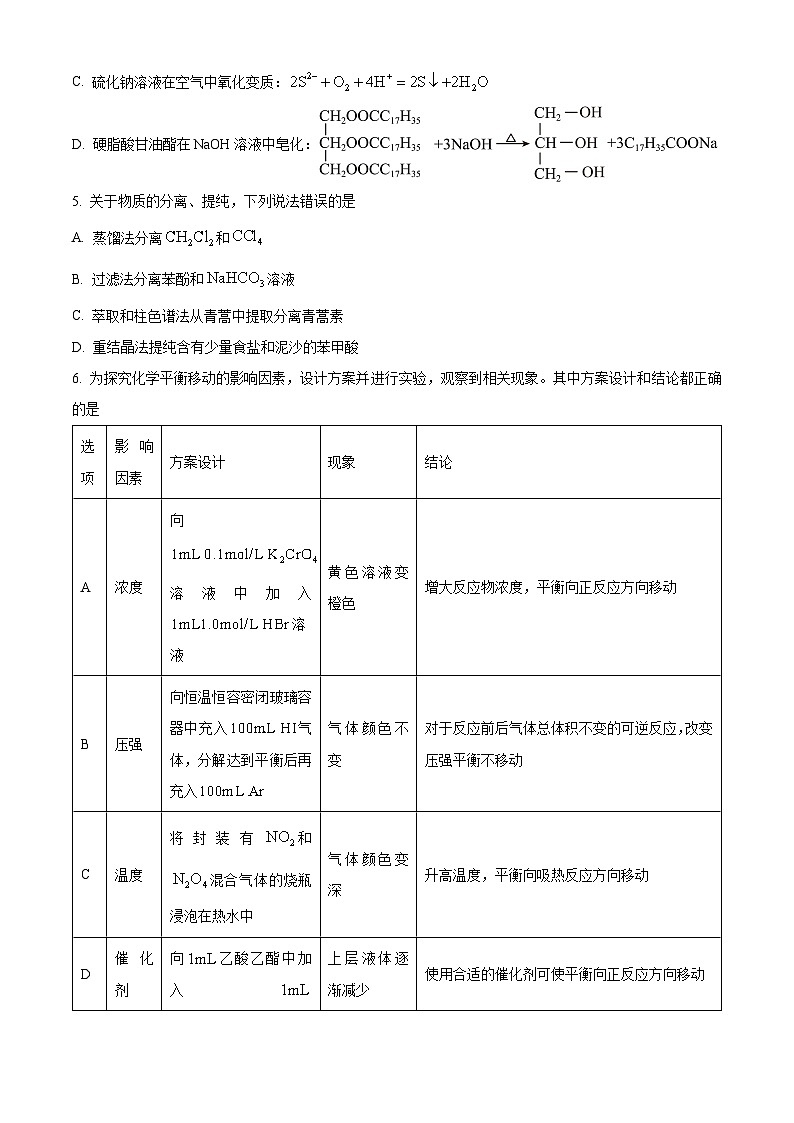
选项
影响因素
方案设计
现象
结论
A
浓度
向溶液中加入溶液
黄色溶液变橙色
增大反应物浓度,平衡向正反应方向移动
B
压强
向恒温恒容密闭玻璃容器中充入气体,分解达到平衡后再充入
气体颜色不变
对于反应前后气体总体积不变的可逆反应,改变压强平衡不移动
C
温度
将封装有和混合气体的烧瓶浸泡在热水中
气体颜色变深
升高温度,平衡向吸热反应方向移动
D
催化剂
向乙酸乙酯中加入溶液,水浴加热
上层液体逐渐减少
使用合适的催化剂可使平衡向正反应方向移动
物质
NO
n(投料)
19
34
6.5
25
0
0
n(平衡)
50
1
20
25
2
2
物质名称
咪唑
呋喃
噻吩
结构简式
沸点/
257
314
84.2
相关试卷
这是一份四川省绵阳市三台中学2024-2025学年高一上学期月考化学试卷(Word版附解析),文件包含四川省绵阳市三台中学2024-2025学年高一上学期月考化学试题Word版含解析docx、四川省绵阳市三台中学2024-2025学年高一上学期月考化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。
这是一份四川省绵阳市南山中学2024-2025学年高一上学期12月月考化学试卷(Word版附解析),文件包含四川省绵阳市南山中学2024-2025学年高一上学期12月月考化学试题Word版含解析docx、四川省绵阳市南山中学2024-2025学年高一上学期12月月考化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。
这是一份四川省绵阳市绵阳中学2024-2025学年高三上学期12月第三次月考化学试卷(Word版附解析),文件包含四川省绵阳市绵阳中学2024-2025学年高三上学期12月第三次月考化学试题Word版含解析docx、四川省绵阳市绵阳中学2024-2025学年高三上学期12月第三次月考化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共36页, 欢迎下载使用。









