
福建省福宁古五校教学联合体2024-2025学年高一上学期期中考试化学试题(含答案)
展开这是一份福建省福宁古五校教学联合体2024-2025学年高一上学期期中考试化学试题(含答案),共11页。试卷主要包含了相对原子质量,反应常被用于除去水中残余氯,下列实验装置,下列离子方程式书写正确的是,氧化二氯等内容,欢迎下载使用。
(考试时间:75分钟 试卷总分:100分)
注意:
1.本学科试卷分试题卷和答题卡两部分。试题卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)(共6页16题),全部答案必须按要求填在答题卡的相应答题栏内,否则不能得分。
2.相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 S 32 Ag 108
第Ⅰ卷 选择题(共48分)
本题包括12小题,每小题4分,共48分。每小题只有一个选项符合题意。
1.生活中处处有化学,下列说法不正确的是( )
A.食盐可作调味剂,也可作食品防腐剂
B.洁厕灵的主要成分是盐酸,不能与84消毒液混用
C.晨雾中的光束如梦如幻,是丁达尔效应带来的美景
D.工业上用氯气和澄清石灰水制漂白粉
2.铜器久置于空气中会和空气中的水蒸气、、作用产生“铜绿”。“铜绿”不稳定,受热生成CuO,且能跟酸反应生成铜盐等。上述过程中,没有涉及的基本反应类型是( )
A.复分解反应B.化合反应C.置换反
应D.分解反应
3.反应常被用于除去水中残余氯。设为阿伏加德罗常数的值,下列说法不正确的是( )
A.25℃、101kPa时,71g 中氯原子的数目为2
B.100mL 1 溶液中含氧原子的数目为0.2
含有质子的数目为1.6
D.通过上述反应除去7.1g ,生成的数为0.2
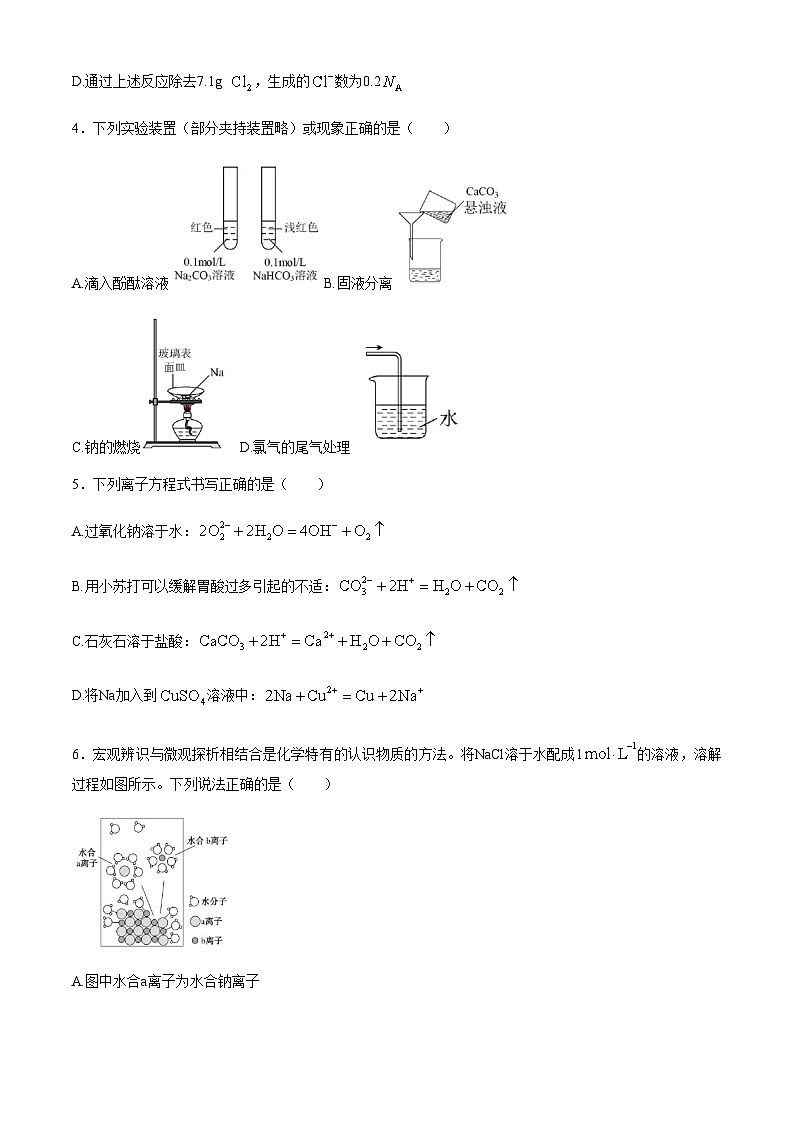
4.下列实验装置(部分夹持装置略)或现象正确的是( )
A.滴入酚酞溶液B.固液分离
C.钠的燃烧D.氯气的尾气处理
5.下列离子方程式书写正确的是( )
A.过氧化钠溶于水:
B.用小苏打可以缓解胃酸过多引起的不适:
C.石灰石溶于盐酸:
D.将Na加入到溶液中:
6.宏观辨识与微观探析相结合是化学特有的认识物质的方法。将NaCl溶于水配成1的溶液,溶解过程如图所示。下列说法正确的是( )
A.图中水合a离子为水合钠离子
B.NaCl溶液可以导电,因此该溶液为电解质
C.溶液中存在
D.NaCl溶解过程需要在容量瓶中进行
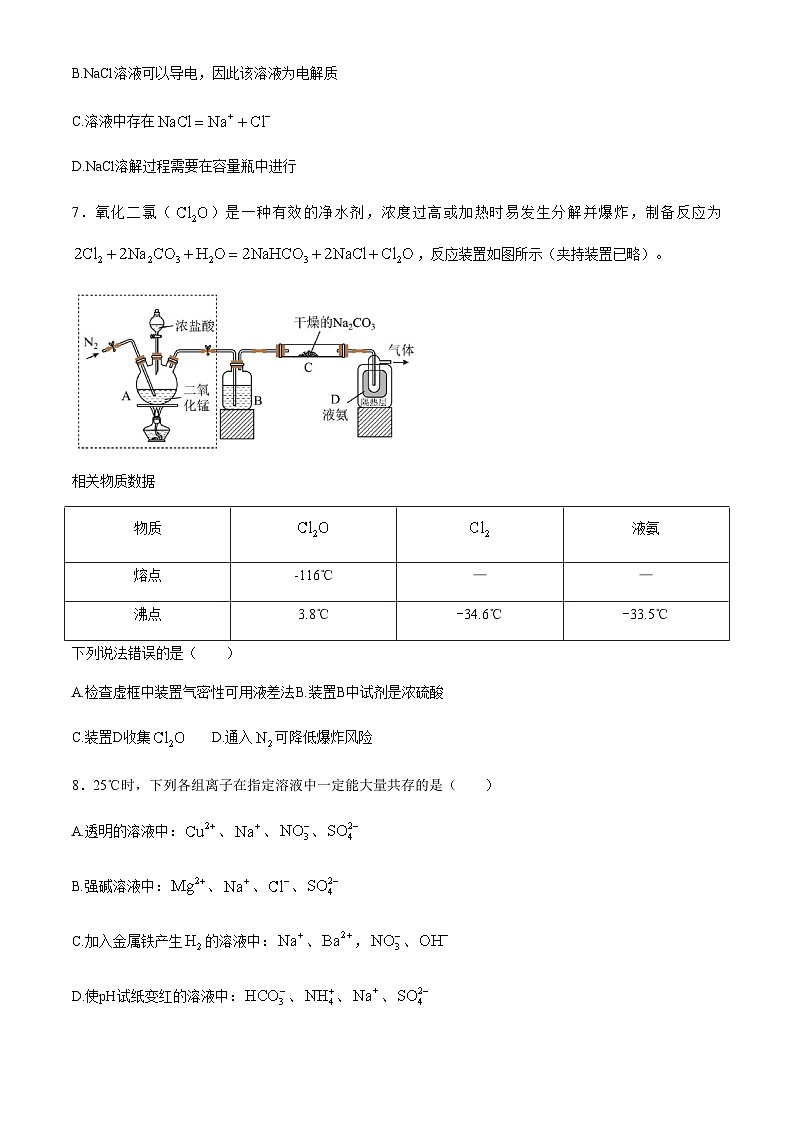
7.氧化二氯()是一种有效的净水剂,浓度过高或加热时易发生分解并爆炸,制备反应为,反应装置如图所示(夹持装置已略)。
相关物质数据
下列说法错误的是( )
A.检查虚框中装置气密性可用液差法B.装置B中试剂是浓硫酸
C.装置D收集D.通入可降低爆炸风险
8.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.透明的溶液中:、、、
B.强碱溶液中:、、、
C.加入金属铁产生的溶液中:、,、
D.使pH试纸变红的溶液中:、、、
9.构建知识网络,厘清物质间的相互转化关系是化学学习中的一种重要方法。如图中线段两端的物质在一定条件下可以发生反应。下列符合图示要求的是( )
A.① ② ③
B.① ② ③
C.① ②CO ③
D.① ②Fe ③
10.如图是利用“手持”技术测定阳光照射不同气体温度变化曲线,其中四个容器均密闭、体积相等(初始温度:25℃,初始压强:101kPa)。
下列说法正确的是( )
A.实验开始时,四种气体质量相同
B.若容器的容积为2.24L,13:00时原子个数等于0.2
C.12:30-13:30时间范围内压强最小
D.是四种气体中温室效应最显著的
11.部分含氯物质的分类与相应氯元素的化合价关系如图所示,其中c、d、f均为钠盐,下列叙述不正确的是( )
A.新制a的水溶液中存在平衡:
B.a→d→e的转化均可以通过一步反应实现
C.新制a的水溶液能使石蕊试液变红后褪色
D.用强光照射e的水溶液,溶液酸性增强,杀菌能力减弱
12.已知一定温度和体积下气体的压强与分子数成正比,表示1个标准大气压。将一定质量的炭粉和氧气在耐压密闭容器中用电热丝引燃使之充分反应,并利用压强传感器测定容器内的气压变化,观察到炭粉完全消失,如图为气压变化图像。下列说法正确的是( )
A.AB段温度达到炭粉着火点
B.D点气体的成分是和
C.参加反应的C和的质量比为3:7
D.生成的CO和的物质的量比为4:3
第Ⅱ卷 非选择题(共52分)
13.(14分)
酸、碱、盐是化学工业中的重要原料。回答下列问题:
(1)纯碱是重要的化工原料之一,写出其在水中的电离方程式_____________。
(2)可作饮用水处理剂,该反应的离子方程式:,处理水中悬浮颗粒物的原理是_____________。
(3)将200mL 0.5 溶液与300mL 0.2 溶液混合,则所得混合溶液中的物质的量浓度为_____________(忽略混合前后溶液体积的变化)。
(4)向两份相同的滴有酚酞的溶液中,分别滴入物质的量浓度相等的、溶液,混合溶液的导电能力随滴入溶液体积的变化曲线如下图所示。
= 1 \* GB3 ①从开始至a点,除电导变化外,还观察到烧杯中的实验现象有_____________。
= 2 \* GB3 ②c点两溶液中含有相同量的离子是_____________,写出b点到d点反应的离子方程式为_______________________________________。
= 3 \* GB3 ③b点溶液中发生中和的与未反应的之比为_____________。
14.(16分)
一种由黄铁矿制备硫酸的工艺流程如图:
根据所学知识,回答下列问题:
(1)上述划线的物质中,属于酸性氧化物的是_____________(填化学式)。
(2)写出黄铁矿在空气中焙烧的产物是_____________(填化学式)。
(3)同温同压下,等质量的气体和气体的体积之比=_____________,氧原子数之比=_____________。
(4)稀释发烟硫酸配制250mL物质的量浓度为2.0的稀硫酸。
①下图为“溶液配制”的部分过程,操作a应重复3次,目的是_____________,定容后还需要的操作为_____________。
②从稀释好的溶液中取出10mL,将此10mL溶液稀释到100mL,稀释后溶液中=__________。
③下列操作可能使配制的溶液浓度偏低的是__________(填标号)。
A.移液时,未洗涤烧杯内壁和玻璃棒
B.稀释后未经冷却就移液
C.定容时,俯视容量瓶刻度线
D.容量瓶用蒸馏水洗净后,直接使用
15.(11分)
氯化铁(,易潮解)是一种重要的铁盐,常用作污水处理、药物等领域。某同学在实验室制备(与HCl反应),装置(部分夹持仪器已省略)如图所示:
回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是___________。
(2)装置B所盛放的试剂应为___________(填试剂名称),装置E中倒置漏斗的作用是_________________________________。
(3)已知:A装置固体产物中酸式盐、正盐的物质的量之比为2:1,A中反应的总化学方程式为______________________,该反应中体现的制酸原理是______________________。
(4)设计简单实验证明E装置中吸收了氯化氢:______________________。
16.(11分)用粗盐(含、、及少量泥沙等杂质)制备精盐的流程如下。
回答下列问题:
(1)步骤①、⑤、⑦中均需用到的仪器为_________。
(2)步骤⑤操作中得到沉淀的成分有泥沙、、、_________(填化学式)。
(3)步骤⑥中发生反应的离子方程式为___________________________。
(4)步骤②、③、④操作中需将溶液加热至微沸,“加热至微沸”的目的除了提高反应速率外还有_________。
(5)产品检验:
称取2.0g氯化钠产品溶于70mL水中,加入指示剂,用1.0 标准液测定,重复2~3次,平均消耗标准液体积32.0mL,则氯化钠的质量分数为_________。
福宁古五校教学联合体2024-2025学年第一学期期中质量监测
化学科评分标准与评分细则
以下化学方程式的书写中,化学式书写错误、反应物、生成物漏写均不得分,“=”写成“→”、未标注“↑”、“↓”、未配平、配平错误、未标注“”等反应条件扣1分,化学方程式写出离子方程式扣1分,离子方程式写成化学方程式不给分。专业名词出现错别字不给1分。
1-12每小题4分,共48分
1-5 DCBAC6-10 CBAAD11-12 AD
13.(14分)
(1)(2分)
(2)与水反应生成胶体,胶体具有吸附性,可吸附水中的悬浮颗粒物(答到“与水反应生成胶体、胶体具有吸附性、可吸附水中的悬浮颗粒物”中的两点就给分)(2分)
(3)0.76(2分)
(4)①有白色沉淀生成,红色逐渐变浅至褪色(答到一点给1分)(2分) ②(2分) (2分) ③1:1(2分)
14.(16分)(每空2分)
(1)、(答对一个给1分,有错不得分)(2分)
(2)、(答对一个给1分,有错不得分)(2分)
(3)4:5(2分) 6:5(2分)
(4)①将溶质全部转移到容量瓶中(2分) 颠倒摇匀、装瓶贴签(答“摇匀、装瓶”也给分,答对一个给1分)(2分) = 2 \* GB3 ②0.4(2分) ③A(2分)
15.(11分)
(1)分液漏斗(1分)
(2)浓硫酸(2分) 防倒吸(2分)
(3)(2分) 难挥发性酸制取挥发性酸(或高沸点酸制取低沸点酸)(2分)
(4)测定溶液pH,pH<7,再滴加溶液,产生白色沉淀(答对一半给1分)(2分)
16.(11分)
(1)玻璃棒(1分)
(2)、(答对一个给1分,有错不得分)(2分)
(3)(2分) (2分)
(4)为了使沉淀颗粒长大而易于沉降和过滤(答“促进沉淀形成、以及促进固液分离”等合理答案均可得分)(2分)
(5)93.6%(答“0.936”也给分)(2分)
物质
液氨
熔点
-116℃
—
—
沸点
3.8℃
-34.6℃
-33.5℃
相关试卷
这是一份福建省福宁古五校教学联合体2024-2025学年高二上学期期中考试 化学试题,共9页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。
这是一份2025福建省福宁古五校教学联合体高一上学期期中考试化学PDF版含答案,共10页。
这是一份福建省福宁古五校教学联合体2024-2025学年高一上学期期中考试化学试卷(PDF版附答案),共10页。












