资料中包含下列文件,点击文件名可预览资料内容



还剩11页未读,
继续阅读
浙江省衢州六校联盟2024-2025学年高一上学期期中联考化学试卷(Word版附解析)
展开这是一份浙江省衢州六校联盟2024-2025学年高一上学期期中联考化学试卷(Word版附解析),文件包含浙江省衢州六校联盟2024-2025学年高一上学期期中联考化学试题Word版含解析docx、浙江省衢州六校联盟2024-2025学年高一上学期期中联考化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共19页, 欢迎下载使用。
考生须知:
1.本卷共6页满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
可能用到的相对原子质量:H1 C12 O16 Na23 Mg24 S32 Cl35.5 Cu64
选择题部分
一、选择题(本大题共20小题,每小题3分,共60分。每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1. 氢气的分子式是
A. COB. NO2C. H2D. O2
【答案】C
【解析】
【详解】A.CO是一氧化碳的分子式,故不选A;
B.NO2是二氧化氮的分子式,故不选B;
C.H2是氢气的分子式,故选C;
D.O2是氧气的分子式,故不选D;
故选C。
2. 甲烷(CH4)可直接用作气体燃料。按物质的组成和性质进行分类,甲烷属于
A. 单质B. 氧化物C. 酸D. 有机物
【答案】D
【解析】
【详解】A.只含一种元素的纯净物为单质,CH4含两种元素,不是单质,A错误;
B.由两种元素组成,且其中一种元素为氧元素的化合物为氧化物,CH4不含氧元素,不是氧化物,B错误;
C.水溶液中电离出的阳离子只有氢离子的化合物为酸,CH4不能电离出氢离子,不是酸,C错误;
D.CH4含碳、氢两种元素,属于有机烃类物质,D正确;
答案选D。
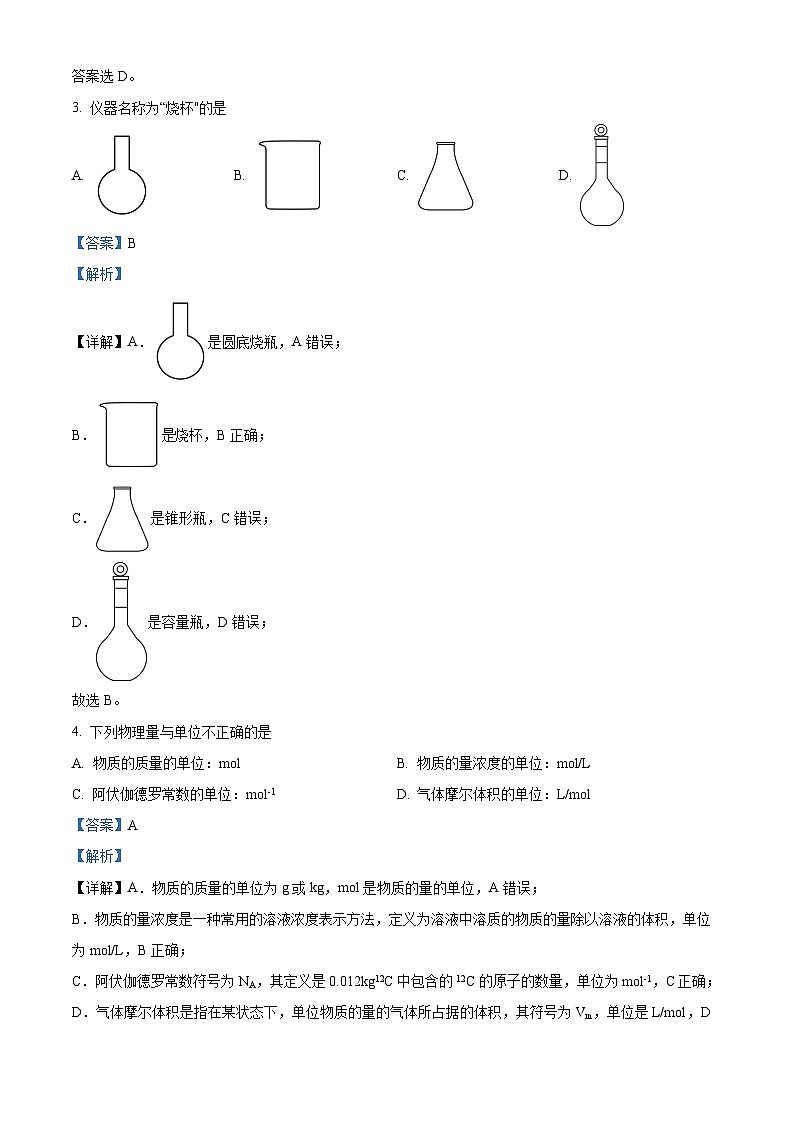
3. 仪器名称为“烧杯"的是
A. B. C. D.
【答案】B
【解析】
【详解】A.是圆底烧瓶,A错误;
B.烧杯,B正确;
C.是锥形瓶,C错误;
D.是容量瓶,D错误;
故选B。
4. 下列物理量与单位不正确的是
A. 物质的质量的单位:mlB. 物质的量浓度的单位:ml/L
C. 阿伏伽德罗常数的单位:ml-1D. 气体摩尔体积的单位:L/ml
【答案】A
【解析】
【详解】A.物质的质量的单位为g或kg,ml是物质的量的单位,A错误;
B.物质的量浓度是一种常用的溶液浓度表示方法,定义为溶液中溶质的物质的量除以溶液的体积,单位为ml/L,B正确;
C.阿伏伽德罗常数符号为NA,其定义是0.012kg12C中包含的12C的原子的数量,单位为ml-1,C正确;
D.气体摩尔体积是指在某状态下,单位物质的量的气体所占据的体积,其符号为Vm,单位是L/ml,D正确;
故选A。
5. 实验室制取氢气的反应Zn+H2SO4=ZnSO4+H2↑中,还原剂是
A. ZnB. H2SO4C. ZnSO4D. H2
【答案】A
【解析】
【详解】反应Zn+H2SO4=ZnSO4+H2↑中,锌元素化合价升高,Zn失去电子,被氧化,还原剂是Zn,故选A。
6. 下列各组物质,按化合物、单质、混合物顺序排列的是
A. 烧碱、氯水、碘酒B. 生石灰、白磷、冰水混合物
C. 干冰、铁、盐酸D. 空气、氮气、硫酸铜
【答案】C
【解析】
【分析】不同元素组成的纯净物为化合物,同种元素组成的纯净物为单质,不同物质组成的物质为混合物。
【详解】A.烧碱氢氧化钠,属于化合物,氯水和碘酒均是混合物,故A不符合题意;
B.生石灰是CaO为化合物,白磷是单质,冰水混合物的组成只有H2O,是纯净物,故B不符合题意;
C.干冰是固体二氧化碳,属于化合物,铁是单质,盐酸是氯化氢的水溶液,属于混合物,故C符合题意;
D.空气为混合物,氮气单质,硫酸铜是化合物,是纯净物,故D不符合题意;
故选C。
7. 下列物质属于电解质的是
A. 熔融NaClB. FeCl3溶液C. FeD. 葡萄糖
【答案】A
【解析】
【详解】A.氯化钠的水溶液或熔融状态下能够导电,熔融的氯化钠属于电解质,A符合题意;
B.氯化铁溶液是混合物,既不是电解质也不是非电解质,B不合题意;
C.铁是单质,既不是电解质也不是非电解质,C不合题意;
D.葡萄糖的水溶液和熔融状态下都不能导电,葡萄糖属于非电解质,D不合题意;
故答案为A。
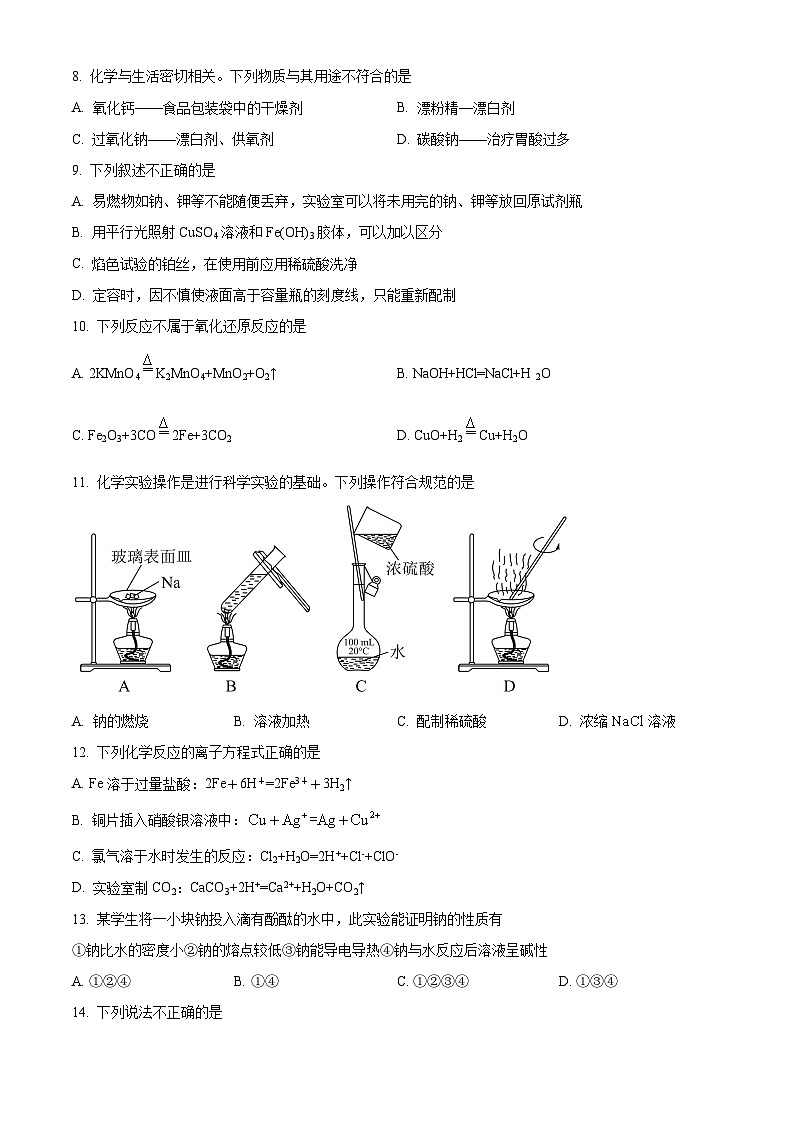
8. 化学与生活密切相关。下列物质与其用途不符合的是
A. 氧化钙——食品包装袋中的干燥剂B. 漂粉精—漂白剂
C. 过氧化钠——漂白剂、供氧剂D. 碳酸钠——治疗胃酸过多
【答案】D
【解析】
【详解】A.生石灰具有吸水性,常用作干燥剂, A符合;
B.漂白精的有效成分是次氯酸钙,具有强的氧化性,可作漂白剂,B符合;
C.过氧化钠能够与水、二氧化碳反应产生氧气,因此可作供氧剂;其具有强氧化性,能够将有色物质氧化变为无色物质,因此又可作漂白剂,C符合;
D.碳酸钠碱性较强,对人有强烈的刺激性,不能用于治疗胃酸过多,应该使用小苏打治疗胃酸过多,D不符合;
答案选D。
9. 下列叙述不正确的是
A. 易燃物如钠、钾等不能随便丢弃,实验室可以将未用完的钠、钾等放回原试剂瓶
B. 用平行光照射CuSO4溶液和Fe(OH)3胶体,可以加以区分
C. 焰色试验的铂丝,在使用前应用稀硫酸洗净
D. 定容时,因不慎使液面高于容量瓶的刻度线,只能重新配制
【答案】C
【解析】
【详解】A.剩余钠、钾如直接放入废液缸会与水剧烈反应容易造成危险,则易燃物如钠、钾等不能随便丢弃,实验室可以将未用完的钠、钾等放回原试剂瓶,A正确;
B.溶液没有丁达尔效应,胶体有丁达尔效应,用平行光照射CuSO4溶液和Fe(OH)3胶体,可以加以区分,B正确;
C.盐酸为强酸,可以除掉铂丝上有可能含有的杂质,灼烧时盐酸高温挥发,不会残留在铂丝上,则焰色试验的铂丝,在使用前应用稀盐酸洗净,不能用稀硫酸洗,C不正确;
D.定容时,因不慎使液面高于容量瓶的刻度线,导致体积偏大所配制的溶液浓度偏低,则只能重新配制,D正确;
选C。
10. 下列反应不属于氧化还原反应的是
A. 2KMnO4K2MnO4+MnO2+O2↑B. NaOH+HCl=NaCl+H2O
C. Fe2O3+3CO2Fe+3CO2D. CuO+H2Cu+H2O
【答案】B
【解析】
【详解】A.2KMnO4K2MnO4+MnO2+O2↑中Mn、O元素化合价发生变化,属于氧化还原反应,A不满足题意;
B.NaOH+HCl=NaCl+H2O中元素化合价不发生变化,不属于氧化还原反应,B满足题意;
C.Fe2O3+3CO2Fe+3CO2中Fe、C元素化合价发生变化,属于氧化还原反应,C不满足题意;
D.CuO+H2Cu+H2O中Cu、H元素化合价发生变化,属于氧化还原反应,D不满足题意;
答案选B。
11. 化学实验操作是进行科学实验的基础。下列操作符合规范的是
A. 钠的燃烧B. 溶液加热C. 配制稀硫酸D. 浓缩溶液
【答案】D
【解析】
【详解】A.钠是固体,灼烧固体药品应该用坩埚,不能用表面皿,故A错误;
B.加热溶液时液体的体积不超过试管容积的三分之一,故B错误;
C.不能在容量瓶中稀释浓硫酸,应在烧杯中稀释,待冷却后再转移至容量瓶,故C错误;
D.可选蒸发皿浓缩NaCl溶液,故D正确;
故选:D。
12. 下列化学反应的离子方程式正确的是
A. Fe溶于过量盐酸:2Fe+6H+=2Fe3++3H2↑
B. 铜片插入硝酸银溶液中:
C. 氯气溶于水时发生的反应:Cl2+H2O=2H++Cl-+ClO-
D. 实验室制CO2:CaCO3+2H+=Ca2++H2O+CO2↑
【答案】D
【解析】
【详解】A.Fe溶于过量盐酸反应生成FeCl2和H2,离子方程式为:Fe+2H+=Fe2++H2↑,A错误;
B.铜片插入硝酸银溶液中发生置换反应生成Ag和Cu(NO3)2,离子方程式为:,B错误;
C.氯气溶于水时发生反应生成HCl和HClO,离子方程式为:Cl2+H2O=H++Cl-+HClO,C错误;
D.CaCO3和盐酸反应生成二氧化碳和氯化钙,离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,D正确;
故选D。
13. 某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠的性质有
①钠比水的密度小②钠的熔点较低③钠能导电导热④钠与水反应后溶液呈碱性
A. ①②④B. ①④C. ①②③④D. ①③④
【答案】A
【解析】
【详解】将一小块钠投入滴有酚酞的水中,迅速融化成小球,且浮在水面上,发出嘶嘶的响声,且烧杯发烫,溶液变红色;①浮在水面上说明钠比水的密度小;②钠迅速融化成小球,说明钠的熔点较低;③烧杯发烫说明钠与水反应时放出热量,不能说明钠能导电;④碱性溶液能使酚酞变红,溶液变红色说明钠与水反应后溶液呈碱性,故选:A。
14. 下列说法不正确的是
A. 金刚石和石墨互为同素异形体
B. Na在空气中点燃,生成的主要产物为白色的Na2O
C. 可用水来检验某Na2O样品中是否含有Na2O2
D. 碱性氧化物都是金属氧化物
【答案】B
【解析】
【详解】A.金刚石和石墨是C元素的不同单质,互为同素异形体,A正确;
B.Na在空气中点燃,生成的主要产物为淡黄色的Na2O2,B错误;
C.Na2O和水反应生成NaOH,Na2O2和水反应生成NaOH和O2,可用水来检验某Na2O样品中是否含有Na2O2,C正确;
D.碱性氧化物是指和酸反应只能生成盐和水的氧化物,这类氧化物都是金属氧化物,D正确;
故选B。
15. 下列各组中的离子,能在溶液中大量共存的是
A. OH-、H+、、K+B. 、OH-、Fe3+、Na+
C. 、Ca2+、H+、Cl-D. Na+、Ba2+、Cl-、OH-
【答案】D
【解析】
【详解】A.OH-与H+反应生成水,不能大量共存,A不符合题意;
B.OH-与Fe3+反应生成氢氧化铁沉淀,不能大量共存,B不符合题意;
C.与H+反应生水和二氧化碳,不能大量共存,C不符合题意;
D.离子间互相不反应,可以大量共存,D符合题意;
答案选D。
16. 表示阿伏加德罗常数的值,下列叙述正确的是
A. 常温常压下,含有的分子数为
B. 镁变成时,失去的电子数目为0.2
C. 的溶液中含数目为
D. 标准状况下,含有的分子数为
【答案】B
【解析】
【详解】A.常温常压下,的物质的量不是0.5ml,氯气分子个数不是,A错误;
B.镁的物质的量为0.1ml,变成时,失去的电子数目为0.2,B正确;
C.溶液体积未知,无法计算钠离子个数,C错误;
D.标况下水为液态,水的物质的量不是0.5ml,水分子数不是,D错误;
故选B。
17. 实验室需要配制2ml/L的NaCl溶液450mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是
A. 450mL52.65gB. 500mL58.5gC. 450mL52.7gD. 任意规格58.5g
【答案】B
【解析】
【详解】实验室常见的容量瓶没有450mL规格的,根据容量瓶“大而近”的选择原理可知,应该选择500mL容量瓶,需要称量NaCl的质量为:2ml/L×0.5L×58.5g/ml=58.5g,故答案为:B。
18. 下列有关Na2CO3和NaHCO3的性质,叙述错误的是
A. 鉴别Na2CO3和NaHCO3可以用BaCl2溶液
B. Na2CO3、NaHCO3的水溶液均呈碱性
C. 向Na2CO3粉末和NaHCO3晶体中滴入少量水,前者温度升高,后者温度下降
D. NaHCO3热稳定性大于Na2CO3
【答案】D
【解析】
【详解】A. Na2CO3和NaHCO3溶液中分别加入BaCl2溶液,前者反应生成白色碳酸钡沉淀,后者不发生反应、无明显现象,则鉴别Na2CO3和NaHCO3可以用BaCl2溶液,A正确;
B. Na2CO3、NaHCO3的水溶液均呈碱性,且等物质的量浓度时Na2CO3的碱性比NaHCO3的强,B正确;
C. Na2CO3粉末和NaHCO3晶体分别加水溶解时,前者放热、后者吸热,则向Na2CO3粉末和NaHCO3晶体中滴入少量水,前者温度升高,后者温度下降,C正确;
D.NaHCO3受热分解产生二氧化碳、水和Na2CO3, 则NaHCO3热稳定性小于Na2CO3,D不正确;
选D。
19. NaCl溶于水,溶解过程如图所示。下列说法不正确的是
A. a离子为Cl−,b离子为Na+
B. NaCl在水分子的作用下,形成自由移动的水合钠离子和水合氯离子
C. NaCl溶液导电的原因是溶液中有自由移动的离子
D. 在通电后,NaCl固体发生电离
【答案】D
【解析】
【分析】由图可知,NaCl固体加入水中可发生电离,产生可自由移动的水合钠离子和水合氯离子;
【详解】A.Cl-半径大,Na+半径小,且氯离子带负电荷能吸引水中的氢原子,钠离子带正电荷能吸引水中的氧原子,则a离子为Cl−,b离子为Na+,故A正确;
B.由图可知,NaCl在水分子的作用下,形成自由移动的水合钠离子和水合氯离子,故B正确;
C.结合选项B可知,NaCl溶液导电的原因是溶液中有自由移动的离子,故C正确;
D.NaCl固体发生电离不需要通电,故D错误;
答案选D。
20. 下列有关实验操作、实验现象及实验结论都正确的是
A. 向溶液中通入少量CO2,有白色沉淀生成,白色沉淀为CaCO3
B. 某试样做焰色试验,火焰呈黄色,该试样一定是钠盐
C. 把小块钠投入到硫酸铜溶液中,钠熔化成闪亮的小球,在水面上四处游动,有“嘶嘶”的响声发出,有蓝色絮状沉淀生成
D. 向某无色溶液中滴加硝酸银溶液,有白色沉淀生成,原无色溶液中一定含有氯离子
【答案】C
【解析】
【详解】A.向溶液中通入少量CO2,两者不发生反应,不会产生白色沉淀,A错误;
B.某试样做焰色试验,火焰呈黄色,说明其中含有Na元素,该试样不一定是钠盐,可能为氧化钠或氢氧化钠,B错误;
C.将小块钠投入到硫酸铜溶液中,先发生反应:,生成的氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:,则现象为:钠熔化成闪亮的小球,在水面上四处游动,有“嘶嘶”的响声发出,有蓝色絮状沉淀生成,C正确;
D.向某无色溶液中滴加硝酸银溶液,有白色沉淀生成,该白色沉淀不一定是AgCl,可能是Ag2SO4,原无色溶液中不一定含有氯离子,D错误;
故选C。
非选择题部分
二、非选择题(本大题共5小题,共40分)
21. 按要求回答下列问题:
(1)氯化铁的化学式_______。
(2)硫酸钾在水溶液中的电离方程式_______。
(3)碳酸钠与足量稀盐酸反应的离子方程式_______。
(4)向沸水中逐滴加入5~6滴饱和溶液,继续加热至沸腾,液体呈现_______色,停止加热,即可制得胶体。
【答案】(1)FeCl3
(2)K2SO4=2K++
(3)+2H+=CO2↑+H2O
(4)红褐
【解析】
【小问1详解】
氯化铁的化学式为FeCl3。
【小问2详解】
硫酸钾在水溶液中完全电离为K+、,电离方程式为K2SO4=2K++。
【小问3详解】
碳酸钠与足量稀盐酸反应,生成氯化钠、CO2、H2O,离子方程式为+2H+=CO2↑+H2O。
【小问4详解】
氢氧化铁胶体呈红褐色,则向沸水中逐滴加入5~6滴饱和溶液,继续加热至液体呈红褐色,停止加热,即可制得胶体。
22. 以氯化钠为原料可以制备纯碱,烧碱,漂白粉等多种工业产品,流程示意图,如下:
请回答:
(1)氯气可以用来制备漂白粉,写出氯气的其他一种用途_______。
(2)漂白粉的有效成分_______(填化学式)。
(3)写出实验室制取氯气的离子方程式_______。
(4)写出晶体Z加热的化学方程式_______。
(5)下列说法不正确的是_______。
A. 步骤I能制得金属钠
B. 步骤II制备漂白粉的试剂W为冷的石灰乳
C. 铁在氯气中燃烧生成氯化铁
D. 干燥的氯气不能使有色鲜花变色
【答案】(1)杀菌、消毒
(2)Ca(ClO)2
(3)MnO2+4H++2Cl-Mn2++Cl2↑+2H2O
(4)2NaHCO3Na2CO3+CO2↑+H2O (5)AD
【解析】
【分析】电解饱和食盐水生成Cl2,将Cl2通入石灰乳中生成次氯酸钙制漂白粉;先使氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,其化学反应原理是:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,碳酸氢钠受热分解:2NaHCO3Na2CO3+CO2↑+H2O,生成的二氧化碳循环使用,碳酸氢钠受热分解制得Na2CO3,据此解答。
【小问1详解】
氯气与水反应生成次氯酸,次氯酸具有很强的氧化性,能够杀死水中的细菌、病毒和其他微生物,氯气可应用于饮用水的杀菌、消毒。
【小问2详解】
漂白粉的有效成分是Ca(ClO)2。
【小问3详解】
实验室用MnO2和浓盐酸在加热条件下反应制取氯气,离子方程式为:MnO2+4H++2Cl-Mn2++Cl2↑+2H2O。
【小问4详解】
由分析可知,Z为NaHCO3,NaHCO3受热分解生成Na2CO3、CO2和H2O,化学方程式为:2NaHCO3Na2CO3+CO2↑+H2O。
【小问5详解】
A.步骤I电解饱和食盐水得到氯气、氢气和氢氧化钠溶液,不能制得金属钠,A错误;
B.氢氧化钙的溶解度随温度的升高而降低,冷的石灰乳中氢氧化钙较多,步骤II制备漂白粉的试剂W为冷的石灰乳,B正确;
C.氯气氧化性较强,铁在氯气中燃烧生成氯化铁,C正确;
D.干燥氯气没有漂白性,鲜花中含有水,氯气和水反应生成的次氯酸具有漂白性,能使有色鲜花褪色,D错误;
故选AD。
23. 铜与浓硫酸可发生如下反应:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O。
(1)用单线桥标出电子转移的方向和数目:_______。
(2)该反应中氧化产物是_______(填化学式)
(3)该反应中氧化剂与还原剂物质的量之比是_______。
【答案】(1) (2)CuSO4
(3)1:1
【解析】
【小问1详解】
该反应中Cu化合价升高,失去电子,硫元素化合价降低,得到电子,反应转移2个电子,用单线桥标出电子转移的方向和数目:。
【小问2详解】
该反应中铜元素化合价升高,Cu被氧化,生成硫酸铜,Cu是还原剂,氧化产物是CuSO4;
【小问3详解】
该反应中硫元素化合价降低,2ml硫酸中只有1ml做氧化剂生成二氧化硫,1ml硫酸表现酸性生成硫酸铜,还原剂是Cu,则氧化剂与还原剂物质的量之比是1:1。
24. 用如图所示装置进行实验,证明过氧化钠(Na2O2)可在呼吸面具和潜水艇中作供氧剂。
请回答:
(1)A中盛放稀盐酸的装置的名称_______。
(2)装置C中过氧化钠与二氧化碳反应的化学方程式是_______。
(3)装置B作用是_______。
(4)当装置内气流平稳后开始用试管收集气体,该气体能_______,证明过氧化钠可作供氧剂。
【答案】(1)分液漏斗
(2)2Na2O2+2CO2=2Na2CO3+O2
(3)除去CO2中的HCl
(4)使带火星的木条复燃
【解析】
【分析】A中碳酸钙与稀盐酸反应制备CO2,B中饱和碳酸氢钠溶液除去CO2中的HCl,C中主要是过氧化钠与二氧化碳反应生成碳酸钠和氧气:2Na2O2+2CO2=2Na2CO3+O2,D吸收未反应完的二氧化碳,E中排水法收集氧气。
【小问1详解】
A中盛放稀盐酸的装置的名称:分液漏斗;
【小问2详解】
C中过氧化钠与二氧化碳反应的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2;
【小问3详解】
装置B作用是:除去CO2中的HCl;
【小问4详解】
当装置内气流平稳后开始用试管收集气体,该气体能使带火星的木条复燃,说明为氧气,证明过氧化钠可作供氧剂。
25. 填空。
(1)128g铜的物质的量是_______ml。
(2)等质量的O2和O3所含的原子个数之比是_______。
(3)44gCO2气体在标准状态下体积是_______L。
(4)配制500mL1.0ml/LH2SO4溶液,需要18ml/LH2SO4溶液的体积为_______mL。
【答案】(1)2 (2)1:1
(3)22.4 (4)27.8
【解析】
【小问1详解】
128g铜的物质的量是。
【小问2详解】
O2和O3虽然分子不同,但均是氧元素的单质,等质量的O2和O3所含的原子质量相等,则原子个数之比是1:1。
【小问3详解】
44g CO2气体在标准状态下的体积是。
【小问4详解】
稀释时溶质的物质的量不变,则配制500mL1.0ml/LH2SO4溶液,需要18ml/LH2SO4溶液的体积为。
相关试卷
浙江省衢州六校联盟2024~2025学年高一(上)期中联考化学试卷(含答案):
这是一份浙江省衢州六校联盟2024~2025学年高一(上)期中联考化学试卷(含答案),共1页。
浙江省衢州六校联盟2024-2025学年高一上学期 期中联考化学试题:
这是一份浙江省衢州六校联盟2024-2025学年高一上学期 期中联考化学试题,文件包含高一化学试卷docx、高一化学试卷pdf、高一化学答题纸docx、高一化学答题纸pdf、高一化学试卷答案docx、高一化学试卷答案pdf等6份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。
浙江省衢州六校联盟2024-2025学年高一上学期 期中联考化学试题:
这是一份浙江省衢州六校联盟2024-2025学年高一上学期 期中联考化学试题,文件包含高一化学试卷docx、高一化学试卷pdf、高一化学答题纸docx、高一化学答题纸pdf、高一化学试卷答案docx、高一化学试卷答案pdf等6份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。








