


云南省保山市智源高级中学2024-2025学年高一上学期11月期中考试 化学试题
展开
这是一份云南省保山市智源高级中学2024-2025学年高一上学期11月期中考试 化学试题,文件包含云南省保山市智源高级中学2024-2025学年高一上学期11月期中化学试卷docx、云南省保山市智源高级中学2024-2025学年高一上学期11月期中化学答案docx、云南省保山市智源高级中学2024-2025学年高一上学期11月期中化学答题卡pdf等3份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
(考试时间75分钟 满分100分)
命题人:吴文超 审题人:杨希望
注意事项:
1.答题前,考生先将自己的姓名、准考证号码填写清楚。
2.选择题必须使用2B铅笔填涂在答题卡对应题目;非选择题必须用黑色字迹的签字笔填写在答题卡,字体工整,在试卷上作答无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 Mn-55 Cu-64 S-32
第Ⅰ卷 选择题
一、选择题(3分每题,共42分,每题只有一个正确选项,请选出最佳选项)
1.我国传统文化源远流长。对下列古文或诗词的解读错误的是( )
A.“野火烧不尽”涉及氧化还原反应
B.“曾青得铁则为铜”过程发生了复分解反应
C.“日照澄洲江雾开,淘金女伴满江隈”涉及丁达尔效应
D.“方以类聚,物以群分”表达了对于世界体系的分类概念
2.下列生活中的物质与其有效成分的化学式、用途的对应关系中,不正确的是( )
A.AB.BC.CD.D
3.下列各组中的离子,能在溶液中大量共存的是( )
A.H+、Ca2+、Cl−、CO32−B.Na+、Mg2+、SO42−、OH−
C.K+、Na+、OH−、Cl−D.Cu2+、Ba2+、Cl−、SO42−
4.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.常温常压下,16gO2和16gO3中所含氧原子的数目均为NA
B.标准状况下,11.2LH2O中所含氢原子的数目为NA
C.0.5ml/LMgCl2溶液中所含Cl-的数目为NA
D.1L 1ml/L KOH溶液中含氧原子数目为1NA
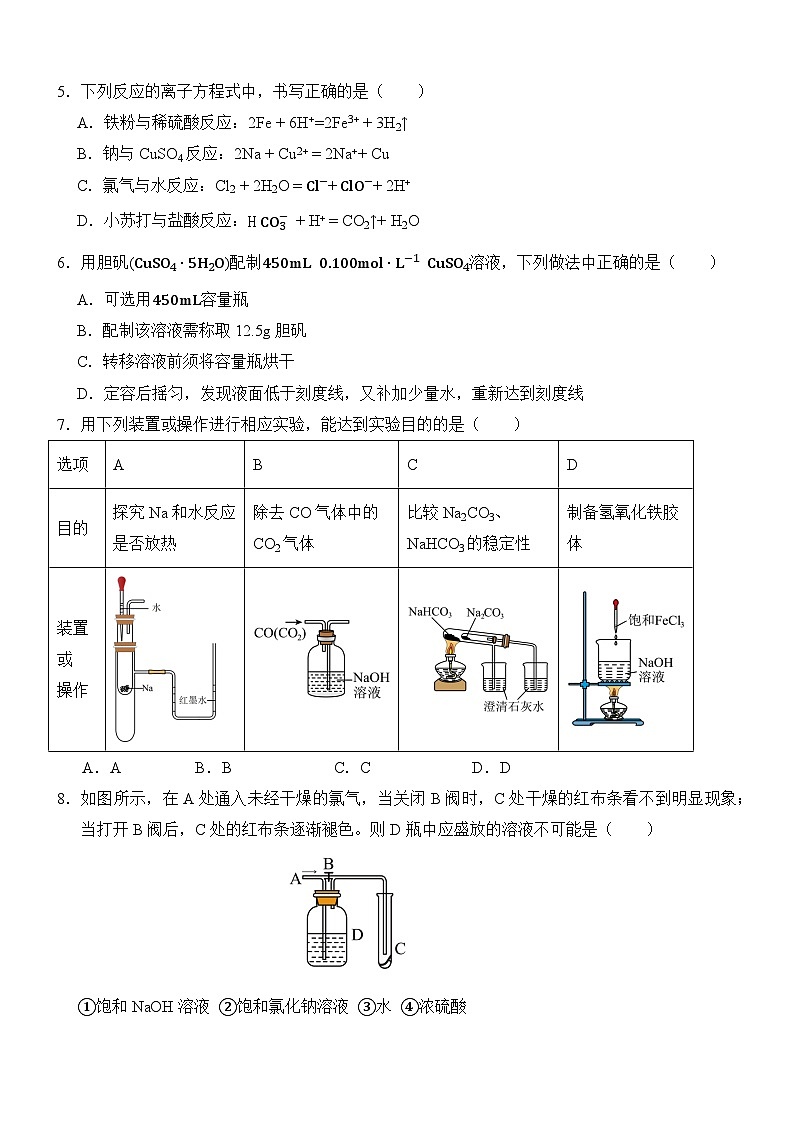
5.下列反应的离子方程式中,书写正确的是( )
A.铁粉与稀硫酸反应:2Fe + 6H+=2Fe3+ + 3H2↑
B.钠与CuSO4反应:2Na + Cu2+ = 2Na++ Cu
C.氯气与水反应:Cl2 + 2H2O = Cl−+ ClO−+ 2H+
D.小苏打与盐酸反应:HCO3− + H+ = CO2↑+ H2O
6.用胆矾(CuSO4⋅5H2O)配制450mL 0.100ml⋅L−1 CuSO4溶液,下列做法中正确的是( )
A.可选用450mL容量瓶
B.配制该溶液需称取12.5g胆矾
C.转移溶液前须将容量瓶烘干
D.定容后摇匀,发现液面低于刻度线,又补加少量水,重新达到刻度线
7.用下列装置或操作进行相应实验,能达到实验目的的是( )
A.AB.BC.CD.D
8.如图所示,在A处通入未经干燥的氯气,当关闭B阀时,C处干燥的红布条看不到明显现象;当打开B阀后,C处的红布条逐渐褪色。则D瓶中应盛放的溶液不可能是( )
①饱和NaOH溶液 ②饱和氯化钠溶液 ③水 ④浓硫酸
A.①④B.①③C.②③D.②④
9.常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br- ②2Br-+Cl2=Br2+2Cl- ③2Fe3++2I-=2Fe2++I2。由此判断下列说法错误的是( )
A.氧化性强弱顺序为:Cl2>Br2>Fe3+>I2
B.①中当有1mlBr2被还原时,反应转移2ml电子
C.③中当有1mlFe3+被还原时,可生成0.5ml氧化产物
D.Br2+2I-= I2+2Br-不能反应
10.下列有关氯及其化合物的说法不正确的是( )
A.常温下氯气与铁不反应,可以用钢瓶储运液氯
B.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状
C.漂白粉在空气中长时间放置,最终固体产物中存在CaCO3
D.含146g HCl的浓盐酸与足量的MnO2共热,能收集到71g氯气
11.下列有关Na、Na2CO3与NaHCO3叙述中错误的是( )
A.金属钠和氧气反应,条件不同,产物则不同
B.由于钠比较活泼,所以它能从盐溶液中置换出金属活动性顺序中钠后面的金属
C.相同状况下,等质量的NaHCO3和Na2CO3分别与足量盐酸反应,Na2CO3产生的CO2气体体积小于NaHCO3
D.NaHCO3溶液中混有少量Na2CO3杂质,可通入CO2除去
12.实验室惜助电导率传感器研究溶液中离子反应的实质。将电导率传感器插入滴有酚酞的一定体积、一定浓度的Ba(OH)2溶液中,匀速逐滴加入与Ba(OH)2溶液等浓度的H2SO4溶液,测得混合溶液的导电能力随时间的变化曲线如图所示。下列说法不正确的是( )
A.实验中观察到溶液中立即产生白色沉淀,同时溶液由红色逐渐变为无色
B.AB段反应的离子方程式为Ba2++OH−+H++SO42−=BaSO4↓+H2O
C.B点时导电能力最低说明H2SO4和Ba(OH)2恰好完全反应
D.BC段导电能力不断增强,主要是由于过量的H2SO4电离的离子导电
13.三颈烧瓶内盛放氯水,将pH传感器、氯离子传感器、氧气传感器分别插入三颈烧瓶中(图1),用强光照射氯水,进行实验并采集数据,获得相关变化曲线(如图2、3所示)。下列说法正确的是( )
A.由图1、2、3可验证HClO见光分解的产物
B.由图3可推知光照可催化水分解,产生氧气
C.由图2可推知cCl−增大的主要原因是Cl2在强光照下逐渐被氧化为Cl−
D.随着强光照射氯水,氯水的pH值增大
14.120℃时,将1.6g由CO2、H2O组成的混合气体通入盛有足量Na2O2的密闭容器中,充分反应后容器中残留的固体比反应前增重0.64g。下列说法错误的是( )
A.反应过程中生成O2的质量为0.96g B.1.6g该混合气体的总物质的量为0.06ml
C.该混合气体中CO2的质量分数为33% D.该混合气体中氧原子的物质的量为0.08ml
第II卷 非选择题
二、填空题(本题共4个题,共58分)
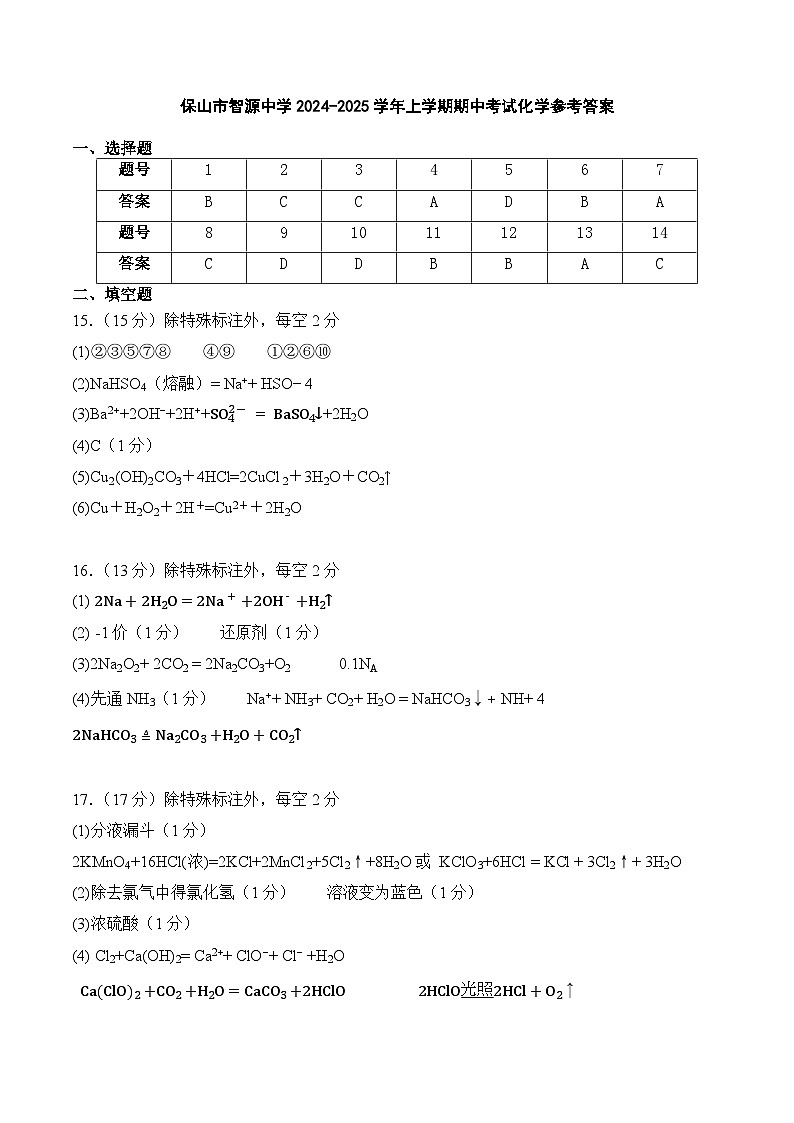
15.(15分)据题意回答下列问题。
Ⅰ 下列物质:①Cu ②熔融KCl ③NaHSO4 ④CO2 ⑤BaSO4 ⑥盐酸 ⑦NaHCO3 ⑧Ba(OH)2 ⑨C2H5OH ⑩NaCl溶液。
(1)属于电解质的是 (填序号,下同),属于非电解的是 ,能导电的是 。
(2)写出③在熔融状态的电离方程式: 。
(3)写出NaHSO4溶液中滴加Ba(OH)2 溶液至恰好呈中性时的离子反应方程式:
。
Ⅱ 下图为出土于昌宁县战国时期万家坝型铜鼓,是保山市博物馆镇馆之宝之一。流行于春秋至战国早期,是古代西南少数民族权利和财富的象征,是召集部族征战、祭祀的重器。由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为Cu2(OH)2CO3,“铜绿”难溶于水,能跟酸反应生成相应的铜盐。
(4)从物质分类标准看,“铜绿”属于 (填字母)。
A.酸B.碱C.盐D.氧化物
(5)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去。试写出用盐酸除去铜绿而不损伤器物的反应的化学反应方程式 。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为 。
16.(13分)物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
(1)物质①与水反应的离子方程式为 。
(2)从核心元素价态的视角看,NaH中H元素的化合价为 ,从H元素的价态分析,NaH常用作 (填“氧化剂”或“还原剂”)。
(2)淡黄色固体②常做潜水艇或呼吸面具的供氧剂,写出淡黄色固体②与二氧化碳反应的化学方程式: 。每消耗7.8g的淡黄色固体转移电子数为 。
(3) 我国制碱工业先驱侯德榜先生改进西方制碱工艺并发明了侯氏制碱法,使氯化钠的利用率大大提高,为纯碱和氮肥工业发展做出了杰出贡献。某学习小组在实验室模拟侯氏制碱法:第一步:向饱和NaCl溶液中通入CO2和NH3的顺序为 (选填“先通CO2”、“先通NH3”或“同时通入”) ,该过程中所涉及的离子反应方程为:
。第二步:将过滤所得固体受热分解得到纯碱,该发生反应的化学方程式: 。
17.(16分)某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如图装置进行实验
(1)盛有浓盐酸的仪器名称为 ,实验室制取氯气除用图中方法外,也能用KMnO4或KClO3与浓盐酸反应,请写出其中一种的化学反应方程 。
(2)饱和食盐水的作用为 ,淀粉碘化钾溶液中观察到的现象为 。
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放 。
(4)Cl2与石灰乳反应制取漂白粉的离子反应方程式为 ;漂白粉应密封避光保存,原因为 、 (用化学方程式解释)。
(5)用下列两种方法制取氯气,则所得氯气 。
①用含氯化氢146克的浓盐酸与足量的二氧化锰反应
②用87克二氧化锰与足量的浓盐酸反应
A.②比①多 B.①比②多 C.一样多 D.无法比较
(6)工业上可用氢氧化钠与氯气反应制取84消毒液,在生活中84消毒液不可与洁厕灵混用,其原因是 (用离子方程式解释)。
(7)将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时反应的离子方程式为 。
18.(14分)我校某化学兴趣小组发现有一瓶无色澄清透明溶液,已知其只含下列离子中的若干种,且每种离子的数目相等:K+、Na+、Ba2+、CO32−、Cl−、MnO4−、OH−、NO3−、Ag+,分别取100ml溶液进行以下4组实验:
①向其中加入过量盐酸,滴加过程中均无气泡和沉淀生成。
②用pH试纸检测溶液呈碱性。
③做焰色试验,发现火焰呈黄色。
④加入足量Na2SO4溶液,产生白色沉淀。
(1)由步骤①可以判断一定不存在的离子有 。
(2)由以上实验操作能够判断的阳离子一定有 ,根据电中性原则能否确定含有Cl−, (填“能”或“否”),请设计实验检验Cl−: ,书写检验Cl−的离子方程式: 。
(3)取实验①的酸性溶液加入铜片,产生气泡,经测定该气体为NO,溶液变蓝,请写出该反应的离子方程式: 。
(4)电荷守恒是学习化学的重要思维方法。某Al2SO43、H2SO4混合溶液中含有Al3+、SO42−物质的量分别为0.4ml、0.9ml,求溶液中H+的物质的量为 ml。选项
A
B
C
D
生活中的物质
小苏打
复方氢氧化铝
84消毒液
食盐
有效成分中的化学式
NaHCO3
Al(OH)3
Ca(ClO)2
NaCl
用途
做发酵粉
做抗酸药
做消毒剂
做调味品
选项
A
B
C
D
目的
探究Na和水反应是否放热
除去CO气体中的CO2气体
比较Na2CO3、NaHCO3的稳定性
制备氢氧化铁胶体
装置或
操作
相关试卷
这是一份云南省会泽县茚旺高级中学2024-2025学年高一上学期期中考试 化学试题(无答案),共6页。试卷主要包含了满分100分,考试时间75分钟,本卷命题范围,反应可用于检测氯气管道是否泄漏,下列离子方程式正确的是,自然界中氮的循环如图所示,设阿伏加德罗常数的值为等内容,欢迎下载使用。
这是一份[化学]云南省保山市智源高级中学2024~2025学年高一上学期10月第一次月考试题(有答案),共9页。
这是一份[化学]云南省保山市智源高级中学2024~2025学年高二上学期10月第一次月考试题(有答案),共10页。





![[化学]云南省保山市智源高级中化学2023-2024学年高一下学期化学期中考试试题](http://jx-previews-01.oss-cn-hangzhou.aliyuncs.com/3/7/15871311/0-1718663751542/0.jpg?x-oss-process=image/resize,w_202)



