


天津市南开中学2024-2025学年高一上学期10月月考化学试题(含答案)
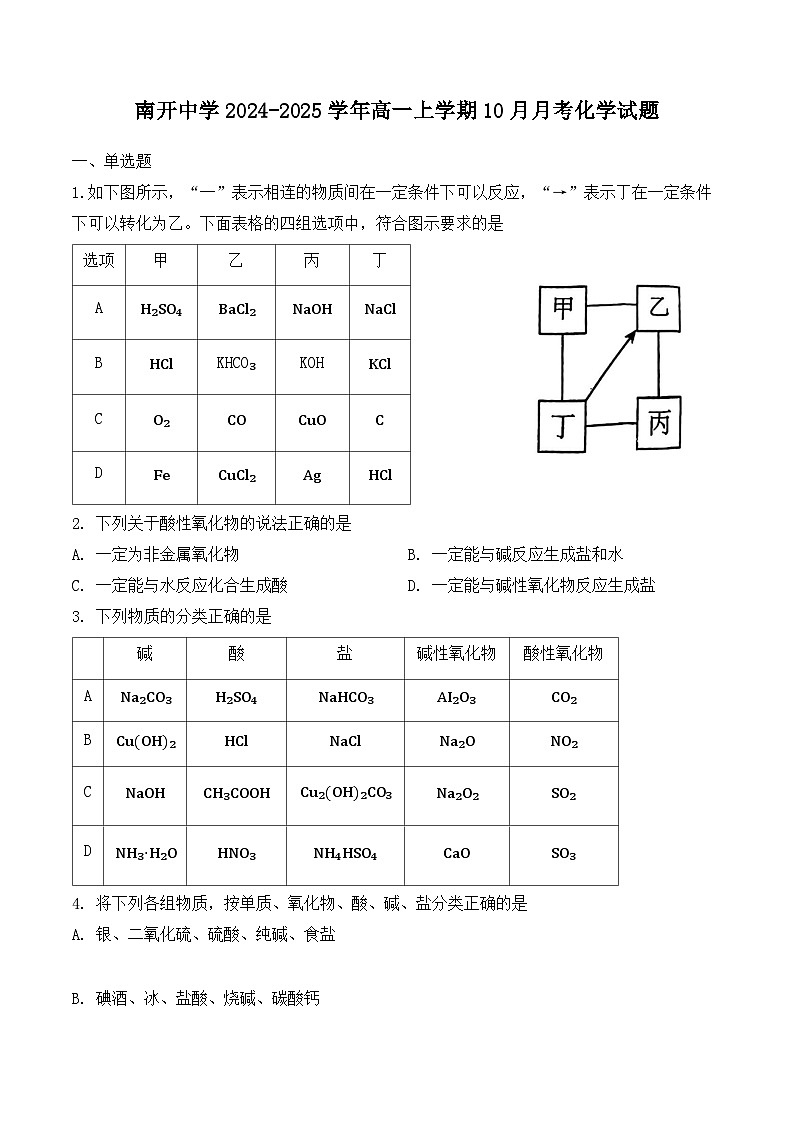
展开1.如下图所示,“一”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙。下面表格的四组选项中,符合图示要求的是
2. 下列关于酸性氧化物的说法正确的是
A. 一定为非金属氧化物 B. 一定能与碱反应生成盐和水
C. 一定能与水反应化合生成酸 D. 一定能与碱性氧化物反应生成盐
3. 下列物质的分类正确的是
4. 将下列各组物质,按单质、氧化物、酸、碱、盐分类正确的是
A. 银、二氧化硫、硫酸、纯碱、食盐
B. 碘酒、冰、盐酸、烧碱、碳酸钙
C. 氢气、干冰、硝酸、火碱、胆矾
D. 水银、氧化铜、醋酸、石灰乳、碳酸氢钠
5. 下列说法错误的是
A. 图1表示干燥的NaCl固体不导电,分析其原因是 Na⁺、Cl⁻这些离子不能自由移动
B. 图2表示熔融的NaCl能导电,分析其原因是随温度升高,离子运动加快,克服了离子间的互作用,产生了自由移动的离子
C. 图3表示 NaCl溶液能导电,分析其原因是在水分子的作用下NaCl 电离出了自由移动的离子
D. 图2和图3 说明NaCl固体溶于水和受热熔化时,均发生了电离,产生了完全相同的离子
6. 下列说法中,不正确的是
A. 氨气溶于水后能导电,所以氨水是电解质
B. HCl溶于水能导电,所以HCl是电解质
C. 酒精在水溶液和熔融状态下都不能导电,所以酒精是非电解质
D. 铁能导电,但铁既不是电解质也不是非电解质
7. 下列关于电解质的叙述,正确的是
A. 强电解质溶液的导电性比弱电解质溶液强
B. CO₂的水溶液可以导电,所以CO₂为电解质
C. 固体氯化钠不导电,但氯化钠是电解质
D, CaCO₃水溶液不导电, 所以CaCO₃是非电解质
8. 下列关于电解质与非电解质的说法正确的是
A. 电解质指在水溶液中或熔融状态下能导电的物质
B. 电解质一定能导电,能导电的物质一定属于电解质
C. BaSO₄难溶于水且不导电,所以 BaSO₄是非电解质
D. SO₃溶于水形成的溶液能导电,但 SO₃是非电解质
9. 某学生利用如图装置对电解质溶液导电性进行实验探究。下列说法正确的是
A. 闭合开关K,电流表指针发生偏转,证明盐酸是电解质
B. 闭合开关K, 向烧杯中加入NaCl固体, 由于HCl 与NaCl不反应,故电流表指针不发生变化
C. 闭合开关K,向溶液中加入CaCO₃固体,电流表示数几乎不变
D. 选取相同浓度的硫酸替换盐酸,电流表的示数相同
10. 下列各组离子能大量共存且澄清透明的是
A. Na⁺、MnO;、K⁺、NO₃ B.Na⁺、S²⁻、H⁺、Cl−
C. Ba²⁺、OH⁻、K⁺、NH₄⁺ D.HCO3−H+、Na+、Ca2+
11. 某白色粉末可能含有 Ba(NO₃)₂、CaCl₂、K₂CO₃, 进行如下实验: ①将少量粉末加入水中, 振荡,有白色沉淀生成; ②向①的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生; ③取少量②的溶液,滴入AgNO₃溶液,有白色沉淀生成,依据实验现象,下列关于白色粉末的判断正
A. 只含有K₂CO₃
B. 一定含有 K₂CO₃, 还含有 CaCl₂和Ba(NO₃)₂ 中的一种
C. 一定含有 K₂CO₃和 CaCl₂, 可能含有 Ba(NO₃)₂
D. 一定含有K₂CO₃、CaCl₂和 Ba(NO₃)₂
12. 下列各组物质的分类正确的是
①氯水、氨水、碱石灰、波尔多液、医用酒精均属于混合物
③含有氧元素的化合物叫氧化物
③非金属氧化物为酸性氧化物,金属氧化物为碱性氧化物
④根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
⑤强电解质溶液的导电能力一定强
⑥盐酸属于混合物,而液氯、醋酸均属于纯净物
⑦电解质熔融时均可以导电
⑧能电离出H⁺的纯净物属于酸
全部正确 B. ①②⑤⑦ ②③⑥⑧ D. ①⑥
13. 下列叙述正确的是
A. 煮沸 FeCl₃饱和溶液可以制得 FcOkl₃胶体
B. 明矾溶于水生成的胶体具有吸附性,可以用作净水剂
C. FeCl₃溶液和 Fe(OH)₃胶体都呈透明的红褐色
D. FeCl₃溶液是电中性的, FeOH₃胶体是带电的
14. 某无色溶液中只可能含有 K+、Ag+、Bi2+、Cu2+、Cl−、CO32−、SO42−中的一种或几种,对其进行如下实验操作:
①另取少量溶液,加入足量 BaCl₂溶液,产生白色沉淀;
②向①所得混合物中加足量盐酸,沉淀部分溶解,并有气泡生成;
③将②所得混合物过滤,向滤液中加入. AgNO₃溶液,有白色沉淀生成。
下列对该溶液的说法正确的是
A. 一定含有 K+、CO32−、SO42− B. 可能含有 K⁺、Cl⁻
C. 一定不含有 Cu²⁺、K⁺、Ag⁺、Ba²⁺ D. 可能含有 Cu2+、SO42−
15. 下列离子方程式书写正确的是
A. 将氨水滴入FeCl₃溶液中: Fe³⁺+3OH⁻=FeOH₃↓
B. 烧碱与小苏打溶液混合反应: HCO3−+OH−=H2O+CO32−
C. 向FeCl₃溶液中加入铜粉: Cu²⁺+Fe³⁺=Fe²⁺+Cu²⁺
D. 向 H₂SO₄溶液中加入铁粉: 2Fe+3H⁺=2Fe³⁺+3H₂↑
16. 下列关于分散系的说法正确的是
A. 光束通过 NaCl溶液时,可以看到一条光亮的“通路”
B. 溶液、胶体、浊液的本质区别是能否产生丁达尔效应
C. 按照分散剂的不同,胶体可分为液溶胶、气溶胶和固溶胶
D. 将铝片粉碎到直径为1~100mm的铝粉时,该铝粉属于胶体
17、已知物质在纳米级时因微粒大小不同而具有不同的颜色、性质,故在医疗、科技等多个领域有重大意义。下列说法正确的是
A. 葡萄糖溶液的分散质直径在1~10nm
B. 根据分散质粒子直径大小,可以用滤纸分离溶液和胶体
C. 利用丁达尔效应可以鉴别 Fe(OH)₃胶体和氯化钠溶液
A . 科学家研究过程中制得了直径为4.5nm的硫化镉,这种硫化镉是胶体
18. 室温下,下列各组离子在指定溶液中能大量共存的是
A. 滴入酚酞变红色的溶液: K+、Ca2+、HCO3−、CO32−
⋅L⁻¹Fe₂SO₄₃溶液: Cu2+、NH4+、NO3−、SO42−
C. pH=1的溶液: Ba2+、K+、CH3COO−、NO3−
D. 无色透明的溶液: Cu2−、Na+、SO42−、NO3−
19. 分类是化学研究中常用的方法。下列分类方法正确的是
A..漂白粉、氢氧化铁胶体、冰水混合物、氯水、赤铁矿都属于混合物
B. 已知次磷酸H₃PO₂与足量的NaOH反应只能生成一种盐 NaH₂PO₂,则该盐为正盐
C. NO₂溶于氢氧化钠可以发生 2HO₂+2NaOH=NaNO₃+NaNO₂+H₂O, 故 NO₂为酸性氧化物
D. SO₂溶于水能导电,故SO₂属于电解质
20. 下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是
A.CuOH₂和盐酸; Cu(OH)₂和CH₃COOH
B. BaCl₂和 Na₂SO₄; Ba(OH)₂和 CuSO₄
C.NaHCO₃和NaHSO₄; Na₂CO₃和 NaHSO₄
D. NaHCO₃(过量)和 CaOH₂;CaHCO₃₂和NaOH(过量)
21. 下列离子方程式正确的是
A. 用醋酸除水垢: CaCO₃+2H⁺=Ca²⁺+H₂O+CO₂↑
B. 用小苏打治疗胃酸过多: HCO3−+H+=CO2↑+H2O
C. 钠与水反应: Na+2H₂O=Na⁺+2OH⁻+H₂↑
D. 向氢氧化钠溶液中通入过量二氧化碳: 2OH−+CO2=CO32−+H2O
22. 两种溶液相互滴加,反应过程中现象相同但离子方程式不同的是
A.CaHCO₃₂溶液与NaOH 溶液 B.Na₂CO₃溶液与稀盐酸
C. H₂SO₄溶液与 Ba(OH)₂溶液 D. MgCl₂ 溶液与NaOH 溶液
23. 在两份相同的 BaOH₂溶液中,分别滴入物质的量浓度相等的 H₂SO₄、NaHBO₄溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列说法正确的是
A. ①代表滴加 NaHSO₄溶液的变化曲线
D、a处溶液的导电能力几乎为0,所以BaSO₄是非电解质
C. c点两溶液中: SO42−的物质的量关系:①>②
D. b~d的离子方程式为 H⁺+OH⁻=H₂O
24. 某地区的雾霾中可能含有 Na+、Bc2+、Mg2τ,Fe3+,SO42−,Cl、CO32−、HCO3−等离子。某同学收集雾霾样品,经必要的预处理配成试样溶液,设计如下实验探究其中含有的离子。
①取一定体积的溶液,加入足量 BaCl₂溶液,产生白色沉淀,继续滴加足量盐酸,沉淀不溶解,同时得到无色气体。
②另取一定体积的溶液,加入足量NaOH 溶液,产生白色沉淀,继续滴加足量稀盐酸,沉淀全部溶解。
下列判断不正确的是
A. 操作①中产生的无色气体为CO₂ B. 可能含有 Na+、CO32−
C. 肯定含有 Mg2+、SO42−、HCO3− D. 一定不存在 Ba²⁺、Fe³⁺、CO32−
25. NaOH和 CaOH₂的混合液中Na⁺和Ca²⁺的数目相等. 向混合溶液中通入一定量 CO₂。下列离子方程式与事实不相符的是
A.OH−+CO2→HCO3−
B.2OH−+CO2→CO32−+H2O
C.Ca2++2OH−+CO2→CaCO3↓+H2O
D.Ca2++3OH−+2CO2→CaCO3↓+HCO3−+H20
二、填空题
26. 有以下几种物质: ①食盐晶体; ②Fe; ③蔗糖; ④酒精; ⑤醋酸晶体;⑥BaSO₄;⑦盐酸;⑧熔融的 Na₂O, ⑨干冰; ⑩氨水。填空回答(填序号):
(1)以上物质可以导电的是
(2)以上物质中属于电解质的是 ;
(3)以上物质中属于非电解质的是 。
27. Ⅰ.现有下列9种物质:
①金属钠; ②CO₂; ③稀盐酸; ④小苏打晶体; ⑤熔融NaCl; ⑥NaOH固体;⑦BaOH₂溶液;⑧苏打粉末; ⑨乙醇
(1)其中属电解质的是 (填序号,下同),能导电的是
(2)上述物质中少量②与⑦发生反应的离子方程式为 。
(3)上述物质中少量④的溶液与⑦发生反应的离子方程式为 。上述物质中④溶于水时主要发生的电离方程式 。
II.今有一混合物的水溶液,初步确定只可能含有下列离子中的若干种: K+、NH4+、Cl−、Ca2+、 Ba2+、CO32−、SO42−,且含有的各离子的个数相等。
现取三份该溶液各 100mL 进行如下实验:
①第一份溶液中,滴加AgNO₃溶液,有沉淀产生:
②第二份溶液中,加入足量NaOH 浓溶液共热,有无色气体生成:
③第三份溶液中,加入足量BaCl₂溶液后,得到白色沉淀,加入足量的稀盐酸,沉淀全部溶解。根据上述实验,回答以下问题:
(4)请写出第三份溶液中,沉淀溶解的离子方程式:
(5)综合上述实验结果,关于该混合物的组成,依认为以下说法正确的是 (填标号)。
A. 一定有 NH4+、CO32−,一定没有Cl⁻ B. 一定有K⁺,一定没有 SO42−,可能有Cl⁻
C. 一定没有Ca²⁺、Ba²⁺,可能有K⁺,Cl⁻ D. 一定有 NH4+、SO42−、Cl⁻,可能有Ca²⁺、K⁺
28. 有三种物质A、B、C,其中一种是碱,其余两种是盐。它们均可溶于水,电离只产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A 溶液与B溶液反应生成无色气体 X,气体X 可以与C溶液反应生成沉淀 E,沉淀 E 可与B 溶
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请回答下列问题:
(1)X (填“是”或“不是”)电解质。
(2)C在水中的电离方程式为 。
(3)写出以下水溶液中反应的离子方程式。
①A 溶液与B 溶液反应生成无色气体X: 。
②B 溶液与C溶液反应至溶液呈中性:
③X与C 溶液反应生成沉淀E:
四、离子方程式的书写
29. 氧化镁和醋酸溶液的反应
30.二氧化硫和氢氧化钠溶液的反应
31.氨水和醋酸反应
32.硫酸氢钠溶液和氢氧化镁反应
33.碳酸氢钠溶液和氢氧化钠溶液混合
34.碳酸氢钠溶液与醋酸溶液混合
35.醋酸钠溶液与足量稀盐酸
36.氯化铵和氢氧化钡溶液反应
37.硫酸氢铵和足量氢氧化钡溶液反应
38.硫酸亚铁铵 NH₄₂FeSO₄₂]溶液与足量澄清石灰水的反应选项
甲
乙
丙
丁
A
H₂SO₄
BaCl₂
NaOH
NaCl
B
HCl
KHCO₃
KOH
KCl
C
O₂
CO
CuO
C
D
Fe
CuCl₂
Ag
HCl
碱
酸
盐
碱性氧化物
酸性氧化物
A
Na₂CO₃
H₂SO₄
NaHCO₃
AI₂O₃
CO₂
B
Cu(OH)₂
HCl
NaCl
Na₂O
NO₂
C
NaOH
CH₃COOH
Cu₂(OH)₂CO₃
Na₂O₂
SO₂
D
NH₃·H₂O
HNO₃
NH₄HSO₄
CaO
SO₃
阳离子
Na⁺、H`、Ba2⁺
阴离子
OH⁻、CO³⁻、s²⁻
天津市南开中学2024-2025学年高三上学期10月月考 化学试题: 这是一份天津市南开中学2024-2025学年高三上学期10月月考 化学试题,共7页。试卷主要包含了 下列常见物质及用途,错误的是,下列叙述正确的是, 过量 SO₂与以下 0等内容,欢迎下载使用。
重庆市南开中学校2024-2025学年高一上学期开学考试化学试题: 这是一份重庆市南开中学校2024-2025学年高一上学期开学考试化学试题,共2页。
天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题(含答案解析): 这是一份天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题(含答案解析),文件包含精品解析天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题原卷版docx、精品解析天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题解析版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。












