

河南省开封市河南大学附属中学2024-2025学年高二上学期10月月考化学试题
展开
这是一份河南省开封市河南大学附属中学2024-2025学年高二上学期10月月考化学试题,共9页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
一、单选题(每题3分,共42分)
1.“极地破冰”“太空养鱼”等彰显了我国科技发展的巨大成就。下列说法正确的是()
A.“雪龙2”号破冰船极地科考:破冰过程中水发生了化学变化
B.大型液化天然气运输船成功建造:天然气液化过程中形成了新的化学键
C.嫦娥六号运载火箭的助推器采用液氧煤油发动机:燃烧时化学能转化成热能
D.神州十八号乘组带着水和斑马鱼进入空间站进行科学实验:水的电子式为H:O:H
2.下列说法正确的是
A.已知:,则碳的燃烧热
B.已知:C(石墨,s)=C(金刚石,s),则石墨比金刚石稳定
C.已知:;,则
D.已知:,则
3.酸碱中和反应是典型的放热反应,在测定中和热的实验中,下列叙述正确的是()
A.将50mL0.55ml/LNaOH溶液与50mL0.50ml/L盐酸改为50mL0.65ml/LNaOH
溶液与50mL0.60ml/L盐酸,所得中和热的数值保持不变
B.测定中和反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度
C.测盐酸溶液温度的温度计未洗涤立马测氢氧化钠溶液温度,会使得偏小
D.实验中可使用相同浓度的氨水替代氢氧化钠溶液
4.一定条件,水煤气变换反应:,下列说法错误的是()
A.增大CO浓度,使单位体积内活化分子数增多,可加快反应速率
B.升高温度,活化分子百分数增大,加快反应速率
C.适当压缩容积,单位体积内活化分子数增大,加快反应速率
D.催化剂降低反应活化能,活化分子百分数增大,反应速率及平衡转化率都增大
5.N2O5是一种新型硝化剂,在T1温度下可发生下列反应:。温度下的平衡常数为。下列说法错误的是()
A.反应的B.该反应在高温下可自发进行
C.温度下的平衡常数为,温度下的平衡常数为,若,则
D.温度下,在体积为1L的恒温密闭容器中充入2mlN2O5,4mlNO2,1mlO2,此时反应将向正反应方向进行
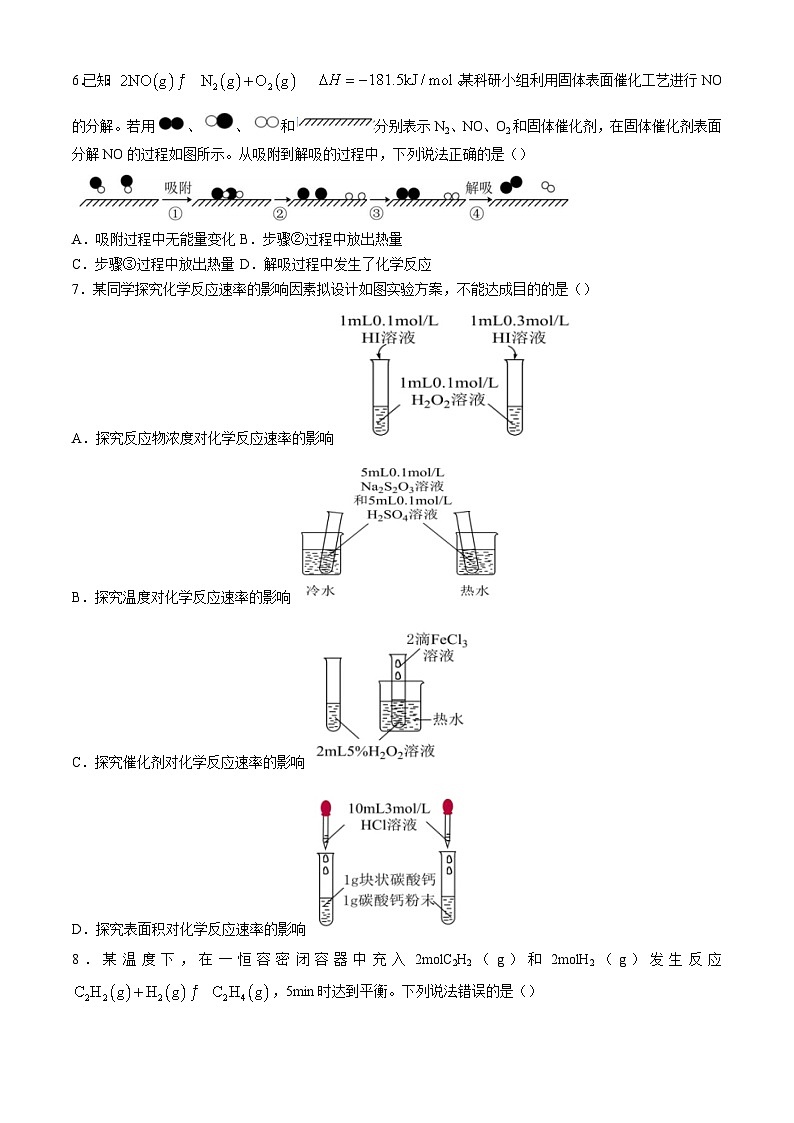
6.已知:。某科研小组利用固体表面催化工艺进行NO的分解。若用、、和分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,下列说法正确的是()
A.吸附过程中无能量变化B.步骤②过程中放出热量
C.步骤③过程中放出热量D.解吸过程中发生了化学反应
7.某同学探究化学反应速率的影响因素拟设计如图实验方案,不能达成目的的是()
A.探究反应物浓度对化学反应速率的影响
B.探究温度对化学反应速率的影响
C.探究催化剂对化学反应速率的影响
D.探究表面积对化学反应速率的影响
8.某温度下,在一恒容密闭容器中充入2mlC2H2(g)和2mlH2(g)发生反应,5min时达到平衡。下列说法错误的是()
A.若升高温度,体系达到平衡的时间小于5min
B.达到平衡时,气体的物质的量可能减小为原来的一半
C.加入催化剂可提高C2H2(g)的转化速率
D.反应开始至达到平衡时,体系的压强一直减小
9.H2O2可在催化剂Fe2O3或Fe3O4作用下产生OH,OH能将烟气中的NO、SO2氧化。OH产生机理如下:
慢反应:
快反应:
对于H2O2脱除,下列说法错误的是()
A.加入催化剂Fe2O3,可提高SO2的脱除速率
B.该反应能在低温下自发进行,则此反应的
C.向固定容积的反应体系中充入氦气,反应速率加快
D.与Fe2O3作催化剂相比,相同条件下Fe3O4作催化剂时SO2的脱除速率可能更高
10.探究温度、催化剂的比表面积对的化学反应速率的影响,设计了以下实验,下列说法不正确的是()
A.,
B.实验Ⅰ中,0~5min用O2表示的化学反应速率为
C.实验Ⅱ中,0~5min内SO2的转化率为75.0%
D.根据表中数据可推出:其他条件相同时,催化剂的比表面积越大,化学反应速率越大
11.二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应:
Ⅰ.
Ⅱ.
向容积为10L的密闭容器中投入262mlCH和23mlCO,不同温度下,测得5min时(反应均未平衡)的相关数据见下表,下列说法不正确的是()
注:乙烯选择性
A.反应活化能:ⅠⅠ
D.反应平衡常数K(Ⅱ)v逆
C.T℃时,该反应的平衡常数
D.向a点平衡体系中充入一定量的NO2(g),到达新平衡时,NO2(g)的转化率比原平衡小
14.向恒容密闭容器中通入物质的量浓度均为的CH4与CO2,一定条件下发生反应:。测得平衡时CH4的体积分数与温度及压强的关系如图1所示。为探究速率与浓度的关系,根据相关实验数据,粗略地绘制出了两条速率—浓度关系曲线:v正~c(CH4)和v逆~c(CO),如图2。
下列说法不正确的是()
图1
图2
A.压强为时,b点处v正v逆
B.
C.与曲线v正~c(CH4)相对应的是图2中曲线甲
D.降低温度,反应重新达到平衡时,v正、v逆相应的平衡点分别为B、F
二、解答题(共58分)
15.(15分)某化学小组在实验室中采用如图装置模拟用NH3还原法除去工业尾气中的NOx。
回答下列问题:
(1)盛放稀硝酸的仪器名称为______,实验过程中,为使稀硝酸顺利滴下,可对该仪器进行的操作是______。
(2)装置A中发生反应的化学方程式为______。
(3)浓氨水的作用____________。
(4)装置D中盛放试剂的名称为______。
(5)装置E中发生反应的化学方程式为______。
(6)装置F中浓硫酸的作用为______。
(7)写出氮氧化物对环境造成的一种危害:______。
16.(14分)氟硅酸钾(K2Si6F)常用于木材防腐和陶瓷制造,一种以石英砂和氢氟酸为原料制备氟硅酸钾的工艺流程如图所示。
回答下列问题:
(1)K2SiF6中Si元素的化合价为______。
(2)“还原1”中,发生反应的化学方程式为______。
(3)“还原2”中,发生反应的H2与SiHCl3的物质的量之比为______。
(4)“转化2”中发生反应的化学方程式为______。
(5)“沉淀”后,分离出K2SiF6的操作为______,该操作需要使用的玻璃仪器有______。
(6)该工艺中可循环使用的物质______(填化学式)。
(7)写出氢氟酸的一种用途:______。
17.(15分)H2S是一种有毒气体,利用H2S与CH4的反应可将其转化为有价值的H2、S2等。发生的反应有:
反应ⅰ:
反应ⅱ:
回答下列问题:
(1)已知相关化学键的键能如下表:
反应ⅰ:的______。
(2)一定温度下,在体积为2L的刚性容器中,充入1mlCH4和2mlH2S,发生反应ⅰ和反应ⅱ,5min时反应达到平衡,H2S的平衡转化率为40%,。
①下列叙述中能说明反应ⅱ达到平衡状态的是______(填字母)。
A.v正(CH4)=v逆(CS2)B.混合气体的密度不再变化
C.断裂1mlC-H的同时生成1mlC=SD.混合气体的平均摩尔质量不再变化
②0~5min内v(CS2)=______。
③此温度下,反应ⅱ的平衡常数Kx=______(Kx是以平衡物质的量分数代替平衡浓度计算的平衡常数)。
(3)在常压和不同温度下,将H2S和CH4按照2:1的体积比充入热解器中,用N2稀释,发生反应ⅰ和反应ⅱ。反应相同时间后,H2、S2和CS2的体积分数随温度的变化关系如图所示。
①______(填“>”“(2分)不能(1分)
②3.6%(2分)
③反应ⅰ正向进行的程度小于反应ⅱ正向移动的程度(2分)
18.(共14分)
(1)加成反应(2分)羟基(2分)
(2)HCOOCH2CH2CH3、HCOOCH(CH3)2和CH3CH2COOCH3(3分)
(3)(2分)
(4)(2分)分液漏斗(1分)
(5)BD(2分)编号
T(℃)
SO2初始浓度()
O2初始浓度()
催化剂的比表面积()
5min时SO2的浓度()
Ⅰ
450
82
Ⅱ
450
b
124
Ⅲ
500
a
82
温度(℃)
400
500
600
乙烷转化率(%)
2.2
9.0
17.8
乙烯选择性(%)
92.6
80.0
61.8
化学键
H—H
H—S
S2(化学键视为S—S)
键能/()
436
339
298
题号
1
2
3
4
5
6
7
8
9
10
答案
C
B
A
D
C
C
C
B
C
B
题号
11
12
13
14
答案
D
A
A
C
相关试卷
这是一份北京工业大学附属中学2024-2025学年高二上学期10月月考 化学试题(无答案),共12页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
这是一份北京理工大学附属中学2024-2025学年高二上学期10月月考化学试题,文件包含北京市海淀区北京理工大学附属中学高二化学10月月考pdf、北京市海淀区北京理工大学附属中学高二化学10月月考答案pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。
这是一份河南省开封市五县联考2023-2024学年高二上学期12月月考化学试题含答案,共22页。试卷主要包含了考试结束后,只需上交答题卷,下列说法正确的是,的稀溶液可作手术刀的消毒剂,下列说法中,错误的是等内容,欢迎下载使用。









