

还剩8页未读,
继续阅读
山东省济宁市邹城市第一中学2024-2025学年高二上学期10月月考化学试题(Word版附解析)
展开这是一份山东省济宁市邹城市第一中学2024-2025学年高二上学期10月月考化学试题(Word版附解析),共11页。试卷主要包含了10,25,2 kJ∙ml-1等内容,欢迎下载使用。
可能用到的相对原子质量:H_1 B_11 C_12 N_14 O_16 Na_23 Fe_56
第I卷 选择题(共40分)
单选题:本题共10小题,每小题2分,共20分。
1. 党的二十大提出要加快发展方式绿色转型,而氢能源作为一种绿色能源在日常生活中的应用越来越广泛。下列有关说法正确的是
A.研制新型催化剂,降低水分解时的ΔH是氢能发展的方向之一
B.已知氢在氯气中燃烧的热化学方程式为H2(g)+Cl2(g)=2HCl(g) ΔH=-285.8 kJ·ml-1,所以H2(g)的燃烧热是285.8kJ·ml-1
C.已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·ml-1,则氢气的燃烧热
ΔH<-241.8 kJ·ml-1
D.反应2H2O(g) =2H2(g)+O2(g) ΔH>0,则反应物的总键能小于生成物的总键能
2.热解H2S可以制H2。根据文献,将H2S和CH4的混合气体导入石英管反应器热解,发生如下反应:2H2S(g)+CH4(g) CS2 (g)+4H2(g) ,若将整个反应看成由反应 Ⅰ 和反应 Ⅱ 两步进行,反应过程能量如图所示,下列说法错误的是
A.2 ml H2S(g)的能量低于1 ml S2(g)和
2 ml H2(g)的能量
B.反应II决定了整个化学反应的速率
C.反应II的热化学方程式为
S2(g)+CH4(g) CS2 (g)+2H2(g)
ΔH2 = (E4-E3) kJ·ml-1
D.反应时,每生成4 ml H2,吸收的能量为(E1+E3-E2-E4) kJ
3.在一定温度下发生反应:2NO2(g)N2O4(g)△H<0,在密闭容器中达平衡后,改变下列条件达到新平衡后可使混合气体颜色加深的是
A.缩小容器的容积 B.保持温度压强不变,充入NO2(g)
C.降温 D.保持容器容积不变,充入氮气
4.在4 L密闭容器中充入5 ml A和5 ml B,在一定条件下发生反应:2A(g)+B(g)2C(s)+xD(g),5s达到平衡。达到平衡时,生成了2 ml C,经测定D的浓度为0.5 ml·L−1,下列判断正确的是
A.x=1 B.B的转化率为10%
C.用A表示的平均反应速率为0.1 ml·L−1·s−1
D.该条件下反应的平衡常数为2.25
5.2SO2+O22SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
A.大于p%B.等于p%C.小于p%D.无法判断
6.随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。以CO2和NH3为原料合成尿素的反应如下:2NH3(g)+CO2(g)CO(NH2)2(s)+H2O(g) ΔH=-87 KJ∙ml-1。一定温度下,将2 ml NH3和1 ml CO2充入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
7.在密闭容器中通入物质的量均为0.2 ml的CH4和CO2,在一定条件下发生反应CH4(g)+CO2(g)2CO(g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如下图所示。下列说法错误的是
A.该反应的逆反应为放热反应
B.P1 < P2
C.X点与Z点的平衡常数相等
D.若Y点所处的压强为P2,此时的
正反应速率大于逆反应速率
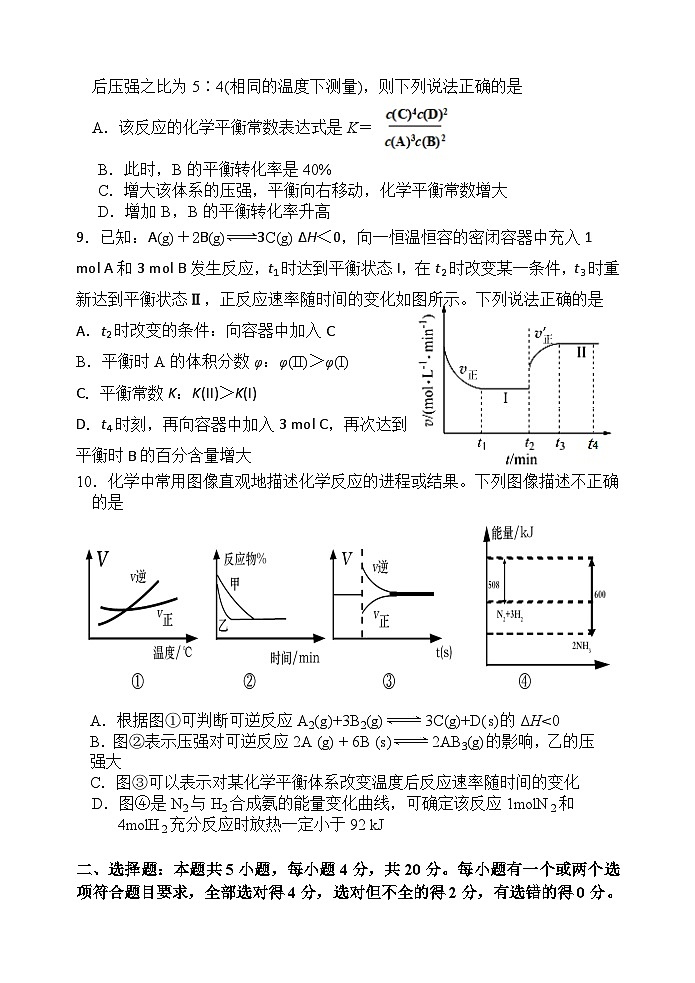
8.某温度下,在一个2 L的密闭容器中,加入4 ml A和2 ml B进行如下反应:3A(g)+2B(g)4C(s)+2D(g),反应一段时间后达到平衡,且反应的前后压强之比为5∶4(相同的温度下测量),则下列说法正确的是
A.该反应的化学平衡常数表达式是K=
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加B,B的平衡转化率升高
9.已知:A(g)+2B(g)3C(g) ΔH<0,向一恒温恒容的密闭容器中充入1 ml A和3 ml B发生反应,t1时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
A.t2时改变的条件:向容器中加入C
B.平衡时A的体积分数φ:φ(II)>φ(I)
C.平衡常数K:K(II)>K(I)
D.t4时刻,再向容器中加入3 ml C,再次达到
平衡时B的百分含量增大
10.化学中常用图像直观地描述化学反应的进程或结果。下列图像描述不正确的是
A.根据图①可判断可逆反应A2(g)+3B2(g)3C(g)+D(s)的ΔH<0
B.图②表示压强对可逆反应2A (g) + 6B (s)2AB3(g)的影响,乙的压强大
C.图③可以表示对某化学平衡体系改变温度后反应速率随时间的变化
D.图④是N2与H2合成氨的能量变化曲线,可确定该反应1mlN2和4mlH2充分反应时放热一定小于92 kJ
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 根据实验目的,下列实验及现象、结论都正确的是
12.一定温度下,向某容积可变的密闭容器中加入足量碳酸钙,发生反应CaCO3(s)⇌CaO(s)+CO2(g),并达到平衡。下列说法正确的是( )
A.保持容器容积不变,充入He,平衡向逆反应方向移动
B.将容器容积增大为原来的2倍,当体系再次达到平衡时,气体密度不变
C.增加CaCO3(s)的物质的量,平衡向正反应方向移动,CO2的浓度增大
D.将容器容积缩小为原来的 eq \f(1,2) ,当体系再次达到平衡时,CO2的浓度与原来相同
13.现有两个热化学方程式:
(l)+H2(g)―→(l) ΔH>0①
(l)+2H2(g)―→(l) ΔH<0②
下列说法正确的是( )
A.反应①②中都存在ΔS>0 B.反应②一定不能自发进行
C.在通常情况下,反应①②都能自发进行 D.反应②在低温时易自发进行
14.已知2A2(g)+B2(g)⇌2C3(g) ΔH=-Q1 kJ·ml-1(Q1>0)。在一个有催化剂、容积不变的密闭容器中加入2 ml A2和1 ml B2,在500 ℃时充分反应,达到平衡。改变某一条件,得到下图所示的变化规律(图中T表示温度,n表示物质的量),下列结论正确的是( )
A.反应速率:b>a> c
B.达到平衡时A2的转化率:b>a>c
C.T2>T1
D.b点对应的状态,A2和B2的起
始物质的量之比为2∶1
15.在某密闭容器中,反应aA(g)+bB(g)⇌cC(g)+dD(g)达到平衡时,B的浓度为0.6 ml·L-1,若保持温度不变,将容器的容积扩大到原来的4倍,达到新平衡时B的浓度降为0.2 ml·L-1。下列判断不正确的是( )
A、D的体积分数减小
B.达到新平衡时,A、B 的浓度减小,C、D的浓度增大
C.a+b
第Ⅱ卷 非选择题(共60分)
三、非选择题:本题共3小题,共60分
16.2021年我国打造了一台目前全球性能最先进的海上钻井平台“蓝鲸二号”,用于开采深埋在南海海底的特殊资源可燃冰,可燃冰主要成分为CH4。请回答下列问题:
(1)已知1g CH4完全燃烧生成二氧化碳和液态水放出的热量为55.625kJ,则CH4燃烧热的热化学方程式为 ;
N2与O2反应生成NO的过程如下:
则CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(l) △H=______kJ∙ml-1。
(2) CH4可用于生产合成气(CO和H2) 其反应的热化学方程式为
CH4(g)+H2O(g)CO(g)+3H2(g) △H= +206.2 kJ∙ml-1。
①恒温恒压条件下,向容器中加入2 ml CH4、2ml H2O(g)以及催化剂进行生产合成气,起始压强为p KPa,一段时间后达到平衡时,CH4的转化率是50%,其平衡常数Kp为_______(用各气体物质的分压替代浓度计算的平衡常数叫压强平衡常数KP,某气体的分压=气体总压强×该气体的物质的量分数)。保持其他反应条件不变,把恒压容器改为改成恒容容器,反应达平衡后吸收的热量较多的是_______(填“恒压” 或“恒容”)容器。可同时提高化学反应速率和CH4转化率的措施是 (写出一条即可)。
②在某一给定进料比的情况下,温度、压强对平衡时H2物质的量分数的影响如图所示。在相同温度下,CH4的转化率随压强的增大而______(填“增大”“减小”或“不变”),原因是 。若要达到H2的物质的量分数>65%,以下条件中最合适的是_____(填序号)。
a.600℃,0.1MPa b.600℃,0.9MPa c.700℃,0.9 MPa d.800℃,1.5MPa
17.二十大报告明确指出,协同推进降碳、减污、扩绿、增长,推进生态优先、节约集约、绿色低碳发展。工业上可用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
(1)△H2= (用 △H1、△H3来表示)
(2)b= 。500 ℃时测得反应②在某时刻CO(g)、H2O(g)、H2(g)、CO2(g)的浓度分别为0.3ml·L-1、0.2ml·L-1、0.1ml·L-1、0.15ml·L-1,则此时v正________v逆(填“>”、“=”或“<”)。
(3)在恒容的密闭容器中发生反应②,已知n(CO)—反应时间t的变化曲线 Ⅰ 如图1所示,若在t0时刻分别改变一个条件,曲线 Ⅰ 变为曲线 Ⅱ 和曲线 Ⅲ。当曲线 Ⅰ 变为曲线 Ⅱ 时,改变的条件是_______________。当曲线 Ⅰ 变为曲线 Ⅲ 时,改变的条件是______________。
(4)一定条件下,在容积为V L的密闭容器中发生反应①,开始时充入a ml CO与2a ml H2,平衡转化率与温度、压强的关系如图2所示。p1________(填“>”、“<”或“=”)p2,该甲醇合成反应在A点的平衡常数K=______________(用a和V表示)。该反应达到平衡时,反应物转化率的关系是CO________(填“>”、“<”或“=”)H2。
18. 水煤气是的主要来源,研究对体系制的影响,涉及主要反应如下:
回答列问题:(1)的焓变_______(用代数式表示)。
(2)压力p下,体系达平衡后,图示温度范围内已完全反应,在温度时完全分解。气相中,和摩尔分数随温度的变化关系如图所示,则a线对应物种为_______(填化学式)。当温度高于时,随温度升高c线对应物种摩尔分数逐渐降低的原因是_______。
(3)压力p下、温度为时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应的平衡常数_______;此时气体总物质的量为,则的物质的量为_______;若向平衡体系中通入少量,重新达平衡后,分压将_______(填“增大”“减小”或“不变”),将_______(填“增大”“减小”或“不变”)。
10月月考化学答案
1--5CCACA 6--10DCBBC 11--15CD BD D D BC
18【答案】(1)++ (2) ①. ②. 当温度高于T1,已完全分解,只发生反应Ⅱ,温度升高,反应Ⅱ逆向移动,所以的摩尔分数减小。
(3) ①. ②. 0.5 ③. 不变 ④. 不变
【解析】
已知三个反应:
Ⅰ.
Ⅱ.
Ⅲ.
设目标反应为Ⅳ,根据盖斯定律,Ⅳ=Ⅰ+Ⅱ+Ⅲ,所以++。
【小问2详解】
图示温度范围内已完全反应,则反应Ⅰ已经进行完全,反应Ⅱ和Ⅲ均为放热反应,从开始到T1,温度不断升高,反应Ⅱ和Ⅲ逆向移动,依据反应Ⅱ,量减小,摩尔分数减小,量升高,摩尔分数,且二者摩尔分数变化斜率相同,所以a曲线代表的摩尔分数的变化,则c曲线代表的摩尔分数随温度的变化,开始到T1,的摩尔分数升高,说明在这段温度范围内,反应Ⅲ占主导,当温度高于T1,已完全分解,只发生反应Ⅱ,所以的摩尔分数减小。
【小问3详解】
①压力p下、温度为时,、、和摩尔分数分别为0.50、0.15、0.05,则H2O(g)的摩尔分数为:,则反应的平衡常数 ;
②设起始状态1mlC(s),xmlH2O(g),反应Ⅰ进行完全。
则依据三段式:
根据平衡时、、和摩尔分数分别为0.50、0.15、0.05,则有、、,解出,,则,而由于平衡时n(总)=4ml,则y=4,y=,则n(CaCO3)= ==0.5。
③若向平衡体系中通入少量,重新达平衡后,反应的Kp=,温度不变,Kp不变,则分压不变;体系中增加了,若反应Ⅱ逆向移动,在CO2分压不变的前提下,CO、H2O的分压增大,H2分压减小,则反应Ⅱ的Kp将会发生变化,与事实不符, 所以为了保证Ⅱ的Kp也不变,最终所有物质的分压均不变,即不变。A
B
C
D
选项
实验目的
实验及现象
结论
A
验证压强对平衡的影响
先将注射器充满NO2气体,然后将活塞往里推压缩体积,观察到注射器内气体颜色加深
增大压强,平衡向生成NO2的方向移动
B
探究KI与FeCl3反应的限度
取5 mL 0.1 ml•L-1KI溶液于试管中,加入10mL0.1 ml•L-1FeCl3溶液,充分反应后滴入5滴KSCN溶液
若溶液变血红色,则KI与FeCl3的反应有一定限度
C
探究氢离子浓度对CrO42-(黄色)、Cr2O72-(橙色)相互转化的影响
向K2CrO4溶液中缓慢滴加硫酸,黄色变为橙色
增大氢离子浓度,转化平衡向生成Cr2O72-的方向移动
D
探究化学反应的热效应
取2mL 0.5 ml•L-1的CuCl2溶液于试管中,置于冷水中,一段时间后取出逐渐加热。冷水中的CuCl2溶液为蓝色,加热后逐渐变黄
[Cu(H2O)4]2++4Cl-
4H2O+[Cu(Cl)4]2-ΔH>0
化学反应
平衡常数
温度/℃
500
800
①CO(g)+2H2(g) CH3OH(g) △H1
K1
2.5
0.15
②H2(g)+CO2(g) H2O(g)+CO(g) △H2
K2
a
b
③3H2(g)+CO2(g) CH3OH(g)+H2O(g) △H3
K3
2.5
0.375
相关试卷
山东省泰安市宁阳县第一中学2024-2025学年高二上学期10月月考化学试题(Word附答案):
这是一份山东省泰安市宁阳县第一中学2024-2025学年高二上学期10月月考化学试题(Word附答案),共14页。试卷主要包含了3kJ·ml-1,若将0, 反应I等内容,欢迎下载使用。
重庆市第一中学2024-2025学年高二上学期9月月考化学试题(Word版附解析):
这是一份重庆市第一中学2024-2025学年高二上学期9月月考化学试题(Word版附解析),文件包含重庆市第一中学2024-2025学年高二上学期9月月考化学试题Word版含解析docx、重庆市第一中学2024-2025学年高二上学期9月月考化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。
湖南省长沙市长郡中学2024-2025学年高二上学期第一次月考化学试题(Word版附解析):
这是一份湖南省长沙市长郡中学2024-2025学年高二上学期第一次月考化学试题(Word版附解析),文件包含湖南省长沙市长郡中学2024-2025学年高二上学期第一次月考化学试卷Word版含解析docx、湖南省长沙市长郡中学2024-2025学年高二上学期第一次月考化学试卷Word版无答案docx等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。








