








浙江省强基联盟2024-2025学年高三上学期10月联考化学试题word版(附参考答案与解析版)
展开这是一份浙江省强基联盟2024-2025学年高三上学期10月联考化学试题word版(附参考答案与解析版),文件包含精品解析浙江省强基联盟2024-2025学年高三上学期10月联考化学试题原卷版docx、精品解析浙江省强基联盟2024-2025学年高三上学期10月联考化学试题原卷版pdf、精品解析浙江省强基联盟2024-2025学年高三上学期10月联考化学试题解析版docx、精品解析浙江省强基联盟2024-2025学年高三上学期10月联考化学试题解析版pdf等4份试卷配套教学资源,其中试卷共70页, 欢迎下载使用。
考生注意:
本试卷满分100分,考试时间90分钟。
考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Cl 35.5 Fe 56 Ag 108
一、选择题(本大题共16小题,每小题3分,共48分,每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1. 下列依据不同角度分类正确的是
A. 既能与氢氟酸反应,又能与氢氧化钠溶液反应,属于两性氧化物
B. “长征七号”采用了液氧煤油发动机,煤油是混合物
C. 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D. 根据物质能否电离,将其分为强电解质和弱电解质
2. 下列有关物质的结构、性质与用途具有对应关系的是
A. 在淀粉的主链上再接入带有强亲水基团的支链,可以提高吸水能力
B. 浓硫酸具有脱水性,可用浓硫酸干燥、等气体
C. 具有强氧化性,可用作呼吸面具的供氧剂
D. 氮化镓硬度大,可用作半导体材料
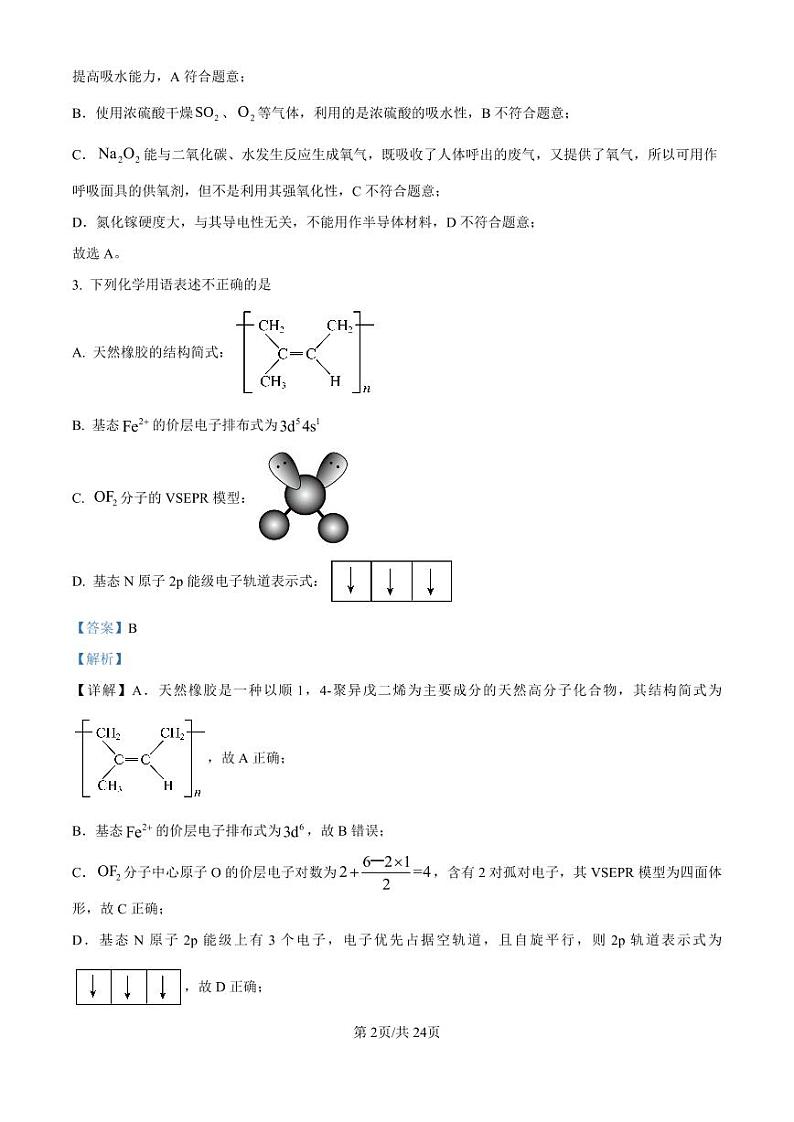
3. 下列化学用语表述不正确的是
A. 天然橡胶的结构简式:
B. 基态的价层电子排布式为
C. 分子的VSEPR模型:
D. 基态N原子2p能级电子轨道表示式:
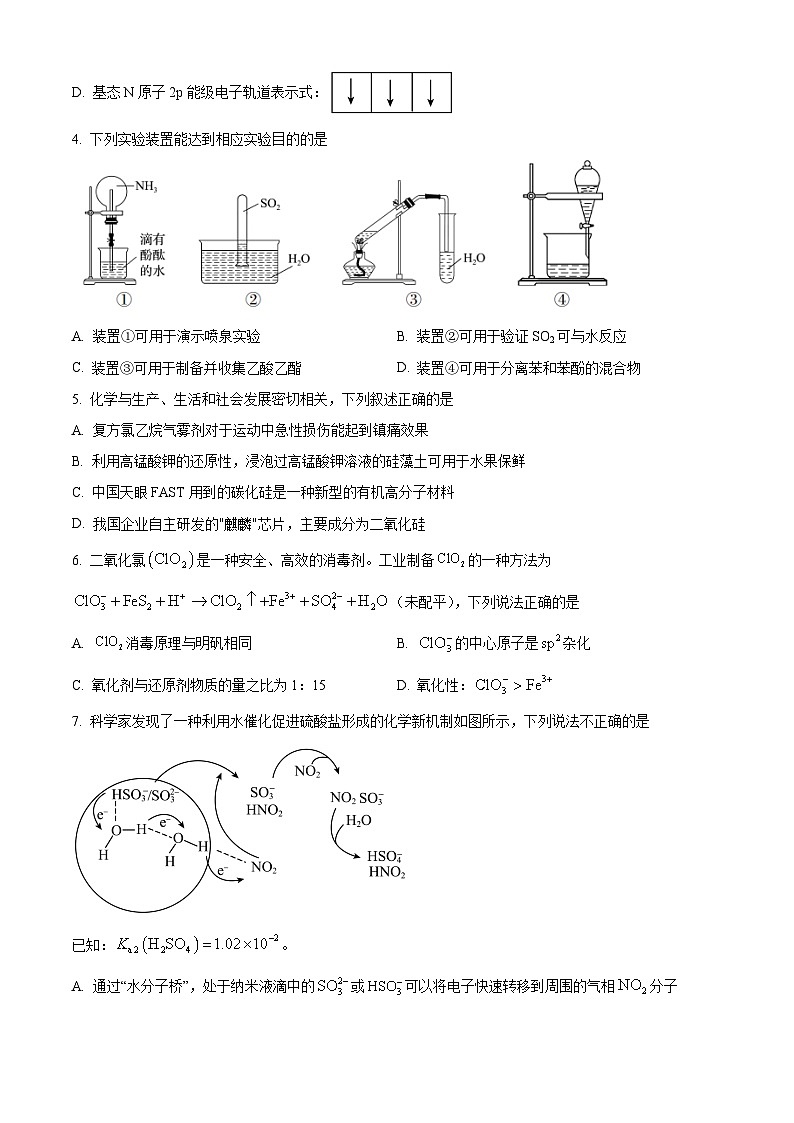
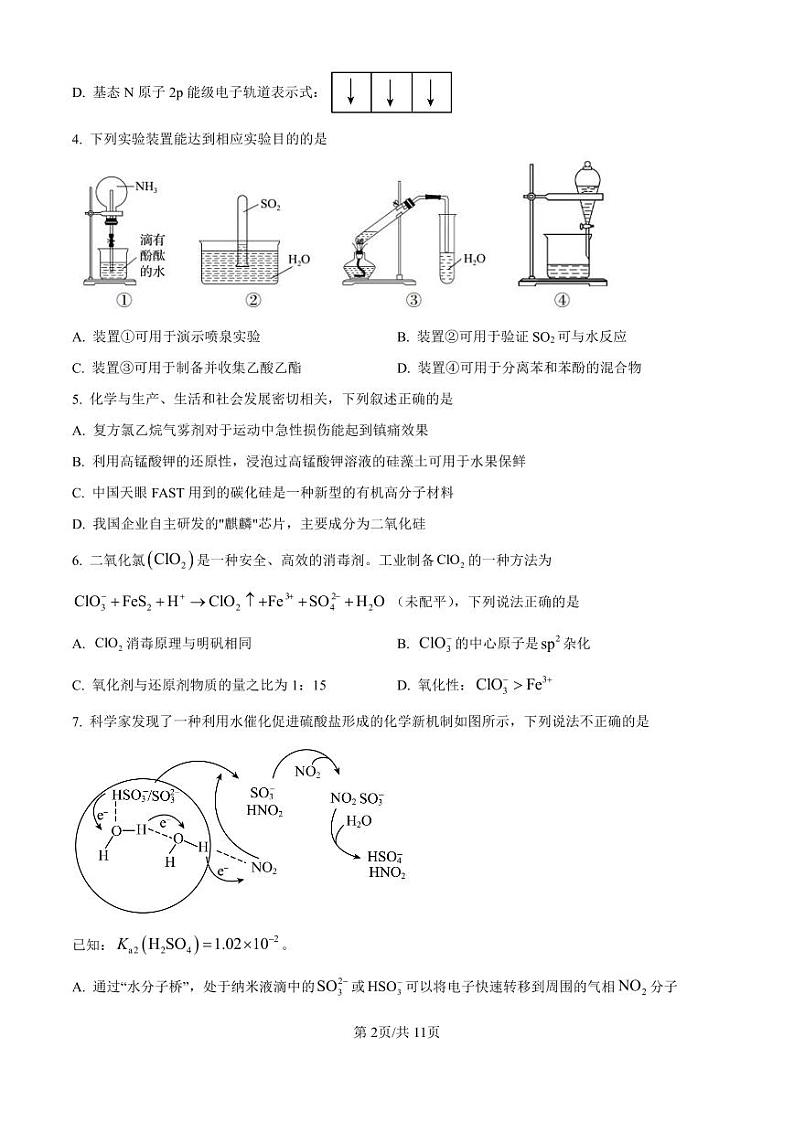
4. 下列实验装置能达到相应实验目的的是
A. 装置①可用于演示喷泉实验B. 装置②可用于验证SO2可与水反应
C. 装置③可用于制备并收集乙酸乙酯D. 装置④可用于分离苯和苯酚的混合物
5. 化学与生产、生活和社会发展密切相关,下列叙述正确的是
A. 复方氯乙烷气雾剂对于运动中急性损伤能起到镇痛效果
B. 利用高锰酸钾的还原性,浸泡过高锰酸钾溶液的硅藻土可用于水果保鲜
C. 中国天眼FAST用到的碳化硅是一种新型的有机高分子材料
D. 我国企业自主研发的"麒麟"芯片,主要成分为二氧化硅
6. 二氧化氯是一种安全、高效的消毒剂。工业制备的一种方法为(未配平),下列说法正确的是
A. 消毒原理与明矾相同B. 的中心原子是杂化
C. 氧化剂与还原剂物质的量之比为1:15D. 氧化性:
7. 科学家发现了一种利用水催化促进硫酸盐形成的化学新机制如图所示,下列说法不正确的是
已知:。
A. 通过“水分子桥”,处于纳米液滴中的或可以将电子快速转移到周围的气相分子
B. 观察图示可知“水分子桥”主要靠氢键形成
C. 与间发生总反应的离子方程式:
D. 利用水催化促进硫酸盐形成的化学新机制中,硫和氮都有三种化合价价态
8. 下列解释事实的方程式不正确的是
A. 汽车催化转化器使CO和NO反应生成和
B. 在任何条件下都不能发生反应:
C. 涤纶的合成:
D. 碱性锌锰电池工作原理:
9. 质谱可广泛用于化合物的结构测定,如只含C、H、O三种元素的某化合物的质谱图如图所示。从碎片峰看,有m/z 77、51、39等峰,说明化合物有苯环;有m/z107峰,说明化合物有C2H5取代基;有m/z 118峰,说明化合物有醇羟基,则下列说法正确的是
A. 该化合物的相对分子质量为107
B. 该化合物的分子式为C9H10O
C. 该化合物中至少存在7种不同环境的氢原子
D. 该化合物可能的结构简式为C6H5CH(OH)CH2CH3
10. 一种麻醉剂的分子结构式如图所示,其中X的原子核只有1个质子;元素Y、Z、W的原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子,下列说法不正确的是
A. 键角:
B. 物质的碱性:
C. 分子的极性:
D. X、Y、Z、W四种原子的电负性的大小顺序是
11. 工业上制备BaS涉及如下反应:
I.BaSO4(s)+4C(s)4CO(g)+BaS(s) △H=+571.2kJ•ml-1
II.BaSO4(s)+4CO(g)4CO2(g)+BaS(s) △H=-118.8kJ•ml-1
将物质的量之比为1:3的BaSO4和C加入密闭容器发生反应,实验测得体系中生成物平衡物质的量分数与温度的变化关系如图所示,下列说法错误的是
A. 温度升高,反应物和生成物粒子的有效碰撞几率均增大
B. T1℃之后,CO2平衡物质的量分数改变由C(s)+CO2(g)2CO(g)导致
C. 增大起始BaSO4和C的物质的量之比,可增大C的平衡转化率
D. 平衡后缩小容器容积,BaS的平衡产率降低
12. 维纶(聚乙烯醇缩甲醛)的合成路线如下:
下列说法正确的是
A. 1ml乙水解时最多消耗1mlNaOHB. 甲乙发生的是缩聚反应
C. 丙的结构简式为D. 丙丁过程中发生了加成反应和取代反应
13. 将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境中,下列有关说法正确的是
A. 阴极的电极反应式为
B. 金属M的活动性比Fe的活动性弱
C. 钢铁设施表面因积累大量电子而被保护
D. 钢铁设施在河水中的腐蚀速率比在海水中的快
14. 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是
A. 金属离子以离子键与阴离子或阴离子骨架结合
B. 具有吸水性,需要密封保存
C. 能与反应生成新盐
D. 所有Si被Al取代则得到铝硅酸盐
15. 常温下,往溶液中通入至饱和,有微量生成,溶液中(溶液体积和浓度的变化忽略不计).[已知:的电离常数],下列说法不正确的是
A. 溶液中,
B. 反应的
C. 溶液中,
D. 溶液中,约为5
16. 根据实验目的设计方案并进行实验,观察到相关现象,下列方案设计、结论均正确的是
A. AB. BC. CD. D
二、非选择题(本大题共5小题,共52分)
17. 氢的有效储存与释放是氢能应用的关键问题之一。
I.有机储氢材料
(1)N-乙基咔唑是具有应用前景储氢材料,其储氢、释氢原理如图1所示。
①N—乙基咔唑中碳原子杂化方式分别有和___________。
②晶体中离子键的百分数为。分析、、、中离子键的百分数小于的有____________。
③比较在水中的溶解性:乙基咔唑___________乙胺(填“”或“”)。
(2)HCOOH是安全方便的具有应用前景的液态储氢材料。HCOOH催化释氢的可能机理如图2所示。
①依据VSEPR模型,中心原子上的价层电子对数是___________。
②为证实上述机理,用HCOOD代替HCOOH进行实验。在图3(答题卡相应的位置)中补充HCOOD催化释氢部分过程的相应内容________。
II.复合储氢材料
(3)一种新型储氢材料的晶胞形状为正方体,如图4所示。
①该物质的化学式为____________。(电负性:B元素为2.0,H元素为2.1)
②已知阿伏加德罗常数的值为,该物质的摩尔质量为,该晶体的密度为,则晶胞边长为_____________nm。
18. 如图所示可以分离并回收废旧芯片中的几种贵金属。
请回答:
(1)溶液Z中存在的阳离子主要有__________。
(2)写出步骤VI反应的离子方程式__________。
(3)金的分离还可以加王水,银钯的分离可重复利用某些溶液。
①下列说法正确的是_____________。
A.芯片中的金是芯片连接的绝佳材料,利用其物理性质和化学性质
B.步骤I中硝酸只体现氧化性
C.步骤Ⅱ溶液W可以是和NaCl的混合溶液,步骤Ⅲ溶液X可以是NaCl溶液
D.步骤V中利用其还原性获得Ag
②步骤VII加入盐酸,调,解释pH不可过低的原因___________。
(4)设计实验验证溶液Z中银元素的存在____________。
19. 氨是化肥工业和基本有机化工的主要原料。
(1)“哈伯法”合成氨的反应:
相关键能数据如下表:
①_________。
②合成氨的反应在低温能自发进行,推动反应在该条件下自发进行的主要因素是反应的_________(填“焓变”或“熵变”)。
③向密闭容器中按1:3体积比通入和,反应达平衡时的体积分数为,则氮气的平衡转化率__________。
(2)“球磨法”是在温和的条件下(和,)合成氨,氨的最终体积分数可高达。该法分为两个步骤(如图):第一步,铁粉在球磨过程中被反复剧烈碰撞而活化,产生高密度的缺陷,氮分子被吸附在这些缺陷上,有助于氮分子的解离;第二步,发生加氢反应得到,剧烈碰撞中,从催化剂表面脱附得到产物氨。
“球磨法”合成氨过程示意图如上
①“球磨法”与“哈伯法”相比较,下列说法正确的是___________。
A.“球磨法”催化剂(Fe)缺陷密度越高,的吸附率越高
B.“哈伯法”采用高温主要用于解离氮氮三键,而“球磨法”不用解离氮氮三键
C.“球磨法”中"剧烈碰撞"产生"活化缺陷",是为了提高平衡转化率
D.“球磨法”不采用高压,是因为低压产率已经较高,加压会增大成本
②机械碰撞有助于催化剂缺陷的形成,而摩擦生热会使体系温度升高。图中是吸附量、体系温度随球磨转速变化曲线,则应选择的最佳转速约400转/min。若选择500转的转速,的吸附量降低的原因是______________。
(3)用氨气研发燃料电池,电池反应为,通入a气体一极的电极反应式为___________。
20. 亚硝酰氯(NOCl,熔点,沸点)为黄色气体,易与水反应生成和HCl,常用作有机合成中间体。实验室可由氯气与一氧化氮反应制备,其装置如图所示:
已知:既有氧化性又有还原性;微溶于水,能溶于硝酸。请回答:
(1)仪器a的名称为____________。
(2)下列说法不正确的是_________。
A. B装置的作用吸收NO中混有的和气体
B. 为使冷凝效果更好,可用冰水浴替代D中的冰盐浴
C. 装置G中浓盐酸起到提供氯元素和充当氧化剂的作用
D. 无水的作用是防止水蒸气进入三颈烧瓶中,使NOCl水解
(3)尾气含有、、,某同学建议用NaOH溶液处理、,用溶液吸收NO气体。要证明NaOH溶液吸收NOCl后,溶液中存在除外的两种阴离子,下列操作步骤顺序合理的是___________。
a向烧杯中滴加酸性溶液,溶液紫色褪去
b.取1.0mL装置D中的产品于烧杯中,加入充分反应
c.向烧杯中滴加足量溶液,有白色沉淀生成,加入稀硝酸,搅拌,仍有白色沉淀
(4)制得的NOCl中可能含有少量杂质,为测定产品纯度,进行如下实验:称取2.0000g样品溶于50.00mLNaOH溶液中,加入几滴溶液作指示剂,用足量硝酸酸化溶液滴定至终点,消耗溶液50.00mL。[已知:为砖红色固体,,]
①滴定终点的现象:当滴入最后半滴标准溶液后,____________。
②计算产品的纯度为__________%(保留1位小数)。
21. 化合物G是一种合成降血压药物中间体,其合成如下:
请回答:
(1)C中含氧官能团的名称是___________。
(2)写出F的结构简式____________。
(3)下列说法正确的是___________。
A. 1ml化合物B最多消耗2mlNaOH
B. 化合物E分子结构中存在两个手性碳原子
C. 的转化条件为NaOH的乙醇溶液、加热
D. 化合物G的分子式为
(4)反应A→B的化学方程式为____________。
(5)写出满足下列条件的E的同分异构体的结构简式__________。
①分子中除苯环外还有一个含两个氧原子的五元杂环
②苯环上只有两个取代基
③能与溶液反应生成二氧化碳
④核磁共振氢谱图中只有4组吸收峰
(6)设计以苯酚和为原料制备的合成路线(无机试剂任选)____________。选项
实验目的
方案设计
现象
结论
A
探究铜和浓硫酸反应的产物
将铜丝放入浓硫酸中,加热
开始时铜丝表面变黑,产生无色气体,后黑色固体溶解
由氧化还原反应规律可知黑色固体一定是CuO
B
判断的化学键类型
将固体溶于水,进行导电性实验
溶液可导电
中含有离子键
C
探究浓硝酸与碳在加热条件下能否反应
将红热的木炭投入浓硝酸中
产生红棕色气体
碳与浓硝酸在加热条件下反应生成
D
探究和的反应{已知含的溶液呈红棕色}
将气体通入溶液中
溶液先变为红棕色,过一段时间又变成浅绿色
与络合反应速率比氧化还原反应速率大,但氧化还原反应的平衡常数更大
化学键
键能
946.0
436.0
3908
相关试卷
这是一份浙江省强基联盟2025届高三上学期10月联考化学试题(Word版附解析),共18页。试卷主要包含了下列依据不同角度的分类正确的是,下列化学用语表述不正确的是,下列解释事实的方程式不正确的是等内容,欢迎下载使用。
这是一份浙江省强基联盟2024-2025学年高三上学期10月联考化学试题(含解析),共18页。试卷主要包含了下列依据不同角度的分类正确的是,下列化学用语表述不正确的是,下列解释事实的方程式不正确的是等内容,欢迎下载使用。
这是一份浙江省强基联盟2024-2025学年高三上学期8月联考化学试卷(Word版附解析),文件包含浙江省强基联盟2024-2025学年高三上学期8月联考化学试题Word版含解析docx、浙江省强基联盟2024-2025学年高三上学期8月联考化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共35页, 欢迎下载使用。












