



福建省宁德市博雅培文学校2024-2025学年高二上学期9月月考化学试题+
展开这是一份福建省宁德市博雅培文学校2024-2025学年高二上学期9月月考化学试题+,文件包含试题docx、福建省宁德市某校2024-2025学年高二9月月考化学试题docx、参考答案1pdf等3份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。
可能用到的相对原子质量
O -16S -32Cl- 35.5 Ag -108 Al -27Cu -64Fe-56Zn-65H-1
一、单选题(每题 4 分,共 40 分)
1.下列设备工作时,将化学能转化为电能的是
2.在化学变化中能量越低越稳定。如图表示反应 C(s,金刚石)=C(s,石墨)过程中的能量变化情况,下列有关说法正确的是
A.该过程是一个物理变化
B.常温下,石墨比金刚石稳定
C.该反应是吸热反应
D.反应物的总键能大于生成物的总键能
3.下列能形成原电池的是
4.爱迪生蓄电池在充电和放电时发生的反应为 Fe NiO 2 2H 2O Fe OH 2 Ni OH 2,下列对该蓄电池的叙述错误的是
A.放电时,Fe 参与负极反应, NiO2 参与正极反应
B.放电时,电解质溶液中的阴离子向负极移动
C.放电时,负极上的电极反应式为 Fe 2H 2O 2e-= Fe(OH )2+ 2H+
D.充电时,该蓄电池的负极连接电源的负极
5.化学电源在日常生活和高科技领域中都有广泛应用。下列说法正确的是
A.图甲:锌铜原电池工作时,电子由锌经电解质溶液流向
B.图乙:纽扣式银锌电池中,正极的电极反应式为 Ag2 O 2e- 2H +=2Ag H2 O
C.图丙:锌锰干电池中,锌筒作负极,发生氧化反应,且外电路中每转移 1ml 电子消耗锌 32.5g
D.图丁:铅蓄电池为二次电池,其负极的电极反应式为 Pb 2e =Pb2
6.下列各组热化学方程式中,化学反应的ΔH 前者大于后者的是
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)ΔH1;2H2S(g)+O2(g)=2S(s)+2H2O(l)ΔH2
②S(s)+O2(g)=SO2(g)ΔH3;S(g)+O2(g)=SO2(g)ΔH4
③NH3·H2O(aq)+H+(aq)=NH4 (aq)+H2O(l)ΔH5;H+(aq)+OH-(aq)=H2O(l)ΔH6
④CaCO3(s)=CaO(s)+CO2(g)ΔH7;CaO(s)+H2O(l)=Ca(OH)2(s)ΔH8
A.②③④B.④C.①D.①②③
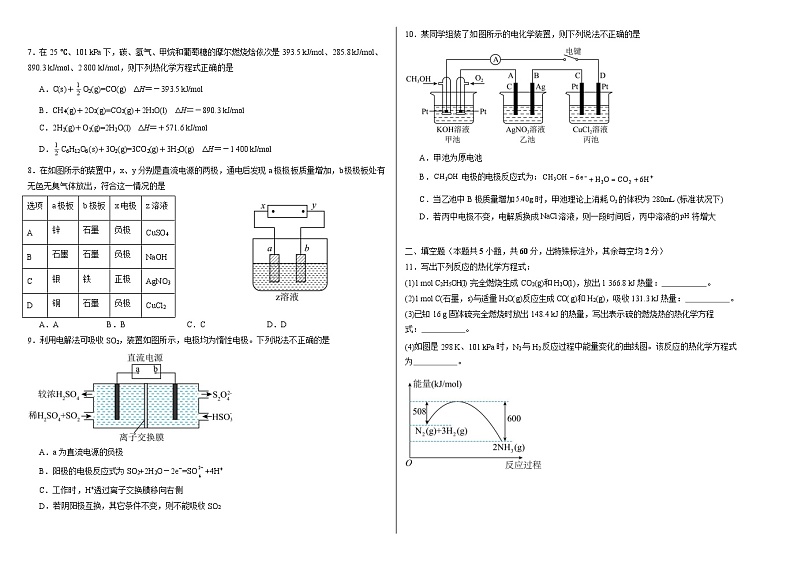
7.在 25 ℃、101 kPa 下,碳、氢气、甲烷和葡萄糖的摩尔燃烧焓依次是 393.5 kJ/ml、285.8 kJ/ml、890.3 kJ/ml、2 800 kJ/ml,则下列热化学方程式正确的是
A.C(s)+ O2 (g)=CO(g)ΔH=-393.5 kJ/ml
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890.3 kJ/ml
C.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ/ml
D. C6H12O6 (s)+3O2 (g)=3CO2 (g)+3H2O(g)ΔH=-1 400 kJ/ml
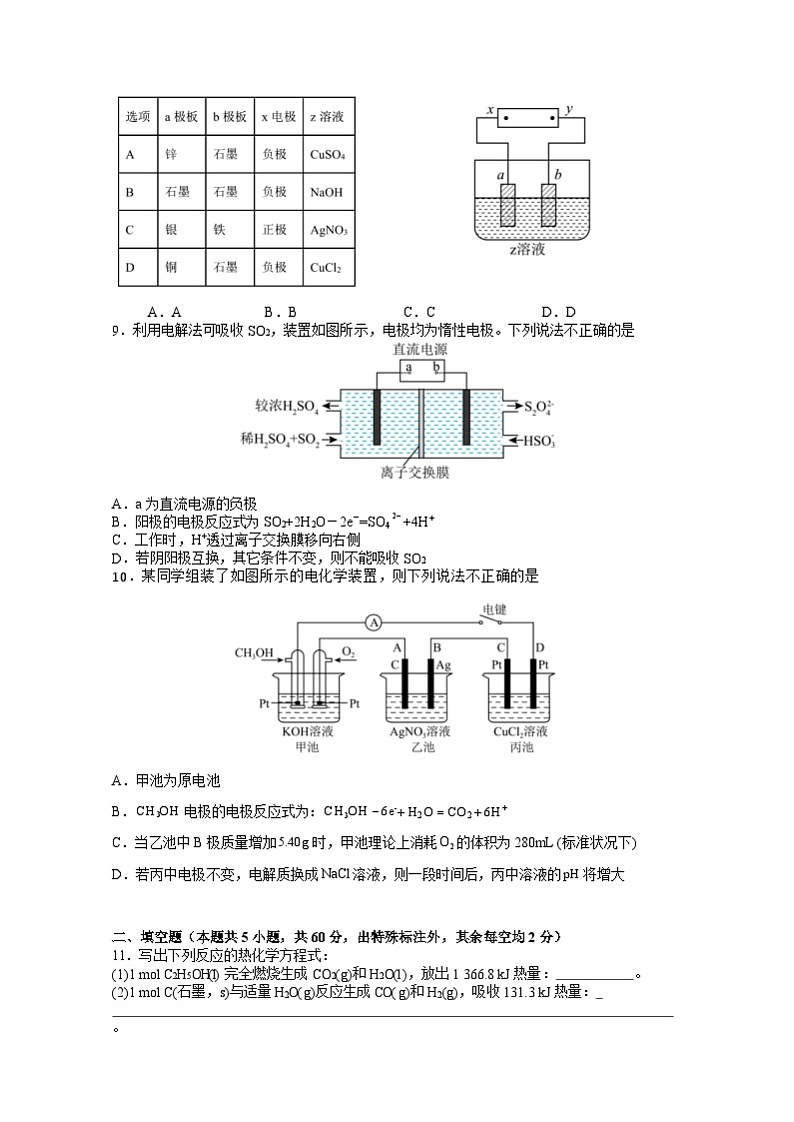
8.在如图所示的装置中,x、y 分别是直流电源的两极,通电后发现 a 极极板质量增加,b 极极板处有无色无臭气体放出,符合这一情况的是
A.AB.BC.CD.D
9.利用电解法可吸收 SO2,装置如图所示,电极均为惰性电极。下列说法不正确的是
A.a 为直流电源的负极
B.阳极的电极反应式为 SO2+2H2O-2e-=SO4 2 +4H+
C.工作时,H+透过离子交换膜移向右侧
D.若阴阳极互换,其它条件不变,则不能吸收 SO2
10.某同学组装了如图所示的电化学装置,则下列说法不正确的是
A.甲池为原电池
B. CH3OH 电极的电极反应式为: CH3OH 6e- H2O CO2 6H
C.当乙池中 B 极质量增加 5.40g 时,甲池理论上消耗 O2 的体积为 280mL (标准状况下)
D.若丙中电极不变,电解质换成 NaCl 溶液,则一段时间后,丙中溶液的 pH 将增大
二、填空题(本题共 5 小题,共 60 分,出特殊标注外,其余每空均 2 分)
11.写出下列反应的热化学方程式:
(1)1 ml C2H5OH(l)完全燃烧生成 CO2(g)和 H2O(l),放出 1 366.8 kJ 热量: 。
(2)1 ml C(石墨,s)与适量 H2O(g)反应生成 CO(g)和 H2(g),吸收 131.3 kJ 热量: 。
(3)已知 16 g 固体硫完全燃烧时放出 148.4 kJ 的热量,写出表示硫的燃烧热的热化学方程 式: 。
(4)如图是 298 K、101 kPa 时,N2 与 H2 反应过程中能量变化的曲线图。该反应的热化学方程式为 。
12.如图所示装置,C、D、E、F、X、Y 都是惰性电极,A、B 为外接直流电源的两极。将直流电源接 通后,F 极附近呈红色。请回答:
(1)电源电极 A 名称为 。(1 分)
(2)写出 C 和 F 的电极名称,以及电极反应式
C: (1 分) ;
F: (1 分) ;
(3)若通过 0.02ml 电子时,通电后甲中溶液体积为 200mL,则通电后所得的硫酸溶液的物质的量浓度 为 。
(4)若通过 0.02ml 电子时,丁中电解足量 R(NO3)m 溶液时,某一电极析出了 a g 金属 R,则金属 R 的相 对原子质量 Mr(R)的计算公式为 Mr(R)= (用含 a、m 的代数式表示)。
(5)戊中 X 极附近的颜色逐渐变浅,Y 极附近的颜色逐渐变深,这表明 Fe(OH) 3 胶体粒子带
(1 分)电荷(填“正”或“负”),在电场作用下向 Y 极移动。
(6)若甲、乙装置中的 C、D、E、F 电极均只有一种单质生成时,对应单质的物质的量之比 为 。
(7)现用丙装置给铜件镀银,则 H 应该是(填“铜件”或“银”)。(1 分)
13.钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一
Ⅰ.如图装置中,U 形管内为红墨水,a、b 试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块, 放置一段时间均被腐蚀,这两种腐蚀都属于电化学腐蚀。
(1)红墨水柱两边的液面变为左低右高,则 (填“a”或“b”)边盛有食盐水。
(2)b 试管中铁发生的是 腐蚀。
Ⅱ.下面两个图都是金属防护的例子。
(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料
R 可以采用 (从下面选项中选择),此方法叫做 保护法。
A.铜B.钠C.锌D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的 极。 (5)采取以上两种方法, (填“甲”或“乙”)种能使铁闸门保护得更好。
14.结合所学知识,回答下列问题。
(1)按要求写出电极反应式
①碱性锌锰电池的总反应为 Zn 2MnO2 2H2 O 2MnO(OH) Zn(OH)2 ,写出负极电极反应式 。
②将 2FeCl3 2KI I2 2FeCl2 2KCl设计成双液电池:正极烧杯中盛放的溶液为 (1 分),电池正 极的电极反应式为 。
(2)某同学设计了如下图所示装置,用氢氧燃料电池作为电源探究粗铜精炼原理,根据要求回答下列问题:
①甲装置中通入氧气的电极为 (1 分)(填“正极”或“负极”),该极发生的电极反应式为 。
②如果粗铜中含有铁、银等杂质,粗铜电极发生的电极反应式有 。乙装置中反应一段时间后,CuSO4溶液的 c(Cu 2 ) (1 分) (填“增大”、“减小”或“不变”)。
③在标准状况下,甲装置有 2.24L 氧气参加反应,则乙装置中阴极析出铜的质量理论上为 g。
15.2022 年 12 月 4 日神舟十四号载人飞船成功返回地面,圆满完成飞行任务。载人航天工程对科学研 究及太空资源开发具有重要意义。
(1)氢氧燃料电池(如图所示)反应生成的水可作为航天员的饮用水,由图示的电子转移方向判断 Y气体是 (1 分),为保证电解质溶液浓度不至于随着反应而变稀,需要在 (填“正极”或“负极”)添加冷凝装置排出多余水分,负极的电极反应式为 。
(2)我国“神舟”飞船的电源系统有太阳能电池帆板、镉镍蓄电池和应急电池等。
①飞船在光照区运行时,太阳能电池帆板的能量转化形式是: 能转化为电能等。(1 分)
②镉镍蓄电池的工作原理为:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。当飞船运行到地影区时,镉镍蓄电池为飞船供电,此时在正极电极反应方程式是 ,负极附近溶液的碱性 (填“增强”“减弱”或“不变”)。
③应急电池在紧急状况下会自动启动,工作原理为 Zn+Ag2O+H2O 2Ag+Zn(OH)2,工作时,正极电极方程式为 。
相关试卷
这是一份2023届福建省宁德市博雅培文学校高三上学期一模化学试题(含答案),共8页。
这是一份福建省宁德市博雅培文学校2023-2024学年高一下学期6月月考化学试题,文件包含福建省宁德市博雅培文学校2023-2024学年高一6月月考化学试题pdf、宁德博雅培文学校6月份月考高一化学答题卷3pdf、高一月考答案2pdf等3份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。
这是一份福建省宁德市博雅培文学校2023-2024学年高一下学期第一次月考化学试题(原卷版+解析版),文件包含福建省宁德市博雅培文学校2023-2024学年高一下学期第一次月考化学试题原卷版docx、福建省宁德市博雅培文学校2023-2024学年高一下学期第一次月考化学试题解析版docx等2份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。












