

湖北省宜昌市第一中学2024-2025学年高一上学期10月月考 化学试卷(无答案)
展开
这是一份湖北省宜昌市第一中学2024-2025学年高一上学期10月月考 化学试卷(无答案),共6页。试卷主要包含了4L时,该气体一定处于标准状况等内容,欢迎下载使用。
命题教师:谭玉园 审题教师:陈爱红 陈语炘
本试卷共6页,19题。全卷满分:100分。考试时间75分钟。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 P-31 S-32 Cl-35.5 K-39 Ca-40 Fe-56 Cu-64
一、选择题(本题包括15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.新闻报道称,以碳基CMOS集成电路技术的5纳米栅长的碳管晶体管为元器件的商用碳基芯片,有望在芯片研究技术上赶超国外同行。已知碳晶体管是采用石墨为原料制造而成,是一种碳纳米材料。下列说法错误的是( )
A.石墨与金刚石互为同素异形体
B.碳纳米材料是胶体
C.碳纳米管是非金属导体
D.碳纳米管具有优良性能和应用前景
2.分类与归类是识别化学物质的基本方法,也是理解化学语言的基本途径。下列各项中的物质,能满足如图中阴影部分关系的是( )
3.在溶液中能大量共存,若加入有沉淀析出,若加入能放出气体的是( )
A.、、、B.、、、
C.、、、D.、、、
4.下列有关焰色试验说法中正确的是( )
A.用光洁的铂丝蘸取某无色溶液,灼烧时观察到黄色火焰,说明一定含,不含
B.焰色试验中需用盐酸洗净铂丝
C.焰色试验均应透过蓝色钴玻璃观察
D.只有金属单质灼烧时火焰才有颜色
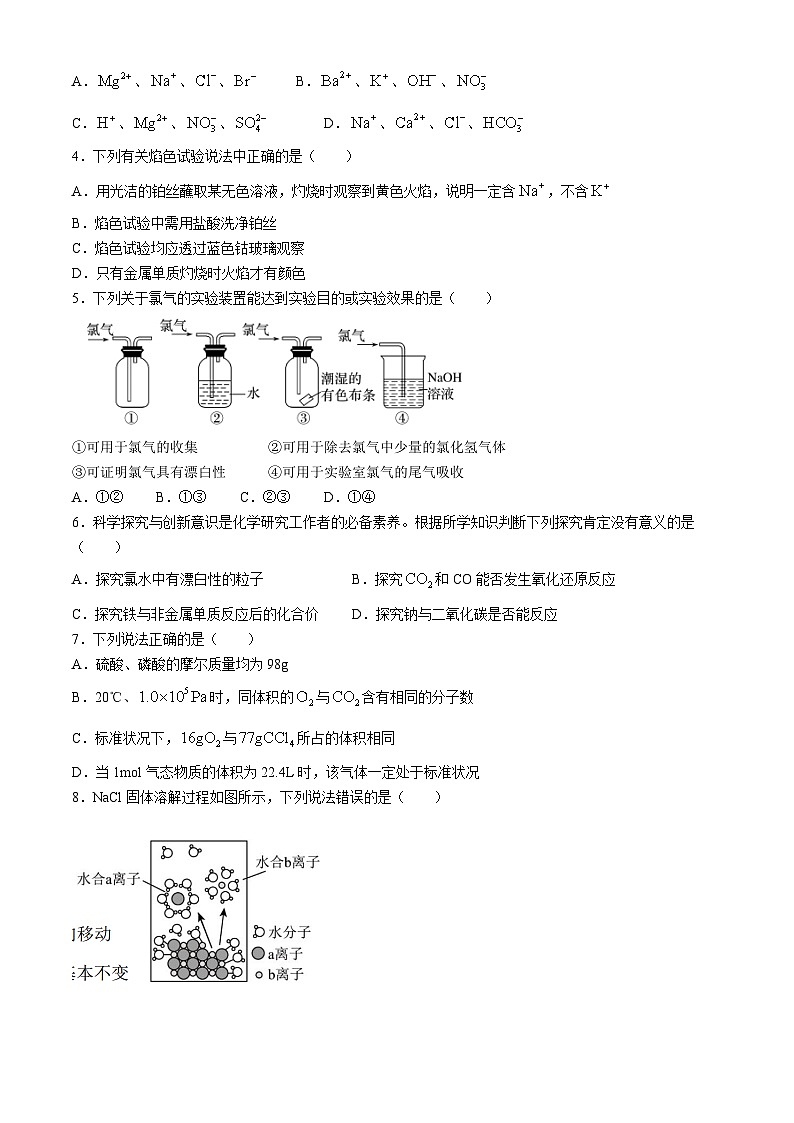
5.下列关于氯气的实验装置能达到实验目的或实验效果的是( )
①可用于氯气的收集②可用于除去氯气中少量的氯化氢气体
③可证明氯气具有漂白性④可用于实验室氯气的尾气吸收
A.①②B.①③C.②③D.①④
6.科学探究与创新意识是化学研究工作者的必备素养。根据所学知识判断下列探究肯定没有意义的是( )
A.探究氯水中有漂白性的粒子B.探究和CO能否发生氧化还原反应
C.探究铁与非金属单质反应后的化合价D.探究钠与二氧化碳是否能反应
7.下列说法正确的是( )
A.硫酸、磷酸的摩尔质量均为98g
B.20℃、时,同体积的与含有相同的分子数
C.标准状况下,与所占的体积相同
D.当1ml气态物质的体积为22.4L时,该气体一定处于标准状况
8.NaCl固体溶解过程如图所示,下列说法错误的是( )
A.a离子为,b离子为
B.NaCl的电离方程式为:
C.该溶液导电时,水合a离子向与电源正极相连的电极方向移动
D.加入少量固体(假设溶液体积不变),溶液导电性基本不变
9.化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述错误的是( )
A.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
B.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合会产生有毒的
C.过氧化钠可以用作呼吸面具的供氧剂,是因其可以和水、二氧化碳反应生成氧气
D.漂白粉在空气中久置变质,是因为其中的与空气中的反应生成
10.设表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A.所含有的原子数为
B.常温常压下,22.4L氧气所含的原子数为
C.常温常压下,中所含的氧原子数为
D.溶液中所含的数为
11.某反应可表示为:,则值为( )
A.2B.4C.6D.9
12.在反应中,下列说法中正确的是( )
A.KCl是氧化产物,是还原产物B.每消耗,转移2ml电子
C.KOH和均为电解质D.在反应中既作氧化剂又作还原剂
13.下列离子方程式正确的是( )
①碳酸氢钙溶液与过量烧碱溶液混合:
②碳酸镁与稀硫酸:
③醋酸与大理石:
④向溶液中逐滴加入溶液至刚好沉淀完全:
⑤溶液中通入少量氯气:
A.①②③④⑤B.②③④⑤C.②③④D.①③④
14.将的溶液和溶液混合,若不考虑混合后溶液体积的变化,溶液中的物质的量浓度为( )
A.B.C.D.
15.已知:①;②;③。则下列判断正确的是( )
A.氧化性:
B.①中氧化剂和还原剂的物质的量之比为1:8
C.只有氧化性,只有还原性
D.由信息推测:反应不可以进行
二、非选择题(本题包括4小题,共50分)
16.(14分)(1)现有下列9种物质,① ②淀粉溶液 ③ ④ ⑤ ⑥ ⑦纯醋酸 ⑧溶液 ⑨,根据所学知识回答下列问题:属于电解质的是______(填写序号)。
(2)标准状况下,11.2L由④和⑤组成的混合气体的质量为13.9g,则④和⑤物质的量之比为______。向⑧中滴加少量稀盐酸,该反应的离子方程式:______。
(3)已知:向溶液中通入,溶液浑浊,发生反应的离子方程式:。请用单线桥标出该反应的电子转移情况:______。
(4)实验室用胆矾配制的溶液(已知胆矾溶于水使溶液温度降低)。
①以下操作会引起所配制溶液浓度偏低的是______(填序号)。
a.容量瓶底部有少量水b.胆矾溶于水后立即转移到容量瓶中
c.定容时俯视刻度线d.定容后摇匀、静置,发现液面下降,再加蒸馏水至刻度线
②现利用上述CuSO4溶液配制的溶液,选用______mL容量瓶,需用量筒量取______mL上述溶液。
17.(12分)从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。以下是氯元素形成物质的价类二维图的部分信息。
(1)根据图中信息,写出任意两种氯的氧化物的化学式:______。
(2)写出高氯酸与NaOH反应的化学方程式:______。
(3)HCl既具有氧化性,又具有还原性。
①请任意写出一个体现HCl氧化性的离子方程式:______。
②浓盐酸可作为还原剂在加热条件下与发生反应制备,写出该反应的化学方程式:______。
(4)既具有氧化性,又具有还原性。
①请结合上图说明原因:______。
②潮湿的与消石灰混合制取漂白粉的反应中,既体现了氧化性,也体现了还原性。写出反应的化学方程式:______。
18.(14分)Ⅰ.某无色透明溶液中可能大量存在、、、、、、中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是______。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。有关的离子方程式______,取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀。
(3)综上所述,原溶液中一定存在的离子有______,可能存在的离子是______。
Ⅱ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾,碘酸钾和碘化钾在酸性溶液中能发生下列反应:。回答下列问题:
(4)该反应中,氧化剂是______。
(5)当有生成时,转移电子的数目约为______。
(6)为淡棕黄色气体,可由新制的HgO和反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。则制备的化学方程式为______。
19.(15分)2021年10月16日,神舟十三号载人飞船顺利进入预定轨道。飞船的轨道舱内安装盛有颗粒的装置,为宇航员供氧。某兴趣小组利用下列装置(夹持仪器省略),用金属钠和空气来制备(不考虑空气中与Na反应)。
(1)若规定气流的方向为从左到右,各仪器连接的接口顺序(每个装置只用一次)是:空气____________________________________(填字母)。
(2)装置Ⅱ的仪器作用是______。
(3)Ⅳ中反应的离子方程式为______,若没有装置Ⅳ可能导致生成的中含有______(填化学式)。
(4)该小组同学称取ag所制备的样品,利用下列装置测定样品的纯度(夹持仪器省略)。
①有同学提出该实验装置存在缺陷,应该在、装置之间增加一个盛有饱和溶液的洗气瓶,该同学这样做的目的是______,该同学想法是否必要?______(填“是”或“否”),理由是______。
②读出量筒内水的体积后,折算成标准状况下的体积为VmL,计算样品中的质量分数约为______。①
②
③
④
A
NaCl
KCl
B
NaCl
KCl
C
D
相关试卷
这是一份山东省实验中学2024-2025学年高一上学期10月月考化学试题(无答案),共6页。试卷主要包含了10),试卷共8页,考试时间60分钟,5 Cu 64,72 L等内容,欢迎下载使用。
这是一份湖北省荆州中学2024-2025学年高一上学期9月月考 化学试卷,共8页。
这是一份黑龙江省嫩江市高级中学2024-2025学年高一上学期月考 化学试题 (无答案),共3页。试卷主要包含了分类思想是研究化学的常用方法,下列不属于同素异形体的是等内容,欢迎下载使用。








