

河北省邯郸市2025届高三上学期第一次调研考试一模化学试题
展开
这是一份河北省邯郸市2025届高三上学期第一次调研考试一模化学试题,共22页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
一、单选题
1.邯郸“城南夜市”是盛夏市民消夏纳凉、品味美食的理想去处,人间烟火气,最抚凡人心,居民烟火气点亮城市夜经济。下列关于夜市美食的说法正确的是
A.炸薯条用的植物油主要成分是天然有机高分子B.煎饼主要成分(淀粉)的分子式为
C.甜品含有的蔗糖是还原糖D.烤肉过程中蛋白质发生盐析
2.关于试剂保存、取用和除杂,下列表述错误的是
A.实验结束后剩余的金属钠不能放回原试剂瓶
B.液溴保存在棕色细口瓶中,加水液封
C.FeCl2溶液中混有FeCl3杂质,加过量铁粉除去
D.除去乙醇中混有的乙酸,加生石灰后蒸馏
3.如今高分子材料已经渗透到我们生活的方方面面,下列说法错误的是
A.聚乙烯分子结构中只有键,故聚乙烯保鲜膜形变伴随键旋转
B.聚对苯二甲酰对苯二胺(芳纶1414)是通过加聚反应制得的,可用作防弹装甲
C.聚乳酸在人体内可降解,可用作手术缝合线
D.聚乙炔含有共轭大键,可用作导电材料
4.市面上一种空气净化凝胶对甲醛的去除具有明显的效果,其去除原理为为阿伏加德罗常数的值。下列说法正确的是
A.含有的电子数目为
B.标准状况下,吸收转移电子数目为
C.的盐酸溶液中含有数目大于
D.冰中含有氢键数目为
5.有机物M是一种新型靶向药物,能够用作“分子胶水”将蛋白“黏住”,结构如图所示。下列关于M的说法错误的是
A.所有原子可能共平面
B.可能发生取代反应、加成反应、缩聚反应
C.分别与和反应,最多消耗二者的物质的量之比为
D.环上有8种一氯代物
6.下列实验操作能够验证实验目的的是
A.AB.BC.CD.D
7.大苏打是一种常见的硫代硫酸盐,在酸性溶液中会迅速分解生成乳白色浑浊和有刺激性气味的气体,反应的化学方程式为,分别为短周期元素,且原子序数依次增大。下列说法正确的是
A.简单离子半径:B.电负性:
C.简单氢化物沸点:D.最高价氧化物对应水化物的酸性:
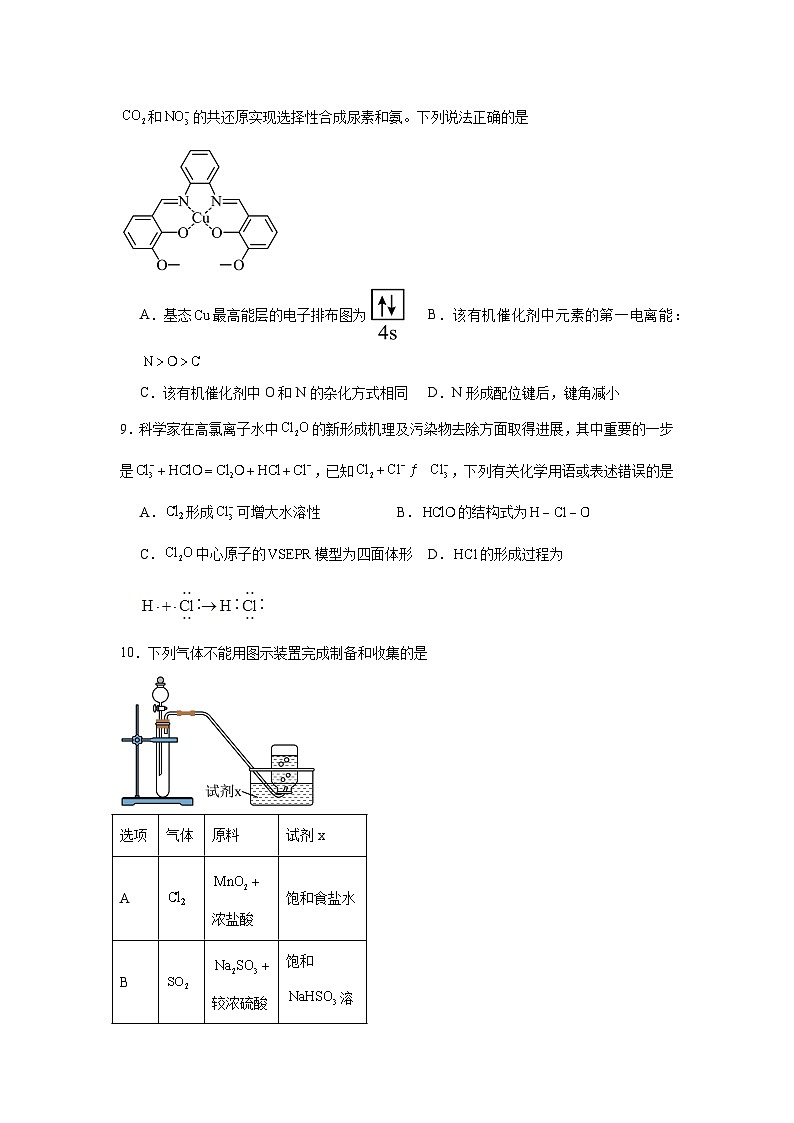
8.我国科学家成功研制出了一种铜基有机催化剂(结构如图所示),在常温常压条件下通过和的共还原实现选择性合成尿素和氨。下列说法正确的是
A.基态最高能层的电子排布图为B.该有机催化剂中元素的第一电离能:
C.该有机催化剂中O和N的杂化方式相同D.N形成配位键后,键角减小
9.科学家在高氯离子水中的新形成机理及污染物去除方面取得进展,其中重要的一步是,已知,下列有关化学用语或表述错误的是
A.形成可增大水溶性B.的结构式为
C.中心原子的模型为四面体形D.的形成过程为
10.下列气体不能用图示装置完成制备和收集的是
A.AB.BC.CD.D
11.,。向浓度均为的和混合溶液中逐滴加入的醋酸溶液,溶液电导率、随醋酸体积增加的变化趋势如图所示。已知,下列说法正确的是
A.a点,B.b点,
C.若d点,则D.水的电离程度:
12.半导体材料砷化铟是制备高速低功耗电子器件、红外光电子器件及自旋电子器件的理想材料。是ⅢA族元素,如图所示为的六方结构示意图,下列说法错误的是(设为阿伏加德罗常数的值)
A.两种元素均位于p区B.晶体中和的配位数均为4
C.晶体中两种原子之间存在配位键D.1个晶胞(平行六面体)的质量为
阅读以下材料,回答下列问题:
化石能源的过度开采和利用导致严重的环境问题和能源危机。可再生能源驱动的电催化还原产生高附加值有机物,可有效地实现碳中和能源转化。在众多的还原产物中,甲酸盐是电化学还原最具有市场竞争力和经济可行性的产物。开发高效的催化剂具有重要研究价值,铜是电还原反应生产多碳产物的唯一金属催化剂,氧化铜基催化剂能通过组成和结构工程调整目标产物的产率和选择性。
13.采用还原耦合甲醛氧化,可实现超低电压下两极同时制备甲酸盐。双极膜中间层的解离成和,通电时分别向两极迁移。下列说法错误的是
A.电极电势低于电极
B.阳极的电极反应式为
C.一段时间后,两电极室均减小
D.装置中生成时,双极膜内有解离
14.不同价态的位点电还原制反应机理如图所示。*表示吸附在催化剂表面,下列说法错误的是
A.0价位点催化还原的反应步骤与另两种价态位点的反应步骤不同,但总反应热效应相同
B.价位点催化还原反应过程中的速控步骤反应式为,生成了非极性键
C.产物从价位点表面解吸时放出的能量最少
D.适中的氧化态(价)是最有利的
二、解答题
15.碳酸亚铁不溶于水,可用作阻燃剂。已知在空气中,碳酸亚铁干燥品稳定,而湿品因被氧化为变成茶色。实验室中,可在还原性气氛中使用亚铁盐与碱金属碳酸盐制备碳酸亚铁,制备装置如图所示,反应体系均为水相。回答下列问题:
(1)仪器a和b的名称分别为 、 。
(2)向气密性良好的装置中添加药品。打开,关闭,待在m处检验到较纯净后, (填操作),再关闭,打开中出现白色浑浊。
(3)实验中铁粉和稀硫酸用量远高于理论值,原因是 。
(4)碳酸亚铁在潮湿空气中变茶色的化学方程式为 。
(5)碳酸亚铁在空气中受热发生反应,则碳酸亚铁可用作阻燃剂的原因是消耗、 、 、生成覆盖在燃烧物表面。
(6)某碳酸亚铁样品久置于空气中会部分变质生成为测定其纯度,称取样品,加入足量盐酸溶解并配成溶液。取配制好的溶液加入过量溶液充分反应,加入几滴淀粉溶液,再用标准溶液滴定,三次滴定平均消耗标准溶液,则样品中的质量分数为 %(用含V的代数式表示,已知)。
16.从钴锰渣(主要成分为)中提取钴并制备草酸钴的工艺流程如下:
已知:不溶于稀硫酸,可溶于稀硫酸。回答下列问题:
(1)钴原子的价层电子排布式为 ;“还原浸出”步骤中浸出率与用量的关系曲线如图所示,则钴锰渣中和二者物质的量较多的是 (填化学式),适宜的用量为 。该步骤发生的氧化还原反应的离子方程式分别是和 。
(2)沉钴渣的成分为 (填化学式),当恰好沉淀完全时,溶液中 。[保留两位有效数字,溶液中离子浓度时可认为沉淀完全,]
(3)“溶钴”时不能选用盐酸,原因是 。
(4)“氧化除锰”步骤中消耗的与生成的的物质的量之比为 ,还原性: (填“>”“R>Y>Z,A错误;
B.X为H,Y为O,Q为S,R为Cl,,同周期从左往,电负性依次增大;同族从上到下,电负性依次减小,则电负性:,即Y>R>Q>X,B错误;
C.Y为O,Q为S,水中存在氢键,故简单氢化物的沸点,,即Y>Q,C正确;
D.Q为S,R为Cl,非金属性,则最高价氧化物对应水化物的酸性:,即Q0.01ml/L, ,故A错误;
B.根据电荷守恒可知,b点,,,溶液呈碱性,故,因此,故B错误;
C.若d点,当=0.01时恰好完全中和,溶液中溶质为CH3COONa、CH3COONH4,,溶液呈碱性,若要pOH=7即中性,则应该醋酸的量增加,则,故C正确;
D.c点后,醋酸过量,电离出H+抑制水的电离,所以c>d,故D错误;
答案选C。
12.C
【详解】A.In是第49号元素,价电子排布5s25p1,As是第33号元素,价电子排布4s24p3,两种元素均位于p区,A正确;
B.In原子位于四个As原子形成的四面体的内部,所以In原子的配位数为4,,As原子位于四个In原子形成的四面体的内部,所以As原子的配位数为4,,B正确;
C.晶体中两种原子之间不存在配位键,C错误;
D.如图所示的晶胞中In原子在顶点、面心和内部,In原子的个数为个,As原子在棱上和内部,As原子的个数为个,1个晶胞(平行六面体)的质量为,D正确;
故选C。
13.D 14.C
【分析】左侧电极由→得电子,为阴极,电极反应为,右侧为阳极,电极反应为,据此分析;
13.A.为负极,电极电势低于电极(正极),A正确;
B.根据分析可知,阳极的电极反应式为,B正确;
C.一段时间后,甲酸酸性强于碳酸,则甲酸根水解程度小于碳酸氢根,左侧电极室减小,右侧两电极室小,C正确;
D.装置中生成时,转移1ml电子,双极膜内有解离,D错误;
故选D。
14.A.0价位点催化还原的反应步骤与另两种价态位点的反应步骤不同,0价经历了生成过程,但总反应热效应相同,A正确;
B.价位点催化还原反应过程中的速控步骤反应式为,因活化能最大,同时生成了非极性键,B正确;
C.产物从价位点表面解吸时吸收的能量最少,C错误;
D.适中的氧化态(价) 各过程能量壁垒较小,是最有利的,D正确;
故选C。
15.(1) 分液漏斗 三颈烧瓶
(2)将m插入装有水的烧杯中
(3)需要用Fe与稀硫酸生成H2排尽装置中的空气
(4)4FeCO3+6H2O+O2=4Fe(OH)3+4CO2
(5) 生成CO2,降低可燃物表面O2的浓度 吸收热量,降低可燃物的温度
(6)
【分析】A中稀硫酸与铁粉反应生成硫酸亚铁和氢气,打开活塞K1和K3,关闭活塞K2,生成的氢气将装置内原有的空气全部排出,待在m处检验到较纯净H2后,将m插入装有水的烧杯中,防止空气中的O2进入装置,随后关闭活塞K1、K3,打开活塞K2,生成的氢气将硫酸亚铁溶液压入B中,B中亚铁离子与碳酸根离子反应生成碳酸亚铁。
【详解】(1)由仪器的结构可知,a为分液漏斗,b为三颈烧瓶;
(2)由于碳酸亚铁潮湿品易被氧化,因此需隔绝空气,但装置中有H2,不能将m用止水夹夹住,故在确保H2已经将空气排尽后,将可延长橡胶管m插入装有水的烧杯中液封,防止空气中的O2进入装置;
(3)Fe与稀硫酸反应除了生成Fe2+与反应制备FeCO3之外,还需要用H2排尽装置中的空气并作为保护气,因此铁粉和稀硫酸用量远高于理论值;
(4)FeCO3在潮湿的空气中被氧化成Fe(OH)3,方程式为4FeCO3+6H2O+O2=4Fe(OH)3+4CO2;
(5)FeCO3在空气中反应可以生成CO2,CO2不支持燃烧,降低可燃物表面O2的浓度;该反应可以吸收热量,降低可燃物的温度,温度降到着火点以下后就不再燃烧;
(6)根据离子方程式,,可找出关系式:n(I-)=n()=n(Fe3+)=0.1mlL×V×10-3L= V×10-4ml,原固体中Fe(OH)3的质量为4×107V×10-4g=4.28V×10-2g,则样品中FeCO3的质量分数为×100%=%。
16.(1) 3d74s2 400
(2) 、
(3)盐酸会与高锰酸钾反应生成污染大气的氯气
(4) 2∶5
相关试卷
这是一份河北省邯郸市2025届高三年级第一次调研监测化学试题,共4页。
这是一份河北省邯郸市2025届高三上学期第一次调研考试一模+化学试题,共4页。
这是一份河北省邯郸市2024年高三下学期一模(第三次调研)考试化学试题(无答案),共9页。试卷主要包含了已知,物质的结构决定其性质等内容,欢迎下载使用。








