

重庆市南开中学校2025届高三上学期开学第一次质量检测化学试题
展开考生注意:
1.本试卷满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。必须在题号所指示的答题区域作答,超出答题区域书写的答案无效,在试题卷、草稿纸上答题无效。
可能用到的相对原子质:H-1 C-12 O-16 Mg-24 C1-35.5 Ca-40 Cu-64 I-127
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.近年来我国航空航天事业取得了很多令世界瞩目的成就。下列说法错误的是( )
A.液氢、液氧以及高氯酸铵等物质可应用于火箭推进剂
B.航天器表面防热材料所用的镍基合金熔点高于镍
C.月壤中发现的石墨烯与地球上的金刚石属于同素异形体
D.航天器使用的太阳能电池帆板的主要成分是多晶硅
2.下列表示正确的是( )
A.丙烯腈的结构简式:
B.肼的电子式:
C.的结构示意图:
D.二氯甲烷分子结构模型:
3.下列反应的离子方程式书写正确的是( )
A.铜与浓硝酸反应:
B.将通入烧碱溶液:
C.溶于醋酸:
D.过是氨水与硫酸铜溶液反应:
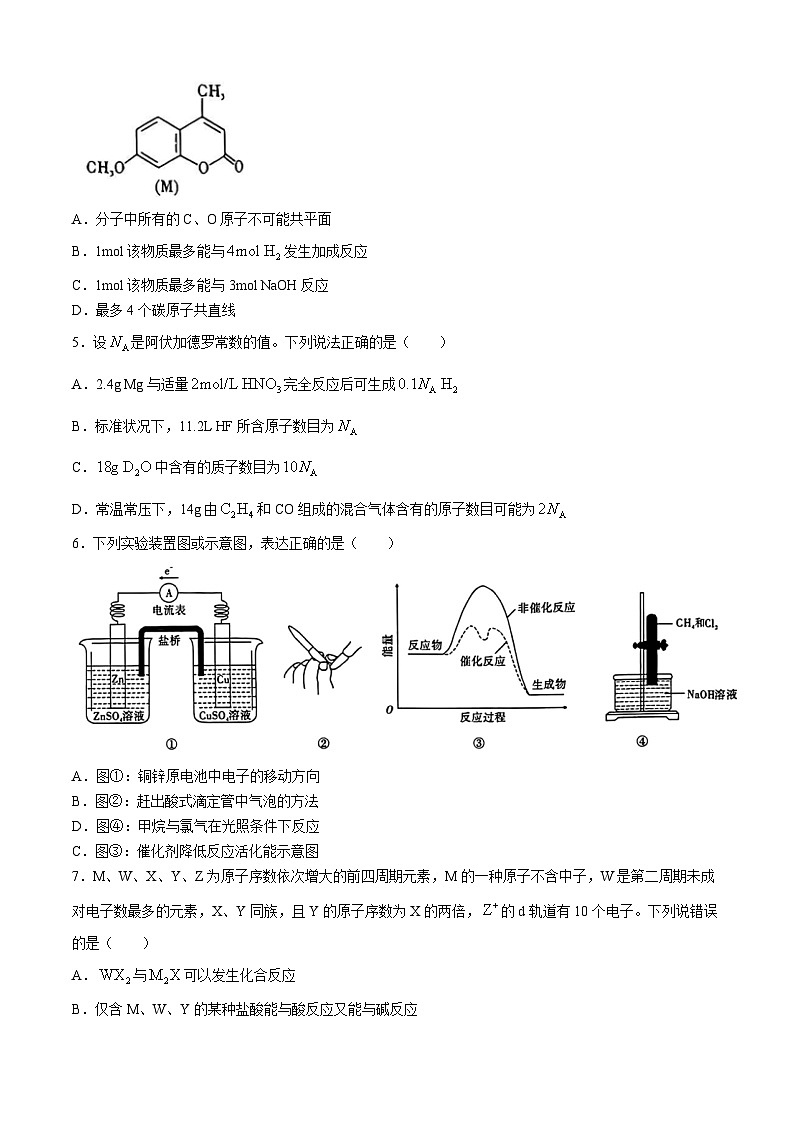
4.有机物M是合成抗过敏药物色甘酸钠的中间体,结构简式如题图。下列关于该有机物的说法正确的是( )
A.分子中所有的C、O原子不可能共平面
B.1ml该物质最多能与发生加成反应
C.1ml该物质最多能与3ml NaOH反应
D.最多4个碳原子共直线
5.设是阿伏加德罗常数的值。下列说法正确的是( )
A.2.4g Mg与适量完全反应后可生成
B.标准状况下,11.2L HF所含原子数目为
C.中含有的质子数目为
D.常温常压下,14g由和CO组成的混合气体含有的原子数目可能为
6.下列实验装置图或示意图,表达正确的是( )
A.图①:铜锌原电池中电子的移动方向
B.图②:赶出酸式滴定管中气泡的方法
D.图④:甲烷与氯气在光照条件下反应
C.图③:催化剂降低反应活化能示意图
7.M、W、X、Y、Z为原子序数依次增大的前四周期元素,M的一种原子不含中子,W是第二周期未成对电子数最多的元素,X、Y同族,且Y的原子序数为X的两倍,的d轨道有10个电子。下列说错误的是( )
A.与可以发生化合反应
B.仅含M、W、Y的某种盐酸能与酸反应又能与碱反应
C.第一电离能由大到小的顺序为
D.工业上可采用热还原法冶炼Z的单质
8.下列叙述错误的是( )
A.向含足量AgCl固体的悬浊液中加少量水,减小
B.醋酸钠溶液中离子浓度的关系满足
C.已知溶液呈酸性,则溶液中
D.除去酸性溶液中的,可在加热并搅拌条件下加入适量MgO
9.使用丙烯可将汽车尾气中的还原为除去。主要反应为( )
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
反应Ⅳ:
则为( )
A.B.C.D.
10.我国科学家在国际上率先用稻壳制备成高性能的电池级碳材料,该材料是多孔结构,有吸附作用导电性强。将该材料混合到传统铅酸蓄电池的铅电极中,即得到高性价比的铅碳电池。下列有关说法正确的是( )
A.比高性能碳活泼,故作铅碳电池的负极
B.传统铅酸蓄电池放电时的总反应为
C.传统铅酸蓄电池比能最高,对环境友好
D.铅碳电池可有效减缓电池的“负极硫酸盐化”,延长电池使用寿命
11.如题11图是一种Cu和Cl组成的二元化合物的晶胞示意图。该晶胞呈立方体结构,边长为apm。为阿伏加德罗常数的值,下列说法正确的是( )
A.该化合物的化学式为
B.晶体中的配位数为12
C.若图中A的原子坐标为,则B的原子坐标为
D.若CuCl晶体的密度为,则
12.下列实验操作、现象、结论都正确的是( )
13.利用含铑(Rh)配合物A将烯烃转化为醛的原理如题13图所示(L表示一种配体)。下列说法正确的是( )
A.若以异丁烯为原料,可以制得异丁醛
B.物质A和CO均为该反应的催化剂
C.步骤①和步骤③中,均有碳原子的杂化方式发生了改变
D.步骤④)中,使用代替反应一段时间,则所得醛中,D只会出现在醛基上
14.甲醇催化脱氢法制备甲酸甲酯时主要涉及如下反应:
I.
Ⅱ.
在400kPa、铜基催化剂存在下,向密闭容器中通入,平衡时部分气体物质的量分数随温度变化的情况如题14图所示。
下列说法正确的是( )
A.温度较低时,生成的CO较少,所以该反应的最适温度应低于400K
B.其他条件不变,压缩容器体积,达到新的平衡时的浓度减小
C.550K时,的平衡转化率为60%
D.550K时,反应Ⅰ的压强平衡常数
二、非选择题:本题共4小题,共58分。
15.(14分)俗称锑白,可用作白色颜料和阻燃剂。以辉锑矿(主要成分为)为原料干法制备较纯锑白的工艺流程如下:
已知:与具有相似的化学性质。
(1)基态S原子价电子轨道表示式为____________。
(2)Sb在元素周期表中位于第______周期第______族。
(3)“氧化炉”中主要反应的化学方程式为__________________。
(4)在空气中受热,会继续生成。与相似,可看作两种氧化物结合成的化合物,其中Sb的价态是______。
(5)在实验室中,可利用的水解反应制备。
①水解第一步生成白色沉淀SbOCl,写出该步反应的化学方程式__________________。
②为了得到更多的,操作时要将缓慢加入大量水中,反应后期还要加入少量氨水。用平衡移动原理说明这两项操作的作用____________________________________。
选用氨水而不用NaOH溶液的原因____________________________________(用化学方程式表示)
16.(15分)在食品和饲料添加剂中,广泛使用的补碘剂是。有良好化学稳定性,难溶于水和乙醇。制备的一种实验装置如题图(加热及夹持装置略)。
Ⅰ.的制备
将碘、氯酸钾、水依次加入三颈烧瓶,再滴入盐酸,使溶液。水浴温度保持在85℃充分反应,用导管把反应产生的黄绿色气体导入盛有NaOH液的烧杯中吸收。
Ⅱ.的制备
将三颈烧瓶中的溶液转入烧杯中,滴加KOH溶液,使溶液,再逐滴加入溶液,充分反应后,经抽滤洗涤得产品。
Ⅲ.的纯度测定
准确称取1.250g样品,用高酸溶解,定容至250mL,取出25.00ml试样于锥形瓶中,加入足量KI溶液充分反应。用0.1000ml/L硫代硫酸钠溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点。平行滴定三次,所测得实验数据如下:
已知:
(1)仪器C的名称为______。
(2)①步骤I中生成的化学方程式为____________。
②)步骤Ⅱ中,滴加入溶液时发生的化学方程式为____________。
(3)洗涤时,选用的试剂依次是水、无水乙醇,请从结构角度解释水和乙醇互溶的原因______。
(4)写出高氯酸在水中的电离方程式____________。
(5)该滴定实验达到终点的现象是________________________。
(6)①的纯度为______。
②)下列操作可能导致测定结果偏高的是______。
A.配制样品溶液时,容量瓶中液面超过刻度线
B.滴定管水洗后,未用硫代硫酸钠溶液润洗
C.滴定近终点时,用洗瓶冲洗锥形瓶内壁
D.滴定前俯视读数,滴定后仰视读数
17.(14分)2024年,北京大学吴凯团队和复旦大学刘智攀团队实现了利用AuPd合金催化低碳烯烃(如乙烯、丙烯和1-丁烯)的选择性断键产出乙炔。相关反应如下:
Ⅰ.
Ⅱ.
Ⅲ.
(1)反应Ⅰ在______(填“高温”“低温”或“任何温度”)下能自发进行。
(2)在密闭容器中充入丙烯发生反应Ⅱ,测得丙烯平衡转化率与温度、压强关系如题17-1图所示。则X代表______(填“温度”或“压强”),______(填“>”“<”或“=”)。
17-1
(3)在刚性密闭容器中充入乙烯和丙烯,恒温条件下发生反应Ⅰ的反应Ⅱ下列叙述正确的是______。
A.使用合适的催化剂后,活化分子百分比增大
B.每有,消耗的同时,有被消耗,说明反应已经达到平衡
C.平衡后,充入少量He,反应Ⅰ、Ⅱ平衡均正向移动
D.平衡后,充入少量,达到新的平衡时的浓度增大
(4)一定温度下,向体积为2L的密闭容器中加入催化剂和,发生反应亚和副反应Ⅳ:。初始压强为100kPa,经2min后反应达到平衡。测得平衡气体中的分压占总压的,的选择性S为80%( )。
2min内以表示的化学反应速率为______ml/(L·min),该温度下,反应亚的压强平衡常数为______kPa(表示用分压计算的平衡常数,分压=总压×物质的量分数)。
(5)原料1-丁烯可基于电化学原理,利用固体氧化物电解池实现正丁烷脱氢制备。装置如题17-2图所示。
17-2图
①可收集到的电极为______极,由生成的电极反应式为_________________________。
②电解过程中,会有副产物2-丁烯生成,通过调节电压可以控制反应速率和1-丁烯的选择性(所得丁烯中1-丁烯所占的物质的量之比)。根据表格数据判断,使用电压电解5min,比使用电压电解同样时间制得的-丁烯质量多______g(用含a的代数式表示)。
18.(15分)化合物J是一种苯丙胺类药物中间体,使用苯酚为原料合成J的一条合成路线如题图所示。
(1)化合物A的分子式为______,B的名称为______。
(2)化合物C的官能团名称为______。
(3)D→E的反应类型是______。
(4)C→D的化学方程式为______。
(5)E的同分异构体中,符合下列条件的有______种。
①含有对位二取代苯环的结构
②苯环上其中一个取代基为乙基
③含有酰胺基
其中,核磁共振氢谱图中含有五组峰的化合物的结构简式为____________。
(6)请参照上述合成路线,以环已酮()和必要的其他试剂为原料,制备药物中间体N-甲基环已胺盐酸盐()的合成路线____________________________________________________________。
重庆市高2025届高三第一次质量检测
化学试题参考答案与评分细则
一、选择题:本题共14小题,每小题3分,共42分。
1.B【解析】B项,镍基合金熔点低于镍。
2.D【解析】A项,内烯腈结构简式:;
B项,肼的电子式:
C项,的结构示意图:。
3.B【解析】A项,未满足得失电子守恒和电荷守恒;
C项,醋酸钙是易溶于水的强电解质,要拆开;
D项,过量氨水与硫酸铜反应会生成
4.B【解析】A项,C、O原子可能共平面;
C项.1ml该物质最多能与2ml NaOH反应;
D项,最多3个原子共线。
5.D【解析】A项,该反应不会生成;
B项,标准状况下,HF是液态;
C项,的物质的量不是1ml。
6.C【解析】A项,电子移动方向:从Zn到Cu;
B项,图为碱式滴定管排气泡的方法;
D项,水槽中应为饱和食盐水。
7.A【解析】M、W、X、Y、Z分別为H、N、O、S、Cu;
A项,反应为:,不是化合反应。
8.A【解析】A项,向含足量AgCl固体的悬浊液中加少量水,不变。
9.B【解析】根据盖斯定律,。
10.D【解析】A项,Pb作铅碳电池的负极;
B项,传统铅酸蓄电池放电总反应:;
C项,传统铅酸蓄电池的缺点是比能量低、笨重。且由于含有重金属、酸,随意丢弃会对生态环境和人体健康造成危害。
11.C【解析】A项,该化合物的化学式为CuCl;
B项,晶体中的配位数为4;
D项,。
12.B【解析】A项,常温Al与浓硝酸饨化;其他条件相同时,浓硝酸的氧化性大于稀硝酸;
C项,反应生成和HCl,是非氧化还原反应;
D项,蔗糖水解产物中有葡萄糖,该实验冷却后未调节溶液为碱性。
13.C【解析】A项,若以异丁烯为原料,可以制得异戊醛;
B项,CO是该反应的反应物;
D项,D不仅会出现在醛基上,还会在烃基上。
14.D【解析】A项,温度较低时,的转化率也低;
B项,其他条件不变,压缩容器体积,达到新的平衡时的浓度增大;
C项,550K时,的平衡转化率为47.4%。
二、非选择题:本题共4小题,共58分。
15.【答案】(每空2分,14分)
(1)
(2)5 VA(共2分,任错一个为0分)
(3)
(4)、
(5)①
②加入大量水的目的是降低的浓度,加氨水的目的是中和水解生成的HC1,使水解平衡正向移动,以此产生更多的
16.【答案】除标注外,每空2分,15分)
(1)恒压滴液漏斗(1分)
(2)①
②
(3)乙醇结构中的-OH与水分子中的-OH相近,满足“相似相溶”规律;乙醇与水分子之间可以形成氢键,会增大溶解性,因而乙醇与水互溶
(4)
(5)加入最后半滴标准液,溶液由蓝色变为无色,且30s不复原
(6)①78.00%
②BD
17.【答案】(除标注外,每空2分,14分)
(1)高温(1分)<(各1分)
(2)温度
(3)AD
(4)0.12532
(5)①阳(1分)
②1.12a
18.【答案】(除标注外,每空2分,15分)
(1) (1分)邻羟基苯甲醛(或2-羟基苯甲醛)
(2)醛基醚键
(3)还原反应(1分)
(4)
(5)12
(6)(3分)
选项
实验操作
现象
结论
A
常温下将铝片分别插入稀硝酸、浓硝酸中
前者产生无色气体,后者无明显现象
稀硝酸的氧化性比浓硝酸强
B
向沸水中逐滴加入5~6滴饱和溶液,持续煮沸
溶液先变成红褐色,再析出沉淀
先水解得胶体,再聚集成沉淀
C
向盛有10mL水的锥形瓶中滴加8~10滴
液面上有白雾形成,并有刺激性气味气体逸出
水与发生了氧化还原反应
D
取少量蔗糖溶液于试管中,滴加3~5滴稀硫酸,混合煮沸,冷却后加入银氨溶液水浴加热
试管中没有银镜产生
蔗糖的水解产物中没有葡萄糖
1
2
3
滴定起始读数/mL
1.18
1.45
0.98
滴定终点读数/mL
31.19
34.54
30.97
电压
消耗的速率
1-丁烯的选择性
a g/min
95%
1.8 ag/min
43%
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
选项
B
D
B
B
D
C
A
A
B
D
C
B
C
D
重庆市南开中学校2024-2025学年高三上学期第一次质量检测化学: 这是一份重庆市南开中学校2024-2025学年高三上学期第一次质量检测化学,文件包含2025届重庆南开中学高三上学期开学第一次质检化学试卷pdf、2025届重庆南开中学高三上学期开学第一次质检化学答案pdf等2份试卷配套教学资源,其中试卷共11页, 欢迎下载使用。
重庆市南开中学校2024-2025学年高三上学期第一次质量检测化学: 这是一份重庆市南开中学校2024-2025学年高三上学期第一次质量检测化学,文件包含2025届重庆南开中学高三上学期开学第一次质检化学试卷docx、2025届重庆南开中学高三上学期开学第一次质检化学试卷pdf、2025届重庆南开中学高三上学期开学第一次质检化学答案docx、2025届重庆南开中学高三上学期开学第一次质检化学答案pdf等4份试卷配套教学资源,其中试卷共22页, 欢迎下载使用。
2024届重庆市南开中学校高三上学期1月第五次质量检测化学试题: 这是一份2024届重庆市南开中学校高三上学期1月第五次质量检测化学试题,共9页。












