

2024年高考化学真题分类汇编10化学工艺流程综合含解析答案
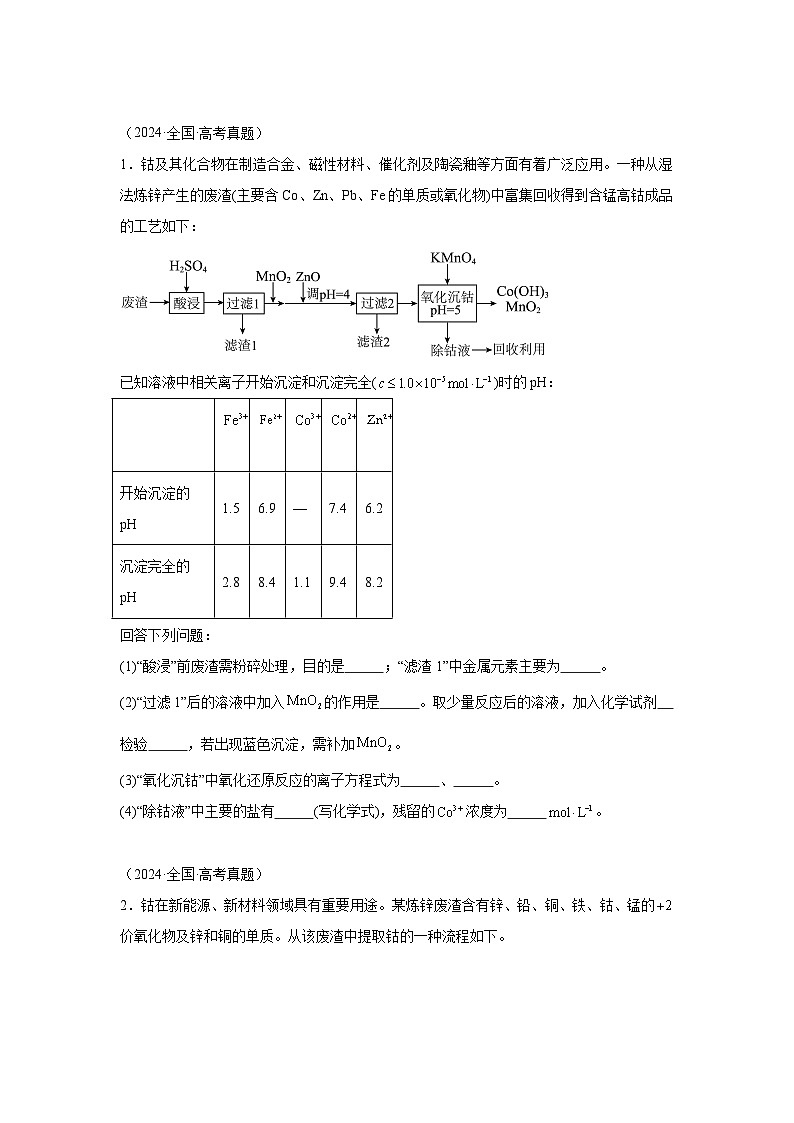
展开1.钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。一种从湿法炼锌产生的废渣(主要含C、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成品的工艺如下:
已知溶液中相关离子开始沉淀和沉淀完全()时的pH:
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是 ;“滤渣1”中金属元素主要为 。
(2)“过滤1”后的溶液中加入的作用是 。取少量反应后的溶液,加入化学试剂 检验 ,若出现蓝色沉淀,需补加。
(3)“氧化沉钴”中氧化还原反应的离子方程式为 、 。
(4)“除钴液”中主要的盐有 (写化学式),残留的浓度为 。
(2024·全国·高考真题)
2.钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
注:加沉淀剂使一种金属离子浓度小于等于,其他金属离子不沉淀,即认为完全分离。
已知:①。
②以氢氧化物形式沉淀时,和溶液的关系如图所示。
回答下列问题:
(1)“酸浸”前,需将废渣磨碎,其目的是 。
(2)“酸浸”步骤中,发生反应的化学方程式是 。
(3)假设“沉铜”后得到的滤液中和均为,向其中加入至沉淀完全,此时溶液中 ,据此判断能否实现和的完全分离 (填“能”或“不能”)。
(4)“沉锰”步骤中,生成,产生的物质的量为 。
(5)“沉淀”步骤中,用调,分离出的滤渣是 。
(6)“沉钴”步骤中,控制溶液,加入适量的氧化,其反应的离子方程式为 。
(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是 。
(2024·山东·高考真题)
3.以铅精矿(含,等)为主要原料提取金属和的工艺流程如下:
回答下列问题:
(1)“热浸”时,难溶的和转化为和及单质硫。溶解等物质的量的和时,消耗物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时挥发外,另一目的是防止产生 (填化学式)。
(2)将“过滤Ⅱ”得到的沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属,“电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为 。
(3)“还原”中加入铅精矿的目的是 。
(4)“置换”中可选用的试剂X为 (填标号)。
A. B. C. D.
“置换”反应的离子方程式为 。
(5)“电解II”中将富银铅泥制成电极板,用作 (填“阴极”或“阳极”)。
(2024·浙江·高考真题)
4.固态化合物Y的组成为,以Y为原料实现如下转化。
已知:与溶液A中金属离子均不能形成配合物。
请回答:
(1)依据步骤Ⅲ,、和中溶解度最大的是 。写出溶液C中的所有阴离子 。步骤Ⅱ中,加入的作用是 。
(2)下列说法正确的是_______。
A.气体D是形成酸雨的主要成分B.固体E可能含有
C.可溶于溶液D.碱性:
(3)酸性条件下,固体(微溶于水,其还原产物为无色的)可氧化为,根据该反应原理,设计实验验证Y中含有元素 ;写出转化为的离子方程式 。
(2024·浙江·高考真题)
5.矿物资源的综合利用有多种方法,如铅锌矿(主要成分为)的利用有火法和电解法等。
已知:①;
②电解前后总量不变;③易溶于水。
请回答:
(1)根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果,中硫元素体现的性质是 (选填“氧化性”、“还原性”、“酸性”、“热稳定性”之一)。产物B中有少量,该物质可溶于浓盐酸,元素转化为,写出该反应的化学方程式 ;从该反应液中提取的步骤如下:加热条件下,加入 (填一种反应试剂),充分反应,趁热过滤,冷却结晶,得到产品。
(2)下列说法正确的是_______。
A.电解池中发生的总反应是(条件省略)
B.产物B主要是铅氧化物与锌氧化物
C.化合物C在水溶液中最多可中和
D.的氧化性弱于
(3)D的结构为(或),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液探究X为何种元素。
①实验方案:取D的溶液,加入足量溶液,加热充分反应,然后 ;
②写出D(用表示)的溶液与足量溶液反应的离子方程式 。
(2024·江苏·高考真题)
6.回收磁性合金钕铁硼()可制备半导体材料铁酸铋和光学材料氧化钕。
(1)钕铁硼在空气中焙烧转化为、等(忽略硼的化合物),用盐酸酸浸后过滤得到溶液和含铁滤渣。Nd、Fe浸出率()随浸取时间变化如图所示。
①含铁滤渣的主要成分为 (填化学式)。
②浸出初期Fe浸出率先上升后下降的原因是 。
(2)含铁滤渣用硫酸溶解,经萃取、反萃取提纯后,用于制备铁酸铋。
①用含有机胺()的有机溶剂作为萃取剂提纯一定浓度的溶液,原理为:
(有机层)
已知:
其他条件不变,水层初始pH在0.2~0.8范围内,随水层pH增大,有机层中Fe元素含量迅速增多的原因是 。
②反萃取后,经转化可得到铁酸铋。铁酸铋晶胞如图所示(图中有4个Fe原子位于晶胞体对角线上,O原子未画出),其中原子数目比 。
(3)净化后的溶液通过沉钕、焙烧得到。
①向溶液中加入溶液,可转化为沉淀。该反应的离子方程式为 。
②将(摩尔质量为)在氮气氛围中焙烧,剩余固体质量随温度变化曲线如图所示。时,所得固体产物可表示为,通过以上实验数据确定该产物中的比值 (写出计算过程)。
(2024·河北·高考真题)
7.是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂从石煤中提取的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程如下。
已知:i石煤是一种含的矿物,杂质为大量和少量等;苛化泥的主要成分为等。
ⅱ高温下,苛化泥的主要成分可与反应生成偏铝酸盐;室温下,偏钒酸钙和偏铝酸钙均难溶于水。回答下列问题:
(1)钒原子的价层电子排布式为 ;焙烧生成的偏钒酸盐中钒的化合价为 ,产生的气体①为 (填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为 (填化学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为 ;加压导入盐浸工序可提高浸出率的原因为 ;浸取后低浓度的滤液①进入 (填工序名称),可实现钒元素的充分利用。
(4)洗脱工序中洗脱液的主要成分为 (填化学式)。
(5)下列不利于沉钒过程的两种操作为 (填序号)。
a.延长沉钒时间 b.将溶液调至碱性 c.搅拌 d.降低溶液的浓度
(2024·湖南·高考真题)
8.铜阳极泥(含有Au、、、等)是一种含贵金属的可再生资源,回收贵金属的化工流程如下:
已知:①当某离子的浓度低于时,可忽略该离子的存在;
② ;
③易从溶液中结晶析出;
④不同温度下的溶解度如下:
回答下列问题:
(1)Cu属于 区元素,其基态原子的价电子排布式为 ;
(2)“滤液1”中含有和,“氧化酸浸”时反应的离子方程式为 ;
(3)“氧化酸浸”和“除金”工序均需加入一定量的:
①在“氧化酸浸”工序中,加入适量的原因是 。
②在“除金”工序溶液中,浓度不能超过 。
(4)在“银转化”体系中,和浓度之和为,两种离子分布分数随浓度的变化关系如图所示,若浓度为,则的浓度为 。
(5)滤液4中溶质主要成分为 (填化学式);在连续生产的模式下,“银转化”和“银还原”工序需在℃左右进行,若反应温度过高,将难以实现连续生产,原因是 。
(2024·湖北·高考真题)
9.铍用于宇航器件的构筑。一种从其铝硅酸盐中提取铍的路径为:
已知:
回答下列问题:
(1)基态的轨道表示式为 。
(2)为了从“热熔、冷却”步骤得到玻璃态,冷却过程的特点是 。
(3)“萃取分液”的目的是分离和,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的现象是 。
(4)写出反萃取生成的化学方程式 。“滤液2”可以进入 步骤再利用。
(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是 。
(6)与醋酸反应得到某含4个的配合物,4个位于以1个O原子为中心的四面体的4个顶点,且每个的配位环境相同,与间通过相连,其化学式为 。
(2024·吉林·高考真题)
10.中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的颗粒被、包裹),以提高金的浸出率并冶炼金,工艺流程如下:
回答下列问题:
(1)北宋时期我国就有多处矿场利用细菌氧化形成的天然“胆水”冶炼铜,“胆水”的主要溶质为 (填化学式)。
(2)“细菌氧化”中,发生反应的离子方程式为 。
(3)“沉铁砷”时需加碱调节,生成 (填化学式)胶体起絮凝作用,促进了含微粒的沉降。
(4)“培烧氧化”也可提高“浸金”效率,相比“培烧氧化”,“细菌氧化”的优势为_______(填标号)。
A.无需控温B.可减少有害气体产生
C.设备无需耐高温D.不产生废液废渣
(5)“真金不怕火炼”,表明难被氧化,“浸金”中的作用为 。
(6)“沉金”中的作用为 。
(7)滤液②经酸化,转化为和的化学方程式为 。用碱中和可生成 (填溶质化学式)溶液,从而实现循环利用。
(2024·安徽·高考真题)
11.精炼铜产生的铜阳极泥富含等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
回答下列问题:
(1)位于元素周期表第 周期第 族。
(2)“浸出液1”中含有的金属离子主要是 。
(3)“浸取2”步骤中,单质金转化为的化学方程式为 。
(4)“浸取3”步骤中,“浸渣2”中的 (填化学式)转化为。
(5)“电沉积”步骤中阴极的电极反应式为 。“电沉积”步骤完成后,阴极区溶液中可循环利用的物质为 (填化学式)。
(6)“还原”步骤中,被氧化的与产物的物质的量之比为 。
(7)可被氧化为。从物质结构的角度分析的结构为(a)而不是(b)的原因: 。
(2024·甘肃·高考真题)
12.我国科研人员以高炉渣(主要成分为,,和等)为原料,对炼钢烟气(和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:
已知:
(1)高炉渣与经焙烧产生的“气体”是 。
(2)“滤渣”的主要成分是和 。
(3)“水浸2”时主要反应的化学方程式为 ,该反应能进行的原因是 。
(4)铝产品可用于 。
(5)某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞底面显示为图丙,晶胞参数。图丙中与N的距离为 ;化合物的化学式是 ,其摩尔质量为,阿伏加德罗常数的值是,则晶体的密度为 (列出计算表达式)。
开始沉淀的pH
1.5
6.9
—
7.4
6.2
沉淀完全的pH
2.8
8.4
1.1
9.4
8.2
温度/℃
0
20
40
60
80
溶解度/g
14.4
26.1
37.4
33.2
29.0
参考答案:
1.(1) 增大固液接触面积,加快酸浸速率,提高浸取效率 Pb
(2) 将溶液中的氧化为,以便在后续调pH时除去Fe元素 溶液
(3)
(4) 、
【分析】由题中信息可知,用硫酸处理含有C、Zn、Pb、Fe的单质或氧化物的废渣,得到含有、、、、等离子的溶液,Pb的单质或氧化物与硫酸反应生成难溶的,则“滤渣1”为“酸浸”时生成的;向滤液中加入将氧化为,然后加入ZnO调节pH=4使完全转化为,则“滤渣Ⅱ”的主要成分为,滤液中的金属离子主要是、和;最后“氧化沉钴”,加入强氧化剂,将溶液中氧化为,在时形成沉淀,而则被还原为,还会与溶液中的发生归中反应生成,得到和的混合物,“除钴液”主要含有ZnSO4、K2SO4,据此解答。
【详解】(1)在原料预处理过程中,粉碎固体原料能增大固体与液体的接触面积,从而加快酸浸的反应速率,提高浸取效率;由分析可知,“滤渣1”的主要成分为PbSO4,则“滤渣1”中金属元素主要为Pb;
(2)酸浸液中含有、、、、等离子。由题表中数据可知,当完全沉淀时,未开始沉淀,而当完全沉淀时,已有一部分沉淀,因此为了除去溶液中的Fe元素且不沉淀,应先将氧化为,然后调节溶液的pH使完全水解转化为沉淀,因此,的作用是将氧化为,以便在后续调pH时除去Fe元素。常用溶液检验,若生成蓝色沉淀,则说明溶液中仍存在,需补加;
(3)由分析可知,该过程发生两个氧化还原反应,根据分析中两个反应的反应物、产物与反应环境(),结合得失电子守恒、电荷守恒和原子守恒可写出两个离子方程式:、;
(4)最终得到的“除钴液”中含有的金属离子主要是最初“酸浸”时与加入ZnO调pH时引入的、加入“氧化沉钴”时引入的,而阴离子是在酸浸时引入的,因此其中主要的盐有和。当溶液时,恰好完全沉淀,此时溶液中,则,则。“除钴液”的,即,则,此时溶液中。
2.(1)增大固体与酸反应的接触面积,提高钴元素的浸出效率
(2)
(3) 不能
(4)
(5)
(6)
(7)向滤液中滴加溶液,边加边搅拌,控制溶液的pH接近12但不大于12,静置后过滤、洗涤、干燥
【分析】炼锌废渣含有锌、铅、铜、铁、钴、锰的价氧化物及锌和铜的单质,经稀硫酸酸浸时,铜不溶解,Zn及其他价氧化物除铅元素转化为硫酸铅沉淀外,其他均转化为相应的+2价阳离子进入溶液;然后通入硫化氢沉铜生成CuS沉淀;过滤后,滤液中加入Na2S2O8将锰离子氧化为二氧化锰除去,同时亚铁离子也被氧化为铁离子;再次过滤后,用氢氧化钠调节pH=4,铁离子完全转化为氢氧化铁沉淀除去;第三次过滤后的滤液中加入次氯酸钠沉钴,得到C(OH)3。
【详解】(1)“酸浸”前,需将废渣磨碎,其目的是增大固体与酸反应的接触面积,提高钴元素的浸出效率。
(2)“酸浸”步骤中,Cu不溶解,Zn单质及其他价氧化物除铅元素转化为硫酸铅沉淀外,其他均转化为相应的+2价阳离子进入溶液,即为转化为CSO4,反应的化学方程式为。
(3)假设“沉铜”后得到的滤液中和均为,向其中加入至沉淀完全,此时溶液中,则,小于,说明大部分也转化为硫化物沉淀,据此判断不能实现Zn2+和C2+的完全分离。
(4)“沉锰”步骤中,Na2S2O8将Mn2+氧化为二氧化锰除去,发生的反应为,因此,生成,产生的物质的量为。
(5)“沉锰”步骤中,同时将氧化为,“沉淀”步骤中用调pH=4,可以完全沉淀为,因此,分离出的滤渣是。
(6)“沉钴”步骤中,控制溶液pH=5.0~5.5,加入适量的NaClO氧化,为了保证被完全氧化,NaClO要适当过量,其反应的离子方程式为。
(7)根据题中给出的信息,“沉钴”后的滤液的pH=5.0~5.5,溶液中有元素以形式存在,当pH>12后氢氧化锌会溶解转化为,因此,从“沉钴”后的滤液中回收氢氧化锌的方法是:向滤液中滴加溶液,边加边搅拌,控制溶液的pH接近12但不大于12,静置后过滤、洗涤、干燥。
3.(1) 1:1 H2S
(2)热浸
(3)将过量的Fe3+还原为Fe2+
(4) C
(5)阳极
【分析】本题以铅精矿(含,等)为主要原料提取金属和, “热浸”时,难溶的和转化为和及单质硫,被还原为Fe2+,过滤I除掉单质硫滤渣,滤液中在稀释降温的过程中转化为PbCl2沉淀,然后用饱和食盐水热溶,增大氯离子浓度,使PbCl2又转化为,电解得到Pb;过滤II后的滤液成分主要为、FeCl2、FeCl3,故加入铅精矿主要将FeCl3还原为FeCl2,试剂X将置换为Ag,得到富银铅泥,试剂X为铅,尾液为FeCl2。
【详解】(1)“热浸”时,将和中-2价的硫氧化为单质硫,被还原为Fe2+,在这个过程中Pb和Ag的化合价保持不变,所以等物质的量的和时,S2-物质的量相等,所以消耗的物质的量相等,比值为1:1;溶液中盐酸浓度过大,这里主要考虑氢离子浓度会过大,会生成H2S 气体。
(2)“过滤Ⅱ”得到的沉淀反复用饱和食盐水热溶,会溶解为,电解溶液制备金属,在阴极产生,阳极Cl-放电产生Cl2, 尾液成分为FeCl2,FeCl2吸收Cl2后转化为FeCl3,可以在热浸中循环使用。
(3)过滤Ⅱ所得的滤液中有过量的未反应的Fe3+,根据还原之后可以得到含硫滤渣,“还原”中加入铅精矿的目的是将过量的Fe3+还原为Fe2+。
(4)“置换”中加入试剂X可以可以得到富银铅泥,为了防止引入其他杂质,则试剂X应为Pb,发生的反应为:。
(5)“电解II”中将富银铅泥制成电极板,电解Ⅱ得到金属银和金属铅,将银和铅分离出来,所以不可能作为阴极,应作为阳极板,阳极放电时,银变成阳极泥而沉降下来,铅失电子为Pb2+,阴极得电子得到Pb,所以电极板应作阳极。
4.(1) MgCO3 、、OH-、Cl- 调节溶液pH值,防止钙离子、镁离子、锰离子转化为氢氧化物的沉淀
(2)BC
(3) 取一定量Y于试管中,加入适量硝酸溶解,再加入适量NaBiO3,观察到溶液变为紫红色,则证明Y中含有锰元素
【分析】Y中加入盐酸将碳酸根转化为二氧化碳,溶液A中主要有镁离子、锰离子、钙离子、亚铁离子,氯离子,若酸过量,还有H+,加入氨气和氯化铵将亚铁离子转化为氢氧化亚铁,溶液B中主要含有镁离子、锰离子、钙离子、铵根离子,氯离子,Ⅲ中又通入CO2将钙离子与锰离子转化为沉淀,据此回答。
【详解】(1)①MnCO3、CaCO3 和 MgCO3是同种类型的沉淀,溶解度大的最后沉淀出来,由于通入二氧化碳,生成的沉淀是CaCO3 和 MgCO3,所以 MgCO3溶解度最大;
②溶液中加入盐酸引入阴离子氯离子,Ⅲ中又通入CO2引入碳酸根离子,溶液中还有碳酸氢根和氢氧根;
(2)A.气体是CO2不是形成酸雨的主要成分,故A错误;
B.固体E可能含有Na2CO3,当二氧化碳过量时反应方程式为:,当二氧化碳少量时,所以可能含有Na2CO3,故B正确;
C.Mn(OH)2可溶于NH4Cl溶液,由于NH4Cl溶液呈酸性,NH4Cl水解产生的H+与Mn(OH)2反应,故C正确;
D.碱性是Ca(OH)2>Fe(OH)2,氢氧化钙是强碱,氢氧化亚铁是弱碱,故D错误;
故选BC。
(3)①酸性条件下,固体NaBiO3可氧化Mn2+为,取一定量Y于试管中,加入适量硝酸溶解,再加入适量NaBiO3,观察到溶液变为紫红色,则证明Y中含有锰元素;
②根据题目信息可知。
5.(1) 还原性 Pb3O4+14HCl(浓)=+4H2O+Cl2↑ PbO或Pb(OH)2或PbCO3
(2)AB
(3) 加入足量Ba(NO3)2溶液充分反应,静置后取上层清液,再加入硝酸酸化的AgNO3溶液,若产生白色沉淀,则有Cl-,反之则有F- H++SO3X-+3OH-=+X-+2H2O
【分析】
铅锌矿(主要成分为)富氧煅烧得到SO2和Pb、Zn元素的氧化物,SO2与等物质的量的ClF反应得到化合物C,结构简式为,化合物C()水解生成液态化合物D(,X=F或Cl)和气态化合物E(HCl或HF)。
【详解】(1)根据富氧煅烧和通电电解的结果,中硫元素化合价升高,体现的性质是还原性。产物B中有少量,该物质可溶于浓盐酸,元素转化为,该反应的化学方程式:Pb3O4+14HCl(浓)=+4H2O+Cl2↑;根据可得反应:,要从该反应液中提取,则所加试剂应能消耗H+使平衡逆向移动,且不引入杂质,则步骤为:加热条件下,加入PbO或Pb(OH)2或PbCO3,充分反应,趁热过滤,冷却结晶;
(2)A. 根据图示和已知②可知,电解池中阳极上Fe2+生成Fe3+,Fe3+氧化PbS生成S、Pb2+和Fe2+,阴极上PbCl2生成Pb,发生的总反应是:(条件省略),A正确;
B. 据分析,铅锌矿(主要成分为)富氧煅烧得到SO2和Pb、Zn元素的氧化物,则产物B主要是铅氧化物与锌氧化物,B正确;
C. 据分析,化合物C是,卤素原子被-OH取代后生成H2SO4和HCl、HF,则化合物C在水溶液中最多可中和4mlNaOH,C错误;
D. 的氧化性由+1价的Cl表现,Cl2的氧化性由0价的Cl表现,则ClF的氧化锌强于,D错误;
故选AB。
(3)
①D的结构为(X=F或Cl),加入足量NaOH溶液,加热充分反应,生成Na2SO4和NaX,则实验方案为:取D的溶液,加入足量NaOH溶液,加热充分反应,然后加入足量Ba(NO3)2溶液充分反应,静置后取上层清液,再加入硝酸酸化的AgNO3溶液,若产生白色沉淀,则有Cl-,反之则有F-;
②D(用HSO3X表示)的溶液与足量NaOH溶液反应生成Na2SO4和NaX,HSO3X为强电解质,需要拆开,发生反应的离子方程式为H++SO3X-+3OH-=+X-+2H2O。
6.(1) Fe2O3 浸出初期,c(H+)较大,Fe2O3溶解使铁的浸出率升高,一段时间后,溶液酸性减弱,水解生成沉淀,使铁的浸出率下降
(2) 随水层pH增大,的浓度减小,的化学平衡向正反应方向移动,的化学平衡逆向移动,该平衡逆向移动引起浓度的增大,进一步促进萃取平衡向萃取方向移动,导致的浓度增大,因此,有机层中Fe元素含量迅速增多 2:1
(3) 2:1
【详解】(1)①由图可知,Fe的浸出率比Nd的浸出率低很多,因此大多数铁元素在浸取过程中以氧化铁的形式存在,则含铁滤渣的主要成分是未反应的Fe2O3;
②浸出初期Fe浸出率先上升后下降的原因是:浸出初期,Fe2O3溶解,Fe的浸出率增大,一段时间后随着Nd的浸出率增大,溶液中的的浓度逐渐减小,逐渐增大导致水解生成进入滤渣,Fe的浸出率又减小。
(2)①减小生成物浓度,化学平衡向正反应方向移动,因此,其他条件不变,水层初始pH在0.2~0.8范围内,随水层pH增大,的浓度减小,的化学平衡向正反应方向移动,又的浓度减小使平衡逆向移动,引起浓度的增大,进一步促进平衡向萃取方向移动,导致的浓度增大,因此,有机层中Fe元素含量迅速增多。
②由铁酸铋晶胞结构示意图可知,晶胞中体内有4个Fe原子,面上有8个Fe原子,根据均摊法可知,Fe原子的数目为;原子全部在晶胞的面上,共有,因此,其中原子数目比2:1。
(3)①向溶液中加入溶液,和相互促进对方水解生成沉淀和,该反应的离子方程式为。
②的物质的量为,其在氮气氛围中焙烧后,金属元素的质量和化合价均保持不变,因此,=;时剩余固体的质量为7.60,固体减少的质量为,由于碱式盐在受热分解时易变为正盐,氢氧化物分解得到氧化物和,碳酸盐分解得到氧化物和,因此,可以推测固体变为时失去的质量是生成和的质量;根据H元素守恒可知,固体分解时生成的质量为,则生成的质量为-=,则生成的物质的量为,由C元素守恒可知,分解后剩余的的物质的量为4×10-5ml-=,因此可以确定该产物中的比值为。
7.(1)
(2)
(3) 提高溶液中浓度,促使偏钒酸钙转化为碳酸钙,释放 离子交换
(4)
(5)bd
【分析】石煤和苛化泥通入空气进行焙烧,反应生成、、、、和等,水浸可分离焙烧后的可溶性物质(如)和不溶性物质[、等],过滤后滤液进行离子交换、洗脱,用于富集和提纯,加入氯化铵溶液沉钒,生成,经一系列处理后得到V2O3;滤渣①在,的条件下加入3%NH4HCO3溶液进行盐浸,滤渣①中含有钒元素,通过盐浸,使滤渣①中的钒元素进入滤液①中,再将滤液①回流到离子交换工序,进行的富集。
【详解】(1)钒是23号元素,其价层电子排布式为;焙烧过程中,氧气被还原,被氧化生成,偏钒酸盐中钒的化合价为价;在以上开始分解,生成的气体①为。
(2)由已知信息可知,高温下,苛化泥的主要成分与反应生成偏铝酸钠和偏铝酸钙,偏铝酸钠溶于水,偏铝酸钙难溶于水,所以滤液中杂质的主要成分是。
(3)在弱碱性环境下,与和反应生成、和,离子方程式为:; CO2加压导入盐浸工序可提高浸出率,因为C可提高溶液中浓度,促使偏钒酸钙转化为碳酸钙,释放;滤液①中含有、等,且浓度较低,若要利用其中的钒元素,需要通过离子交换进行分离、富集,故滤液①应进入离子交换工序。
(4)由离子交换工序中树脂的组成可知,洗脱液中应含有,考虑到水浸所得溶液中含有,为避免引人其他杂质离子,且廉价易得,故洗脱液的主要成分应为。
(5)a.延长沉钒时间,能使反应更加完全,有利于沉钒,a不符合题意;
b.呈弱酸性,如果将溶液调至碱性,与反应,不利于生成,b符合题意;
c.搅拌能使反应物更好的接触,提高反应速率,使反应更加充分,有利于沉钒,c不符合题意;
d.降低溶液的浓度,不利于生成,d符合题意;
故选bd。
8.(1) ds 3d104s1
(2)
(3) 使银元素转化为AgCl沉淀 0.5
(4)0.05
(5) 高于40℃后,的溶解度下降,“银转化”和“银还原”的效率降低,难以实现连续生产
【分析】铜阳极泥(含有Au、Ag2Se、Cu2Se、PbSO4等)加入H2O2、H2SO4、NaCl氧化酸浸,由题中信息可知,滤液1中含有Cu2+和H2SeO3,滤渣1中含有Au、AgCl、PbSO4;滤渣1中加入NaClO、H2SO4、NaCl,将Au转化为Na[AuCl4]除去,滤液2中含有Na[AuCl4],滤渣2中含有AgCl、PbSO4;在滤渣2中加入Na2SO3,将AgCl转化为Ag2SO3,过滤除去PbSO4,滤液3含有Ag2SO3;滤液2中加入Na2S2O4,将Ag元素还原为Ag单质,Na2S2O4转化为Na2SO3,滤液4中溶质主要为Na2SO3,可继续进行银转化过程。
【详解】(1)Cu的原子序数为29,位于第四周期第ⅠB族,位于ds区,其基态原子的价电子排布式为3d104s1;
(2)滤液1中含有Cu2+和H2SeO3,氧化酸浸时Cu2Se与H2O2、H2SO4发生氧化还原反应,生成、和,反应的离子方程式为:;
(3)①在“氧化酸浸”工序中,加入适量的原因是使银元素转化为AgCl沉淀;
②由题目可知,在“除金”工序溶液中,若加入过多,AgCl则会转化为,当某离子的浓度低于1.0×10−5ml⋅L−1时,可忽略该离子的存在,为了不让AgCl发生转化,则另,由,可得,即浓度不能超过;
(4)在“银转化”体系中,和浓度之和为,溶液中存在平衡关系:,当时,此时,则该平衡关系的平衡常数,当时,,解得此时;
(5)由分析可知滤液4中溶质主要成分为Na2SO3;由不同温度下的溶解度可知,高于40℃后,的溶解度下降,“银转化”和“银还原”的效率降低,难以实现连续生产。
9.(1)
(2)快速冷却
(3)先产生白色沉淀,后白色沉淀快速溶解
(4) 反萃取
(5)增强熔融氯化铍的导电性
(6)
【分析】本题是化工流程的综合考察,首先铝硅酸盐先加热熔融,然后快速冷却到其玻璃态,再加入稀硫酸酸浸过滤,滤渣的成分为H2SiO3,“滤液1”中有Be2+和Al3+,加入含HA的煤油将Be2+萃取到有机相中,水相1中含有Al3+,有机相为,加入过量氢氧化钠反萃取Be2+使其转化为进入水相2中,分离出含NaA的煤油,最后对水相2加热过滤,分离出Be(OH)2,通过系列操作得到金属铍,据此回答。
【详解】(1)
基态Be2+的电子排布式为1s2,其轨道表达式为。
(2)熔融态物质冷却凝固时,缓慢冷却会形成晶体,快速冷却会形成非晶态,即玻璃态,所以从“热熔、冷却”中得到玻璃态,其冷却过程的特点为:快速冷却。
(3)“滤液1”中有Be2+和Al3+,加入含HA的煤油将Be2+萃取到有机相中,则水相1中含有Al3+,则向过量烧碱的溶液中逐滴加入少量水相1的溶液,可观察到的现象为:先产生白色沉淀,后白色沉淀快速溶解。
(4)反萃取生成的化学方程式为,滤液2的主要成分为NaOH,可进入反萃取步骤再利用。
(5)氯化铍的共价性较强,电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用为增强熔融氯化铍的导电性。
(6)由题意可知,该配合物中有四个铍位于四面体的四个顶点上,四面体中心只有一个O,Be与Be之间总共有六个CH3COO-,则其化学式为:。
10.(1)CuSO4
(2)
(3)
(4)BC
(5)做络合剂,将Au转化为从而浸出
(6)作还原剂,将还原为Au
(7) NaCN
【分析】矿粉中加入足量空气和H2SO4,在pH=2时进行细菌氧化,金属硫化物中的S元素转化为硫酸盐,过滤,滤液中主要含有Fe3+、、As(Ⅵ),加碱调节pH值,Fe3+转化为胶体,可起到絮凝作用,促进含As微粒的沉降,过滤可得到净化液;滤渣主要为Au,Au与空气中的O2和NaCN溶液反应,得到含的浸出液,加入Zn进行“沉金”得到Au和含的滤液②。
【详解】(1)“胆水”冶炼铜,“胆水”的主要成分为CuSO4;
(2)“细菌氧化”的过程中,FeS2在酸性环境下被O2氧化为Fe3+和,离子方程式为:;
(3)“沉铁砷”时,加碱调节pH值,Fe3+转化为胶体,可起到絮凝作用,促进含As微粒的沉降;
(4)A.细菌的活性与温度息息相关,因此细菌氧化也需要控温,A不符合题意;
B.焙烧氧化时,金属硫化物中的S元素通常转化为SO2,而细菌氧化时,金属硫化物中的S元素转化为硫酸盐,可减少有害气体的产生,B符合题意;
C.焙烧氧化需要较高的温度,因此所使用的设备需要耐高温,而细菌氧化不需要较高的温度就可进行,设备无需耐高温,C符合题意;
D.由流程可知,细菌氧化也会产生废液废渣,D不符合题意;
故选BC;
(5)“浸金”中,Au作还原剂,O2作氧化剂,NaCN做络合剂,氰化钠能够与金离子形成稳定的络合物从而提升金单质的还原性,将Au转化为从而浸出;
(6)“沉金”中Zn作还原剂,将还原为Au;
(7)滤液②含有,经过H2SO4的酸化,转化为ZnSO4和HCN,反应得化学方程式为:;用碱中和HCN得到的产物,可实现循环利用,即用NaOH中和HCN生成NaCN,NaCN可用于“浸金”步骤,从而循环利用。
11.(1) 四 ⅠB
(2)Cu2+
(3)
(4)AgCl
(5)
(6)3:4
(7)(a)结构中电子云分布较均衡,结构较为稳定,(b)结构中正负电荷中心不重合,极性较大,较不稳定,且存在过氧根,过氧根的氧化性大于I2,故Na2S2O3不能被I2氧化成(b)结构
【分析】精炼铜产生的铜阳极泥富含Cu、Ag、Au等元素,铜阳极泥加入硫酸、H2O2浸取,Cu被转化为Cu2+进入浸取液1中,Ag、Au不反应,浸渣1中含有Ag和Au;浸渣1中加入盐酸、H2O2浸取,Au转化为HAuCl4进入浸取液2,Ag转化为AgCl,浸渣2中含有AgCl;浸取液2中加入N2H4将HAuCl4还原为Au,同时N2H4被氧化为N2;浸渣2中加入,将AgCl转化为,得到浸出液3,利用电沉积法将还原为Ag。
【详解】(1)Cu的原子序数为29,位于第四周期第ⅠB族;
(2)由分析可知,铜阳极泥加入硫酸、H2O2浸取,Cu被转化为Cu2+进入浸取液1中,故浸取液1中含有的金属离子主要是Cu2+;
(3)浸取2步骤中,Au与盐酸、H2O2反应氧化还原反应,生成HAuCl4和H2O,根据得失电子守恒及质量守恒,可得反应得化学方程式为:;
(4)根据分析可知,浸渣2中含有AgCl,与反应转化为;
(5)电沉积步骤中,阴极发生还原反应,得电子被还原为Ag,电极反应式为:;阴极反应生成,同时阴极区溶液中含有Na+,故电沉积步骤完成后,阴极区溶液中可循环利用得物质为;
(6)还原步骤中, HAuCl4被还原为Au,Au化合价由+3价变为0价,一个HAuCl4转移3个电子,N2H4被氧化为N2,N的化合价由-2价变为0价,一个N2H4转移4个电子,根据得失电子守恒,被氧化的N2H4与产物Au的物质的量之比为3:4;
(7)(a)结构中电子云分布较均衡,结构较为稳定,(b)结构中正负电荷中心不重合,极性较大,较不稳定,且存在过氧根,过氧根的氧化性大于I2,故Na2S2O3不能被I2氧化成(b)结构。
12.(1)NH3
(2)SiO2
(3) ,微溶的硫酸钙转化为更难溶的碳酸钙
(4)净水
(5) Ca3N3B
【分析】高炉渣(主要成分为,,和等)加入在400℃下焙烧,生成硫酸钙、硫酸镁、硫酸铝,同时产生气体,该气体与烟气(和水蒸气)反应,生成,所以该气体为NH3;焙烧产物经过水浸1,然后过滤,滤渣为以及未反应的SiO2,滤液溶质主要为硫酸镁、硫酸铝及硫酸铵;滤液浓缩结晶,析出,剩余富镁溶液;滤渣加入溶液,滤渣中的会转化为更难溶的碳酸钙。
【详解】(1)由分析可知,高炉渣与经焙烧产生的“气体”是NH3;
(2)由分析可知,“滤渣”的主要成分是和未反应的SiO2;
(3)“水浸2”时主要反应为硫酸钙与碳酸铵生成更难溶的碳酸钙,反应方程式为,该反应之所以能发生,是由于,,,微溶的硫酸钙转化为更难溶的碳酸钙;
(4)铝产品溶于水后,会产生,水解生成胶体,可用于净水;
(5)图丙中,Ca位于正方形顶点,N位于正方形中心,故与N的距离为pm;由均摊法可知,晶胞中Ca的个数为,N的个数为,B的个数为,则化合物的化学式是Ca3N3B;其摩尔质量为,阿伏加德罗常数的值是,晶胞体积为则晶体的密度为。
2024年高考化学真题分类汇编16化学实验综合含解析答案: 这是一份2024年高考化学真题分类汇编16化学实验综合含解析答案,共28页。试卷主要包含了可用于合成光电材料,某小组采用如下实验流程制备,亚铜配合物广泛用作催化剂等内容,欢迎下载使用。
2024年高考化学真题分类汇编09化学反应原理综合含解析答案: 这是一份2024年高考化学真题分类汇编09化学反应原理综合含解析答案,共33页。试卷主要包含了丙烯腈是一种重要的化工原料,已知等内容,欢迎下载使用。
专题12 工艺流程综合题-三年(2022-2024)高考化学真题分类汇编(全国通用)(含解析): 这是一份专题12 工艺流程综合题-三年(2022-2024)高考化学真题分类汇编(全国通用)(含解析),共93页。












