福建省龙岩市连城县第一中学2024-2025学年高三上学期开学考试化学试题
展开可能用到的相对原子质量:H-1 B-11 C-12 F-19 K-39 Ca-40
一、选择题(每小题只有一个选项符合题意,每题3分,共14题,共42分)
1.下列有关食品的说法错误的是( )
A.面条的主要成分为淀粉
B.牛肉丸蒸煮过程中蛋白质发生变性
C.烤鸭富含油脂,油脂能发生水解反应
D.杏鲍菇中富含的氨基酸属于天然高分子化合物
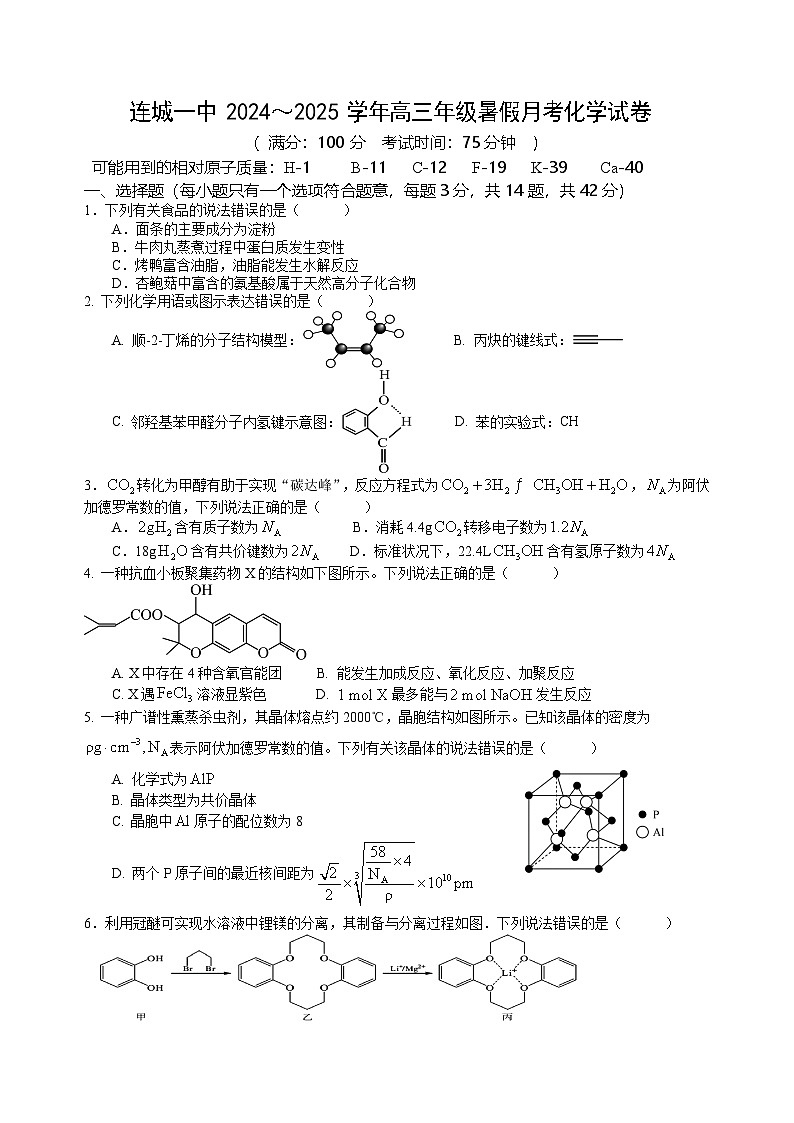
2. 下列化学用语或图示表达错误的是( )
A. 顺-2-丁烯的分子结构模型: B. 丙炔的键线式:
C. 邻羟基苯甲醛分子内氢键示意图: D. 苯的实验式:CH
3.转化为甲醇有助于实现“碳达峰”,反应方程式为,为阿伏加德罗常数的值,下列说法正确的是( )
A.含有质子数为 B.消耗4.4g转移电子数为
C.18g含有共价键数为 D.标准状况下,22.4L含有氢原子数为
4. 一种抗血小板聚集药物X的结构如下图所示。下列说法正确的是( )
A. X中存在4种含氧官能团 B. 能发生加成反应、氧化反应、加聚反应
C. X遇溶液显紫色 D. 最多能与发生反应
5. 一种广谱性熏蒸杀虫剂,其晶体熔点约2000℃,晶胞结构如图所示。已知该晶体的密度为表示阿伏加德罗常数的值。下列有关该晶体的说法错误的是( )
A. 化学式为
B. 晶体类型为共价晶体
C. 晶胞中原子的配位数为8
D. 两个P原子间的最近核间距为
6.利用冠醚可实现水溶液中锂镁的分离,其制备与分离过程如图.下列说法错误的是( )
甲→乙的反应类型为取代反应
B.丙中通过共价键与O原子结合
C.甲、乙、丙中仅有一种物质属于超分子
D.通过空间结构和作用力协同实现锂镁分离
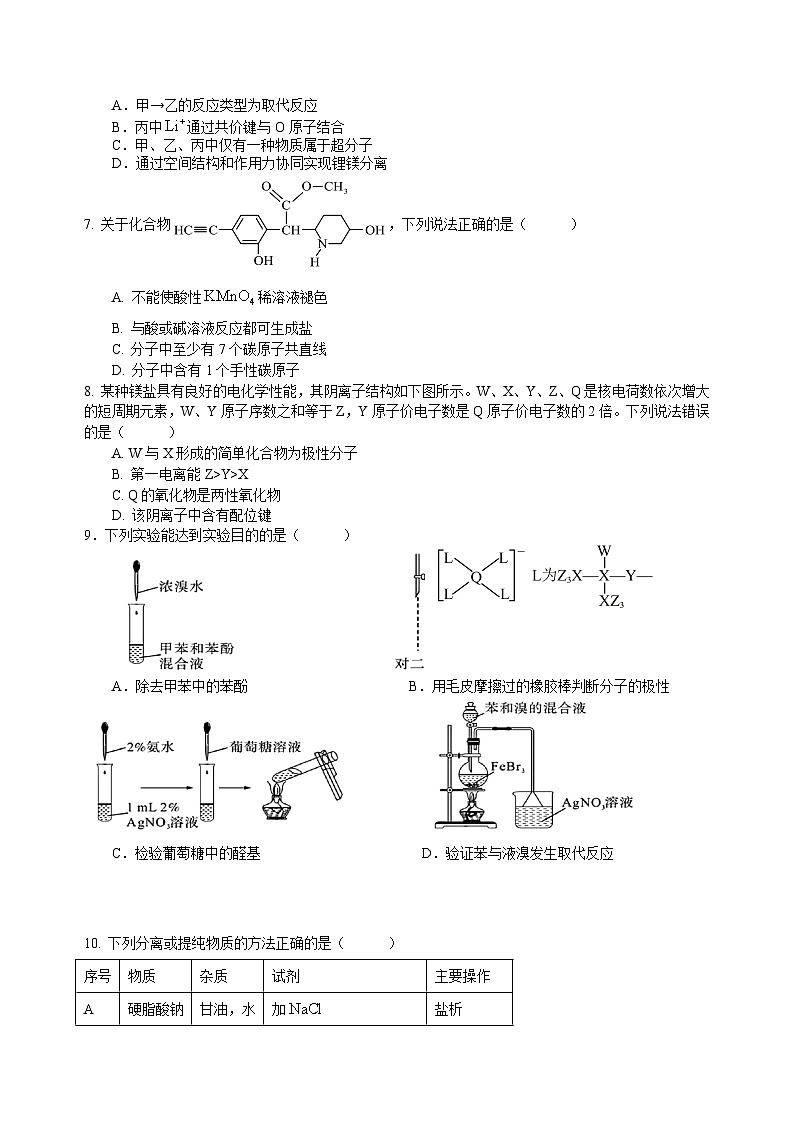
7. 关于化合物,下列说法正确的是( )
A. 不能使酸性稀溶液褪色
B. 与酸或碱溶液反应都可生成盐
C. 分子中至少有7个碳原子共直线
D. 分子中含有1个手性碳原子
8. 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是( )
A. W与X形成的简单化合物为极性分子
B. 第一电离能Z>Y>X
C. Q的氧化物是两性氧化物
D. 该阴离子中含有配位键
9.下列实验能达到实验目的的是( )
A.除去甲苯中的苯酚 B.用毛皮摩擦过的橡胶棒判断分子的极性
C.检验葡萄糖中的醛基 D.验证苯与液溴发生取代反应
10. 下列分离或提纯物质的方法正确的是( )
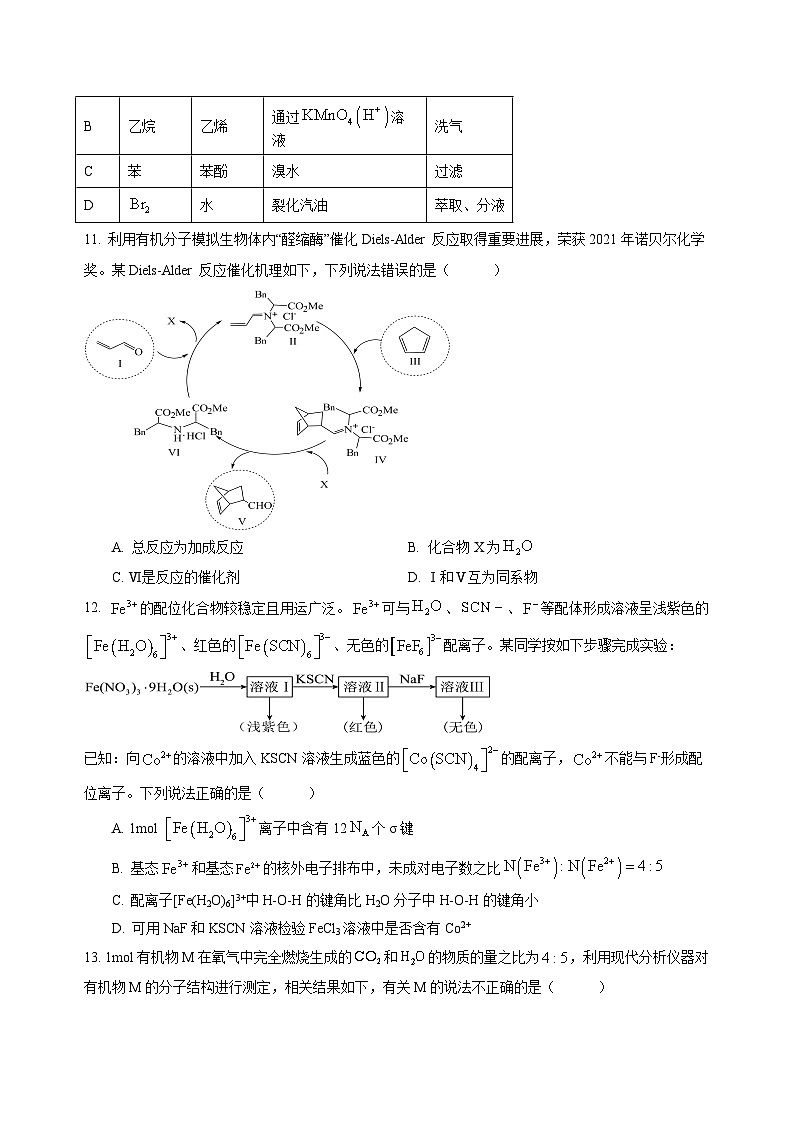
11. 利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021年诺贝尔化学奖。某Diels-Alder反应催化机理如下,下列说法错误的是( )
A. 总反应为加成反应B. 化合物X为
C. Ⅵ是反应的催化剂D. Ⅰ和Ⅴ互为同系物
12. 的配位化合物较稳定且用运广泛。可与、、等配体形成溶液呈浅紫色的、红色的、无色的配离子。某同学按如下步骤完成实验:
已知:向的溶液中加入KSCN溶液生成蓝色的的配离子,不能与F-形成配位离子。下列说法正确的是( )
A. 1ml 离子中含有12个σ键
B. 基态和基态的核外电子排布中,未成对电子数之比
C. 配离子[Fe(H2O)6]3+中H-O-H的键角比H2O分子中H-O-H的键角小
D. 可用NaF和KSCN溶液检验FeCl3溶液中是否含有C2+
13. 1ml有机物M在氧气中完全燃烧生成的和的物质的量之比为,利用现代分析仪器对有机物M的分子结构进行测定,相关结果如下,有关M的说法不正确的是( )
A. 根据图1,M的相对分子质量应为74
B. 根据图1、图2,推测M的分子式是
C. 根据图1、图2、图3信息,可确定M是2-甲基-2-丙醇
D. 根据图1、图2、图3信息,M分子内有三种化学环境不同的H,个数比为
14.科学家利用氨硼烷设计成原电池装置如题图所示,常温下该电池总反应为。下列说法正确的是( )
A.a室的电极反应式为
B.放电过程中,通过质子交换膜由b室移向a室
C.b室为该原电池的负极区
D.其他条件不变时,向溶液中加入适量溶液能增大电流强度
二、非选择题(本题共4小题,共58分)
15. 按要求回答下列问题:
(1)有机物的核磁共振氢谱出现的峰面积之比为_______________。
(2)取有机物,完全燃烧后生成和(标准状况)。已知相同状况下,A蒸气的密度是氢气的44倍,则A的分子式为________________。
(3)的系统命名法名称___________。
(4)某卤代烃与氢氧化钠醇溶液加热反应,会生成________种有机产物。
(5)胡椒酚是一种植物挥发油,它的结构简式为,若要制备胡椒酚钠,不可以选择的试剂有___________(填序号)。
A.Na B.NaOH C. D.
(6)乳酸分子()在一定条件下发生缩聚反应的化学方程式:______________。
(7)乙酰水杨酸分子与溶液共热反应的化学方程式:___________。
16. 芳香烃A是基本有机化工原料,由A制备高分子E和医药中间体K的合成路线(部分反应条件略去)如下图所示:
已知①; ②(苯胺,易被氧化)。
回答下列问题:
(1)A的化学名称是___________。⑧的反应类型分别是___________。
(2)D中含氧官能团名称是___________,E的结构简式为___________。
(3)反应⑤的化学方程式___________。
(4)反应⑦的作用是___________。
(5)1ml D与1ml 的加成产物同时满足下列条件的同分异构体有___________种。
写出其中一种符合下列条件的结构简式为___________。
①有五种不同化学环境的氢原子;
②能与发生显色反应;
③分子中只存在一个环不含其它环状结构。
17.精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
回答下列问题:
(1)基态的价电子排布式为___________。
(2)“浸出液1”中含有的金属离子主要是 。
(3)“浸取2”步骤中,单质金转化为HAuCl4的化学方程式为 。
(4)“浸取3”步骤中,“浸渣2”中的 (填化学式)转化为[Ag(S2O3)2]3-。
(5)“电沉积”步骤中阴极的电极反应式为 。
(6)的结构式为,与其互为等电子体的一种阴离子是:___________。
(7)的键角小于的键角,请说明理由: 。
18. 苯甲醛()是有机制备中的一种重要原料。实验室常用苯甲醛与NaOH反应制备苯甲醇和苯甲酸钠:2+NaOH+,再将苯甲酸钠酸化得到苯甲酸。
相关物质的物理性质如下表:
已知:a.RCHO+;
b.亚硫酸氢钠不与苯甲醇反应。
实验步骤:
步骤①:向如图所示三颈烧瓶c中加入碎瓷片、适量NaOH、水和m g苯甲醛,向冷凝管中通入冷水。
步骤②:搅拌、加热三颈烧瓶c,充分反应后,将c中液体冷却后倒入分液漏斗中,用乙醚萃取、分液,将乙醚层依次用25%亚硫酸氢钠溶液、水洗涤,水层保留待用。
步骤③:将乙醚层倒入盛少量无水MgSO4的锥形瓶中进行干燥,混匀、静置、过滤后采用一定的方法分离,收集苯甲醇。
步骤④:将步骤②中得到的水层和适量浓盐酸混合均匀,析出白色固体。冷却、抽滤得粗产品,将粗产品提纯得n g的苯甲酸。回答下列问题:
(1)步骤①中,冷凝管的作用是 ,从 (填“a”或“b”)口通入冷水。
(2)步骤②中,乙醚层用25%亚硫酸氢钠溶液洗涤的作用是 ;再用水洗涤的作用是 。将分液漏斗中两层液体分离开时,乙醚层在 (填“上层”或“下层”)。
(3)步骤③中,分离出苯甲醇的方法是 ,先出来的物质是 。
(4)步骤④中,水层和浓盐酸混合后产生苯甲酸的离子方程式为 ;将反应后混合物冷却的目的是 。
(5)苯甲酸的产率为 。(列出计算式)
连城一中2024~2025学年高三年级暑假月考化学试卷答案
一、选择题(每小题只有一个选项符合题意,每题3分,共42分)
二、非选择题(共4大题,共58分)
15.(除标注外,每空2分,共14分)
(1)3∶2(或2∶3) (2) (3)5-甲基-2-庚烯(4)2 (5) C
( 6 )
( 7 )
16.(除标注外,每空2分,共15分)
(1) ①.甲苯 ②氧化反应
(2) ①. (酮)羰基 (1分) ②.
(3)+HNO3+H2O
(4)保护氨基
(5)3 (三种任写一种即可)
17.(除标注外,每空2分,共14分)
(1) 3d9
(2)Cu2+
(3)
(4)AgCl
(5)
(等)
二者中心原子杂化类型不同,的中心硫原子是杂化,而的中心硫原子是杂化
18.(除标注外,每空2分,共15分)
(1)冷凝回流(1分) b (1分)
(2)除去乙醚层中少量的苯甲醛 除去亚硫酸氢钠等杂质 上层(1分)
(3)蒸馏(1分) 乙醚(1分)
(4)C6H5COO-+H+C6H5COOH↓ 降低苯甲酸的溶解度,使其尽可能多地析出
(5) 或序号
物质
杂质
试剂
主要操作
A
硬脂酸钠
甘油,水
加
盐析
B
乙烷
乙烯
通过溶液
洗气
C
苯
苯酚
溴水
过滤
D
水
裂化汽油
萃取、分液
名称
性质
熔点/℃
沸点/℃
溶解性
水
乙醇
乙醚
苯甲醛
无色液体,具有苦杏仁味
-26
178.1
微溶
混溶
混溶
苯甲酸
白色片状或针状晶体
122.4
248
微溶
易溶
易溶
苯甲醇
无色液体,具有芳香味
-15.3
205.35
微溶
易溶
易溶
乙醚
无色透明液体,具有特殊刺激性气味
-116.2
34.6
微溶
易溶
—
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
D
C
C
B
C
B
B
A
B
A
D
D
C
A
福建省龙岩市连城县第一中学2024-2025学年高一上学期开学考试化学试题(含答案): 这是一份福建省龙岩市连城县第一中学2024-2025学年高一上学期开学考试化学试题(含答案),共6页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
福建省龙岩市连城县第一中学2024-2025学年高二上学期开学化学试题(含答案): 这是一份福建省龙岩市连城县第一中学2024-2025学年高二上学期开学化学试题(含答案),共8页。试卷主要包含了请将答案填在答题卡上,可能用到的相对原子质量,下列有关装置的说法正确的是,下列有关反应热的说法不正确的是等内容,欢迎下载使用。
新疆石河子第一中学2024-2025学年高三上学期开学考试化学试题: 这是一份新疆石河子第一中学2024-2025学年高三上学期开学考试化学试题,共6页。












