





2025届高中化学全程复习构想课件全套32晶胞及其相关计算
展开1.掌握均摊法计算的一般方法,能根据晶胞中微粒的位置计算晶胞的化学式。2.掌握晶体密度与晶胞参数计算的一般步骤。
1.晶胞(1)概念:描述晶体结构的基本单元。(2)晶体中晶胞的排列——无隙并置①无隙:相邻晶胞之间没有任何间隙。②并置:所有晶胞平行排列、取向相同。
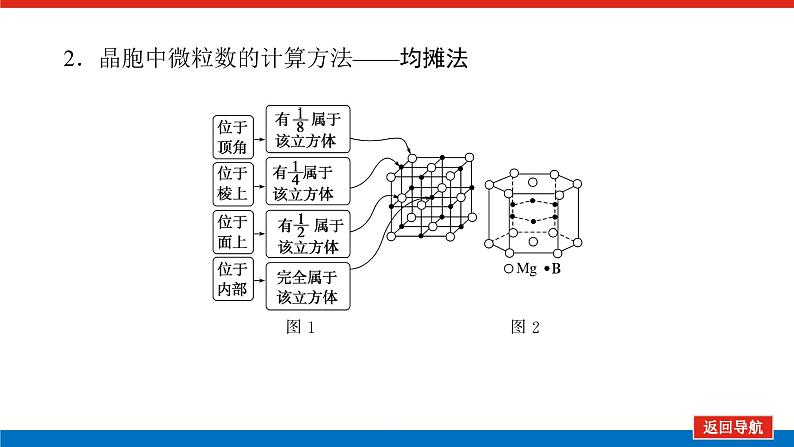
2.晶胞中微粒数的计算方法——均摊法
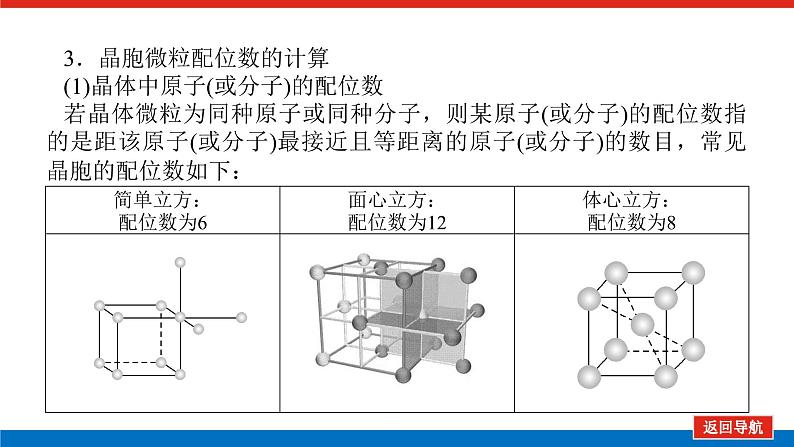
3.晶胞微粒配位数的计算(1)晶体中原子(或分子)的配位数若晶体微粒为同种原子或同种分子,则某原子(或分子)的配位数指的是距该原子(或分子)最接近且等距离的原子(或分子)的数目,常见晶胞的配位数如下:
(2)离子晶体的配位数指一个离子周围最接近且等距离的异种电性离子的数目。以NaCl晶体为例①找一个与其他粒子连接情况最清晰的粒子,如上图中心的黑球(Cl-)。②数一下与该粒子周围距离最近的粒子数,如上图标数字的面心白球(Na+),确定Cl-的配位数为6,同样方法可确定Na+的配位数也为6。
【教考衔接】典例1 [2023·湖南卷,11A]科学家合成了一种高温超导材料,其晶胞结构如图所示。该晶体最简化学式为________。
典例2 [2023·辽宁卷,14改编]晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2),判断下列说法是否正确。(1)图1中O原子的配位数为6( )(2)Mg2+取代产生的空位有利于Li+传导( )(3)图2表示的化学式为LiMg2OClxBr1-x( )
【对点演练】考向一 计算晶胞微粒数目——均摊法1.某离子晶体的晶体结构中最小重复单元如图所示。A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为( )A.B2A B.BA2C.B7A4 D.B4A7
2.Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式为________。
3.(1)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,下图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为________。
解析:每个Mg周围有6个B,而每个B周围有3个Mg,所以其化学式为MgB2。
(2)在硼酸盐中,阴离子有链状、环状等多种结构形式。如图是一种链状结构的多硼酸根,则多硼酸根离子符号为________。
考向二 晶胞中粒子配位数的计算5.硅化镁是一种窄带隙n型半导体材料,在光电子器件、能源器件、激光、半导体制造等领域具有重要应用前景。硅化镁的晶胞参数a=0.639 1 nm,属于面心立方晶胞,结构如图所示。Si原子的配位数为________。
解析:根据晶胞结构,以面心Si原子为基准,同一晶胞内等距离且最近的Mg原子有4个,紧邻晶胞还有4个Mg原子,共8个,故Si原子的配位数为8。
6.如图是一种由Y(与Sc同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中心和八面体中心的球代表Fe,其余小球代表O。(1)该晶体的化学式为__________。(2)其中Y的配位数为________。
3.宏观晶体密度与微观晶胞参数的关系
【教考衔接】典例 [2023·辽宁卷,14A改编]某富锂超离子导体的晶胞是立方体,如下图:计算该晶体的密度________________。
2.如图是Fe单质的晶胞模型。已知晶体密度为d g·cm-3,铁原子的半径为_____________ nm(用含有d、NA的代数式表示)。
4.氮化硼是一种性能优异的新型材料,主要结构有六方氮化硼(图1)和立方氮化硼(图2)。前者与石墨结构类似。(1)50.0 g六方氮化硼晶体中含有六元环的数目为________。(2)立方氮化硼中N的配位数为________。已知立方氮化硼密度为d g·cm-3,NA代表阿伏加德罗常数的值,立方氮化硼晶胞中面心上6个N原子相连构成正八面体,该正八面体的边长为_____________ pm(列式即可)。
微专题11 晶胞中原子分数坐标与投影图【要点归纳】1.原子分数坐标(1)概念以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。(2)原子分数坐标的表示方法晶胞中的任意一个原子的中心位置均可用3个分别小于1的数在立体坐标系中表示出来。
2.常见典型晶胞的投影图
3.典型晶胞结构模型的原子坐标参数与投影图(1)简单立方体模型粒子坐标与投影图①粒子坐标:若1(0,0,0),2(0,1,0),则确定3(1,1,0),7(1,1,1)②x、y平面上的投影图:________________
典例2 [2022·湖南卷,18(4)]钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:①该超导材料的最简化学式为________。②Fe原子的配位数为________。③该晶胞参数a=b=0.4 nm、c=1.4 nm。阿伏加德罗常数的值为NA,则该晶体的密度为_______________________g·cm-3(列出计算式)。
4.铜与氧元素形成的晶胞如图所示:
6.AgN5的晶体结构与AgI相似。AgI的结构分为α-AgI和γ-AgI,γ-AgI立方晶胞的示意图见图1,图2是晶胞正上方的俯视投影图,图中黑球(实心球)表示I-,请在图2中用白球(空心球)表示出Ag+的位置。
解析:根据γ-AgI立方晶胞的示意图,可以理解为有八个小立方体,银离子在其中四个小立方体体心位置,根据从上方的俯视图得出银离子在每个小正方形的中心位置,即白球(空心球)表示出Ag+的位置
7.[2022·广东卷,20节选]我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
(1)X的化学式为________。(2)设X的最简式的式量为Mr,晶体密度为ρ g·cm-3,则X中相邻K之间的最短距离为________________nm(列出计算式,NA为阿伏加德罗常数的值)。
2025届高中化学全程复习构想课件全套19硫及其氧化物: 这是一份2025届高中化学全程复习构想课件全套19硫及其氧化物,共50页。PPT课件主要包含了考点一,考点二,考点三,答案D,答案A,④漂白性,答案B,BaSO4,BaSO3,品红溶液等内容,欢迎下载使用。
2025届高中化学全程复习构想课件全套04氧化还原反应的相关概念: 这是一份2025届高中化学全程复习构想课件全套04氧化还原反应的相关概念,共42页。PPT课件主要包含了考点一,考点二,H2O,答案A,5mol,Cl2S,ZnCu,①③⑥⑦,⑤⑥⑦⑧,YQZX等内容,欢迎下载使用。
2025届高中化学全程复习构想课件全套16氯及其化合物: 这是一份2025届高中化学全程复习构想课件全套16氯及其化合物,共34页。PPT课件主要包含了考点一,考点二,2歧化反应,答案D,产生白色沉淀,HOCl,漂白粉,答案A,答案B,ClO2等内容,欢迎下载使用。












