

2025版高考化学一轮复习微专题小练习专练30结构与性质综合应用
展开将酞菁—钴钛菁—三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二氧化碳的催化剂。回答下列问题:
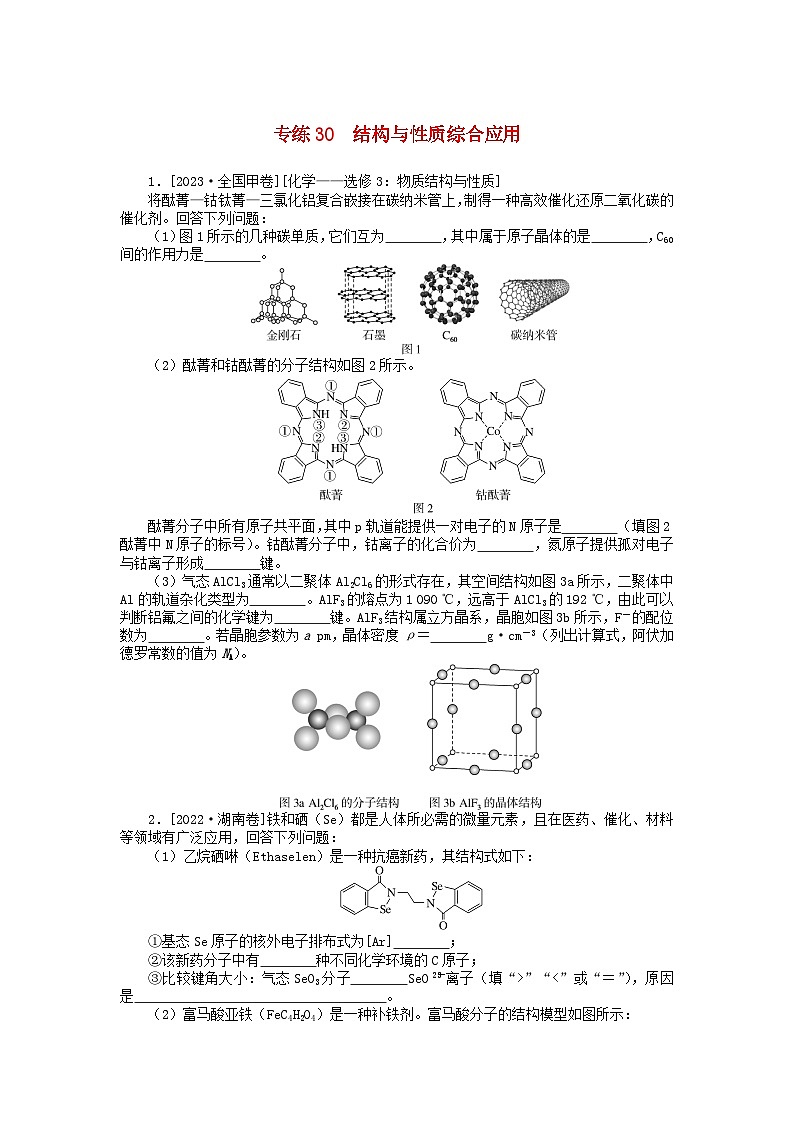
(1)图1所示的几种碳单质,它们互为 ,其中属于原子晶体的是 ,C60间的作用力是 。
(2)酞菁和钴酞菁的分子结构如图2所示。
酞菁分子中所有原子共平面,其中p轨道能提供一对电子的N原子是 (填图2酞菁中N原子的标号)。钴酞菁分子中,钴离子的化合价为 ,氮原子提供孤对电子与钴离子形成 键。
(3)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为 。AlF3的熔点为1 090 ℃,远高于AlCl3的192 ℃,由此可以判断铝氟之间的化学键为 键。AlF3结构属立方晶系,晶胞如图3b所示,F-的配位数为 。若晶胞参数为a pm,晶体密度ρ= g·cm-3(列出计算式,阿伏加德罗常数的值为NA)。
2.[2022·湖南卷]铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态Se原子的核外电子排布式为[Ar] ;
②该新药分子中有 种不同化学环境的C原子;
③比较键角大小:气态SeO3分子 SeO eq \\al(2-,3) 离子(填“>”“<”或“=”),原因是 。
(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:
①富马酸分子中σ键与π键的数目比为 ;
②富马酸亚铁中各元素的电负性由大到小的顺序为 。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化NH eq \\al(-,2) ,反应过程如图所示:
①产物中N原子的杂化轨道类型为 ;
②与NH eq \\al(-,2) 互为等电子体的一种分子为 (填化学式)。
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为
________________________________________________________________________;
②Fe原子的配位数为 ;
③该晶胞参数a=b=0.4 nm、c=1.4 nm,阿伏加德罗常数的值为NA,则该晶体的密度为 g·cm-3(列出计算式)。
3.[2024·重庆渝北中学检测]2023年11月23日,2023亚洲通用航空展在广东珠海国际航展中心开幕,为期4天的航展集中展示了通用航空领域最新技术产品和成果。国产飞机的制造使用了较多含硼材料(如硼纤维、氮化硼等),且多项技术打破了国外垄断。回答下列问题:
(1)基态B原子的价层电子排布图(轨道表示式)为 。
(2)耐高温材料立方BN制备流程中用到了NH3、BCl3和触媒剂Ca3B2N4。
①Ca、B、N三种元素的电负性从大到小的顺序为 。
②BCl3中B原子的 轨道与Cl原子的 轨道形成σ键。
③BCl3在四氯化碳中的溶解度远大于NH3在四氯化碳中的溶解度,原因是________________________________________________________________________
________________________________________________________________________。
(3)硼砂是非常重要的含硼矿物。一种硼砂阴离子的结构如图1所示,则1 ml该阴离子中含有配位键的物质的量为 ,n= 。
(4)制造硼合金的原料硼化钙(CaB6)晶胞结构如图2所示,硼原子全部组成B6正八面体,各个顶点通过B—B互相连接成三维骨架。已知该晶体的晶胞参数为a pm,B6正八面体中B—B的键长为d pm,M原子的坐标参数为( eq \f(1,2) , eq \f(1,2) , eq \f(1,2) ),则N原子的坐标参数为 ;设阿伏加德罗常数的值为NA,则该晶体的密度为 g·cm-3(列出计算式)。
4.[2022·河北卷]含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为 。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是 ,原因是
________________________________________________________________________
________________________________________________________________________。
(3)SnCl eq \\al(-,3) 的几何构型为 ,其中心离子杂化方式为 。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是 (填标号)。
A.[Cu(NH3)2]Cl B.[Cu(NH3)4]SO4
C.[Zn(NH3)4]SO4 D.Na2[Zn(OH)4]
(5)如图是硫的四种含氧酸根的结构:
根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO eq \\al(-,4) 的是 (填标号),理由是________________________________________________________________________。
(6)如图是CZTS四元半导体化合物的四方晶胞。
①该物质的化学式为 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中A原子的坐标为( eq \f(3,4) , eq \f(1,4) , eq \f(1,8) ),则B原子的坐标为 。
答案
1答案:(1)同素异形体 金刚石 范德华力
(2)③ +2 配位
(3)sp3 离子 2 eq \f(84×1030,NA·a3)
解析:(1)同一元素形成的不同单质之间互为同素异形体。图1所示的几种碳单质,它们的组成元素均为碳元素,因此,它们互为同素异形体;其中金刚石属于原子晶体,石墨属于混合型晶体,C60属于分子晶体,碳纳米管不属于原子晶体;C60间的作用力是范德华力;
(2)已知酞菁分子中所有原子共平面,则其分子中所有的C原子和所有的N原子均为sp2杂化,且分子中存在大π键,其中标号为①和②的N原子均有一对电子占据了一个sp2杂化轨道,其p轨道只能提供1个电子参与形成大π键,标号为③的N原子的 p轨道能提供一对电子参与形成大π键,因此标号为③的N原子形成的N—H键易断裂从而电离出H+;钴酞菁分子中,失去了2个H+的酞菁离子与钴离子通过配位键结合成分子,因此,钴离子的化合价为+2,氮原子提供孤对电子与钴离子形成配位键。
(3)由Al2Cl6的空间结构结合相关元素的原子结构可知,Al原子价层电子对数是4,其与其周围的4个氯原子形成四面体结构,因此,二聚体中Al的轨道杂化类型为sp3。AlF3的熔点为1 090 ℃,远高于AlCl3的192 ℃,由于F的电负性最大,其吸引电子的能力最强,因此,可以判断铝氟之间的化学键为离子键。由AlF3的晶胞结构可知,其中含大球的个数为12× eq \f(1,4) =3,小球的个数为8× eq \f(1,8) =1,则大球为F-,距F-最近且等距的Al3+有2个,则F-的配位数为2。若晶胞参数为a pm,则晶胞的体积为(a pm)3=a3×10-30 cm3,晶胞的质量为 eq \f(84 g,NA) ,则其晶体密度ρ= eq \f(84×1030,NA·a3) g·cm-3。
2答案:(1)①3d104s24p4 ②8 ③> 前者中Se为sp2杂化、后者中Se为sp3杂化
(2)①11∶3 ②O>C>H>Fe
(3)①sp3 ②H2O
(4)①KFe2Se2 ②4
③ eq \f(2×(39+56×2+79×2),NA×0.42×1.4) ×1021
解析:(1)①Se为34号元素,根据构造原理可写出基态Se原子的核外电子排布式为[Ar]3d104s24p4。②该物质结构对称,具有如图所示8种不同化学环境的C原子:
。③SeO3中Se的价层电子对数为3,孤电子对数为0,SeO eq \\al(2-,3) 中Se的价层电子对数为3,孤电子对数为 eq \f(6+2-3×2,2) =1,故SeO3和SeO eq \\al(2-,3) 中Se原子分别为sp2和sp3杂化,则SeO3分子中键角大于SeO eq \\al(2-,3) 中键角。(2)①由富马酸分子的结构模型可确定其结构简式为,由单键均为σ键,双键有1个σ键和1个π键,知该分子中σ键和π键的数目比为11∶3。②富马酸亚铁中含C、H、O、Fe四种元素,由电负性递变规律可知,电负性由大到小的顺序为O>C>H >Fe。(3)①产物中N原子形成4个共价键,则其采取sp3杂化。(4)①分析晶胞在xz、yz、xy平面的投影图可知,占据顶点和体心位置的为K原子,故K原子个数为8× eq \f(1,8) +1=2,每个竖直棱上有2个Se原子,体内有2个Se原子,故Se原子个数为8× eq \f(1,4) +2=4,每个竖直面上有2个Fe原子,故Fe原子个数为8× eq \f(1,2) =4,该物质的晶胞结构如图所示:
其最简化学式为KFe2Se2。③以1号Fe原子为研究对象,2号和3号铁原子及其对称位置的2个Fe原子距离1号Fe原子最近,故Fe的配位数为4。③该晶胞的质量为 eq \f(2×(39+56×2+79×2),NA) g,体积为0.4×0.4×1.4×10-21 cm3,故该晶体的密度为 eq \f(2×(39+56×2+79×2),NA×0.42×1.4) ×1021 g·cm-3。
3答案:(1)
(2)①N>B>Ca ②sp2杂化 3p ③BCl3和四氯化碳均为非极性分子,而NH3为极性分子
(3)2 ml 2 (4)( eq \f(\r(2)d,2a) ,1,0) eq \f(40+11×6,a3×10-30×NA)
解析:(1)基态B原子的价层电子排布图(轨道表示式)为
(2)①金属的电负性较小,同周期主族元素的电负性从左到右逐渐增大,故电负性N>B>Ca。②BCl3中B原子的价层电子对数为3,其杂化方式为sp2,故BCl3中B原子的sp2杂化轨道与Cl原子的3p轨道形成σ键。③BCl3和四氯化碳均为非极性分子,NH3为极性分子,根据“相似相溶”原理,BCl3在四氯化碳中的溶解度远大于NH3在四氯化碳中的溶解度。
(3)由题图1可知,形成4个键的B原子含有1个配位键,故1 ml该阴离子中含有配位键的物质的量为2 ml,在该阴离子中B显+3价,O显-2价,H显+1价,则计算可得n=2。
(4)将8个正八面体的体心连接成晶胞的立方晶系图。由M原子的坐标参数知,该原子位于晶胞的体心,且坐标系的单位长度为1,正八面体的体心到正八面体的顶点的距离为 eq \f(\r(2),2) d pm,则N点在x轴的 eq \f(\r(2)d,2a) 处。根据N原子在晶胞中的位置可知,其坐标参数为( eq \f(\r(2)d,2a) ,1,0)。一个晶胞中含有一个CaB6,则该晶体密度为 eq \f(40+11×6,a3×10-30×NA) g·cm-3。
4答案:(1)2∶1(或1∶2)
(2)Cu Cu的价电子排布式为3d104s1,Zn的价电子排布式为3d104s2,Zn为全充满稳定结构,Cu的第一电离能比Zn的第一电离能小,Cu失去一个电子后形成的Cu+的价电子排布式为3d10,为全充满稳定结构,较难失去电子,Zn失去1个电子后形成的Zn+的价电子排布式为3d104s1,较易失去一个电子达到更稳定状态,Cu的第二电离能比Zn的第二电离能大
(3)三角锥形 sp3 (4)B
(5)D D(S2O eq \\al(2-,8) )中含有过氧键,具有强氧化性
(6)①Cu2ZnSnS4 ②( eq \f(1,4) , eq \f(3,4) , eq \f(5,8) )
解析:(1)基态S原子的价电子排布式为3s23p4,价电子的轨道表示式为,两种自旋状态的电子数之比为2∶1。(3)SnCl eq \\al(-,3) 中Sn的孤电子对数为 eq \f(4+1-1×3,2) =1、成键电子对数为3,杂化方式为sp3,因此SnCl eq \\al(-,3) 的几何构型为三角锥形。(4)主族元素形成的离子或配体中一般不含有未成对电子,因此该题只需判断配合物的中心离子是否存在未成对电子。[Cu(NH3)2]Cl中Cu+的价电子排布式为3d10,不含未成对电子,[Cu(NH3)4]SO4中Cu2+的价电子排布式为3d9,含未成对电子,[Zn(NH3)4]SO4中Zn2+的价电子排布式为3d10,不含未成对电子,Na2[Zn(OH)4]中Zn2+的价电子排布式为3d10,不含未成对电子,因此属于顺磁性物质的是[Cu(NH3)4]SO4。(5)Mn2+转化为MnO eq \\al(-,4) ,Mn2+被氧化,则该离子具有强氧化性,中含有过氧键,具有强氧化性,在酸性溶液中可将Mn2+氧化为MnO eq \\al(-,4) 。(6)①结合均摊法进行分析,晶胞中S原子数目为8,Sn原子数目为2× eq \f(1,2) +4× eq \f(1,4) =2,Zn原子数目为8× eq \f(1,8) +1=2,Cu原子数目为8× eq \f(1,2) =4,故该物质的化学式为Cu2ZnSnS4。②结合图中A、B原子的位置及A原子的坐标可得出B原子的坐标。
2025版高考化学一轮复习微专题小练习专练29晶体结构与性质: 这是一份2025版高考化学一轮复习微专题小练习专练29晶体结构与性质,共7页。试卷主要包含了下列关于晶体说法正确的组合是等内容,欢迎下载使用。
2025版高考化学一轮复习微专题小练习专练30结构与性质综合应用: 这是一份2025版高考化学一轮复习微专题小练习专练30结构与性质综合应用,共6页。
2025版高考化学一轮复习微专题小练习专练29晶体结构与性质: 这是一份2025版高考化学一轮复习微专题小练习专练29晶体结构与性质,共6页。试卷主要包含了下列关于晶体说法正确的组合是等内容,欢迎下载使用。












