
新教材宁陕2024届高考化学一轮复习学案第2章元素与物质世界第4讲元素与物质的分类鲁科版
展开考点一 物质的组成与分类
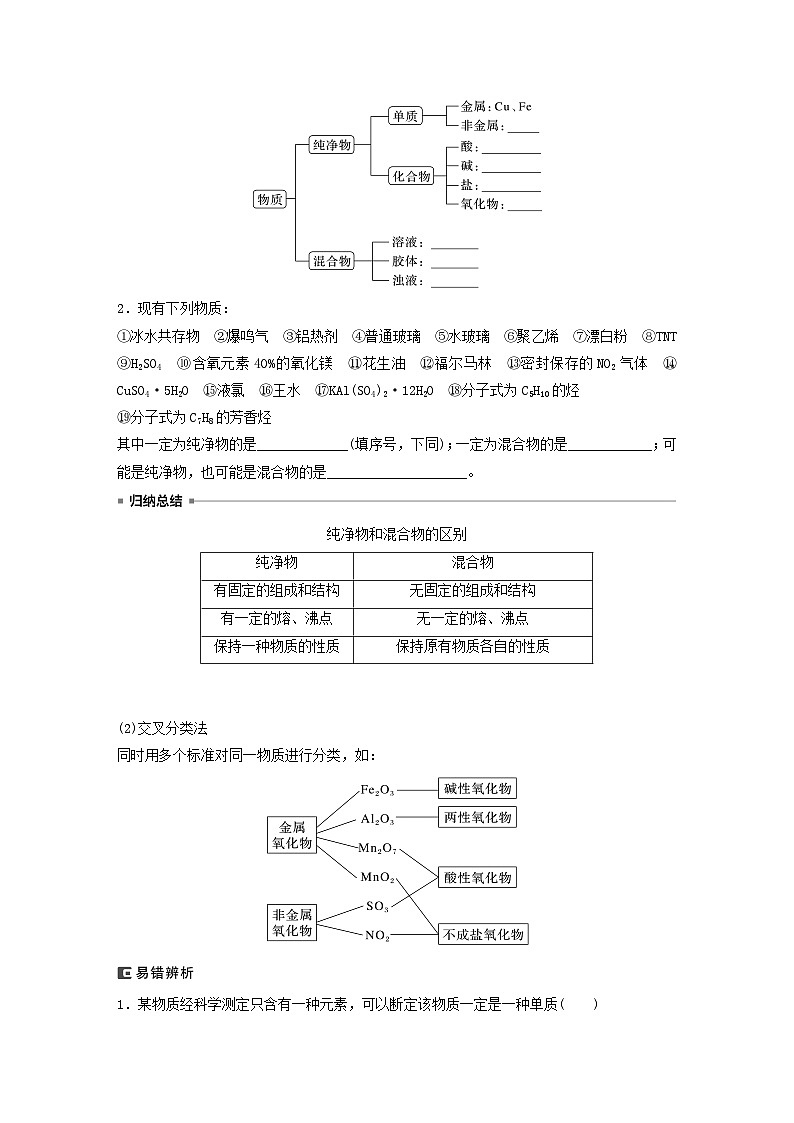
1.物质的组成
(1)
(2)同素异形体
①定义:由同一种元素形成的__________________________________________________。
②性质:物理性质不同,化学性质有差异。同素异形体之间在一定条件下可以相互转化,这种转化是________变化。
③常见元素的同素异形体
氧元素:________;碳元素:________________;磷元素:____________。
2.物质的分类
分类应依据事先设定的“标准”进行,“标准”不同,分类方法也不相同。在化学上常用的分类方法有________分类法和________分类法。
(1)树状分类法
每次用一个标准对物质进行再分类。
物质eq \b\lc\{\rc\ (\a\vs4\al\c1(混合物,纯净物\b\lc\{\rc\ (\a\vs4\al\c1(单质\b\lc\{\rc\ (\a\vs4\al\c1(金属单质,非金属单质)),化合物\b\lc\{\rc\ (\a\vs4\al\c1(无机化合物,有机化合物))))))
应用举例
1.请把下列物质的序号填写到下图的横线上:
①硫黄 ②HClO ③苛性钠 ④明矾 ⑤小苏打 ⑥氧化钠 ⑦Fe(OH)3 ⑧NaCl溶液 ⑨H2SO3 ⑩淀粉溶液 ⑪泥水
2.现有下列物质:
①冰水共存物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃 ⑥聚乙烯 ⑦漂白粉 ⑧TNT ⑨H2SO4 ⑩含氧元素40%的氧化镁 ⑪花生油 ⑫福尔马林 ⑬密封保存的NO2气体 ⑭CuSO4·5H2O ⑮液氯 ⑯王水 ⑰KAl(SO4)2·12H2O ⑱分子式为C5H10的烃
⑲分子式为C7H8的芳香烃
其中一定为纯净物的是_____________(填序号,下同);一定为混合物的是____________;可能是纯净物,也可能是混合物的是____________________。
纯净物和混合物的区别
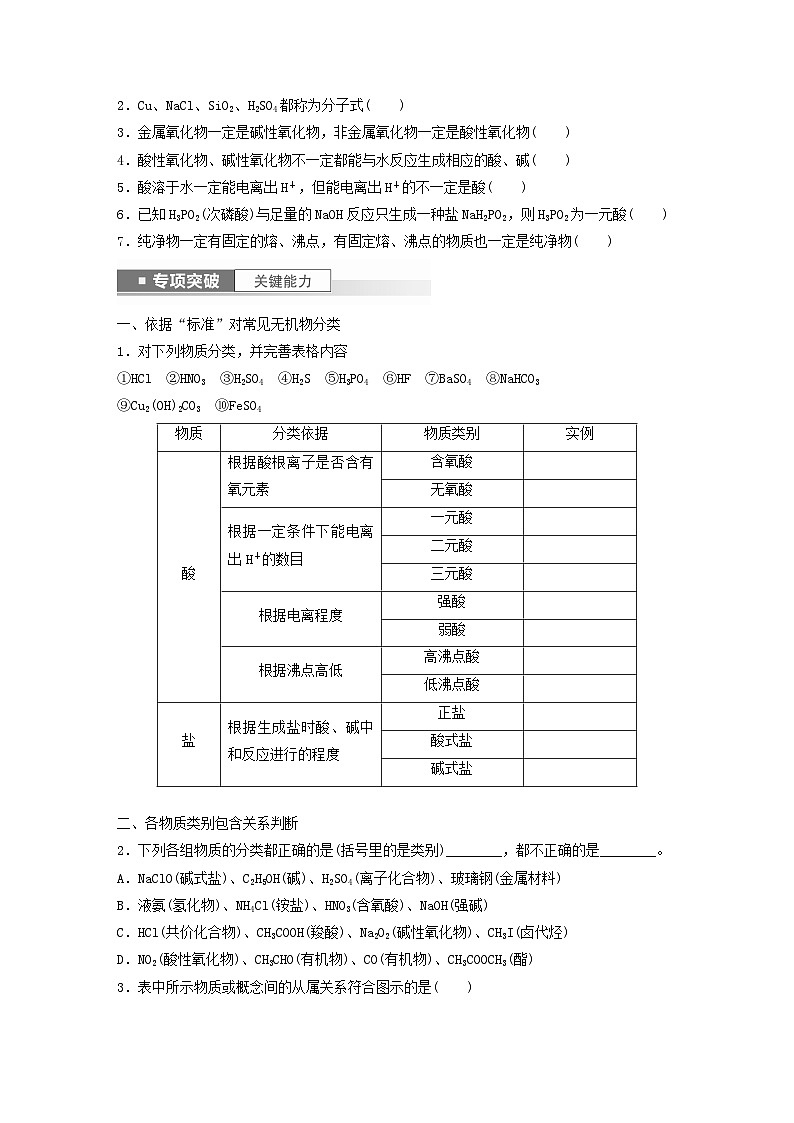
(2)交叉分类法
同时用多个标准对同一物质进行分类,如:
1.某物质经科学测定只含有一种元素,可以断定该物质一定是一种单质( )
2.Cu、NaCl、SiO2、H2SO4都称为分子式( )
3.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物( )
4.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱( )
5.酸溶于水一定能电离出H+,但能电离出H+的不一定是酸( )
6.已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,则H3PO2为一元酸( )
7.纯净物一定有固定的熔、沸点,有固定熔、沸点的物质也一定是纯净物( )
一、依据“标准”对常见无机物分类
1.对下列物质分类,并完善表格内容
①HCl ②HNO3 ③H2SO4 ④H2S ⑤H3PO4 ⑥HF ⑦BaSO4 ⑧NaHCO3
⑨Cu2(OH)2CO3 ⑩FeSO4
二、各物质类别包含关系判断
2.下列各组物质的分类都正确的是(括号里的是类别)________,都不正确的是________。
A.NaClO(碱式盐)、C2H5OH(碱)、H2SO4(离子化合物)、玻璃钢(金属材料)
B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强碱)
C.HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃)
D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯)
3.表中所示物质或概念间的从属关系符合图示的是( )
考点二 物质的性质与变化
1.从宏观和微观两个角度理解物理变化和化学变化
2.不同类别的无机物之间转化的一般规律
(1)金属单质及其化合物的转化
金属单质eq \(――→,\s\up7(O2))碱性氧化物eq \(――→,\s\up7(H2O))碱eq \(――→,\s\up7(酸))盐
如:Naeq \(――→,\s\up7(O2))Na2Oeq \(――→,\s\up7(H2O))NaOHeq \(――→,\s\up7(H2SO4))Na2SO4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转化关系。
(2)非金属单质及其化合物的转化
非金属单质eq \(――→,\s\up7(O2))酸性氧化物eq \(――→,\s\up7(H2O))酸eq \(――→,\s\up7(碱))盐
如:Seq \(――→,\s\up7(O2))SO2eq \(――→,\s\up7(H2O))H2SO3eq \(――→,\s\up7(NaOH))Na2SO3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
3.常见化学反应的分类
化学反应eq \b\lc\{\rc\ (\a\vs4\al\c1(按反应物、生成物种类及数目多少\b\lc\{\rc\ (\a\vs4\al\c1( 反应, 反应, 反应, 反应)),按反应中 \b\lc\{\rc\ (\a\vs4\al\c1(离子反应,非离子反应)),按反应中 \b\lc\{\rc\ (\a\vs4\al\c1(氧化还原反应,非氧化还原反应)),按反应进行的程度和方向\b\lc\{\rc\ (\a\vs4\al\c1( 反应, 反应)),按反应的能量变化\b\lc\{\rc\ (\a\vs4\al\c1( 反应, 反应))))
1.NaCl晶体溶于水是物理变化,过程中没有化学键的改变( )
2.232Th转化成233U是化学变化( )
3.碳在足量氧气中燃烧生成CO2,故硫在足量氧气中燃烧生成SO3( )
4.判断下列转化能否实现,能实现的打“√”,不能实现的打“×”。
①SiO2eq \(――→,\s\up7(H2O))H2SiO3( )
②SO3eq \(――→,\s\up7(H2O))H2SO4( )
③Fe2O3eq \(――→,\s\up7(H2O))Fe(OH)3( )
④Na2Oeq \(――→,\s\up7(H2O))NaOH( )
一、物质变化的判断
1.通过对比物理变化和化学变化的不同,回答下列问题:
①石油的分馏 ②煤的干馏 ③钠的焰色试验 ④碘的升华 ⑤氯化铵分解 ⑥蛋白质的变性 ⑦蛋白质的显色反应 ⑧电解食盐水 ⑨CaCl2的潮解 ⑩冰的融化 ⑪FeCl3的水解 ⑫石油的裂化、裂解 ⑬蛋白质的盐析 ⑭食物的缓慢氧化 ⑮同素异形体间的转化
其中属于物理变化的是_______________(填序号,下同);属于化学变化的是______________。
二、基于物质类别预测陌生物质的性质
2.已知次磷酸(H3PO2)是一元中强酸,请写出其与足量氢氧化钠反应的化学方程式:_______________________________________________________________________________
_______________________________________________________________________________。
3.已知Be(OH)2与Al(OH)3都属于两性氢氧化物,写出Be(OH)2分别溶于NaOH溶液、盐酸的化学方程式:
(1)____________________________________________________________________________。
(2)____________________________________________________________________________。
三、同类物质的特殊性判断
4.下列类比正确的打“√”,错误的打“×”,并指明错误的原因。
(1)O2与Cu加热反应生成CuO,则S与Cu加热反应生成CuS( )
原因:________________________________________________________________________。
(2)CO2与Na2O2反应生成Na2CO3和O2,则SO2与Na2O2反应生成Na2SO3和O2( )
原因:________________________________________________________________________。
(3)CO2通入BaCl2溶液中不产生沉淀,则SO2通入BaCl2溶液中也不产生沉淀( )
原因:________________________________________________________________________。
(4)向碳酸钠中加入少量水后,碳酸钠结块变成晶体,并伴有放热现象,向碳酸氢钠中加入少量水后,碳酸氢钠能溶解,也伴随着放热现象( )
原因:________________________________________________________________________。
(5)酸性:HClO4>HIO4,类比酸性:HCl>HI( )
原因:________________________________________________________________________。
(6)沸点:Cl2
点拨 类比是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,在使用类比法时,要关注物质的特殊性质,不能违背客观实际。
四、置换反应再分类
5.根据反应物和生成物中单质的类别,可对置换反应再分类,请列举重要实例。
(1)金属置换金属
①________________________________________________________________________。
②________________________________________________________________________。
③________________________________________________________________________。
(2)金属置换非金属
①________________________________________________________________________。
②________________________________________________________________________。
③________________________________________________________________________。
(3)非金属置换金属
①________________________________________________________________________。
②________________________________________________________________________。
(4)非金属置换非金属
①________________________________________________________________________。
②________________________________________________________________________。
③________________________________________________________________________。
考点三 分散系 胶体
1.分散系
(1)概念:____________________________________________________所得到的体系。
(2)分类:根据____________________将分散系分为溶液、浊液和胶体,可用如图直观地表示。
2.胶体的分类
依据分散剂的状态将胶体分为____________、________、________。
3.胶体的性质及应用
1.碳纳米管属于胶体分散系,该材料具有超强的吸附能力( )
2.明矾净水时发生了化学及物理变化,能起到杀菌、消毒作用( )
3.胶体不带电荷,胶体粒子因吸附离子往往带有电荷( )
4.向浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体( )
5.将1 mL 1 ml·L-1的FeCl3溶液滴入沸水中制备Fe(OH)3胶体,若FeCl3完全水解,则可制得Fe(OH)3胶体粒子少于0.001NA个( )
6.利用丁达尔效应可区分蛋白质溶液和食盐水( )
Fe(OH)3胶体的制备
(1)制备方法:向沸水中逐滴加入______________,继续煮沸至液体呈________,停止加热,即制得Fe(OH)3胶体。
(2)制备原理:_____________________________________________(用化学方程式表示)。
(3)问题讨论
①可以利用______________证明Fe(OH)3胶体已经制成。
②可以利用________方法来提纯Fe(OH)3胶体。证明Fe(OH)3胶体与Cl-已完全分离的实验方法是___________________________________________________________________________。
③某同学向沸水中滴加氯化铁饱和溶液后,长时间加热,结果会出现浑浊,原因可能是_______________________________________________________________________________。
1.(2022·浙江6月选考,1)下列消毒剂的有效成分属于盐的是( )
A.高锰酸钾溶液 B.过氧乙酸溶液
C.双氧水 D.医用酒精
2.(2022·湖南,1)化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是( )
A.《神农本草经》中记载的“石胆能化铁为铜”
B.利用“侯氏联合制碱法”制备纯碱
C.科学家成功将CO2转化为淀粉或葡萄糖
D.北京冬奥会场馆使用CO2跨临界直冷制冰
3.(2022·广东,2)北京冬奥会成功举办、神舟十三号顺利往返、“天宫课堂”如期开讲及“华龙一号”核电海外投产等,均展示了我国科技发展的巨大成就。下列相关叙述正确的是( )
A.冬奥会“飞扬”火炬所用的燃料H2为氧化性气体
B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C.乙酸钠过饱和溶液析出晶体并放热的过程仅涉及化学变化
D.核电站反应堆所用铀棒中含有的eq \\ar(235, 92)U与eq \\ar(238, 92)U互为同位素
4.(2022·湖北,1)化学与生活密切相关,下列不涉及化学变化的是( )
A.加入明矾后泥水变澄清
B.北京冬奥会用水快速制冰
C.炖排骨汤时加点醋味道更鲜
D.切开的茄子放置后切面变色
5.(2022·山东,1)古医典富载化学知识,下述之物见其氧化性者为( )
A.金(Au):“虽被火亦未熟”
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳(CaCO3):“色黄,以苦酒(醋)洗刷则白”
纯净物
混合物
有固定的组成和结构
无固定的组成和结构
有一定的熔、沸点
无一定的熔、沸点
保持一种物质的性质
保持原有物质各自的性质
物质
分类依据
物质类别
实例
酸
根据酸根离子是否含有氧元素
含氧酸
无氧酸
根据一定条件下能电离出H+的数目
一元酸
二元酸
三元酸
根据电离程度
强酸
弱酸
根据沸点高低
高沸点酸
低沸点酸
盐
根据生成盐时酸、碱中和反应进行的程度
正盐
酸式盐
碱式盐
选项
X
Y
Z
A
硫酸铜晶体
混合物
盐
B
氢氧化铁
胶体
分散系
C
电解质
化合物
纯净物
D
稀硫酸
酸
电解质
宏观
有新物质生成的是化学变化,反之是物理变化
微观
有旧化学键断裂,同时有新化学键形成的是化学变化,本质是原子的重新组合
新教材宁陕2024届高考化学一轮复习学案第8章物质在水溶液中的行为第51讲沉淀溶解平衡鲁科版: 这是一份新教材宁陕2024届高考化学一轮复习学案第8章物质在水溶液中的行为第51讲沉淀溶解平衡鲁科版,共8页。
新教材宁陕2024届高考化学一轮复习学案第8章物质在水溶液中的行为第49讲溶液中“粒子”浓度关系鲁科版: 这是一份新教材宁陕2024届高考化学一轮复习学案第8章物质在水溶液中的行为第49讲溶液中“粒子”浓度关系鲁科版,共5页。
新教材宁陕2024届高考化学一轮复习学案第8章物质在水溶液中的行为第48讲酸碱中和滴定及拓展应用鲁科版: 这是一份新教材宁陕2024届高考化学一轮复习学案第8章物质在水溶液中的行为第48讲酸碱中和滴定及拓展应用鲁科版,共8页。












