





第2讲 离子反应 课件—2025届高考化学大一轮复习
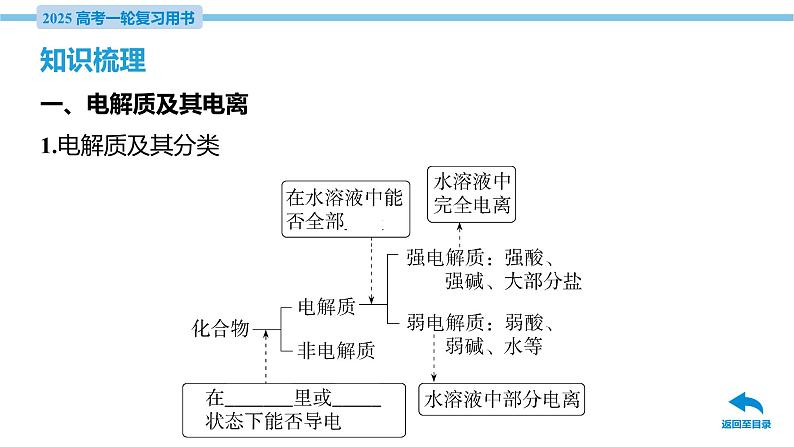
展开第一章 化学物质及其变化
课标要求 1.了解电解质、强电解质和弱电解质的概念,认识酸、碱、盐等电解质在水溶液中或熔融状态下能发生电离。2.通过实验事实认识离子反应及其发生的条件,并能正确书写离子方程式。3.掌握离子共存的条件,会判断溶液中离子能否大量共存。4.掌握常见离子的检验,能根据实验现象推断溶液中的某些离子。5.掌握与量有关的离子方程式的书写。
点拨 一般来说,在书写电离方程式时,弱酸酸式盐在水溶液中电离为阳离子与酸式酸根离子;强酸酸式盐在熔融状态电离为阳离子与酸式酸根离子,在水溶液中酸式酸根离子进一步电离为氢离子和酸根离子。
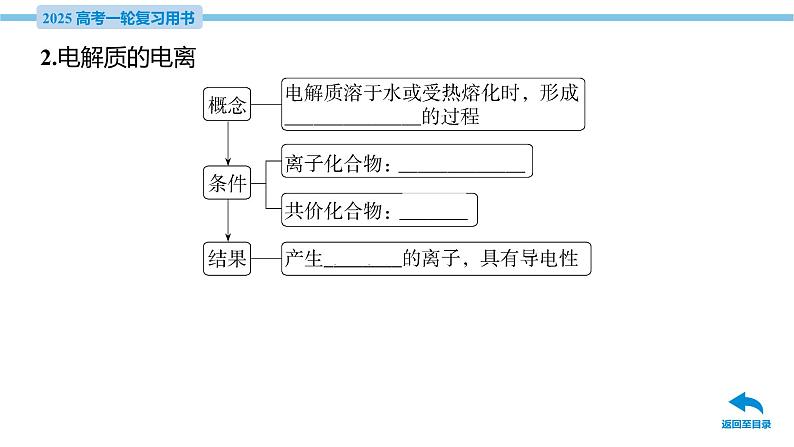
4.电解质溶液的导电能力
1.概念:有离子参加或有离子生成的反应统称为离子反应。2.类型
3.离子方程式(1)概念:用实际参加反应的__________来表示反应的式子。(2)意义:离子方程式不仅可以表示某一个具体的化学反应,还可以表示同一类型的离子反应。
. .
1.离子共存的本质几种离子在同一溶液中能大量共存,即离子之间________________;若离子之间能__________,则不能大量共存。
2.离子不能大量共存的几种类型(1)发生复分解反应①因生成沉淀(或微溶性物质)而不能大量共存
②因生成难电离的物质或气体而不能大量共存
(2)发生氧化还原反应氧化性与还原性的离子在溶液中会发生氧化还原反应不能大量共存。
(3)发生相互促进的水解反应易水解的阳离子和阴离子会发生相互促进的水解反应而不能大量共存,常见离子如下:
3.常见离子的检验与推断依据根据离子性质不同而在实验中所表现出的现象不同,可以把检验离子的方法归纳为三种类型:生成沉淀、生成气体、显现特殊颜色。
(1)依据生成的沉淀检验或推断
先产生白色沉淀,迅速变为灰绿色,最后变为红褐色
(2)依据生成的气体检验或推断
产生使湿润的红色石蕊试纸变蓝的气体
(3)依据显示特殊颜色检验或推断
(1) 氯水能导电,故氯水属于电解质。 ( )
2. (新教材改编)下列各组中的离子,能在溶液中大量共存的是( )
3. (2023·福建莆田期中)下列离子方程式不正确的是( )
考点一 电解质及其电离
考向1 电解质与非电解质 强电解质与弱电解质
1. (2023·福建厦门二模)下列食品添加剂不属于电解质的是( )
A. 二氧化硫B. 亚硝酸钠C. 葡萄糖酸D. 山梨酸钾
[解析] 亚硝酸钠属于盐,为电解质;葡萄糖酸属于有机酸,为电解质;山梨酸钾属于盐,为电解质。A符合题意。
2. (2023·山东威海期末)下列有关物质分类正确的是( )
归纳总结判断某物质是否属于电解质(或强、弱电解质)的思路
3. (2023·湖北武汉期末)模型认知是揭示化学本质的一种方法,下图为氯化钠固体溶于水的微观模型。下列说法正确的是( )
4. 下列电解质在水溶液中的电离方程式书写正确的是( )
考向3 影响电解质溶液导电性的因素
考点二 离子反应与离子方程式
1.离子方程式中物质化学式的拆分(1)一般规律①能拆分书写成离子形式的物质是易溶的强电解质,包括强酸、强碱、大多数可溶性盐。②不能拆分的物质包括单质、氧化物、弱电解质、难溶电解质、气体。
例 (2023·北京卷·6改编)下列离子方程式与所给事实不相符的是( )
2. (2023·山东济宁联考)有些离子方程式能表示一类反应,有些离子方程式却只能表示一个反应。下列离子方程式中,只能表示一个化学反应的是( )
考向2 离子方程式的书写与正误判断
3. (2023·河北秦皇岛三模)对于下列实验,能正确描述其反应的离子方程式的是( )
4. (2023·辽宁营口联考)下列离子方程式书写正确的是( )
5. 下列离子方程式书写正确的是( )
归纳总结离子方程式书写及正误判断
1.离子共存判断的三大步骤(1)细审题干关键点①注意“一定大量共存”“可能大量共存”“不能大量共存”“因发生氧化还原反应而不能大量共存”等关键点。②注意“透明溶液”表示无难溶物和微溶物,但并不表示溶液无色。
例2 (2023·湖北宜昌联考)下列各组离子在指定溶液中一定能大量共存的是( )
【迁移应用1】 (2023·广东江门联考)常温下,下列各组离子在指定溶液中能大量共存的是( )
【迁移应用3】 (2023·辽宁大连一模)下列离子组中加(或通)入相应试剂后,判断和分析均正确的是( )
考点四 离子的检验与推断
1. 下列由实验现象所得结论正确的是( )
2. (2023·辽宁本溪期末)根据下列实验内容得出的结论正确的是( )
下列结论正确的是( )
归纳总结离子推断的“四原则”
考点五 与量有关的离子方程式的书写
考向1 反应连续型(分步分析)
1. 写出下列反应的离子方程式。
2. 写出下列反应的离子方程式。
归纳总结连续型离子方程式书写步骤第一步:写出少量反应物反应的离子方程式;第二步:判断第一步的生成物能否与过量的反应物继续反应,若能反应,写出离子方程式;第三步:将前两步离子方程式相加,消去中间产物,即得反应物过量时的离子方程式。
考向2 反应先后型(先强后弱)
4. 写出下列反应的离子方程式。
归纳总结强弱型离子方程式书写规律(1)氧化还原型离子反应:一般来说,含多种还原剂的溶液中加入一种氧化剂时,还原性强的还原剂(离子)先被氧化;反之,含多种氧化剂的溶液中,加入一种还原剂时,氧化性强的氧化剂(离子)先被还原。(2)复分解型离子反应:若生成难溶物,可根据难溶物的溶解度来判断,溶解度越小的离子越先反应,但有时也要考虑离子共存(例如水解相互促进)的影响;若生成弱电解质,根据弱电解质的电离程度来判断,电离程度越小的离子越先反应。
考向3 物质配比型(少定多变)
1. (2023·浙江6月选考卷·9,3分)下列反应的离子方程式正确的是( )
2. (2021·广东卷·15,4分)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书写正确的是( )
第四讲 离子反应、离子方程式(课件)-【大一轮课堂】2024年高考化学大一轮复习课件+习题: 这是一份第四讲 离子反应、离子方程式(课件)-【大一轮课堂】2024年高考化学大一轮复习课件+习题,共60页。PPT课件主要包含了复习目标,电解质的电离,思想在线,离子反应和离子方程式,真题验收制胜高考,知能训练素养落实等内容,欢迎下载使用。
新高考化学一轮复习课件 第1章 第2讲 离子反应 离子方程式: 这是一份新高考化学一轮复习课件 第1章 第2讲 离子反应 离子方程式,共60页。PPT课件主要包含了高考化学一轮复习策略,离子反应离子方程式,电解质及电离,离子方程式的正误判断,真题演练明确考向,课时精练等内容,欢迎下载使用。
(新高考)高考化学大一轮复习课件第1章第3讲离子反应的应用(含解析): 这是一份(新高考)高考化学大一轮复习课件第1章第3讲离子反应的应用(含解析),共60页。PPT课件主要包含了复习目标,离子共存的判断,离子的检验和推断,依据图像推断离子,真题演练明确考向,课时精练等内容,欢迎下载使用。












