

高考化学一轮复习第1章物质及其变化第1讲物质的分类及转化学案
展开1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类。
2.能从物质类别的视角理解酸、碱、盐、氧化物的性质及转化规律。
3.理解物理变化与化学变化的区别与联系。
4.认识胶体是一种常见的分散系,能举例说明胶体的典型特征。
考点一 物质的组成与分类
1.物质的组成
(1)元素、物质及微粒间的关系。
(2)同素异形体。
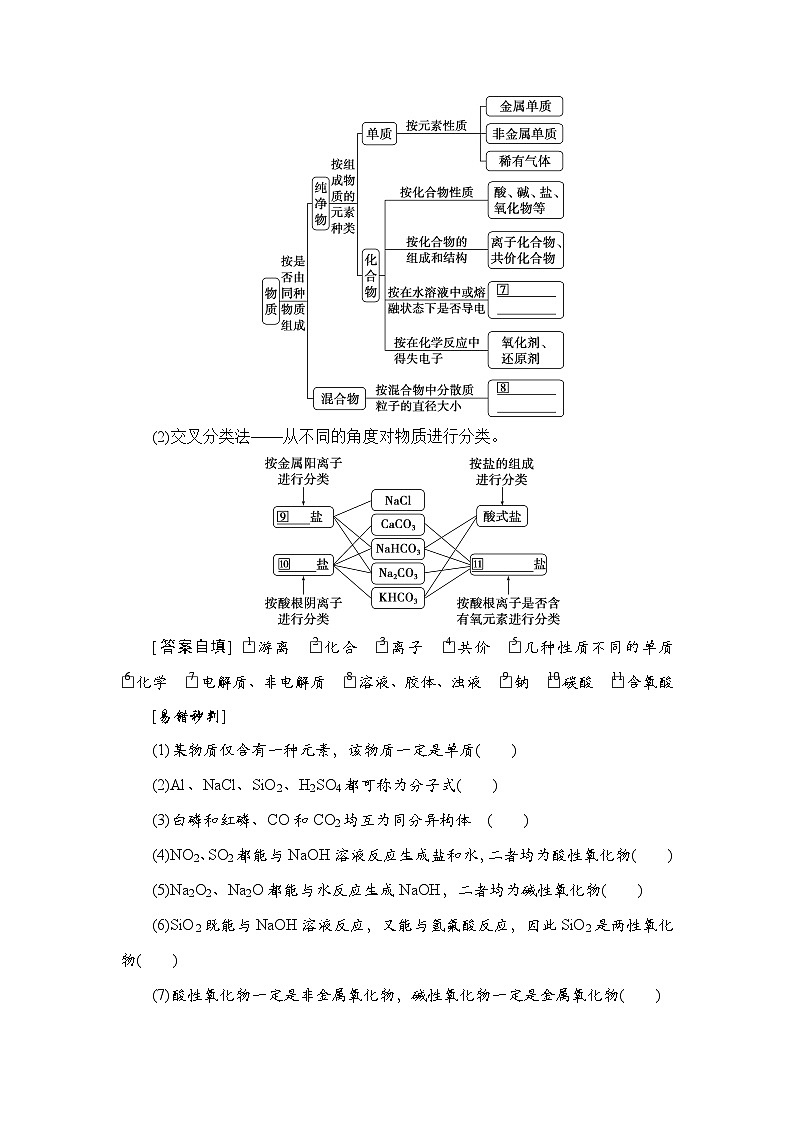
2.物质的分类
(1)树状分类法——对同类事物按照某种属性进行分类。
(2)交叉分类法——从不同的角度对物质进行分类。
[答案自填] eq \(□,\s\up1(1)) 游离 eq \(□,\s\up1(2)) 化合 eq \(□,\s\up1(3)) 离子 eq \(□,\s\up1(4)) 共价 eq \(□,\s\up1(5)) 几种性质不同的单质 eq \(□,\s\up1(6)) 化学 eq \(□,\s\up1(7)) 电解质、非电解质 eq \(□,\s\up1(8)) 溶液、胶体、浊液 eq \(□,\s\up1(9)) 钠 eq \(□,\s\up1(10)) 碳酸 eq \(□,\s\up1(11)) 含氧酸
[易错秒判]
(1)某物质仅含有一种元素,该物质一定是单质( )
(2)Al、NaCl、SiO2、H2SO4都可称为分子式( )
(3)白磷和红磷、CO和CO2均互为同分异构体 ( )
(4)NO2、SO2都能与NaOH溶液反应生成盐和水,二者均为酸性氧化物( )
(5)Na2O2、Na2O都能与水反应生成NaOH,二者均为碱性氧化物( )
(6)SiO2既能与NaOH溶液反应,又能与氢氟酸反应,因此SiO2是两性氧化物( )
(7)酸性氧化物一定是非金属氧化物,碱性氧化物一定是金属氧化物( )
(8)已知NaH2PO2是正盐,其水溶液呈碱性,则H3PO2属于一元弱酸( )
答案:(1)× (2)× (3)× (4)× (5)× (6)× (7)× (8)√
1.现有下列物质:①冰醋酸,②水煤气,③碱石灰,④普通玻璃,⑤水玻璃,⑥漂白粉,⑦H2SO4,⑧含氧40%的氧化镁,⑨汽油,⑩福尔马林,⑪密封保存的NO2气体,⑫胆矾,⑬液氨,⑭纤维素。
其中属于纯净物的是_____________________________(填序号)。
答案:①⑦⑧⑫⑬
2.对下列物质进行分类,并完善表格内容(填序号)。
①HNO3 ②H2S ③H3PO4 ④Ba(OH)2 ⑤NH3·H2O
⑥Cu(OH)2 ⑦BaSO4 ⑧NaHCO3 ⑨Cu2(OH)2CO3
⑩FeSO4·H2O
答案:② ② ① ③ ⑤⑥ ⑥ ⑧ ⑧⑩
3.下表中所示物质或概念间的从属关系符合图示的是( )
解析:选C。硫酸铜晶体是由一种物质组成的纯净物,属于盐,故A错误;氢氧化铁不是胶体,故B错误;稀硫酸为溶液,属于混合物,不属于电解质,故D错误。
考点二 物质的性质与转化
1.物质的性质与变化
a. eq \(□,\s\up1(1)) ________________b. eq \(□,\s\up1(2)) ______________
c. eq \(□,\s\up1(3)) ________________d. eq \(□,\s\up1(4)) ______________
2.化学反应的分类
化学反应 eq \b\lc\{(\a\vs4\al\c1(按\(□,\s\up1(5)) 分为\b\lc\{(\a\vs4\al\c1(离子反应,非离子反应)),按\(□,\s\up1(6)) 分为\b\lc\{(\a\vs4\al\c1(氧化还原反应,非氧化还原反应)),按\(□,\s\up1(7)) 分为\b\lc\{(\a\vs4\al\c1(可逆反应,不可逆反应)),按\(□,\s\up1(8)) 分为\b\lc\{(\a\vs4\al\c1(吸热反应,放热反应))))
3.单质、氧化物、酸(或碱)和盐的转化关系
(1)金属单质及其化合物的转化:金属单质 eq \(――→,\s\up7(O2)) 碱性氧化物 eq \(――→,\s\up7(H2O)) 碱 eq \(――→,\s\up7(酸)) 盐,如Na eq \(――→,\s\up7(O2)) Na2O eq \(――→,\s\up7(H2O)) NaOH eq \(――→,\s\up7(H2SO4)) Na2SO4,符合上述转化关系的常见金属有Na、K、Ca、Ba等,但 eq \(□,\s\up1(9)) ________、 eq \(□,\s\up1(10)) ________、 eq \(□,\s\up1(11)) ________、 eq \(□,\s\up1(12)) ________等不符合上述转化。
(2)非金属单质及其化合物的转化:非金属单质 eq \(――→,\s\up7(O2)) 酸性氧化物 eq \(――→,\s\up7(H2O)) 酸 eq \(――→,\s\up7(碱)) 盐,如S eq \(――→,\s\up7(O2)) SO2 eq \(――→,\s\up7(H2O)) H2SO3 eq \(――→,\s\up7(NaOH)) Na2SO3,符合上述转化关系的常见非金属有C、S、P等,但 eq \(□,\s\up1(13)) ______、 eq \(□,\s\up1(14)) ________等不符合上述转化。
[答案自填] eq \(□,\s\up1(1)) 物理性质 eq \(□,\s\up1(2)) 物理变化 eq \(□,\s\up1(3)) 化学性质
eq \(□,\s\up1(4)) 化学变化 eq \(□,\s\up1(5)) 反应中有无离子参与 eq \(□,\s\up1(6)) 反应中有无电子转移 eq \(□,\s\up1(7)) 反应进行的程度和方向 eq \(□,\s\up1(8)) 反应的能量变化
eq \(□,\s\up1(9)) Mg eq \(□,\s\up1(10)) Fe eq \(□,\s\up1(11)) Al eq \(□,\s\up1(12)) Cu eq \(□,\s\up1(13)) N eq \(□,\s\up1(14)) Si
[易错秒判]
(1)12C转化为13C、石墨转化为金刚石都属于化学变化( )
(2)NH4Cl溶液除铁锈是化学变化,食盐水导电是物理变化( )
(3)碳在足量氧气中燃烧生成CO2,故硫在足量氧气中燃烧生成SO3( )
(4)酸性氧化物都能与水反应生成相应的酸( )
(5)化石能源的燃烧是放热反应( )
(6)FeCl3与铜的反应属于置换反应( )
答案:(1)× (2)× (3)× (4)× (5)√ (6)×
[名师点睛]
物质变化中的“三馏”“四色”“五解”和“十六化”
1.下列变化中,涉及化学变化的是________。
①冰雪融化 ②明矾净水
③钾的焰色试验 ④碘的升华
⑤氯化铵分解 ⑥铝遇浓硫酸钝化
⑦蛋白质的显色反应 ⑧电解食盐水
⑨CaCl2的潮解 ⑩石油的分馏
⑪煤的气化 ⑫石油的裂化、裂解
⑬蛋白质的盐析 ⑭同素异形体间的转化
答案:②⑤⑥⑦⑧⑪⑫⑭
2.铁、稀盐酸、澄清石灰水、氯化铜溶液间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,A、B、C、D依次对应的四种反应类型正确的是( )
A.复分解反应、复分解反应、化合反应、置换反应
B.中和反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
解析:选C。A为Ca(OH)2+2HCl===CaCl2+2H2O(复分解反应或中和反应);B为Ca(OH)2+CuCl2===CaCl2+Cu(OH)2↓(复分解反应);C为Fe+CuCl2===FeCl2+Cu(置换反应);D为Fe+2HCl===FeCl2+H2↑(置换反应)。
3.有关物质之间的部分转化关系如图所示,其中“———”表示物质之间能发生化学反应,“―→”表示物质之间的转化关系。下列说法正确的是( )
A.物质X是一种常见的酸性氧化物
B.反应②一定有盐参加反应
C.向Ca(OH)2溶液中加入CaO,所得溶液的溶质质量分数一定增大
D.图中的部分反应可能是置换反应
解析:选A。物质X是CO2,是一种常见的酸性氧化物,A项正确;反应②可以是Ca(OH)2与CO2反应,B项错误;若Ca(OH)2 溶液是饱和溶液,则加入CaO后所得溶液的溶质质量分数不变,C项错误;题图中的所有反应均为酸、碱、盐、氧化物之间的反应,不可能存在置换反应,D项错误。
考点三 分散系 胶体
1.分散系
(1)概念: eq \(□,\s\up1(1)) __________________________ ________________________所形成的混合物。
(2)分类:根据 eq \(□,\s\up1(2)) ________________________将分散系分为溶液、胶体和浊液,直观表示如下:
2.胶体的性质及应用
3.Fe(OH)3胶体的制备
(1)制备原理: eq \(□,\s\up1(10)) _______________________________________。
(2)具体操作:用烧杯取少量蒸馏水,加热至沸腾,向沸水中逐滴加入5~6滴饱和FeCl3溶液。继续煮沸至液体呈红褐色,停止加热,即得Fe(OH)3胶体。
[答案自填] eq \(□,\s\up1(1)) 一种(或多种)物质以粒子形式分散到另一种(或多种)物质中 eq \(□,\s\up1(2)) 分散质粒子的直径大小 eq \(□,\s\up1(3)) 溶液 eq \(□,\s\up1(4)) 胶体 eq \(□,\s\up1(5)) 浊液 eq \(□,\s\up1(6)) 溶液 eq \(□,\s\up1(7)) 胶体 eq \(□,\s\up1(8)) 电解质 eq \(□,\s\up1(9)) 加热、搅拌 eq \(□,\s\up1(10)) FeCl3+3H2O eq \(=====,\s\up7(△)) Fe(OH)3(胶体)+3HCl
[易错秒判]
(1)雾、云、烟都属于气溶胶( )
(2)胶体区别于其他分散系的本质特征是丁达尔效应( )
(3)利用丁达尔效应可区分蛋白质溶液和食盐水( )
(4)明矾水解时产生具有吸附性的胶体粒子,可用作净水剂( )
(5)碳纳米管属于胶体分散系,该材料具有超强的吸附能力( )
(6)向浓氨水中滴加饱和FeCl3溶液可制得Fe(OH)3胶体( )
(7)16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA( )
答案:(1)√ (2)× (3)√ (4)√ (5)× (6)×
(7)×
1.(2024·东莞光正实验学校月考)中国农业科学院饲料研究所发布,我国在国际上首次实现从一氧化碳到蛋白质的合成。蛋白质是有机高分子,其分子直径为2~20 nm。下列分散质粒子直径为1~100 nm的是( )
A.稀硫酸 B.硫酸铜溶液
C.有色玻璃 D.酒精溶液
解析:选C。分散质粒子直径为1~100 nm的分散系属于胶体。稀硫酸、硫酸铜溶液、酒精溶液均属于溶液,分散质粒子直径小于1 nm,有色玻璃为胶体,分散质粒子直径为1~100 nm,故选C。
2.有两种分散系:①FeCl3溶液;②将饱和FeCl3溶液加入沸水中,得到的红褐色液体。下列有关说法正确的是( )
A.分散质粒子直径:①>②
B.光束照射②时,可以看到一条光亮的“通路”
C.稳定性:①<②
D.①属于混合物,②属于纯净物
解析:选B。胶体的分散质粒子直径大于溶液的分散质粒子直径,故分散质粒子直径:①<②,A错误;②中红褐色液体是胶体,光束照射②时,产生丁达尔效应,可以看到一条光亮的“通路”,B正确;溶液的稳定性强于胶体的,故稳定性:①>②,C错误;溶液和胶体都是分散系,都是混合物,D错误。
3.(2024·广州大学附中测试)下列事实中,与胶体性质无直接关系的是( )
A.浑浊的泥水加入明矾可变澄清
B.澄清的石灰水通入二氧化碳后变浑浊
C.鸡蛋白水溶液加入大量的饱和硫酸铵溶液后产生白色沉淀
D.牛奶稀释后,用凸透镜聚集强光照射该牛奶,从垂直光源方向观察到一条清晰可见的光路
解析:选B。A.明矾净水的原理是明矾电离出的铝离子水解形成氢氧化铝胶体,胶体具有吸附性,可以使水变澄清,与胶体性质有直接关系;B.澄清的石灰水通入二氧化碳后变浑浊是因为生成了碳酸钙沉淀,与胶体性质无直接关系;C.鸡蛋白水溶液是胶体,加入饱和硫酸铵溶液会发生盐析,与胶体性质有直接关系;D.牛奶属于胶体,用光照射胶体,可以观察到丁达尔效应,与胶体性质有直接关系。
1.(2023·新高考江苏卷)我国提出力争2060年实现碳中和的目标,体现了大国担当。碳中和中的碳是指( )
A.碳原子 B.二氧化碳
C.碳元素 D.含碳物质
答案:B
2.(2023·新高考福建卷)唐代陆羽《茶经·三之造》中记载茶叶制作过程:“晴,采之,蒸之,捣之,拍之,焙之,穿之,封之,茶之干矣”。以下操作中最不可能引起化学变化的是( )
A.蒸 B.捣
C.焙 D.封
解析:选D。“蒸”时茶去掉了生腥的草味,加热引起颜色的变化,有新物质产生,故A不符合题意;“捣”时捣泥压榨,去汁压饼,让茶叶的苦涩味大大降低,可能引起物质的变化,故B不符合题意;“焙”时烘焙加热可能引起物质分解、氧化等,故C不符合题意;“封”时保持茶叶干燥、防止氧化,最不可能引起化学变化,故D符合题意。
3.(2023·浙江1月选考)下列物质中属于耐高温酸性氧化物的是( )
A.CO2 B.SiO2
C.MgO D.Na2O
答案:B
4.(2022·浙江6月选考)下列物质对应的化学式正确的是( )
A.白磷:P2
B.2-甲基丁烷:(CH3)2CHCH2CH3
C.胆矾:FeSO4·7H2O
D.硬脂酸:C15H31COOH
解析:选B。白磷的化学式为P4,A项错误;2-甲基丁烷的化学式为(CH3)2CHCH2CH3,B项正确;胆矾的化学式为CuSO4·5H2O,C项错误;硬脂酸的化学式为C17H35COOH,D项错误。
5.(2022·新高考湖南卷)化学促进了科技进步和社会发展。下列叙述中没有涉及化学变化的是( )
A.《神农本草经》中记载的“石胆能化铁为铜”
B.利用“侯氏联合制碱法”制备纯碱
C.科学家成功将CO2转化为淀粉或葡萄糖
D.北京冬奥会场馆使用CO2跨临界直冷制冰
解析:选D。CO2跨临界直冷制冰是利用液态CO2汽化吸热导致周围环境温度下降,从而使水结冰,属于物理变化,D项符合题意。
课时跟踪练
[基础巩固]
1.(2024·广州白云中学高三测试)我国是一个历史悠久的文明古国。下列古代生产工艺中涉及化学变化的是( )
A.烧制瓷器 B.纺纱织布
C.雕刻石像 D.活字印刷
答案:A
2.(2024·广东四校联考)以下物质属于混合物的是( )
A.液氯 B.漂白粉
C.胆矾 D.碳酸氢钠
答案:B
3.顺式Pt(NH3)2Cl2(相对分子质量为300)是临床广泛使用的抗肿瘤药物。下列有关说法正确的是( )
A.Pt的化合价为+4价
B.该物质由PtCl2和NH3组成,属于混合物
C.NH3属于碱
D.该物质由4种元素组成
解析:选D。顺式Pt(NH3)2Cl2中Pt的化合价为+2价,A错误;顺式Pt(NH3)2Cl2是化合物,B错误;NH3是氢化物,不是碱,C错误;顺式Pt(NH3)2Cl2由Pt、N、H、Cl 4种元素组成,D正确。
4.(2024·东莞光正实验学校月考)广东有众多国家级非物质文化遗产,如广东剪纸、粤绣、潮汕工夫茶和香云纱染整技艺等。下列说法不正确的是( )
A.广东剪纸的裁剪过程不涉及化学变化
B.冲泡工夫茶时茶香四溢,体现了分子是不断运动的
C.制作粤绣所用的植物纤维布含有天然高分子
D.染整技艺中去除丝胶所用的纯碱水溶液属于纯净物
解析:选D。A.广东剪纸的裁剪过程中没有新物质生成,故不涉及化学变化,A正确;B.冲泡工夫茶时茶香四溢,是因为茶水的香味分子不停地做无规则运动,扩散到空气中,B正确;C.制作粤绣所用的植物纤维布含有纤维素,属于天然高分子,C正确;D.染整技艺中去除丝胶所用的纯碱水溶液属于混合物,D错误。
5.(2024·广东四校联考)下列说法正确的是( )
A.硫酸、纯碱、碳酸氢钠和生石灰分别属于酸、碱、盐和氧化物
B.只含一种元素的物质可能为混合物,也可能为纯净物
C.生石灰与水混合的过程只发生物理变化
D.H2O、HCOOH、[Cu(NH3)4]SO4中均含有氧元素,都是氧化物
解析:选B。A.纯碱是碳酸钠,属于盐,A错误;B.只含一种元素的物质可能为纯净物,如石墨,也可能为混合物,如金刚石与石墨,B正确;C.CaO俗称生石灰,可与水发生反应CaO+H2O===Ca(OH)2,有新物质生成,故生石灰与水混合的过程中发生了化学变化,C错误;D.氧化物是由两种元素组成,其中一种元素是氧元素的化合物,HCOOH和[Cu(NH3)4]SO4 不属于氧化物,D错误。
6.下图是一种具有磁性的“纳米药物分子车”,可利用磁性引导药物到达人体内的病变部位。该技术可大大提高治疗效果。下列有关说法不正确的是( )
A.该“纳米药物分子车”分散于水中可得到胶体
B.葡萄糖等含碳化合物属于有机化合物
C.该“纳米药物分子车”属于混合物
D.该“纳米药物分子车”中的二氧化硅属于酸性氧化物
解析:选A。该“纳米药物分子车”的直径为200 nm,而胶体分散质粒子的直径为1~100 nm,所以该“纳米药物分子车”分散于水中不能得到胶体,A项错误;葡萄糖等含碳化合物属于有机化合物,B项正确;该“纳米药物分子车”属于混合物,C项正确;酸性氧化物是与碱反应只生成相应的盐和水的氧化物,该“纳米药物分子车”中的二氧化硅属于酸性氧化物,D项正确。
7.将少量含有AlCl3的泥沙倒入120 mL水中,充分搅拌后,注入如图所示装置中(刚好盛满),静置一段时间后,下列说法不正确的是 ( )
A.溶液和胶体中分散质粒子都能透过滤纸
B.溶液中的分散质粒子能透过半透膜
C.用激光笔照射中层分散系,在侧面能看到一条光亮的通路
D.Cl-仅存在于下层的分散系中
解析:选D。溶液和胶体中分散质粒子都能透过滤纸,浊液中分散质粒子不能透过滤纸,溶液中分散质粒子能透过半透膜,胶体中分散质粒子和浊液中分散质粒子不能透过半透膜;中层分散系为胶体分散系,能产生丁达尔效应,故用激光笔照射中层分散系,在侧面能看到一条光亮的通路;Cl-能透过滤纸和半透膜,所以上、中、下层的分散系中都含有Cl-。
8.表格中的各组物质,可以实现X eq \(――→,\s\up7(M)) Y eq \(――→,\s\up7(M)) Z(每步只发生一个反应)的转化的是( )
解析:选B。铁和氯气反应生成氯化铁,A错误;C和O2反应生成CO,CO和O2反应生成CO2,每步反应都可以实现,B正确;碳酸钠不能和氢氧化钠反应,C错误;氢氧化铝不能和CO2反应,D错误。
9.铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”,化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
铜 eq \(――→,\s\up7(①)) 铜绿 eq \(――→,\s\up7(②)) A eq \(――→,\s\up7(③)) Cu(OH)2 eq \(――→,\s\up7(④)) B eq \(――→,\s\up7(⑤),\s\d5(H2)) 铜
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:________________________________________________。
(2)请写出“铜绿”与盐酸反应的化学方程式:
______________________________________________________。
(3)写出反应④⑤的化学方程式:
④____________________________________________________;
⑤____________________________________________________。
(4)上述转化过程中属于化合反应的是________(填序号,下同),属于复分解反应的是________,属于分解反应的是________。
答案:(1)盐、铜盐、碱式盐(或碳酸盐)
(2)Cu2(OH)2CO3+4HCl===2CuCl2+3H2O+CO2↑ (3)Cu(OH)2 eq \(=====,\s\up7(△)) CuO+H2O CuO+H2 eq \(=====,\s\up7(△)) Cu+H2O
(4)① ②③ ④
[素养提升]
10.甲、乙、丙、丁对应的物质与图示类别相符的是( )
A.甲——氧化钠 B.乙——氯化钾
C.丙——次氯酸钠 D.丁——氢氧化钠
解析:选C。碱性氧化物是指能与酸反应生成盐和水的氧化物,氧化钠是碱性氧化物,但其阴离子和阳离子的个数之比为1∶2,A不相符;KCl中无氧元素,不属于含氧酸盐,B不相符;NaClO含有氧元素,属于含氧酸盐,NaClO溶液中的ClO-水解生成HClO,HClO具有强氧化性,可漂白有色物质,C相符;2NaOH+Br2===NaBr+NaBrO+H2O,氢氧化钠能使溴水褪色,但不能漂白有色物质,D不相符。
11.如下图为常见物质的转化关系。下列说法正确的是 ( )
A.氢化物不一定均为气态,但均能与水反应
B.氧化物M2中M的化合价一定比M1中的高
C.最后生成的碱一定为强碱,但生成酸时,不一定是强酸
D.转化关系图中的所有反应一定都是氧化还原反应
解析:选C。由转化关系图可知,单质M可以是金属Na,也可以是非金属单质C、N、S等。若氢化物为CH4、H2S,与水不反应,故A错误;若M2为Na2O2,M1为Na2O,Na2O2与Na2O中Na的化合价均为+1价,故B错误;CO2和H2O反应、SO3和H2O反应均不属于氧化还原反应,故D错误。
12.(2024·梅州模拟)下图是磷酸、亚磷酸、次磷酸的结构式,其中磷酸为三元中强酸,亚磷酸为二元弱酸。下列说法正确的是( )
A.磷酸(H3PO4)的电离方程式为H3PO4⇌3H++PO eq \\al(3-,4)
B.亚磷酸(H3PO3)与足量NaOH溶液反应生成Na3PO3
C.NaH2PO4溶液呈酸性,是因为H2PO eq \\al(-,4) 的水解程度大于其电离程度
D.NaH2PO2溶液呈碱性
解析:选D。磷酸为三元中强酸,分步电离,电离方程式为H3PO4⇌H++H2PO eq \\al(-,4) 、H2PO eq \\al(-,4) ⇌H++HPO eq \\al(2-,4) 、HPO eq \\al(2-,4) ⇌H++PO eq \\al(3-,4) ,故A错误;亚磷酸为二元弱酸,只能电离出两个氢离子,所以与足量NaOH溶液反应生成Na2HPO3,故B错误;NaH2PO4溶液呈酸性,说明H2PO eq \\al(-,4) 的电离程度大于其水解程度,故C错误;磷酸含有三个羟基氢为三元酸,亚磷酸含有两个羟基氢为二元酸,而次磷酸只含一个羟基氢,所以应为一元酸,所以NaH2PO2为正盐,且为强碱弱酸盐,溶液中存在次磷酸根离子的水解,使溶液显碱性,故D正确。
13.由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素的化合价是+3价,则其中铁元素的化合价是________价。CrO eq \\al(-,2) 是一种酸根离子,则Fe(CrO2)2属于________(填“酸”“碱”“盐”或“氧化物”)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是________(填字母)。
A.都不稳定,密封放置会产生沉淀
B.均有丁达尔效应
C.分散质粒子均可透过滤纸
(3)现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜袋内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明Na2SO4中硫酸根离子能够透过半透膜:
_________________________________________________________
________________________________________________________。
(4)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应后得到的FeCl3溶液呈棕黄色。用此溶液进行以下实验:
①取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为____________________________________________________。
②在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至液体呈红褐色,停止加热,制得的分散系为________________,鉴别此分散系和溶液的方法是________________。
答案:(1)+2 盐 (2)C (3)取烧杯中的液体,加入适量的稀盐酸,再加入BaCl2溶液,若产生白色沉淀,则证明SO eq \\al(2-,4) 透过了半透膜(答案合理即可) (4)①FeCl3+3NaOH===Fe(OH)3↓+3NaCl ②Fe(OH)3胶体 丁达尔效应
14.如图为“一些物质与水”的分类图,利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化学反应类型的角度可以将物质分类。将上述物质分为A、B两组的依据是________________________________________;
C组物质与水反应时水既不是氧化剂又不是还原剂,则D组物质为________。
(2)从化合价的角度可以预测Na2O2的性质。
①Na2O2的性质为________(填字母,下同)。
a.只有氧化性 b.只有还原性
c.既有氧化性又有还原性
②Na2O2以氧化性为主,将Na2O2加入含有SO eq \\al(2-,3) 的溶液中反应结束后,硫元素存在形式合理的是________。
a.S2- b.S c.SO eq \\al(2-,4)
(3)从物质分类的角度可以推测物质的性质。化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质分类角度看,不恰当的一种物质是________________(填化学式)。
②“三酸”中一种酸的浓溶液能与氯酸钾反应得到黄绿色气体,该反应的离子方程式为__________________________________。
解析:(1)A组物质与水反应时元素化合价均不发生变化;B组物质与水反应时均有元素化合价的变化,故将题述物质分为A、B两组的依据是与水反应是否为氧化还原反应;已知C组物质与水反应时水既不是氧化剂又不是还原剂,氯气、过氧化钠、二氧化氮符合C组条件,则D组物质为Na。(2)①Na2O2 中氧元素的化合价为-1价,既可降低又可升高,故过氧化钠既有氧化性又有还原性。②Na2O2 以氧化性为主,将Na2O2 加入含有SO eq \\al(2-,3) 的溶液中反应,可将SO eq \\al(2-,3) 氧化为SO eq \\al(2-,4) 。(3)①纯碱是碳酸钠,属于盐,不是碱,故不恰当的一种物质是Na2CO3。②“三酸”(硝酸、硫酸和盐酸)中一种酸的浓溶液能与氯酸钾反应得到黄绿色气体氯气,反应的离子方程式为5Cl-+ClO eq \\al(-,3) +6H+===3Cl2↑+3H2O。
答案:(1)与水反应是否为氧化还原反应 Na
(2)①c ②c
(3)①Na2CO3 ②5Cl-+ClO eq \\al(-,3) +6H+===3Cl2↑+3H2O
类别
分类依据
类型判断
酸
根据酸根离子是否含氧元素:含氧酸、无氧酸
属于无氧酸的是_____________________________________________________________________
根据电离出H+的个数:一元酸、二元酸、多元酸
属于二元酸的是_____________________________________________________________________
根据电离程度:强酸、弱酸
属于强酸的是_______________________________________________________________________
根据沸点高低:高沸点酸、低沸点酸
属于高沸点酸的是_____________________________________________________________________
碱
根据电离程度:强碱、弱碱
属于弱碱的是_____________________________________________________________________
根据水溶性:可溶性碱、难溶性碱
属于难溶性碱的是___________________________________________________________________
盐
根据中和反应进行的程度:正盐、酸式盐、碱式盐
属于酸式盐的是_____________________________________________________________________
根据溶解性:易溶性盐、难溶性盐
属于易溶性盐的是_____________________________________________________________________
选项
X
Y
Z
A
硫酸铜晶体
混合物
盐
B
氢氧化铁
胶体
分散系
C
电解质
化合物
纯净物
D
稀硫酸
酸
电解质
项目
物理变化
化学变化
三馏
蒸馏、分馏
干馏
四色
焰色试验
显色反应、颜色反应、指示剂变色反应
五解
潮解
分解、电解、水解、裂解
十六化
熔化、汽化、
液化、升华
氧化、风化、钝化、催化、皂化、歧化、硝化、酯化、裂化、油脂的硬化、煤的气化、煤的液化
选项
X
Y
Z
M
A
Fe
FeCl2
FeCl3
Cl2
B
C
CO
CO2
O2
C
CO2
Na2CO3
NaHCO3
NaOH
D
[Al(OH)4]-
Al(OH)3
Al3+
CO2
2024年高考化学一轮总复习 第1单元 第1讲 物质的分类及转化 学案(含高考真题和课后作业)(教师版 ): 这是一份2024年高考化学一轮总复习 第1单元 第1讲 物质的分类及转化 学案(含高考真题和课后作业)(教师版 ),共26页。学案主要包含了物质的组成,物质的分类等内容,欢迎下载使用。
人教版高考化学一轮复习第1章物质及其变化第1节物质的分类及转化学案含答案: 这是一份人教版高考化学一轮复习第1章物质及其变化第1节物质的分类及转化学案含答案
人教版高考化学一轮总复习第1章第1节物质的分类及转化课时学案: 这是一份人教版高考化学一轮总复习第1章第1节物质的分类及转化课时学案,共16页。












