






模块3 主题3 第3讲 盐类的水解及应用 课件 2025高考化学一轮复习
展开1. 认识盐类水解的本质,理解盐溶液呈酸碱性的原因。能用化学用语对盐类水解的过程进行表征。2. 会判断浓度、温度、酸碱度等对盐类水解平衡的影响,归纳盐类水解的规律。3. 知道盐类水解在生产、生活中的应用。4. 学会应用所学知识设计实验,并对实验方案进行改进。
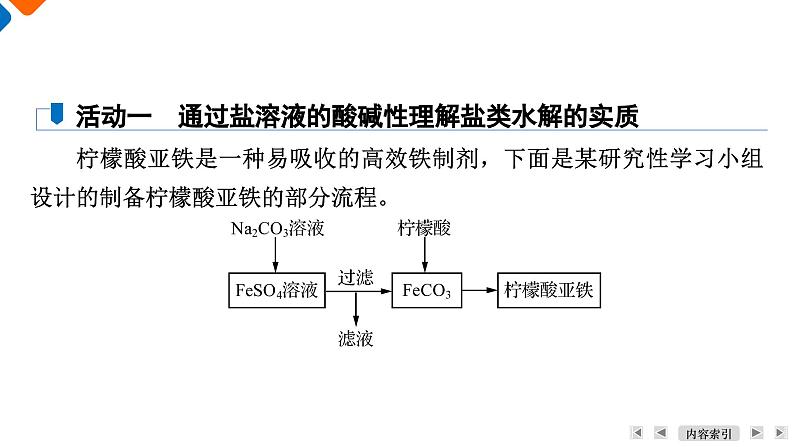
柠檬酸亚铁是一种易吸收的高效铁制剂,下面是某研究性学习小组设计的制备柠檬酸亚铁的部分流程。
活动一 通过盐溶液的酸碱性理解盐类水解的实质
1. 小组成员在制备碳酸亚铁的实验操作过程中将FeSO4溶液滴入碳酸钠溶液中,观察到白色沉淀变成灰绿色最终变成红褐色。试分析该白色沉淀的成分以及产生该沉淀的原因。【答案】 碳酸钠溶液显碱性,操作时滴加的顺序错误,导致碱性条件下亚铁离子变成氢氧化亚铁沉淀。2. 请分别用化学用语表示FeSO4和Na2CO3两种溶液呈现不同酸碱性的原因。
3. 将下列盐溶液根据酸碱性进行分类。盐可以看成是酸碱中和反应的产物,概括盐的酸碱性与生成该盐对应的酸和碱强弱的关系。①KNO3 ②CH3COONa ③Na3PO4 ④FeCl3 ⑤NH4Cl【答案】 ①强酸强碱盐(显中性),②③强碱弱酸盐(显碱性),④⑤强酸弱碱盐(显酸性)4. 制备柠檬酸亚铁的过程中,若要获得较纯净的FeCO3,合理的混合方式是什么?【答案】 将碳酸钠溶液缓慢滴入硫酸亚铁溶液中,并不断搅拌。
1. 分别写出CH3COOH的电离平衡常数(Ka)和CH3COONa的水解平衡常数(Kh)的表达式,并找出两者之间的关系。
活动二 探究影响盐类水解平衡的因素
2. 根据下表提供的数据,比较常温下物质的量浓度相同的四种溶液的pH大小。 ①CH3COONa ②Na2CO3 ③NaHCO3 ④NaCN【答案】 ②>④>③>①
3. 哪些外界条件的改变可以影响Na2CO3的水解平衡?如何影响?【答案】 温度,升高温度,碳酸根离子的水解平衡正向移动。加水稀释,水解平衡正向移动。增加碳酸钠浓度,水解平衡正向移动。加入其他离子如钙离子,结合碳酸根离子,水解平衡逆向移动。4. 判断向碳酸钠溶液中加水稀释,水解平衡的移动方向。并通过计算比较浓度商(Qc)和水解平衡常数(Kh)的大小,证明你的结论。
【答案】 取少量Na2CO3溶液于试管中,往其中滴加几滴酚酞,再滴加足量的氯化钙溶液。开始时,滴加酚酞溶液变红,加入氯化钙之后产生白色沉淀,溶液变成无色。
1. 研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、Al2O3、SiO2)出发,设计了如下流程,制得硫酸亚铁溶液,最终获得柠檬酸亚铁。
活动三 认识盐类水解的知识在生产、生活中的广泛应用
下表列出了有关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1 ml·L-1计算)。
(1) 由硫铁矿烧渣制备柠檬酸亚铁溶液的过程中过量硫酸的作用是什么?【答案】 使硫铁矿烧渣充分反应,提高铁元素的浸出率。抑制铁离子的水解。(2) 请结合所学知识补全流程中缺少的操作步骤。【答案】 向滤液中加入足量的铁粉,调节pH至5.0~5.8,过滤后补加少量稀硫酸。
2. 结合生产、生活中实际,应用盐类水解等知识对下列事实作出合理的解释。(1) 直接加热MgSO4·7H2O晶体可制取无水MgSO4,但却不能直接加热MgCl2·6H2O制取MgCl2。【答案】 直接加热MgSO4·7H2O晶体,水解产生的硫酸会一直抑制镁离子的水解,所以可以制取无水MgSO4,但直接加热MgCl2·6H2O,水解产生的氯化氢会挥发,不断地促进镁离子的水解,直到水解完全变成氢氧化镁。
(2) 纯碱可用于去除油污,热的纯碱溶液去除油污的效果比冷的纯碱溶液效果更好。【答案】 水解反应吸热,温度升高,促进碳酸钠的水解,溶液碱性增强,去污能力增强。(3) 草木灰(K2CO3)和硫酸铵是常用的农业肥料,但两种肥料不能同时使用,同时使用会造成氮元素流失。
(4) 实验室利用向沸水中滴加饱和的氯化铁溶液的方法制备氢氧化铁胶体。【答案】 加热促进铁离子的水解和生成的氯化氢的挥发,从而制得氢氧化铁胶体。(5) 盛放Na2S、Na2CO3的试剂瓶不能用玻璃塞。【答案】 Na2S、Na2CO3溶液因为水解而呈碱性,可与玻璃中的二氧化硅反应生成硅酸钠,导致瓶塞与瓶口粘在一起。(6) 配制氯化铁溶液时,先将氯化铁溶于较浓的盐酸中,然后再进行稀释。【答案】 盐酸中的氢离子抑制铁离子的水解,防止配制时产生沉淀。
1 (浙江卷)25 ℃时,苯酚(C6H5OH)的Ka=1.0×10-10,下列说法正确的是( )A. 相同温度下,等pH的C6H5ONa和CH3COONa溶液中, c(C6H5O-)>c(CH3COO-)B. 将浓度均为0.10 ml·L-1的C6H5ONa和NaOH溶液加热,两种溶液的pH均变大C. 25 ℃时,C6H5OH溶液与NaOH溶液混合,测得pH=10.00,则此时溶液中c(C6H5O-)=c(C6H5OH)D. 25 ℃时,0.10 ml·L-1的C6H5OH溶液中加少量C6H5ONa固体,水的电离程度变小【答案】 C
3 某实验室回收废水中苯酚的过程如下图所示。已知:苯酚的电离常数Ka=1.0×10-10,H2CO3的电离常数Ka1=4.4×10-7, Ka2=5.6×10-11。下列有关说法正确的是( )
4 (浙江卷)下列说法不正确的是( )A. 2.0×10-7ml·L-1的盐酸中c(H+)=2.0×10-7ml·L-1B. 将KCl溶液从常温加热至80 ℃,溶液的pH变小但仍保持中性C. 常温下,NaCN溶液呈碱性,说明HCN是弱电解质D. 常温下,向pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大【答案】 A
5 一定条件下,通过下列实验探究盐类水解的应用。
下列有关说法不正确的是( )A. 实验1中红褐色液体在激光笔照射下会产生光亮的“通路”B. 实验2中明矾电离出的Al3+吸附了水中的悬浮物而产生沉淀
6 室温下,通过下列实验来探究NH4HCO3的性质。实验1:测得0.1 ml·L-1 NH4HCO3溶液的pH=9.68。实验2:向浓度为0.1 ml·L-1 NH4HCO3溶液中加入足量NaOH,有刺激性气味气体产生。实验3:浓度均为2.0 ml·L-1 NH4HCO3溶液和NaCl溶液等体积混合,有晶体析出,过滤。
模块2 主题2 第3讲 氮及其化合物 课件 2025高考化学一轮复习: 这是一份模块2 主题2 第3讲 氮及其化合物 课件 2025高考化学一轮复习,共43页。PPT课件主要包含了学习目标,活动方案,答案略,答案反应①③,答案取代反应,答案显色反应,链接真题,答案B,答案C,倒置的烧瓶内等内容,欢迎下载使用。
模块2 主题1 第4讲 金属资源的开发 课件 2025高考化学一轮复习: 这是一份模块2 主题1 第4讲 金属资源的开发 课件 2025高考化学一轮复习,共28页。PPT课件主要包含了学习目标,活动方案,链接真题等内容,欢迎下载使用。
模块2 主题1 第3讲 铁及其化合物 课件 2025高考化学一轮复习: 这是一份模块2 主题1 第3讲 铁及其化合物 课件 2025高考化学一轮复习,共32页。PPT课件主要包含了学习目标,活动方案,链接真题等内容,欢迎下载使用。












