

2024年天津市和平区中考三模化学试题
展开第Ⅰ卷(选择题 共30分)
注意事项:
1.每题选出答案后,用2B铅笔把“答题卡”上对应题目的答案标号的信息点涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号的信息点。
2.本卷共15题,共30分。
3.可能用到的相对原子质量:
H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
Ca 40 Fe 56 Cu 64 Zn 65 Ag 108 I 127 Ba 137
一、单项选择题(本大题共10小题,每小题2分,共20分)每小题给出的四个选项中,只有一个符合题意。
1.下列变化属于物理变化的是( )
A.粮食酿酒B.海水晒盐C.树叶腐烂D.木材燃烧
2.分类是认识物质的常用方法,下列分类不正确的是( )
A.化合物:氯酸钾B.单质:液氧
C.混合物:冰水混合物D.有机物:甲烷
3.健康人的体液必须维持在一定的酸碱度范围内,下列正常体液一定显碱性的是( )
A.尿液(4.7—8.4)B.乳汁(6.6—7.6)
C.血浆(7.35—7.45)D.胃液(0.9—1.5)
4.正确的化学实验操作是实验成功和人身安全的重要保证。下列实验操作正确的( )
A.给液体加热B.过滤C.检查装置的气密性D.稀释浓硫酸
5.下列说法正确的是( )
A地壳中含量最多的元素是氧B.海洋中含量最多的元素是氯
C.空气中含量最多的元素是碳D.人体中含量最多的元素是钙
6.下列实验现象描述正确的是( )
A.磷在空气中燃烧产生大量的白雾
B.木炭在空气中燃烧发出淡蓝色火焰
C.镁在氧气中燃烧发出耀眼的白光,生成黑色固体
D.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
7.氮化镓是生产5G芯片的关键材料之一,氮的原子结构示意图和镓在元素周期表中的信息如图所示,下列说法错误的是( )
A.镓是金属元素B.氮原子的最外层电子数为7
C.镓元素的相对原子质量是69D.氮化镓中氮元素的化合价为价
8.我们每天摄入的食物不仅要保证一定的数量,还要注意合理的搭配,以保证各种营养素的均衡摄入。某同学的早餐是馒头、牛奶、鸡蛋、苹果。其中馒头中富含的营养素是( )
A.油脂B.维生素C.糖类D.蛋白质
9.下列叙述正确的是( )
A.含洗洁精的水可溶解油污形成溶液
B.化学反应在生成新物质的同时伴随能量变化
C.为提高农作物产量可大量使用农药和化肥
D.有气体生成的反应均为复分解反应
10.下图是工业上生产尿素反应的微观示意图。下列说法正确的是( )
A.尿素是复合肥料B.丁的化学式为
C.反应前后分子种类不变D.参加反应的甲、乙质量比为
二、选择题(本大题共5小题,每小题2分,共10分)每小题给出的四个选项中,有1~2个符合题意。只有一个选项符合题意的多选不得分;有2个选项符合题意的只选一个且符合题意得1分,若选2个有一个不符合题意则不得分。
11.推理是一种重要的科学思维方法,下列推理正确的是( )
A.有机物中都含碳元素,则含碳元素的化合物都是有机物
B.离子是带电的微粒,则所有带电的微粒都是离子
C.常温下,碱溶液的pH大于7,则pH大于7的溶液一定是碱溶液
D.化合物由不同种元素组成,则由不同种元素组成的纯净物一定是化合物
12.下列知识整理的内容中,都正确的选项是( )
13.下列实验方案能达到实验目的的是( )
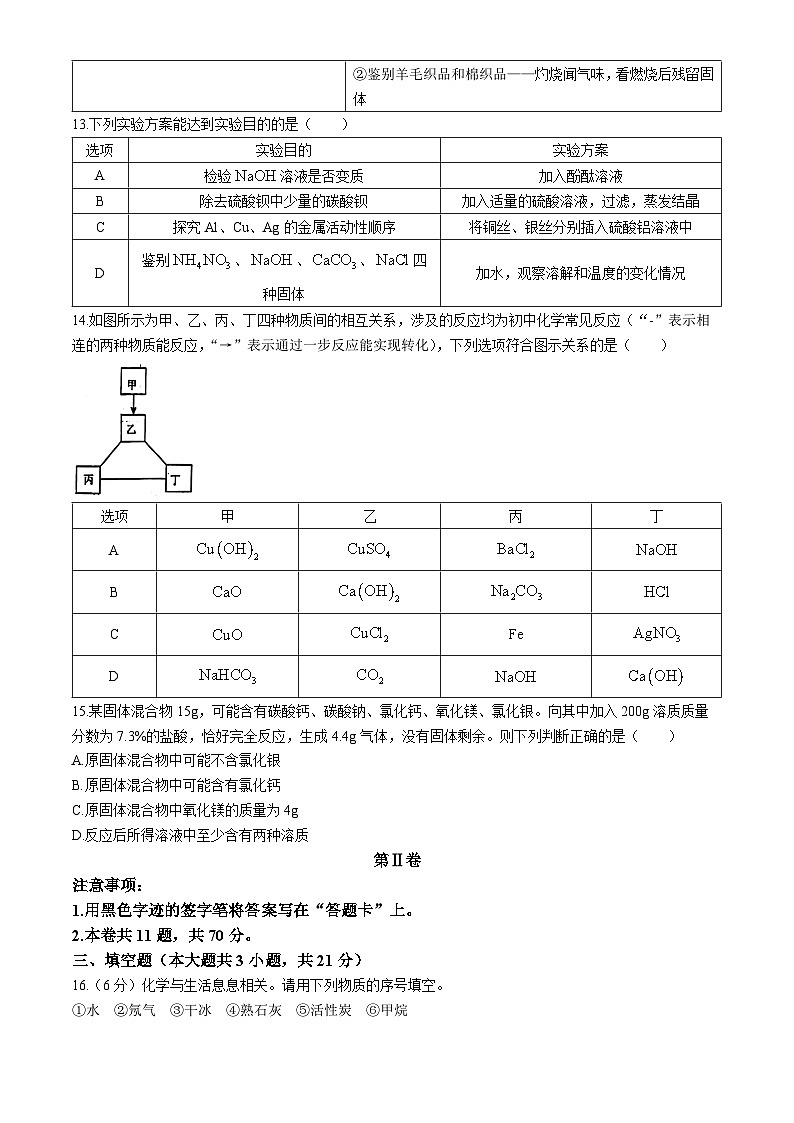
14.如图所示为甲、乙、丙、丁四种物质间的相互关系,涉及的反应均为初中化学常见反应(“-”表示相连的两种物质能反应,“→”表示通过一步反应能实现转化),下列选项符合图示关系的是( )
15.某固体混合物15g,可能含有碳酸钙、碳酸钠、氯化钙、氧化镁、氯化银。向其中加入200g溶质质量分数为7.3%的盐酸,恰好完全反应,生成4.4g气体,没有固体剩余。则下列判断正确的是( )
A.原固体混合物中可能不含氯化银
B.原固体混合物中可能含有氯化钙
C.原固体混合物中氧化镁的质量为4g
D.反应后所得溶液中至少含有两种溶质
第Ⅱ卷
注意事项:
1.用黑色字迹的签字笔将答案写在“答题卡”上。
2.本卷共11题,共70分。
三、填空题(本大题共3小题,共21分)
16.(6分)化学与生活息息相关。请用下列物质的序号填空。
①水 ②氖气 ③干冰 ④熟石灰 ⑤活性炭 ⑥甲烷
(1)可用于制作霓虹灯的是______。
(2)可用作溶剂的是______。
(3)可用作吸附剂的是______。
(4)可用于人工降雨的是______。
(5)可用于改良酸性土壤的是______。
(6)可用于燃料的天然气的主要成分是______。
17.(9分)世界水日的主题“珍惜地下水,珍视隐藏的资源”,水与人类的生活密切相关。
图1 图3
图2
(1)如图1是电解水的实验示意图,b端应该和电源的______极相连(填“正”“负”);该实验说明水是由______组成的。写出该实验的化学反应方程式______。
(2)天然水杂质较多,可用吸附、沉淀、蒸馏等多种方法净化,蒸馏的过程属于______变化(填“物理”或“化学”)。
(3)图2所示是利用海水提取粗盐的过程,图2中①是______池(填“结晶”或“过滤”)。
(4)实验室要由质量分数为20%(密度约为)的氯化钠溶液配制500g6%的氯化钠溶液,常用仪器如图3。
①配制过程有以下步骤a量取b计算c混匀d装瓶贴标签;正确的顺序是______(填序号)。
②若要完成该配置实验,还缺少______(写仪器名称)。
③所需20%氯化钠溶液的体积为______mL。
18.(6分)建立宏观、微观和符号之间的相互联系是化学学科的特点。请根据下列信息回答有关问题:
图1 图2
(1)图1为粒子之间的转化关系图,其中①表示的是______。
(2)图2中A、B位于同于同一周期,因为他们原子的______相同。
(3)图2中A、B形成的化合物的化学式为______。
(4)图2中D为某粒子的结构示意图,当时,则表示该粒子的符号为______。
(5)如图是某化学反应的微观示意图。甲物质代表乙烯,其化学式为。
写出此微观示意图所表示的化学反应方程式:______。
四、简答题(本大题共3小题,共18分)
19.(6分)写出下列反应的化学方程式。
(1)硫在氧气中燃烧______;
(2)铜与硝酸银溶液反应______;
(3)大理石与稀盐酸反应______。
20.(5分)人类的衣食住行、能源利用、环境保护和新材料的开发是我们共同关注的问题。
(1)化石燃料属于______资源(填“可再生”或“不可再生”)。
(2)家用炒菜的铁锅底都沾有许多黑色的物质,且炒菜时火焰的颜色呈黄色,这时应该把燃气灶的进风口______(填“调大”或“调小”)
(3)冬奥会的标志性场馆——国家速滑馆“冰丝带”,利用无处不在的“空气能”为3000平米场馆管理用房供暖,从而每年可实现减排二氧化碳160t,进而有效缓解的环境问题是______(填序号)。
A.酸雨B.白色污染C.温室效应D.臭氧空洞
(4)海带中富含______元素(填写元素名称),可以预防甲状腺肿大。
(5)一定质量的不完全燃烧,生成CO、和。其中CO和混合气体中碳元素与氧元素的质量比为。则参加反应的和的质量比为______。
21.(7分)溶液与人类生产、生活密切相关。
(1)下列少量物质分别放入水中,充分搅拌,可以得到溶液的是______(填字母)。
A.植物油B.面粉C.白糖
(2)根据和的溶解度表和溶解度曲线,回答下列问题:
①由溶解度表可知,20℃时的溶解度为______g。20℃时将36g加入50g水中,形成溶液质量为______g。
②和两种物质的溶解度受温度影响较小的是______。
③中含少量,要提纯应采用的方法是______。
④20℃时,等质量的和的饱和溶液中所含溶剂较多的是______(填“”或“”)。
⑤将40℃时和的饱和溶液同时降温到t℃,溶液中溶质的质量分数______(填“”、“”或“”)溶液中溶质的质量分数。
五、实验题(本大题共3小题,共21分)
22.(10分)化学是一门以实验为基础的科学。根据下列实验装置图,回答有关问题:
(1)写出标示数字的仪器名称:①______ ②______。
(2)实验室用大理石和稀盐酸制取二氧化碳,应选用的发生装置为______(填字母,下同)、收集装置为______,若要制取干燥的二氧化碳,需要在发生装置和收集装置之间连接______装置。
(3)实验室用高锰酸钾制取并收集氧气所选择的装置为______(填字母),该反应的化学方程式为______,该及应属于四种基本反应类型中的______反应。
(4)下列实验设计能达到实验目的的是______。
23.(6分)金属具有广泛的应用。
(1)铝块制铝箔是利用了铝的______。(填字母)
A.导热性B.导电性C.延展性
(2)地铁交通网络的密布方便我们出行。地铁车身的表面都喷上一层漆,目的是为了防止铁与空气中的______接触。
(3)某钢铁厂每天需消耗5000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁96%的生铁的质量是______t(计算结果精确到0.1)。
(4)将镁加入到硝酸银、硝酸铜混合溶液中,充分反应后过滤,得到滤渣和滤液,向滤渣中加稀盐酸有气泡产生。则滤液中一定含有的溶质为______,滤渣中一定有的物质是______。
(5)向铝、锌、氧化铜混合物中加入过量的稀硫酸,充分反应后过滤,得到无色溶液,测得剩余固体的质量为原固体质量的一半。则原固体中金属元素的质量分数为______。
24.(5分)现有一固体混合物A,已知可能含有、、、、、物质中的两种或者多种按图进行试验,出现的现象如图所示,(过程中所发生的发应均恰好完全反应),请回答下列问题:
(1)混合物A加水过滤得到无色溶液B,可以推出混合物A中一定不含有______(填化学式)。
(2)气体F的化学式为______。
(3)请写出反应④的化学方程式______。
(4)为进一步确定混合物的组成,取样品30g,按上述流程图进行实验,产生3.4g气体D,4.4g气体F,白色沉淀H的质量为2.33g,通过计算,确定该混合物中还含有的物质为______。
六、计算题(本大题共2小题,共10分)
25.(4分)钾肥能增强植物抗倒伏能力,农民向土壤中施加草木灰,是因为草木灰中含碳酸钾(化学式为)。
(1)碳酸钾的相对分子质量为______;
(2)碳酸钾中碳、氧元素的质量比______(最简整数比)。
(3)碳酸钾中钾元素质量分数为______(精确到0.1%)。
(4)69g碳酸钾中钾元素质量与______g硝酸钾中钾元素质量相等。
26.(6分)在烧杯中加入一定质量的碳酸钠和氯化钠的混合物,其中钠元素6.9g,再加入163.46g一定溶质质量分数的稀盐酸,恰好完全反应后,生成二氧化碳质量为4.4g,试计算:
(1.)原混合物中氯化钠的质量。(计算结果保留到0.1)
(2)所得溶液的溶质质量分数。
和平区2023-2024学年度第二学期九年级第三次质量调查
九年级化学答案
一、选择题(本大题共10小题,共20分)
二、选择题(本大题共5小题,共10分)
三、填空题(本大题共3题,共21分)
16.(6分)(1)② (2)① (3)⑤ (4)③ (5)④ (6)⑥
17.(9分)(1)负 氢元素、氧元素 (2)物理
(3)结晶 (4)①bacd ②玻璃棒 ③125
18.(6分)(1)原子 (2)电子层数 (3) (4)
(5)
四、简答题(本大题共3小题,共18分)
19.(6分)
(1)
(2)
(3)
20.(5分)(1)不可再生 (2)调大 (3)C (4)碘 (5)
21.(7分)(1)C (2)①31.6 68 ②氯化钠 ③降温结晶 ④ ⑤
五、实验题(本大题共3小题,共21分)
22.(10分)(1)①长颈漏斗 ②集气瓶 (2)B C F
(3)AC或AE, 分解 (4)AC
23.(6分)(1)C (2)氧气和水蒸气 (3)2916.7
(4)硝酸镁Mg、Cu、Ag (5)87.5%
24.(5分)(1) (2) (3)
(4)
六、计算题(本大题共2小题,共10分)
25.(4分)(1)138 (2) (3)56.5% (4)101
26.(6分)解:设碳酸钠的质量为x,生成氯化钠的质量为y。
碳酸钠中钠元素的质量为
原混合物中中钠元素的质量
原混合物中的质量
,
反应后溶液中溶质质量分数
答:(1)原混合物中氯化钠的质量5.9g。(2)所得洛液的溶质质量分数10%。
A.物质构成
B.化学与安全
①分子、原子、离子都是构成物质的粒子
②空气、液氧、过氧化氢中都含有氧分子
①天然气泄漏——立即打开换气扇
②海鲜防腐——甲醛溶液浸泡
C.物质与元素之最
D.物质鉴别与除杂
①空气中含量最多的物质是氧气
②地壳中含量最多的金属元素是铝
①除去氯化钠溶液中少量氯化镁——加入适量氢氧化钠溶液,过滤
②鉴别羊毛织品和棉织品——灼烧闻气味,看燃烧后残留固体
选项
实验目的
实验方案
A
检验溶液是否变质
加入酚酞溶液
B
除去硫酸钡中少量的碳酸钡
加入适量的硫酸溶液,过滤,蒸发结晶
C
探究Al、Cu、Ag的金属活动性顺序
将铜丝、银丝分别插入硫酸铝溶液中
D
鉴别、、、四种固体
加水,观察溶解和温度的变化情况
选项
甲
乙
丙
丁
A
B
C
Fe
D
温度/℃
0
20
40
溶解度/g
35.7
36.0
13.3
31.6
63.9
选项
A
B
C
D
实验目的
证明固体溶于水放热
验证质量守恒定律
证明分子在不停的运动
探究燃烧的条件
实验设计
题号
1
2
3
4
5
6
7
8
9
10
答案
B
C
C
C
A
D
B
C
B
B
题号
11
12
13
14
15
答案
D
D
D
BC
CD
13,2024年天津市和平区中考二模化学试题: 这是一份13,2024年天津市和平区中考二模化学试题,共4页。
2023年天津市和平区中考三模化学试题(无答案): 这是一份2023年天津市和平区中考三模化学试题(无答案),共10页。试卷主要包含了单选题,未知等内容,欢迎下载使用。
2022年天津市和平区中考三模化学试题(含答案): 这是一份2022年天津市和平区中考三模化学试题(含答案),共6页。试卷主要包含了本卷共15题,共30分,可能用到的相对原子质量,下列化学肥料属于复合肥料的是,下列实验设计能达到实验目的的是等内容,欢迎下载使用。












