


必刷题11 表格型实验方案的设计与评价-备战2024年高考化学二轮必刷题(江苏专用)
展开2、锻炼同学的考试心理,训练学生快速进入考试状态。高考的最佳心理状态是紧张中有乐观,压力下有自信,平静中有兴奋。
3、训练同学掌握一定的应试技巧,积累考试经验。模拟考试可以训练答题时间和速度。高考不仅是知识和水平的竞争,也是时间和速度的竞争,可以说每分每秒都是成绩。
4、帮助同学正确评估自己。高考是一种选拨性考试,目的是排序和择优,起决定作用的是自己在整体中的相对位置。因此,模拟考试以后,同学们要想法了解自己的成绩在整体中的位置。
必刷题型11 表格型实验方案的设计与评价
1.(2024·江苏南通·一模)室温下,探究溶液的性质,下列实验方案能达到探究目的的是
A.AB.BC.CD.D
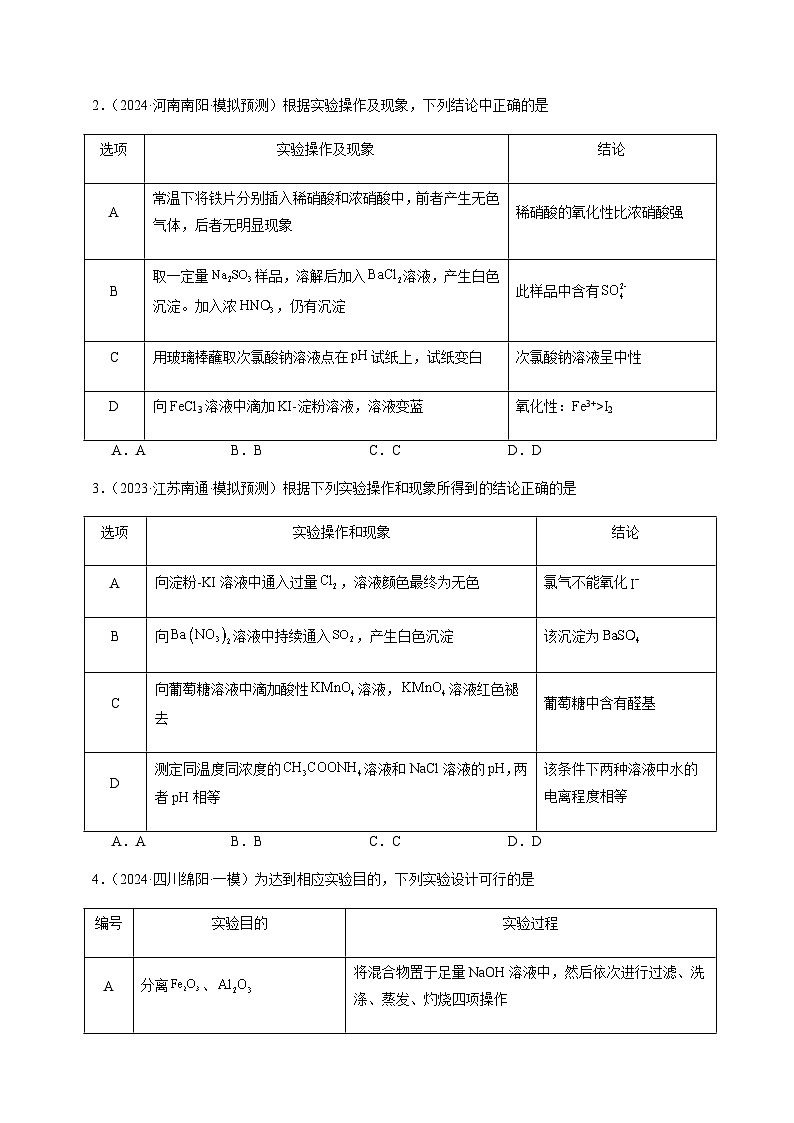
2.(2024·河南南阳·模拟预测)根据实验操作及现象,下列结论中正确的是
A.AB.BC.CD.D
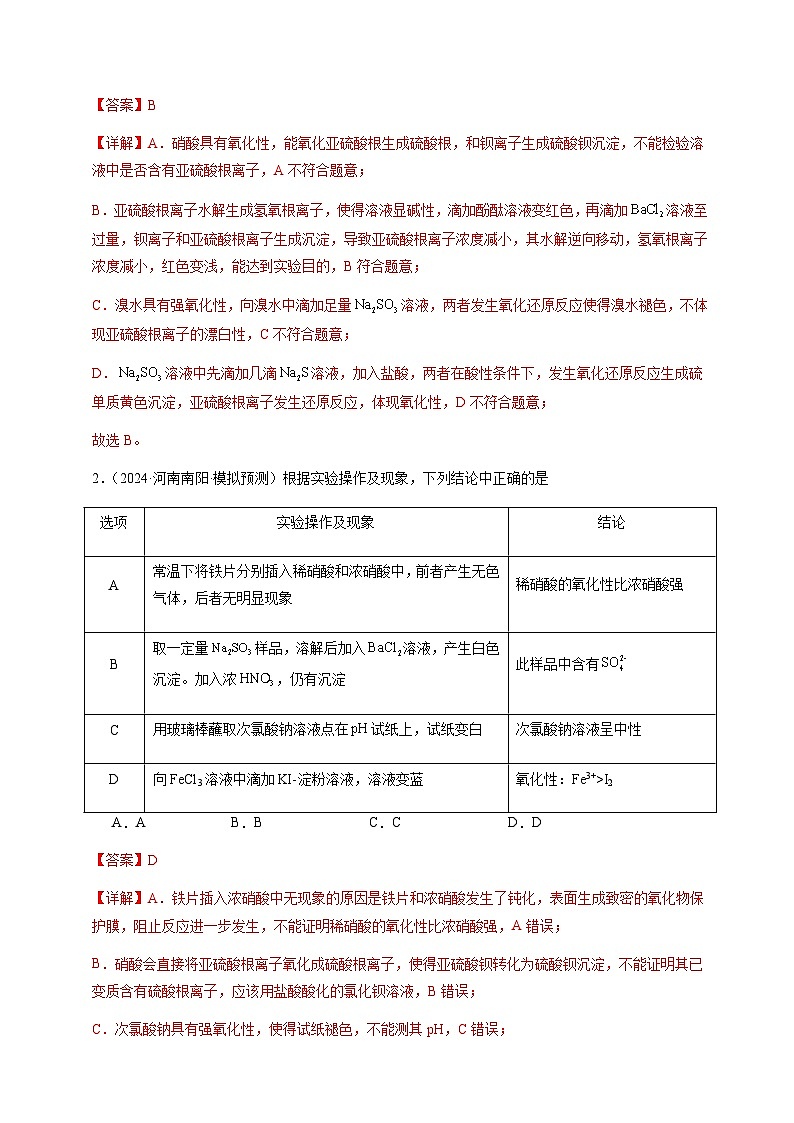
3.(2023·江苏南通·模拟预测)根据下列实验操作和现象所得到的结论正确的是
A.AB.BC.CD.D
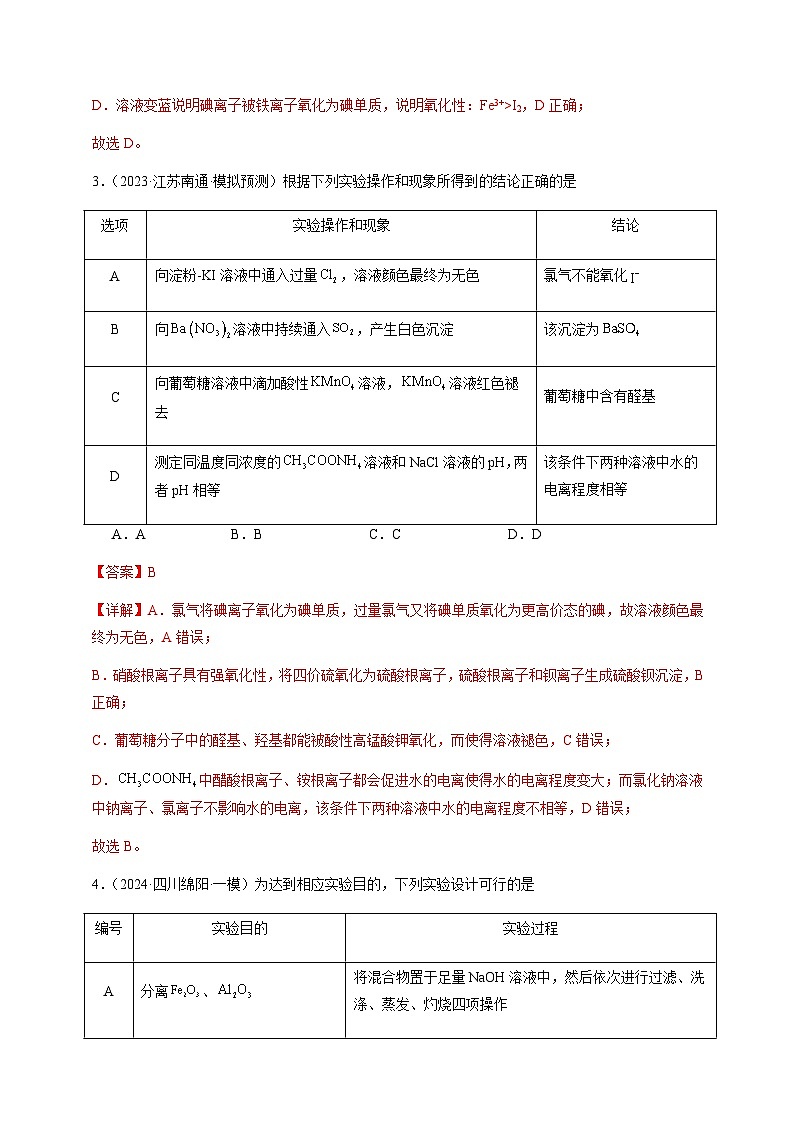
4.(2024·四川绵阳·一模)为达到相应实验目的,下列实验设计可行的是
A.AB.BC.CD.D
5.(2023·吉林·模拟预测)由实验操作和现象,可得出相应正确结论的是
A.AB.BC.CD.D
6.(2024·河北·一模)下列实验操作及现象不能得出相应结论的是
A.AB.BC.CD.D
7.(2024·江苏南京·校考模拟)室温下,探究0.1ml/L KHC2O4溶液的性质(H2C2O4:Ka1=5.9×10-2 Ka2=6×10-5;H2CO3:Ka1=4×10-7 Ka2=5.6×10-11),下列实验方案能达到探究目的的是
A.AB.BC.CD.D
8.(2024·江苏·校考模拟)下列实验方案能达到探究目的的是
A.AB.BC.CD.D
9.(2024·广西河池·一模)根据实验操作及现象,得出结论正确的是
A.AB.BC.CD.D
10.(2024·江苏扬州·校考模拟)室温下,下列实验方案能达到探究目的的是
A.AB.BC.CD.D
11.(2024·江苏扬州·校考模拟)下列实验目的对应的方案设计、现象和结论都正确的是
A.AB.BC.CD.D
12.(2024·湖南岳阳·一模)下列实验方案设计、现象和结论都正确的是
A.AB.BC.CD.D
13.(2024·江苏连云港·校考模拟)室温下,下列实验方案能达到探究目的的是
A.AB.BC.CD.D
14.(2024·江苏南通·校考模拟)室温下,探究0.1 溶液的性质,下列实验方案能达到探究目的的是
A.AB.BC.CD.D
15.(2023·江苏·一模)根据下列实验操作和现象得出的结论不正确的是
A.AB.BC.CD.D
16.(2023·江苏·二模)下列实验探究方案能达到探究目的的是
A.AB.BC.CD.D
17.(2023·江苏南京·二模)下列实验探究方案不能达到探究目的的是
A.AB.BC.CD.D
18.(2023·江苏南通·校考模拟)下列设计的实验方案不能达到实验目的的是
A.AB.BC.CD.D
19.(2023·全国·模拟预测)下列实验方法或操作能达到实验目的的是
A.AB.BC.CD.D
20.(2024·陕西咸阳·一模)下列实验设计及现象能达到实验目的的是
A.AB.BC.CD.D
21.(2023·辽宁丹东·一模)下列实验方法不能达到相应实验目的的是
A.AB.BC.CD.D
22.(2023·山东·模拟预测)下列各项实验为达到实验目的,其实验内容、现象及结论全部正确的是
A.AB.BC.CD.D
23.(2024·陕西西安·三模)下列根据实验操作及现象所得出的结论正确的是
A.AB.BC.CD.D
24.(2024·江苏泰州·校考模拟)室温下,下列实验方案能达到实验目的的是
A.AB.BC.CD.D
25.(2023·江苏·模拟预测)室温下,下列实验探究方案不能达到实验目的的是
A.AB.BC.CD.D
建议完成时间: 75 分钟
选择题:精选 25 题
实际完成时间: 分钟
非选择题:精选 0 题
选项
探究目的
实验方案
A
溶液中是否含有
向溶液中先滴加足量的稀硝酸,再滴加溶液,观察是否有沉淀产生
B
溶液呈碱性的原因
向溶液中先滴加酚酞,再滴加溶液至过量,观察溶液颜色变化
C
是否具有漂白性
向溴水中滴加足量溶液,观察溶液颜色
D
是否具有还原性
向溶液中先滴加几滴溶液,无明显现象,再滴加适量稀盐酸,观察是否有沉淀产生
选项
实验操作及现象
结论
A
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象
稀硝酸的氧化性比浓硝酸强
B
取一定量样品,溶解后加入溶液,产生白色沉淀。加入浓,仍有沉淀
此样品中含有
C
用玻璃棒蘸取次氯酸钠溶液点在试纸上,试纸变白
次氯酸钠溶液呈中性
D
向FeCl3溶液中滴加KI-淀粉溶液,溶液变蓝
氧化性:Fe3+>I2
选项
实验操作和现象
结论
A
向淀粉-KI溶液中通入过量,溶液颜色最终为无色
氯气不能氧化
B
向溶液中持续通入,产生白色沉淀
该沉淀为
C
向葡萄糖溶液中滴加酸性溶液,溶液红色褪去
葡萄糖中含有醛基
D
测定同温度同浓度的溶液和NaCl溶液的pH,两者pH相等
该条件下两种溶液中水的电离程度相等
编号
实验目的
实验过程
A
分离、
将混合物置于足量NaOH溶液中,然后依次进行过滤、洗涤、蒸发、灼烧四项操作
B
判断反应后是否沉淀完全
将溶液与溶液混合,反应后静置,向上层清液中再加1滴溶液
C
观察颜色
向盛有溶液的试管中滴入氨水,立即振荡
D
探究浓度对反应速率的影响
向2支盛有5mL不同浓度溶液的试管中同时加入2mL5%溶液,观察实验现象
实验操作
现象
结论
A
向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液
先变橙色,后变蓝色
氧化性:Cl2>Br2>I2
B
向蔗糖溶液中滴加稀硫酸,水浴加热,加入少量新制的Cu(OH)2悬浊液
无砖红色沉淀
蔗糖未发生水解
C
探究氢离子浓度对、相互转化的影响
向K2CrO4溶液中缓慢滴加硫酸,黄色变为橙红色
增大氢离子浓度,转化平衡向生成的方向移动
D
检验乙醇中是否含有水
向乙醇中加入一小粒金属钠,产生无色气体
乙醇中含有水
选项
实验操作
现象
结论
A
向碘水中加入溶液,观察现象,然后加入溶液,振荡
分层,下层为紫红色;加入溶液后,下层变为浅粉红色,上层呈棕黄色
碘在溶液中的溶解能力大于碘在水中的溶解能力
B
冷却装有的密闭烧瓶
烧瓶内气体颜色变浅
C
分别用计测量的溶液和溶液的
溶液的
溶液的
为强酸,为弱酸
D
向某样品溶液中依次加入溶液、稀硝酸
先产生白色沉淀,后沉淀不溶解
样品溶液中含有
选项
探究目的
实验方案
A
HC2O是否具有还原性
向2mL KHC2O4溶液中滴加几滴酸性KMnO4溶液,观察溶液颜色变化
B
溶液中是否含有K+
用铂丝蘸取少量 KHC2O4溶液,在酒精灯火焰上灼烧,观察火焰颜色变化
C
HC2O是否水解
向2mLKHC2O4溶液中滴加2~3滴酚酞试液,观察溶液颜色变化
D
HC2O是否具有酸性
向2mL 0.1ml/L Na2CO3溶液中逐滴滴加几滴 KHC2O4溶液,观察气泡产生的情况
选项
探究目的
实验方案
A
Na2SO3溶液是否变质
取少量久置的Na2SO3溶液向其中滴加BaCl2,观察现象
B
向5mL浓度均为的NaI、NaCl混合溶液中滴加2滴溶液,观察现象
C
检验乙醇中是否含有水
向乙醇中加入一小粒金属钠,观察现象
D
氯水久置,pH值会逐渐减小
每隔一段时间,使用pH试纸测定氯水的pH值,并记录数据进行比较
选项
实验操作及现象
结论
A
向某溶液中加入稀NaOH溶液,将湿润的红色石蕊试纸放在试管口,试纸不变蓝
该溶液中不含
B
在烧瓶中加入木炭颗粒和浓硝酸,加热,烧瓶中有大量红棕色气体产生
浓硝酸具有强氧化性,能氧化木炭,自身被还原为
C
向圆底烧瓶中加入NaOH和无水乙醇,搅拌,再加入1-溴丁烷,微热。将产生的气体通入酸性溶液,溶液褪色
1-溴丁烷消去反应的产物含有碳碳双键
D
将钠在燃烧匙中点燃,伸入到盛有的集气瓶中,产生大量白烟,瓶内有黑色颗粒生成
钠具有强还原性,瓶内发生了置换反应
选项
实验方案
探究目的
A
向盛有饱和Na2CO3溶液的试管中加入少量苯酚浊液,观察沉淀是否溶解、是否有气体生成
比较苯酚与碳酸的酸性强弱
B
取某有机物(无环状结构单元)与KOH溶液混合加热充分反应,冷却后取上层清液,加入硝酸酸化,再加入硝酸银溶液,观察是否有白色沉淀生成
该有机物中是否含有氯元素
C
将Fe3O4溶于盐酸所得溶液浓缩后,滴入酸性KMnO4溶液,观察溶液颜色的变化
Fe3O4中是否含Fe(Ⅱ)
D
用饱和Na2CO3溶液浸泡BaSO4固体,过滤,将所得固体溶于稀硝酸,观察沉淀是否溶解、是否有气体生成
比较Ksp(BaSO4)、Ksp(BaCO3)大小
实验目的
方案设计
现象和结论
A
探究金属钠在氧气中燃烧所得固体粉末的成分
取少量固体粉末,加入2~3mL蒸馏水
若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2
B
Fe2+是否具有还原性
向2mL1.0ml·L−1FeSO4溶液中滴加几滴0.5ml·L−1酸性KMnO4溶液
若溶液不变紫红色,则Fe2+具有还原性;若溶液变紫红色,则Fe2+不具有还原性
C
比较Cl2、Br2、I2的氧化性
向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置
溶液分层,下层呈紫红色,证明氧化性:Cl2>Br2>I2
D
比较H2CO3与CH3COOH的酸性
用pH计测定pH:①NaHCO3溶液②CH3COONa溶液
pH①>②,证明H2CO3酸性弱于CH3COOH
方案设计
现象
结论
A
将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加溶液
产生蓝色沉淀
食品脱氧剂样品中没有+3价铁
B
将银和溶液与铜和溶液组成原电池。
连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝
Cu的金属性比Ag强
C
用玻璃棒蘸取次氯酸钠溶液点在pH试纸上
试纸变白
次氯酸钠溶液呈中性
D
溴乙烷与氢氧化钠的乙醇溶液共热,将产生的气体通入酸性高锰酸钾溶液中
酸性高锰酸钾溶液的紫红色褪去
溴乙烷发生消去反应
选项
探究目的
探究方案。
A
氯水中是否含有
向淀粉-KI试纸上滴加几滴新制氯水,观察试纸的颜色变化
B
比较和的酸性
用pH计测量相同浓度和溶液的pH
C
探究维生素C的还原性
向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化
D
配制银氨溶液
向洁净的试管中加入1mL2%氨水,然后边振荡试管边逐滴滴入2%溶液
选项
探究目的
实验方案
A
是否具有还原性
向2mL 溶液中滴加几滴酸性溶液,观察溶液颜色变化
B
溶液中是否含有
用铂丝蘸取少量溶液,在酒精灯火焰上灼烧,观察火焰颜色变化
C
是否水解
向2mL 溶液中滴加2~3滴酚酞试液,观察溶液颜色变化
D
是否具有酸性
向2mL 0.1 溶液中逐滴滴加几滴溶液,观察气泡产生的情况
选项
实验操作和现象
实验结论
A
向溶有的溶液中通入气体X,出现白色沉淀
X具有强氧化性
B
向0.1 溶液中滴加KI-淀粉溶液,溶液变蓝
氧化性:
C
向溶液中加入等浓度等体积的溶液,出现白色沉淀
比更容易结合
D
将溴乙烷、乙醇和烧碱的混合物加热,产生的气体经水洗后,再通入酸性溶液中,溶液褪色
溴乙烷发生了消去反应
选项
探究方案
探究目的
A
将硫酸钡粉末和碳酸钠饱和溶液混合,充分振荡、静置,取上层清液1~2mL,滴加盐酸和溶液,观察是否有沉淀产生
探究和的溶度积常数相对大小
B
将二氧化硫气体通入碘和淀粉的混合溶液中,观察溶液颜色的变化
探究还原性:
C
向过氧化氢和氯化钡混合液中滴加亚硫酸钠溶液,观察是否产生沉淀
探究过氧化氢能否将亚硫酸盐氧化
D
加热溴乙烷和氢氧化钠-乙醇混合溶液,将产生的气体通入高锰酸钾溶液中,观察溶液颜色的变化
探究溴乙烷在此条件下发生取代反应还是发生消去反应
选项
探究方案
探究目的
A
向两支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸性高锰酸钾溶液,用力振荡,观察现象
探究有机物中基团间的相互作用
B
用分液漏斗向盛有固体的锥形瓶中滴加乙酸溶液,将产生的气体通入盛有苯酚钠溶液的试管中,观察现象
探究乙酸、碳酸和苯酚的酸性强弱
C
向两支试管中各加入2mL 0.1 溶液,分别放入盛有冷水和热水的两个烧杯中,再同时分别向两支试管中加入2mL 0.1 溶液,振荡,观察现象
探究温度对化学反应速率的影响
D
以Zn、Fe为电极,以酸化的3% NaCl溶液作电解质溶液,连接成原电池装置,过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴溶液,观察现象
探究金属的电化学保护法
选项
实验现象和操作
实验目的
A
向2mL0.1ml·L-1Na2S溶液中滴加0.1ml·L-1ZnSO4溶液至不再有沉淀产生,再滴加几滴0.1ml·L-1CuSO4溶液,出现黑色沉淀
验证Ksp(ZnS)>Ksp(CuS)
B
向含有0.1ml的FeI2溶液中通入0.1mlCl2,再加入淀粉溶液,溶液变蓝色
还原性:I->Fe2+
C
以Zn、Fe为电极,以酸化的3%NaCl溶液作电解质溶液,连接成原电池装置。过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K3[Fe(CN)6]溶液,观察现象
探究金属的牺牲阳极保护法
D
向盛有2mL0.1ml·L-1K2Cr2O7溶液的试管中滴加5~10滴NaOH溶液,再继续滴加5~10滴6ml·L-1H2SO4溶液,观察现象
探究浓度对化学平衡的影响
选项
实验目的
实验方法或操作
A
验证钢铁发生吸氧腐蚀
取钢铁电极附近溶液,向其中滴加溶液,产生蓝色沉淀
B
检验卤代烃中卤素原子种类
向卤代烃水解后的样品溶液中滴加硝酸酸化的溶液,根据沉淀颜色判断卤素原子种类
C
探究温度对反应速率的影响
已知 ,加热溶液,溶液变黄
D
检验乙醇中是否含有水
向乙醇中加入一小粒金属钠,产生无色气体
选项
实验目的
实验设计及现象
A
证明气体中存在平衡
压缩盛有气体的注射器至原来体积的一半,红棕色变浅
B
比较室温下、溶度积的大小
向溶液中滴加少量NaOH溶液,充分振荡后,再滴加几滴溶液,白色沉淀逐渐转化为蓝色
C
比较和的氧化性强弱
常温下,向溶液中加入溶液,将带火星的木条放在试管口,木条复燃
D
证明反应生成乙烯
乙醇和浓硫酸共热至170℃,将产生的气体通入酸性高锰酸钾溶液中,溶液紫色褪去
选项
实验目的
实验方法
A
验证中卤素原子的种类
向中加入过量的NaOH溶液,加热一段时间后静置,取少量上层清液于试管中,加入溶液,观察现象
B
比较和的热稳定性
分别加热和固体,将产生的气体通入澄清石灰水,观察现象
C
验证配位键影响物质的溶解性
向NaCl溶液中滴加少量溶液,产生白色沉淀,继续滴加氨水直至过量,观察现象
D
证明某酸是二元酸
用NaOH标准液滴定溶液,消耗NaOH的物质的量为的2倍
选项
实验目的
实验内容或装置
实验现象
结论
A
验证醋酸的酸性
试管中加少量碳酸钙,滴加冰醋酸
产生无色气泡
醋酸具有酸性
B
制作简单的燃料电池
关闭一段时间,打开关闭
电流表指针偏转
氢气与氧气反应可设计成燃料电池
C
验证卤族元素性质的相似性
在浴液中滴加氯水,震荡后滴加
溶液分层,上层接近无色,下层橙色
氯气可置换溴
D
验证浓硝酸的氧化性
在烧瓶中加入木炭颗粒与浓硝酸,然后加热
烧瓶中有大量红棕色气体产生
浓硝酸具有强氧化性可氧化木炭
选项
实验操作及现象
结论
A
淀粉溶液和稀硫酸混合加热后,再加新制的悬浊液加热,无砖红色沉淀产生
淀粉未水解
B
向氢氧化钠溶液中先加入少量溶液,充分反应后再加入少量溶液,先产生白色沉淀,后产生蓝色沉淀
室温下,比的溶度积小
C
向两支试管中分别加入和溶液,再向盛有溶液的试管中加入蒸馏水,最后同时向两支试管中加溶液,振荡,加入溶液的试管先出现浑浊
其他条件一定时,反应物浓度越大,反应速率越快
D
将通入酸性溶液中,取反应后的溶液于试管中,再向试管中加入溶液,振荡,产生白色沉淀
该环境中的氧化产物为
选项
实验方案
实验目的
A
将1—溴丁烷与NaOH的乙醇溶液混合后加热,将生成的气体通入溴水中,观察溶液颜色变化
1—溴丁烷发生消去反应生成烯烃
B
用铂丝蘸取某溶液进行焰色试验,观察火焰颜色
溶液中存在
C
将中间裹有锌皮的铁钉(如图)放在滴有酚酞的NaCl溶液中,一段时间后观察铁钉周围溶液颜色变化
铁钉能发生吸氧腐蚀
D
用pH计分别测量和HCOONa溶液的pH,比较溶液pH大小
选项
探究方案
探究目的
A
室温下,向一定量饱和Na2CO3溶液中通入足量CO2气体,观察是否有晶体析出
室温下固体在水中的溶解性:
B
向FeBr2溶液中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯水,观察溶液颜色的变化
Fe2+的还原性比Br-的强
C
用计测量相同温度、相同浓度NaClO溶液、溶液的pH,比较pH大小
HClO的酸性比的强
D
向溶液中滴入2滴溶液,有沉淀生成,再滴入4滴溶液,观察沉淀颜色变化
必刷题10 化学反应的方向与限度-备战2024年高考化学二轮必刷题(江苏专用): 这是一份必刷题10 化学反应的方向与限度-备战2024年高考化学二轮必刷题(江苏专用),文件包含必刷题型10化学反应的方向与限度-备战2024年高考化学二轮必刷题型江苏专用原卷版docx、必刷题型10化学反应的方向与限度-备战2024年高考化学二轮必刷题型江苏专用解析版docx等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。
必刷题07 元素化学—物质的性质与应用-备战2024年高考化学二轮必刷题(江苏专用): 这是一份必刷题07 元素化学—物质的性质与应用-备战2024年高考化学二轮必刷题(江苏专用),文件包含必刷题型07元素化学物质的性质与应用-备战2024年高考化学二轮必刷题型江苏专用原卷版docx、必刷题型07元素化学物质的性质与应用-备战2024年高考化学二轮必刷题型江苏专用解析版docx等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。
必刷题03 化学实验基础知识和技能-备战2024年高考化学二轮必刷题(江苏专用): 这是一份必刷题03 化学实验基础知识和技能-备战2024年高考化学二轮必刷题(江苏专用),文件包含必刷题型03化学实验基础知识和技能-备战2024年高考化学二轮必刷题型江苏专用原卷版docx、必刷题型03化学实验基础知识和技能-备战2024年高考化学二轮必刷题型江苏专用解析版docx等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。












